Nguyên tử hydro
 | |
| Thông tin chung | |
|---|---|
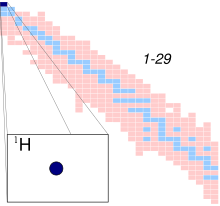
| Ký hiệu | 1H |
| Tên | nguyên tử hydro, 1H, H-1, protium |
| Proton (Z) | 1 |
| Neutron (N) | 0 |
| Nuclide data | |
| Độ phong phú tự nhiên | 99.985% |
| Khối lượng đồng vị | 1.007825 Da |
| Spin | 1/2 |
| Excess energy | 7288.969 keV |
| Binding energy | 0.000 keV |
| Isotopes of hydrogen Complete table of nuclides | |
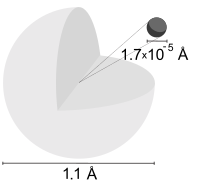
Một nguyên tử hydro là một nguyên tử của nguyên tố hóa học hydro. Nguyên tử điện tích trung lập, chỉ chứa duy nhất một hạt proton mang điện tích dương và một hạt electron mang điện tích âm, bị ràng buộc với hạt nhân bởi lực Coulomb. Nguyên tử hydro cấu thành khoảng 75% khối lượng baryon của vũ trụ.[1]
Trên Trái Đất, các nguyên tử hydro bị cô lập là rất hiếm. Thay vào đó, hydro có xu hướng kết hợp với các nguyên tử trong có mặt trong các hợp chất, hoặc với chính nó để tạo thành khí hydro, H2.
Việc phát triển một lý thuyết để hiểu rõ tính chất của nguyên tử hydro khá quan trọng trong lịch sử cơ học lượng tử.
Đồng vị[sửa | sửa mã nguồn]
Đồng vị giàu nhất, hydro-1, proti, hay còn gọi là hydro nhẹ, không chứa bất kì hạt neutron nào và chỉ đơn giản là một proton và một electron. Proti là ổn định và cấu thành nên 99.9885% các nguyên tử hydro trong tự nhiên.
Deuteri, có hạt nhân chứa một neutron và một proton. Nguyên tử này ổn định và cấu thành nên 0.0115% hydro tự nhiên, được sử dụng trong công nghiệp cho lò phản ứng hạt nhân và cộng hưởng từ hạt nhân.
Triti chứa hai neutron và một proton, không ổn định, phân rã với một chu kì bán rã 12,32 năm. Vì bán rã nên triti không tồn tại trong tự nhiên, ngoại trừ trong các lượng vết.
Các đồng vị cao hơn của hydro chỉ được tạo ra một cách nhân tạo bằng các máy gia tốc hạt và các lò phản ứng, và chúng bán rã trong vòng 10−22 giây.
Các công thức ở dưới đều đúng cho tất cả ba đồng vị của hydro, nhưng phải sử dụng các giá trị hơi khác nhau của hằng số Rydberg (sửa đúng công thức được đưa ra bên dưới) cho mỗi loại đồng vị hydro.
Ion hydro[sửa | sửa mã nguồn]
Hydro tìm thấy trong điều kiện bình thường (nhiệt độ và áp suất phòng) luôn luôn đi kèm theo với electron của nó, do ion hydro rất dễ bị phản ứng. Khi ion hydro viết là "H+" như trong sự sonvat hóa của các axit như axit clohydric, hydroni, H3O+ , có nghĩa là, không phải là một nguyên tử hydro đơn lẻ bị ion hóa. Trong trường hợp đó, acid chuyển proton vào H2O để tạo thành H3O+.
Ion hydro không có electron, hoặc các proton tự do có phổ biến trong môi trường liên sao, và trong gió mặt trời.
Phân tích giả định[sửa | sửa mã nguồn]
Nguyên tử hydro có ý nghĩa đặc biệt trong cơ học lượng tử và lý thuyết trường lượng tử như một hệ thống vật lí vấn đề hai vật đơn giản, đã mang lại nhiều phương pháp giải biểu thức dạng đóng.
Mô phỏng cổ điển thất bại[sửa | sửa mã nguồn]
Thí nghiệm của Ernest Rutherford năm 1909 cho thấy cấu trúc của nguyên tử là một khối đặc, hạt nhân điện dương với một hạt điện âm nhẹ quay xung quanh nó. Việc này ngay lập tức gây ra vấn đề về việc làm thế nào mà một hệ thống như vậy có thể ổn định. Điện từ học cổ điển đã chỉ ra rằng bất kỳ gia tốc phát ra năng lượng nào sẽ được mô phỏng thông qua công thức Larmor. Nếu hạt electron mà nằm trong một quỹ đạo tròn hoàn hảo và phát ra năng lượng liên tục, nó sẽ nhanh chóng rơi xoắn ốc vào trong hạt nhân với một thời gian rơi khoảng:
là bán kính Bohr và là bán kính điện từ cổ điển. Nếu điều này là đúng, tất cả các nguyên tử ngay lập tức sẽ sụp đổ, tuy nhiên các nguyên tử dường như lại ổn định. Hơn nữa, việc rơi xoắn ốc vào bên trong sẽ phát hành ra một tần số điện từ khi quỹ đạo đã nhỏ hơn. Thay vào đó, các nguyên tử được quan sát chỉ phát ra các tần số bức xạ rời rạc. Cách giải quyết sẽ nằm trong việc phát triển của cơ học lượng tử.
Mô hình Bohr-Sommerfeld[sửa | sửa mã nguồn]
Vào năm 1913, Niels Bohr đo được các mức năng lượng và tần số quang phổ của nguyên tử hydro sau khi làm một số giả định đơn giản để cố gắng sửa chữa mô hình cổ điển đã bị thất bại. Giả định bao gồm:
- Electron chỉ có thể tồn tại trong quỹ đạo tròn nhất định, riêng lẻ hay trạng thái tĩnh tại, do đó có những bán kính và năng lượng riêng lẻ nhất định.
- Electron không phát ra phóng xạ khi ở một trong những trạng thái này.
- Một electron có thể đạt được hay mất đi năng lượng bằng cách nhảy từ một quỹ đạo riêng lẻ sang một quỹ đạo khác.
Bohr cho rằng mô men động lượng của electron được lượng tử hóa với các giá trị:
với
với là hằng số Plank trên . Ông ấy cũng nghĩ rằng, lực hướng tâm giữ electron nằm trong quỹ đạo của mình, được phân phát bởi lực Coulomb, và năng lượng đó được bảo tồn. Bohr suy ra được năng lượng của mỗi quỹ đạo của nguyên tử hydro là:[2]
- ,
với là khối lượng nghỉ electron, là điện tích cơ bản, là độ từ thấm, và là số lượng tử (bây giờ được biết đến như là số lượng tử chính). Dự đoán của Bohr phù hợp với những thí nghiệm đo chuỗi quang phổ của Hydro trước đó, tạo thêm cơ sở vững chắc về một lí thuyết sử dụng các giá trị lượng tử.
Cho , giá trị
được gọi là đơn vị năng lượng Rydberg. Nó có liên quan đến hằng số Rydberg của vật lý nguyên tử với
Giá trị chính xác của hằng số Rydberg giả định rằng hạt nhân là lớn vô cùng đối với electron. Với hydro-1, hydro-2 (deuteri), và hydro-3 (triti) hằng số được sửa đổi một chút để sử dụng khối lượng rút gọn của hệ thống, chứ không phải chỉ đơn giản là khối lượng của electron. Tuy nhiên, vì hạt nhân nặng hơn nhiều so với electron nên các giá trị gần như giống nhau. Hằng số Rydberg RM của một nguyên tử hydro (một electron), R được cho là
với là khối lượng hạt nhân nguyên tử. Với hydro-1, tỉ lệ là khoảng 1/1836 (hay nói cách khác là tỉ lệ khối lượng electron-proton). Với deuteri và triti, tỉ lệ này lần lượt là khoảng 1/3670 và 1/5497. Những con số này, khi cộng thêm 1 vào mẫu số cho sửa chữa rất nhỏ giá trị của R, và do đó chỉ sửa chữa một chút cho tất cả mức năng lượng trong các đồng vị tương ứng của hydro.
Vẫn còn một số vấn đề về mô hình của Bohr:
- nó thất bại trong việc dự đoán các chi tiết quang phổ khác như là cấu trúc tinh tế và cấu trúc siêu tinh tế
- nó chỉ có thể dự đoán mức năng lượng chính xác cho bất kì nguyên tử một electron nào thôi (nguyên tử giống hydro)
- những giá trị được dự đoán chỉ chính xác với , là hằng số cấu trúc tinh tế.
Hầu hết những thiếu sót này được sửa chữa bởi mô hình sửa đổi từ Bohr của Arnold Sommerfeld. Ông giới thiệu thêm hai độ tự do, cho phép một electron di chuyển trên một quỹ đạo elip; được biểu thị bởi độ lệch tâm quỹ đạo và xích vĩ của nó đối với một trục được chọn. Điều này tạo ra thêm hai số lượng tử, tương ứng với các mô men động lượng quỹ đạo và hình chiếu của nó lên trục được chọn. Như vậy sẽ sửa lại đúng sự đa dạng của các trạng thái (ngoại trừ cho yếu tố 2 chịu trách nhiệm về spin của electron chưa biết) được tìm thấy. Hơn nữa, khi áp dụng thuyết tương đối hẹp với các quỹ đạo elip, Sommerfeld đã thành công trong việc suy ra được biểu thức đúng cho cấu trúc tinh tế của quang phổ hydro (điều mà giống hệt như trong lí thuyết thuyết Dirac phức tạp nhất). Tuy nhiên, một số hiện tượng được quan sát như hiệu ứng Zeeman bất thường vẫn bỏ ngỏ, không thể giải thích được. Những vấn đề này đã được giải quyết với sự phát triển của cơ học lượng tử và phương trình Dirac. Người ta thường xuyên nhận xét rằng chính phương trình Schrödinger là hoàn hảo hơn lí thuyết Bohr-Sommerfeld trong việc mô phỏng nguyên tử hydro. Tuy nhiên điều này là không phải đúng, vì hầu hết kết quả của việc tiếp cận của cả hai đều trùng lặp hoặc là rất gần giống nhau (một ngoại lệ đáng chú ý là vấn đề của nguyên tử hydro trong từ trường và điện từ trường, không thể giải quyết được trong khuôn khổ của lí thuyết Bohr-Sommerfeld), và cả hai đều thiếu sót do sự vắng mặt của spin electron trong hai lí thuyết. Lí thuyết Bohr-Sommerfeld hoàn toàn thất bại trong việc giải thích các hệ thống nhiều electron (như nguyên tử heli hoặc phân tử hydro), chứng minh sự thiếu hoàn hảo của nó trong việc mô tả hiện tượng lượng tử.
Phương trình Schrödinger[sửa | sửa mã nguồn]
Phương trình Schrödinger thể hiện sự phát triển của hệ thống lượng tử theo thời gian, và có thể cung cấp được các câu trả lời chính xác, đầy đủ cho nguyên tử hydro phi tương đối.
Hàm sóng[sửa | sửa mã nguồn]
Cơ học Hamilton của nguyên tử hydro là toán tử động năng và lực hút coulomb giữa proton điện dương và electron điện âm. Bằng cách sử dụng phương trình Schrödinger độc lập thời gian, bỏ qua tất cả các tương tác spin cặp, và sử dụng khối lượng rút gọn , phương trình được viết ra:
Mở rộng toán tử Laplace vào hệ tọa độ cầu:
Đây là một giá trị riêng phần, phương trình vị phân riêng phần mà có thể được giải quyết trong giới hạn các hàm đặc biệt. Bằng cách đặt Z=1 (cho một proton), vị trí hàm sóng bình thường, được cho trong hệ tọa độ cầu là:
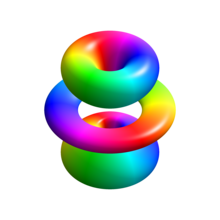
với:
- ,
- là bán kính Bohr,
- là một đa thức Laguerre tổng quát của độ n − ℓ − 1, và
- là một hàm điều hòa cầu của độ ℓ và hạng m. Lưu ý rằng đa thức Laguerre tổng quát được định những nghĩa khác nhau tùy theo tác giả. Sử dụng ở đây phù hợp với định nghĩa được sử dụng bởi Messiah,[4] và Mathematica.[5] Với những định nghĩa khác, đa thức Laguerre tổng quát kèm theo một yếu tố ,[6] hay đa thức Laguerre tổng quát xuất hiện trong hàm sóng hydro lại là .[7]
Các số lượng tử có thể có giá trị như sau:
Ngoài ra, những hàm sóng được bình thường hóa (tức là tích phân mô đun vuông của chúng bằng 1) và trực giao:
với là trạng thái được đại diện bởi hàm sóng trong kí hiệu Bra-ket, và là hàm delta Kronecker.[8]
Các hàm sóng trong không gian mô men có liên quan đến các hàm sóng trong không gian vị trí qua một biến đổi Fourier
cho các trạng thái ràng buộc, cho ra kết quả [9]
với là một đa thức Gegenbauer, và nằm trong đơn vị .
Cách giải cho phương trình Schrödinger cho hydro là giải tích phân, tạo một biểu thức đơn giản cho mức năng lượng của hydro, và cũng cho các tần số của các vạch quang phổ hydro; tái tạo lại một cách đầy đủ mô hình Bohr, vượt ra ngoài nó. Nó cũng mang lại hai số lượng tử khác, và hình dáng hàm sóng của electron ("orbital") cho vô số trạng thái cơ học lượng tử có thể có, nhờ đó giải thích được những tính chất bất đẳng hướng của những liên kết nguyên tử.
Phương trình Schrödinger cũng áp dụng cho các dạng nguyên tử và phân tử phức tạp hơn. Khi có nhiều hơn một electron hoặc một hạt nhân, cách giải quyết là không phải tính tích phân mà cần máy tính hoặc giả định tối giản hóa để thực hiện.
Vì phương trình Schrödinger chỉ đúng cho cơ học lượng tử bất tương đối, phép giải này cho nguyên tử hydro không phải là hoàn toàn chính xác. Phương trình Dirac của lí thuyết lượng tử tương đối cải thiện phép giải trên (xem bên dưới).
Hệ quả của phương trình Schrödinger[sửa | sửa mã nguồn]
Phép giải của phương trình Schrödinger (phương trình sóng) cho nguyên tử hydro sử dụng tính chất lực tĩnh điện được sản xuất bởi hạt nhân là đẳng hướng (nó đối xứng trong không gian và chỉ phụ thuộc vào khoảng cách đến hạt nhân). Mặc dù những trạng thái dừng (orbital) không nhất thiết phải tự đẳng hướng, sự phụ thuộc của chúng vào các tọa độ cầu theo sau là hoàn toàn từ sự đẳng hướng của nguồn nằm dưới: những vector riêng của toán tử Hamilton (trạng thái năng lượng lượng tử) có thể được chọn như những vector riêng đồng thời của toán tử mô men động lượng.Điều này tương ứng với thực tế là mô men động lượng được bảo tồn trong orbital chuyển động của electron xung quanh hạt nhân. Vì vậy, trạng thái năng lượng lượng tử có thể được phân loại bởi hai số lượng tử mô men động lượng, ℓ và m (cả hai đều là số nguyên). Số lượng tử mô men động lượng ℓ = 0, 1, 2,... xác định tầm quan trọng của mô men động lượng. Số lượng tử từ m = −ℓ,..., +ℓ xác định hình chiếu của mô men động lượng (chọn tùy ý) trên trục z.
Ngoài các biểu thức toán học cho mô men động lượng tổng và mô men động lượng chiếu của hàm sóng, một biểu thức cho đặc tính hàm sóng phụ thuộc bán kính phải được tìm thấy. Chỉ ở ngay đây mà các chi tiết của 1/r Coulomb có tiềm năng (dẫn đến đa thức Laguerre trong r). Điều này dẫn đến một số lượng tử thứ ba, số lượng tử chính n = 1, 2, 3,.... Số lượng tử chính hydro liên quan đến tổng năng lượng của nguyên tử.
Lưu ý rằng các giá trị lớn nhất của mô men động lượng bị giới hạn bởi số lượng tử chính: nó chỉ có thể lên tới n − 1, tức là ℓ = 0, 1,..., n − 1.
Do sự chuyển đổi mô men động lượng, các trạng thái của cùng một ℓ nhưng khác m có cùng năng lượng (điều này chịu trách nhiệm cho tất cả các vấn đề với đối xứng quay). Ngoài ra, với nguyên tử hydro, trạng thái cùng n, nhưng khác ℓ cũng thoái hóa (tức là chúng cùng một năng lượng). Tuy nhiên, điều này là một đặc tính riêng biệt của hydro và không còn đúng cho các nguyên tử phức tạp hơn có một tiềm năng (hiệu quả) khác nhau từ dạng 1/r (do sự hiện diện của các hạt nhân tiềm năng).
Thêm vào sự hiện diện của spin của electron thêm vào một số lượng tử cuối cùng, các hình chiếu của mô men động lượng của electron dọc trục z, trong đó có thể có hai giá trị. Vì vậy, bất kỳ trạng thái lượng tử nào của electron trong nguyên tử hydro được mô tả đầy đủ bằng bốn số lượng tử. Theo các quy tắc thông thường của cơ học lượng tử, thực trạng của electron có thể là bất kì chồng chấp lượng tử của những trạng thái này. Điều này giải thích tại sao sự lựa chọn của trục z cho các hướng lượng tử hóa của vector mô men động lượng là phi vật chất: một orbital của ℓ và m' lấy cho một trục z' khác luôn có thể được biểu thị như là một chồng chất lượng tử phù hợp các trạng thái của các m khác nhau (nhưng cùng l), mà đã được lấy cho trục z.
Khái lược toán học của các trạng thái lượng tử của nguyên tử hydro[sửa | sửa mã nguồn]
Năm 1928, Paul Dirac tìm thấy một phương trình hoàn toàn tương thích với thuyết tương đối hẹp, và (như một hệ quả) đã làm hàm sóng thành một "spinor Dirac" 4 phần bao gồm phần spin "lên" và "xuống", với spin dương và âm, (hay là vật chất và phản vật chất). Cách giải phương trình này cho các kết quả chính xác hơn phép giải Schrödinger.
Mức năng lượng[sửa | sửa mã nguồn]
Mức năng lượng của hydro, bao gồm cả cấu trúc tinh tế (ngoại trừ hiệu ứng Lamb và cấu trúc siêu tinh tế), được đưa ra bởi các biểu thức hằng số cấu trúc tinh tế:[10]
với α la hằng số cấu trúc tinh tế và j là số lượng tử "tổng mô men động lượng", là bằng |ℓ ± 1/2| tùy thuộc vào sự hướng của các spin electron. Công thức này đại diện cho một điều chỉnh nhỏ đến năng lượng đạt được bởi lí thuyết Bohr và Schrödinger được đưa ra phía trên. Các yếu tố trong ngoặc vuông cuối cùng gần như là một; thuật ngữ phát sinh từ những hiệu ứng tương đối (xem chi tiết #Tính chất vượt ra ngoài phép giải Schrödinger). Rất đáng chú ý là biểu thức này lần đầu tiên được phát hiện bởi A. Sommerfeld vào năm 1916, dựa trên phiên bản tương đối của lí thuyết Bohr cũ. Tuy nhiên, ông đã dùng những kí hiệu khác cho các số lượng tử.
Mô phỏng orbital electron hydro[sửa | sửa mã nguồn]

Bên phải ảnh cho thấy những orbital nguyên tử hydro đầu tiên (vector riêng năng lượng). Đây là mặt cắt của biên độ xác suất đã được tô màu (đen đại diện cho mật độ không và màu trắng đại diện cho mật độ cao nhất). Số lượng tử mô men động lượng (orbital) ℓ được biểu thị trong mỗi cột, bằng cách sử dụng mã quang phổ thông thường (s có nghĩa là ℓ = 0, p có nghĩa là ℓ = 1, d có nghĩa là ℓ = 2). Số lượng tử chính n (= 1, 2, 3,...) nằm ở phía bên phải mỗi hàng. Trong tất cả các ảnh, số lượng tử từ m đã được đặt về 0, và mặt phẳng cắt ngang là mặt phẳng xz (z là trục đứng). Biên độ xác suất trong ba chiều không gian thu được bằng cách xoay quanh trục z.
"Trạng thái cơ bản", hay nói cách khác là trạng thái năng lượng thấp nhất, trong đó electron thường được tìm là trạng thái đầu tiên, trạng thái 1s (mức lượng tử chính n = 1, ℓ = 0).
Đường thẳng đen xảy ra trong mỗi orbital, nhưng orbital đầu tiên: đây là những giao điểm của hàm sóng, tức là nơi mà có biên độ xác suất bằng không. (Chính xác hơn là, các giao điểm là các hàm điều hòa cầu xuất hiện như là một kết quả của việc giải phương trình Schrödinger ở tọa độ cực.)
Các số lượng tử xác định cách bố trí của những giao điểm.[11] Chúng là:
- các giao điểm tổng,
- là các giao điểm góc:
- đi xung quanh trục (trên mặt phẳng xy). (Hình trên không hiển thị những giao điểm này vì chúng cắt ngang qua mặt phẳng xz.)
- (các giao điểm góc còn lại) xảy ra trên trục (đứng).
- (các giao điểm không phải góc còn lại) là các giao điểm xuyên.
Tính chất vượt ra ngoài phép giải Schrödinger[sửa | sửa mã nguồn]
Có một vài hiệu ứng quan trọng bị bỏ qua trong phương trình Schrödinger, và điều đó là lí do một số vạch quang phổ ngoài thực tế bị lệch đi một chút so với những gì đã dự đoán:
- Mặc dù tốc độ của electron trong hydro chỉ bằng 1/137 tốc độ ánh sáng, nhiều thí nghiệm hiện đại với độ chính xác rất cao yêu cầu một lí thuyết hoàn chỉnh giải thích sự xử lí tương đối của vấn đề. Một kết quả xử lí tương đối cho ra một mô men tăng khoảng 1 phần trong 37,000 cho electron. Vì bước sóng của electron được xác định theo mô men của nó, những orbital có chứa electron tốc độ cao cho thấy sự co rút do bước sóng nhỏ hơn.
- Thậm chí khi không có từ trường bên ngoài, trong các khung quán tính của electron đang chuyển động, trường điện từ của hạt nhân cũng có một phần tử từ trường. Spin của electron có liên quan đến mô men lưỡng cực từ, thứ mà tương tác với từ trường này. Hiệu ứng này cũng đã được giải thích bởi thuyết tương đối hẹp, và nó dẫn đến cái gọi được là spin-quỹ đạo cặp, tức là một sự tương tác giữa orbital chuyển động của electron xung quanh hạt nhân, và spin của nó.
Cả hai năng tính chất này (và nhiều hơn nữa) được tích hợp vào trong phương trình Dirac tương đối với các dự đoán đến gần hơn với thí nghiệm. Một lần nữa, phương trình Dirac có thể được giải tích phân trong những trường hợp đặc biệt của hệ thống hai vật, như nguyên tử hydro. Các kết quả trạng thái lượng tử bây giờ phải được phân loại bởi các số lượng tử mô men động lượng tổng j (phát sinh qua sự cặp giữa spin electron và toán tử mô men động lượng). Trạng thái có cùng j và cùng n vẫn thoái hóa. Vì vậy, phép giải tích phân trực tiếp của phương trình Dirac dự đoán mức Hydro 2S(1/2) và 2(1/2) có chính xác cùng một năng lượng, thứ mâu thuẫn với các quan sát của thí nghiệm Lamb-Retherford.
- Luôn có các dao động chân không của trường điện từ dựa theo cơ học lượng tử. Do những sự thoái hóa dao động như vậy giữa trạng thái của cùng j nhưng khác l được đẩy lên, cho chúng một chút năng lượng khác nhau. Điều này đã được chứng minh trong thí nghiệm Lamb-Rutherford nổi tiếng và là thời điểm khởi đầu cho sự phát triển của những lí thuyết về điện động lực học lượng tử (thứ mà có thể đối phó với những dao động chân không và sử dụng sơ đồ Feynman xấp xỉ bằng lí thuyết nhiễu loạn). Hiệu ứng này ngày nay được gọi là hiệu ứng Lamb.
Với những phát triển này, đó là điều tất yếu với phép giải của phương trình Dirac cho nguyên tử hydro có thể được hoạt động vô cùng chính xác như vậy, nên khi bất kỳ sai lệch nào được quan sát phải được nhận định một cách nghiêm túc như là một tín hiệu của sự thất bại của lí thuyết.
Những lí thuyết khác cho lí thuyết Schrödinger[sửa | sửa mã nguồn]
Trong ngôn ngữ của cơ học ma trận Heisenberg, các nguyên tử hydro đã được giải quyết đầu tiên bởi Wolfgang Pauli bằng cách sử dụng một đối xứng quay trong không gian bốn chiều [đối xứng O(4)] được tạo ra bởi mô men động lượng và vector Laplace-Runge-Lenz. Bằng cách mở rộng nhóm đối xứng O(4) đến nhóm động lực O(4,2), toàn bộ phổ và tất cả các pha chuyển được nhúng trong một đại diện nhóm bất khả giảm duy nhất.[12]
Vào năm 1979, nguyên tử hydro (bất tương đối) đã được giải quyết lần đầu tiên trong công thức tích phân của cơ học lượng tử của Richard Feynman.[12][12] Thành quả này mở rộng rất nhiều phạm vi áp dụng của phương pháp của Feynman.
Xem thêm[sửa | sửa mã nguồn]
|
|
|
Tham khảo[sửa | sửa mã nguồn]
- ^ Palmer, D. (ngày 13 tháng 9 năm 1997). “Hydrogen in the Universe”. NASA. Bản gốc lưu trữ ngày 29 tháng 10 năm 2014. Truy cập ngày 23 tháng 2 năm 2017.
- ^ rter/files/103more/BohrEquations.pdf “Derivation of Bohr's Equations for the One-electron Atom” Kiểm tra giá trị
|url=(trợ giúp) (PDF). University of Massachusetts Boston.[liên kết hỏng] - ^ P.J. Mohr, B.N. Taylor, and D.B. Newell (2011), "The 2010 CODATA Recommended Values of the Fundamental Physical Constants" (Web Version 6.0). This database was developed by J. Baker, M. Douma, and S. Kotochigova. Available: http://physics.nist.gov/constants. National Institute of Standards and Technology, Gaithersburg, MD 20899. Link to R∞, Link to hcR∞
- ^ Messiah, Albert (1999). Quantum Mechanics. New York: Dover. tr. 1136. ISBN 0-486-40924-4.
- ^ LaguerreL.
- ^ Griffiths, p. 152
- ^ Condon and Shortley (1963). The Theory of Atomic Spectra. London: Cambridge. tr. 441.
- ^ Griffiths, Ch. 4 p. 89
- ^ Bransden, B. H.; Joachain, C. J. (1983). Physics of Atoms and Molecules. Longman. tr. Appendix 5. ISBN 0-582-44401-2.
- ^ Sommerfeld, Arnold (1919). Atombau und Spektrallinien'. Braunschweig: Friedrich Vieweg und Sohn. ISBN 3-87144-484-7.
- ^ Summary of atomic quantum numbers Lưu trữ 2015-09-22 tại Wayback Machine.
- ^ a b c Lỗi chú thích: Thẻ
<ref>sai; không có nội dung trong thẻ ref có tênpauli_1926
Sách[sửa | sửa mã nguồn]
- David Jeffery Griffiths (2005). ("Introduction to Quantum Mechanics"), Nhà xuất bản Pearson Prentice Hall, Chương 4.2 đặc biệt nói về nguyên tử hydro, nhưng toàn bộ chương 4 đều có liên quan tới. Có sẵn tại Google Books.
- Kleinert, H. (2009). (Path Integrals in Quantum Mechanics, Statistics, Polymer Physics), bản thứ 4, Worldscibooks.com Lưu trữ 2009-04-24 tại Wayback Machine, Nhà xuất bản Khoa học Thế giới, Singapore (có sẵn trực tuyến tại physik.fu-berlin.de)
























![{\displaystyle -{\frac {\hbar ^{2}}{2\mu }}\left[{\frac {1}{r^{2}}}{\frac {\partial }{\partial r}}\left(r^{2}{\frac {\partial \psi }{\partial r}}\right)+{\frac {1}{r^{2}\sin \theta }}{\frac {\partial }{\partial \theta }}\left(\sin \theta {\frac {\partial \psi }{\partial \theta }}\right)+{\frac {1}{r^{2}\sin ^{2}\theta }}{\frac {\partial ^{2}\psi }{\partial \phi ^{2}}}\right]-{\frac {Ze^{2}}{4\pi \epsilon _{0}r}}\psi =E\psi }](https://wikimedia.org/api/rest_v1/media/math/render/svg/225e9aa3efcd87cf3a0d6353f87340ba6e338514)
















![{\displaystyle {\begin{array}{rl}E_{j\,n}&=-m_{\text{e}}c^{2}\left[1-\left(1+\left[{\dfrac {\alpha }{n-j-{\frac {1}{2}}+{\sqrt {\left(j+{\frac {1}{2}}\right)^{2}-\alpha ^{2}}}}}\right]^{2}\right)^{-1/2}\right]\\&\approx -{\dfrac {m_{\text{e}}c^{2}\alpha ^{2}}{2n^{2}}}\left[1+{\dfrac {\alpha ^{2}}{n^{2}}}\left({\dfrac {n}{j+{\frac {1}{2}}}}-{\dfrac {3}{4}}\right)\right],\end{array}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f37618d51f113219c6d6ba2cc621cb68b6d528fc)





