Dichlor heptoxide
(Đổi hướng từ Điclo heptôxit)
| Dichlor heptoxide | |
|---|---|
 | |
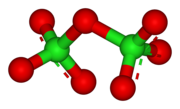 | |
| Danh pháp IUPAC | Dichlorine heptoxide |
| Tên khác | Chlorine(VII) oxide; Perchloric anhydride; (Perchloryloxy)chlorane trioxide |
| Nhận dạng | |
| Số CAS | |
| PubChem | |
| ChEBI | |
| Ảnh Jmol-3D | ảnh |
| SMILES | đầy đủ
|
| InChI | đầy đủ
|
| ChemSpider | |
| Thuộc tính | |
| Công thức phân tử | Cl2O7 |
| Khối lượng mol | 182,9012 g/mol |
| Bề ngoài | tinh thể không màu |
| Khối lượng riêng | 1,9 g/cm³ |
| Điểm nóng chảy | −91,5 °C (181,7 K; −132,7 °F) |
| Điểm sôi | 82 °C (355 K; 180 °F) |
| Độ hòa tan trong nước | tan kèm phản ứng |
| Các nguy hiểm | |
| Nguy hiểm chính | nguồn oxy hóa, dễ nổ[1] |
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |
Dichlor heptoxide là oxide có công thức hóa học Cl2O7, tác dụng với nước tạo thành acid perchloric. Dichlor heptoxide ở nhiệt độ thường là một chất lỏng.
Tính chất[sửa | sửa mã nguồn]
Dichlor heptoxide là Oxide acid, hydroxide của nó là acid perchloric. Dung dịch không màu này là một acid rất mạnh so với acid sunfuric và acid nitric, và cũng là một chất oxy hóa mạnh. Tính chất của Oxide acid đều thể hiện rõ nét ở Cl2O7 (tác dụng nhanh, mạnh và tỏa nhiều nhiệt khi tác dụng với oxide base, base, muối của các acid khác). Ví dụ:
Điều chế[sửa | sửa mã nguồn]
Dichlor heptoxide được điều chế bằng cách khử nước trong acid perchloric:
- 2HClO4 + P4O10 → Cl2O7 + H2P4O11
Ngoài ra, dichlor heptoxide còn được điều chế bằng cách nhiệt phân acid perchloric:
- 2HClO4 → Cl2O7 + H2O
Tham khảo[sửa | sửa mã nguồn]
- ^ Holleman, Arnold F.; Wiberg, Egon (2001). Inorganic chemistry. Translated by Mary Eagleson, William Brewer. San Diego: Academic Press. tr. 464. ISBN 0-12-352651-5.
