Bệnh thận đái tháo đường
| Bệnh thận tiểu đường | |
|---|---|
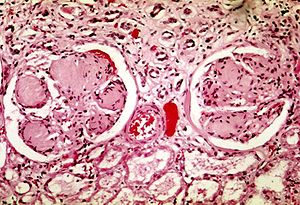 | |
| Hai cầu thận trong tình trạng bệnh thận đái tháo đường: các khu vực màu tím sáng trong các mao mạch là các cặn lắng bao bọc phần ngoài, chúng phá hủy trung mô. | |
| Khoa/Ngành | Nephrology, nội tiết học |
| Yếu tố nguy cơ | Huyết áp cao, Đường huyết không ổn định |
| Phương pháp chẩn đoán | Nồng độ albumin trong nước tiểu bất thường[1] |
| Điều trị | Chất gây ức chế ACE (ACE nghĩa là Enzym chuyển angiotensin)[2] |
Bệnh thận đái tháo đường (DN) hay bệnh thận tiểu đường,[3] là việc mất chức năng thận mãn tính xảy ra ở những người bị tiểu đường. Mất protein trong nước tiểu do tổn thương cầu thận có thể trở nên lớn và gây ra albumin huyết thanh thấp dẫn đến sưng toàn thân (phù) và dẫn đến hội chứng thận hư. Tương tự, mức lọc cầu thận ước tính (eGFR) có thể giảm dần từ mức bình thường trên 90 ml / phút / 1,73m 2 xuống dưới 15, tại thời điểm đó, bệnh nhân được cho là mắc bệnh thận giai đoạn cuối (ESKD).[4] Nó thường chậm tiến triển qua nhiều năm.[5]
Bất thường sinh lý bệnh ở bệnh thận tiểu đường bắt đầu với mức đường huyết được kiểm soát kém trong thời gian dài. Tiếp theo là nhiều thay đổi trong các đơn vị lọc của thận, nephron. (Bình thường có khoảng 750.000-1,5 triệu nephron trong mỗi quả thận trưởng thành).[6] Ban đầu, có sự co thắt của các tiểu động mạch và sự giãn nở của các tiểu động mạch hướng tâm, dẫn đến tăng huyết áp mao mạch cầu thận và tăng huyết áp; điều này dần dần thay đổi để giảm âm theo thời gian.[7] Đồng thời, có những thay đổi trong chính cầu thận: bao gồm sự dày lên của màng đáy, mở rộng màng khe của các tế bào nang, tăng số lượng tế bào trung mô và tăng ma trận trung mô. Ma trận này xâm lấn các mao mạch cầu thận và tạo ra các cặn gọi là nốt Kimmelstiel-Wilson. Các tế bào trung mô và ma trận có thể dần dần mở rộng và tiêu thụ toàn bộ cầu thận, tắt quá trình lọc.[8]
Tình trạng của bệnh thận tiểu đường có thể được theo dõi bằng cách đo hai giá trị: lượng protein trong nước tiểu - protein niệu; và xét nghiệm máu gọi là creatinine huyết thanh. Lượng protein niệu phản ánh mức độ thiệt hại đối với bất kỳ cầu thận nào vẫn còn hoạt động. Giá trị của creatinine huyết thanh có thể được sử dụng để tính toán mức lọc cầu thận ước tính (eGFR), phản ánh tỷ lệ phần trăm của cầu thận không còn lọc máu. Điều trị bằng thuốc ức chế men chuyển angiotensin (ACEI) hoặc thuốc ức chế thụ thể angiotensin (ARB), làm giãn động mạch ra khỏi cầu thận, do đó làm giảm huyết áp trong mao mạch cầu thận, có thể làm chậm (nhưng không dừng) bệnh tật. Ba nhóm thuốc trị tiểu đường - thuốc chủ vận GLP-1, thuốc ức chế DPP-4 và thuốc ức chế SGLT2 - cũng được cho là làm chậm quá trình tiến triển của bệnh thận tiểu đường.[9]
Bệnh thận đái tháo đường là nguyên nhân phổ biến nhất của ESKD và là một biến chứng nghiêm trọng ảnh hưởng đến khoảng một phần tư số người trưởng thành mắc bệnh tiểu đường ở Hoa Kỳ.[10][11] Những người bị ảnh hưởng với bệnh thận giai đoạn cuối thường phải chạy thận nhân tạo và cuối cùng là ghép thận để thay thế chức năng thận thất bại.[12] Bệnh thận tiểu đường có liên quan đến việc tăng nguy cơ tử vong nói chung, đặc biệt là với nguyên nhân bệnh tim mạch.[10][13]
Tham khảo[sửa | sửa mã nguồn]
- ^ Lewis G, Maxwell AP (tháng 2 năm 2014). “Risk factor control is key in diabetic nephropathy”. The Practitioner. 258 (1768): 13–7, 2. PMID 24689163.
- ^ Lim AK (2014). “Diabetic nephropathy – complications and treatment”. International Journal of Nephrology and Renovascular Disease. 7: 361–81. doi:10.2147/IJNRD.S40172. PMC 4206379. PMID 25342915.
- ^ Kittell F (2012). “Diabetes Management”. Trong Thomas LK, Othersen JB (biên tập). Nutrition Therapy for Chronic Kidney Disease. CRC Press. tr. 198.
- ^ Longo D, Fauci A, Kasper D, Hauser S, Jameson J, Loscalzo J (2013). Harrison's manual of medicine (ấn bản 18). New York: McGraw-Hill Medical. tr. 2982. ISBN 978-0-07-174519-2.
- ^ Afkarian M, Zelnick LR, Hall YN, Heagerty PJ, Tuttle K, Weiss NS, de Boer IH (tháng 8 năm 2016). “Clinical Manifestations of Kidney Disease Among US Adults With Diabetes, 1988–2014”. JAMA. 316 (6): 602–10. doi:10.1001/jama.2016.10924. PMC 5444809. PMID 27532915.
- ^ Hall J, Guyton A (2005). Textbook of Medical Physiology (ấn bản 11). Philadelphia: W.B. Saunders. tr. 310. ISBN 978-0-7216-0240-0.
- ^ “diabetic nephropathy”. Truy cập ngày 27 tháng 6 năm 2015.
- ^ Schlöndorff D, Banas B (tháng 6 năm 2009). “The mesangial cell revisited: no cell is an island”. Journal of the American Society of Nephrology. 20 (6): 1179–87. doi:10.1681/ASN.2008050549. PMID 19470685.
- ^ de Boer IH (tháng 8 năm 2017). “A New Chapter for Diabetic Kidney Disease”. The New England Journal of Medicine. 377 (9): 885–887. doi:10.1056/nejme1708949. PMID 28854097.
- ^ a b Mora-Fernández C, Domínguez-Pimentel V, de Fuentes MM, Górriz JL, Martínez-Castelao A, Navarro-González JF (tháng 9 năm 2014). “Diabetic kidney disease: from physiology to therapeutics”. The Journal of Physiology. 592 (18): 3997–4012. doi:10.1113/jphysiol.2014.272328. PMC 4198010. PMID 24907306.
- ^ Ding Y, Choi ME (tháng 1 năm 2015). “Autophagy in diabetic nephropathy”. The Journal of Endocrinology. 224 (1): R15–30. doi:10.1530/JOE-14-0437. PMC 4238413. PMID 25349246.
- ^ Lizicarova D, Krahulec B, Hirnerova E, Gaspar L, Celecova Z (2014). “Risk factors in diabetic nephropathy progression at present”. Bratislavske Lekarske Listy. 115 (8): 517–21. doi:10.4149/BLL_2014_101. PMID 25246291.
- ^ Pálsson R, Patel UD (tháng 5 năm 2014). “Cardiovascular complications of diabetic kidney disease”. Advances in Chronic Kidney Disease. 21 (3): 273–80. doi:10.1053/j.ackd.2014.03.003. PMC 4045477. PMID 24780455.
