Chromi(II) chloride
| Chromi(II) chloride | |
|---|---|
 Cấu trúc 3D của Chromi(II) chloride | |
 Mẫu Chromi(II) chloride | |
| Danh pháp IUPAC | Chromium(II) chloride |
| Tên khác | Chromiơ chloride Chromi đichloride |
| Nhận dạng | |
| Số CAS | |
| PubChem | |
| Số RTECS | GB5250000 |
| Ảnh Jmol-3D | ảnh |
| SMILES | đầy đủ
|
| InChI | đầy đủ
|
| ChemSpider | |
| UNII | |
| Thuộc tính | |
| Công thức phân tử | CrCl2 |
| Khối lượng mol | 122,9034 g/mol (khan) 158,93396 g/mol (2 nước) 194,96452 g/mol (4 nước) 230,99508 g/mol (6 nước) |
| Bề ngoài | bột trắng hoặc xám lục (khan), hút ẩm mạnh |
| Mùi | không mùi |
| Khối lượng riêng | 2,88 g/cm³ (24 °C)[1] |
| Điểm nóng chảy | 824 °C (1.097 K; 1.515 °F) (khan) 51 °C (124 °F; 324 K) (4 nước, phân hủy)[1] |
| Điểm sôi | 1.302 °C (1.575 K; 2.376 °F) (khan)[1] |
| Độ hòa tan trong nước | tan[1] |
| Độ hòa tan | không tan trong etanol, ete |
| Độ axit (pKa) | 2 |
| MagSus | +7230·10-6 cm³/mol |
| Cấu trúc | |
| Cấu trúc tinh thể | Trực thoi (giống rutil, khan), oP6[2] Đơn nghiêng (4 nước)[3] |
| Nhóm không gian | Pnnm, No. 58 (khan)[2] P21/c, No. 14 (4 nước)[3] |
| Hằng số mạng | a = 6,64 Å, b = 5,98 Å, c = 3,48 Å (khan)[2] |
| Tọa độ | Bát diện (Cr2+, khan)[2] |
| Nhiệt hóa học | |
| Enthalpy hình thành ΔfH | -395,4 kJ/mol[1] |
| Entropy mol tiêu chuẩn S | 115,3 J/mol·K[1] |
| Nhiệt dung | 71,2 J/mol·K[1] |
| Các nguy hiểm | |
| NFPA 704 |
|
| LD50 | 1870 mg/kg (rats, oral)[4] |
| Ký hiệu GHS |  [5] [5] |
| Báo hiệu GHS | Cảnh báo |
| Chỉ dẫn nguy hiểm GHS | H302, H315, H319, H335[5] |
| Chỉ dẫn phòng ngừa GHS | P261, P305+P351+P338[5] |
| Các hợp chất liên quan | |
| Anion khác | Chromi(II) fluoride Chromi(II) bromide Chromi(II) iodide |
| Cation khác | Chromi(III) chloride Chromi(IV) chloride Molybden(II) chloride Vonfam(II) chloride |
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |
Chromi(II) chloride mô tả các hợp chất vô cơ có công thức hóa học CrCl2(H2O)n. Chất rắn khan có màu trắng khi tinh khiết, tuy nhiên các mẫu thương mại thường có màu xám hoặc lục; nó hút ẩm và dễ dàng hòa tan trong nước để tạo ra các dung dịch nhạy cảm với không khí màu chàm của tetrahydrat Cr(H2O)4Cl2. Chromi(II) chloride không có công dụng thương mại nhưng được sử dụng ở quy mô phòng thí nghiệm để tổng hợp các phức chất Chromi khác.
Tổng hợp[sửa | sửa mã nguồn]
CrCl2 được tạo ra bằng cách khử Chromi(III) chloride bằng hydro ở mức 500 ℃:
- 2CrCl3 + H2 → 2CrCl2 + 2HCl
hoặc bằng điện phân.[6]
Các chế phẩm quy mô nhỏ có thể sử dụng LiAlH4, kẽm hoặc các thuốc thử liên quan, để khử CrCl3.
- 4CrCl3 + LiAlH4 → 4CrCl2 + LiCl + AlCl3 + 2H2
- 2CrCl3 + Zn → 2CrCl2 + ZnCl2
CrCl2 cũng có thể được điều chế bằng cách xử lý dung dịch Chromi(II) axetat bằng hydro chloride.[7]
- Cr(OAc)2 + 2HCl → CrCl2 + 2AcOH
Cấu trúc và tính chất[sửa | sửa mã nguồn]
CrCl2 khan có màu trắng,[7] tuy nhiên các mẫu thương mại thường có màu xám hoặc lục. Nó kết tinh trong nhóm không gian Pnnm, là một biến thể bị biến dạng trực giao của cấu trúc rutil; làm cho nó đẳng cấu với calci chloride. Các trung tâm Cr là bát diện, bị bóp méo bởi hiệu ứng Jahn-Teller.[8]
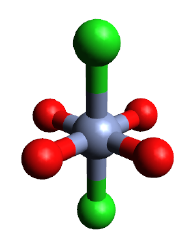
Dẫn xuất hydrat hóa, CrCl2(H2O)4, tạo thành các tinh thể đơn hình với nhóm không gian P21/c. Hình dạng phân tử xấp xỉ bát diện gồm bốn liên kết Cr–O ngắn (2,078 Å) được sắp xếp theo cấu hình phẳng vuông và hai liên kết Cr–Cl dài hơn (2,758 Å) trong cấu hình trans.[3]
Phản ứng[sửa | sửa mã nguồn]
Khả năng khử của Cr3+ + e- ⇄ Cr2+ là -0,41. Vì thế khử của H+ thành H2 trong điều kiện axit là 0, ion Chromi(II) có thể khử axit thành hydro, mặc dù phản ứng này không xảy ra nếu không có chất xúc tác.
Hóa hữu cơ[sửa | sửa mã nguồn]
Chromi(II) chloride được sử dụng làm tiền thân cho các phức Chromi vô cơ và chất hữu cơ khác. Các halide và nitroaromatics bị khử bởi CrCl2. Độ âm điện vừa phải của Chromi và phạm vi các chất mà CrCl2 có thể chứa làm cho thuốc thử organochromium rất linh hoạt về mặt tổng hợp.[9] Nó là một thuốc thử trong phản ứng Nozaki-Hiyama-Kishi, một phương pháp hữu ích để chuẩn bị các vòng có kích thước trung bình.[10] Nó cũng được sử dụng trong quá trình olefination Takai để tạo thành vinyl iodide từ aldehyd với sự hiện diện của iodoform.[11]
Hợp chất khác[sửa | sửa mã nguồn]
- CrCl2 còn tạo một số hợp chất với NH3, như:
- CrCl2 còn tạo một số hợp chất với N2H4, như CrCl2·2N2H4 là chất rắn màu oải hương, tan ít trong nước, có tính nổ.[13]
- Khi kết hợp CrCl2·2N2H4 với NH3 thì thu được dung dịch màu xanh dương hơi đậm.[15]
- CrCl2 còn tạo một số hợp chất với CO(NH2)2, như CrCl2·2CO(NH2)2 là chất rắn màu dương nhạt hay CrCl2·4CO(NH2)2 là chất rắn màu dương.[16]
- CrCl2 còn tạo một số hợp chất với CS(NH2)2, như CrCl2·2CS(NH2)2 là chất rắn màu vàng sáng.[16]
Tham khảo[sửa | sửa mã nguồn]
- ^ a b c d e f g Lide, David R. biên tập (2009). CRC Handbook of Chemistry and Physics . Boca Raton, Florida: CRC Press. ISBN 978-1-4200-9084-0.
- ^ a b c d Tracy, Joseph W.; Gregory, N.W.; Lingafelter, E.C.; Dunitz, J.D.; Mez, H.-C.; Rundle, R.E.; Scheringer, Christian; Yakel, H.L.; Wilkinson, M.K. (1961). “The crystal structure of chromium(II) chloride”. Acta Crystallographica. 4 (9): 927–929. doi:10.1107/S0365110X61002710.
- ^ a b c Schnering, H.G. von; Brand, B.-H. (1973). “Struktur und Eigenschaften des blauen Chrom(II)-chlorid-tetrahydrats CrCl2.4H2O”. Zeitschrift fuer Anorganische und Allgemeine Chemie. 402 (2): 159–168. doi:10.1002/zaac.19734020206.
- ^ Lỗi chú thích: Thẻ
<ref>sai; không có nội dung trong thẻ ref có tênfca - ^ a b c Bản dữ liệu Chromi(II) chloride của Sigma-Aldrich, truy cập lúc {{{Datum}}} (PDF).
- ^ Holah, D. G.; Fackler, Jr. John P. (1967). “Anhydrous Chromium(II) Chloride”. Inorg. Synth. 10: 26-35. doi:10.1002/9780470132418.ch4. Chú thích có tham số trống không rõ:
|1=(trợ giúp) - ^ a b Riley, edited by Georg Brauer; translated by Scripta Technica, Inc. Translation editor Reed F. (1963). Handbook of preparative inorganic chemistry. Volume 1 (ấn bản 2). New York, N.Y.: Academic Press. tr. 1337. ISBN 978-0121266011.Quản lý CS1: văn bản dư: danh sách tác giả (liên kết)
- ^ Greenwood, Norman N.; Earnshaw, A. (1997), Chemistry of the Elements (ấn bản 2), Oxford: Butterworth-Heinemann, ISBN 0-7506-3365-4
- ^ (a) Kazuhiko Takai, K.; Loh, T.-P. "Chromium(II) Chloride" in Encyclopedia of Reagents for Organic Synthesis John Wiley & Sons: New York; 2005. doi:10.1002/047084289X.rc166. (b) Alois Fürstner, "Carbon−Carbon Bond Formations Involving Organochromium(III) Reagents" Chemical Reviews, 1999, 99 (4), 991–1046 doi:10.1021/cr9703360
- ^ (a) MacMillan, D. W. C.; Overman, Larry E. "Enantioselective Total Synthesis of (−)-7-Deacetoxyalcyonin Acetate. First Synthesis of a Eunicellin Diterpene" J. Am. Chem. Soc. 1995, 117 (41), 10391–10392. doi:10.1021/ja00146a028. (b) Lotesta, S. D.; Liu, J.; Yates, E. V.; Krieger, I.; Sacchettini, J. C.; Freundlich, J. S.; Sorensen, E. J. "Expanding the pleuromutilin class of antibiotics by de novo chemical synthesis" Chem. Sci. 2011, 2, 1258-1261. doi:10.1039/C1SC00116G.
- ^ Simple and selective method for aldehydes (RCHO) -> (E)-haloalkenes (RCH:CHX) conversion by means of a haloform-chromous chloride system K. Takai, K. Nitta, K. Utimoto J. Am. Chem. Soc.; 1986; 108(23); 7408-7410. doi:10.1021/ja00283a046.
- ^ a b (uk) d-елементи VIB групи. Підгрупа Хрому. Експериментальна частина.[liên kết hỏng]
- ^ a b Chromium (mellor actitc 11 60 cr), trang 368 – [1]. Truy cập 10 tháng 3 năm 2020.
- ^ a b Dictionary of Inorganic Compounds, trang 3072, 3074 – [2], Truy cập 8 tháng 3 năm 2020.
- ^ A Text-book Of Inorganic Chemistry Vol-x, trang 74 – [3]. Truy cập 11 tháng 3 năm 2020.
- ^ a b COMPLEXES OF CHROMIUM(II) HALIDES WITH WEAK DONOR LIGANDS. Truy cập 17 tháng 5 năm 2020.

