Electron độc thân
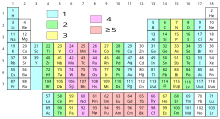

Electron độc thân (tiếng Anh: unpaired electron) là electron đứng một mình trong orbital nguyên tử, mà không hình thành cặp electron. Vì electron dạng cặp ổn định hơn, nên electron độc thân tương đối hiếm thấy trong hoá học, và nguyên tử có sẵn các electron độc thân thì dễ tham gia phản ứng. Trong hoá học hữu cơ, electron độc thân thường có ở các gốc tự do, từ đó có thể giải thích nhiều phản ứng hoá học.
Gốc tự do có electron độc thân thường có ở orbital nguyên tử d và f, vì hai loại orbital nguyên tử này ít định hướng, do đó electron độc thân không thể hình thành hiệu quả phân tử dime ổn định.[1]
Electron độc thân cũng hiện diện trong một số phân tử ổn định. Phân tử ôxi có hai electron độc thân, và nitơ oxide (NO) thì có một hạt. Hướng spin của electron độc thân trong phân tử ôxi cố định, do đó nguyên tố ôxi biểu hiện tính thuận từ.
Electron độc thân trong các nguyên tố họ lanthan là electron ổn định nhất, orbital f của chúng phản ứng kém với tác nhân bên ngoài, và electron độc thân khó hình thành liên kết hoá học. Nguyên tử có nhiều electron độc thân nhất là Gd3+, có 7 electron độc thân.
Tham khảo[sửa | sửa mã nguồn]
- ^ N. C. Norman (1997). Periodicity and the s- and p-Block Elements. Oxford University Press. tr. 43. ISBN 0-19-855961-5.
