Lao siêu kháng thuốc
| Lao siêu kháng thuốc (XDR-TB) | |
|---|---|
 | |
| Mô tả về lao siêu kháng thuốc | |
| Khoa/Ngành | Bệnh truyền nhiễm |
| Triệu chứng | Giống nhiễm lao nhạy cảm |
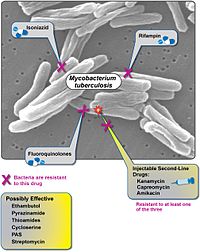
| Nguyên nhân | Mycobacterium tuberculosis |
| Yếu tố nguy cơ | Điều trị sai, không tuân thủ điều trị lao |
Lao siêu kháng thuốc (XDR-TB) là tình trạng bệnh nhân mắc bệnh lao mà vi khuẩn lao có mặt trong cơ thể là chủng kháng một số loại thuốc chống lao hiệu quả nhất. Các chủng lao siêu kháng thuốc dễ dàng xuất hiện khi quản lý và điều trị sai những bệnh nhân mắc lao đa kháng thuốc (MDR-TB).
Gần như cứ 4 người trên thế giới thì có 1 người bị nhiễm vi khuẩn lao (23.0% [từ 20.4% đến 26.4%]).[1] Chỉ khi vi khuẩn hoạt động thì mới tính là bị bệnh lao. Vi khuẩn trở nên hoạt động do bất cứ nguyên nhân gây suy giảm khả năng miễn dịch của người đó, chẳng hạn như HIV, tuổi cao hoặc một số tình trạng bệnh lý. Bệnh lao thường có thể được điều trị bằng một liệu trình gồm bốn loại thuốc chống lao hàng đầu (tức là isoniazid (H), rifampin (R), pyrazinamide (Z), ethambutol (E)) và fluoroquinolone. Nếu các loại thuốc này bị lạm dụng hoặc điều trị sai, bệnh lao đa kháng thuốc (MDR-TB) có thể phát triển. Cần nhiều thời gian hơn để điều trị MDR-TB bằng các loại thuốc hàng hai (tức là amikacin, kanamycin hoặc capreomycin ), đắt hơn và có nhiều tác dụng phụ hơn. XDR-TB xuất hiện khi các loại thuốc hàng hai này cũng bị lạm dụng hoặc quản lý sai. Tổ chức Y tế Thế giới (WHO) định nghĩa XDR-TB là MDR-TB kháng với ít nhất một loại fluoroquinolone và thuốc tiêm hàng hai (amikacin, capreomycin hoặc kanamycin).[2]
Dịch tễ học của XDR-TB vẫn chưa được xác định rõ vì nhiều quốc gia thiếu thiết bị và năng lực cần thiết để chẩn đoán chính xác. Đến tháng 6 năm 2008, 49 quốc gia đã xác nhận các trường hợp XDR-TB.[3] Vào cuối năm 2017, 127 quốc gia thành viên của WHO đã báo cáo tổng cộng 10 800 trường hợp mắc lao kháng kháng thuốc và 8,5% trường hợp mắc MDR-TB trong năm 2017 được ước tính là nhiễm XDR-TB.[4]
Vào tháng 8 năm 2019, Cục Quản lý Thực phẩm và Dược phẩm (FDA) đã phê duyệt việc sử dụng Pretomanid kết hợp với bedaquiline và linezolid để điều trị cho một số lượng hạn chế và cụ thể bệnh nhân trưởng thành mắc bệnh lao phổi siêu kháng thuốc, không dung nạp điều trị hoặc không đáp ứng với nhiều loại thuốc.[5]
Triệu chứng cơ năng và triệu chứng thực thể[sửa | sửa mã nguồn]
Các triệu chứng của XDR-TB không khác với lao thông thường hoặc lao nhạy cảm với thuốc: ho có đờm (hoặc khạc đờm) đặc, đục, đôi khi lẫn máu trong thời gian hơn hai tuần; sốt về chiều, ớn lạnh và đổ mồ hôi ban đêm; mệt mỏi và yếu cơ; giảm cân; và trong một số trường hợp khó thở và đau ngực. Một người có những triệu chứng này không nhất thiết là bị mắc XDR-TB, nhưng họ nên gặp bác sĩ để được chẩn đoán và lên kế hoạch điều trị. Bệnh nhân lao mà các triệu chứng không cải thiện sau một vài tuần điều trị bệnh lao nên thông báo cho bác sĩ lâm sàng.[6]
Quá trình lây truyền[sửa | sửa mã nguồn]
Giống như các chủng lao khác, XDR-TB lây lan qua không khí. Khi một người mắc bệnh lao truyền nhiễm ho, hắt hơi, nói chuyện hoặc khạc nhổ, họ sẽ giải phóng trực khuẩn lao vào không khí. XDR-TB không thể lây lan khi hôn, ăn chung thức ăn hoặc đồ uống hoặc bắt tay với ai đó. Vi khuẩn có khả năng tồn tại trong không khí trong vài giờ.[7]
Chẩn đoán[sửa | sửa mã nguồn]
Chẩn đoán thành công XDR-TB phụ thuộc vào khả năng tiếp cận của bệnh nhân với các dịch vụ chăm sóc sức khỏe có chất lượng. Nếu tìm thấy vi khuẩn lao trong đờm, việc chẩn đoán mắc bệnh lao có thể được thực hiện trong 1 đến 2 ngày, nhưng chẩn đoán không thể phân biệt giữa lao nhạy cảm với thuốc và lao kháng thuốc. Để đánh giá tính nhạy cảm với thuốc, vi khuẩn cần được nuôi cấy và thử nghiệm trong phòng thí nghiệm phù hợp. Chẩn đoán xác định mắc XDR-TB có thể mất từ 6 đến 16 tuần.[8]
Phương pháp ban đầu được sử dụng để xét nghiệm chẩn đoán MDR-TB và XDR-TB là thử nghiệm nhạy cảm với thuốc (DST). DST có khả năng xác định bốn loại thuốc chống lao chính là Isoniazid (H), Rifampin (R), Ethambutol (E) và Pyrazinamide (Z).[9] Thử nghiệm Nhạy cảm với Thuốc được thực hiện bằng cách phết vi khuẩn lên đĩa chứa môi trường Lowenstein-Jensen để nuôi cấy.[10]
Chẩn đoán MDR và XDR-TB ở trẻ em vẫn còn là thách thức. Với số lượng các trường hợp được báo cáo mắc chủng siêu kháng thuốc ngày càng tăng trên toàn thế giới, cần có các công cụ chẩn đoán lao tốt hơn dành cho bệnh nhân nhi.[11]
Điều trị[sửa | sửa mã nguồn]
Nguyên tắc điều trị MDR-TB và XDR-TB là giống hệt nhau. Các loại thuốc hàng hai gây độc cho cơ thể và có thể gây ra một loạt tác dụng phụ nghiêm trọng bao gồm viêm gan, trầm cảm, ảo giác và điếc.[12] Bệnh nhân thường phải nhập viện trong thời gian dài và bị cách ly. Ngoài ra, thuốc hàng hai cực kỳ đắt so với chi phí thuốc điều trị lao hàng đầu.
XDR-TB có mối liên quan đến tỷ lệ tử vong cao hơn nhiều so với MDR-TB, do có ít lựa chọn điều trị hiệu quả.[13] Một nghiên cứu năm 2008 ở vùng Tomsk của Nga, đã báo cáo rằng 14 trong số 29 (48,3%) bệnh nhân mắc lao siêu kháng thuốc đã hoàn thành điều trị.[14] Năm 2018, WHO đã báo cáo rằng tỷ lệ điều trị thành công đối với XDR-TB là 34% (nghiên cứu thuần tập năm 2015), so với 55% đối với MDR/RR-TB (nghiên cứu thuần tập năm 2015), 77% đối với bệnh lao liên quan đến HIV (nghiên cứu thuần tập năm 2016), và 82% đối với bệnh lao nhạy cảm thuốc (nghiên cứu thuần tập năm 2016).[15]
Một phân tích tổng quan năm 2018 trên 12.030 bệnh nhân từ 25 quốc gia trong 50 nghiên cứu đã chứng minh rằng thành công điều trị tăng lên và tỷ lệ tử vong giảm khi điều trị phối hợp bedaquiline, fluoroquinolone thế hệ sau và linezolid.[16][17] Một phác đồ điều trị XDR-TB được gọi là Nix-TB: kết hợp pretomanid, bedaquiline và linezolid,[18] đã cho kết quả đầy hứa hẹn trong các thử nghiệm lâm sàng ban đầu.[19]
Dịch tễ học[sửa | sửa mã nguồn]
Các nghiên cứu đã phát hiện ra rằng nam giới có nguy cơ mắc XDR-TB cao hơn nữ giới.[20] Một nghiên cứu cho thấy nam mắc gấp nữ 3 lần, có ý nghĩa thống kê (p<0,05)[21] Các nghiên cứu về ảnh hưởng của tuổi tác với XDR-TB đã nhận thấy rằng những người từ 65 tuổi trở lên ít có khả năng mắc XDR-TB hơn.[22] Một nghiên cứu ở Nhật Bản cho thấy bệnh nhân mắc XDR-TB thường gặp ở người trẻ.[23]
XDR-TB và HIV/AIDS[sửa | sửa mã nguồn]
Lao là một trong những bệnh nhiễm trùng phổ biến nhất ở những người mắc HIV/AIDS.[24]
Xem thêm[sửa | sửa mã nguồn]
- Lao đa kháng thuốc (MDR-TB)
- Lao kháng thuốc hoàn toàn (TDR-TB)
- Bệnh lao
- Điều trị bệnh lao
Tham khảo[sửa | sửa mã nguồn]
- ^ Houben, Rein M. G. J.; Dodd, Peter J. (25 tháng 10 năm 2016). Metcalfe, John Z. (biên tập). “The Global Burden of Latent Tuberculosis Infection: A Re-estimation Using Mathematical Modelling”. PLOS Medicine. 13 (10): e1002152. doi:10.1371/journal.pmed.1002152. ISSN 1549-1676. PMC 5079585. PMID 27780211.
- ^ “Global tuberculosis report”. World Health Organization (WHO). 28 tháng 2 năm 2019. Truy cập ngày 18 tháng 8 năm 2019.
- ^ World Health Organization (2008). "Countries with XDR-TB confirmed cases as of June 2008"
- ^ “Global tuberculosis report”. World Health Organization (WHO). 28 tháng 2 năm 2019. Truy cập ngày 18 tháng 8 năm 2019.
- ^ “FDA approves new drug for treatment-resistant forms of tuberculosis that affects the lungs” (Thông cáo báo chí). Food and Drug Administration (FDA). 14 tháng 8 năm 2019. Truy cập ngày 18 tháng 8 năm 2019.
- ^ World Health Organization (2006). "Frequently asked questions – XDR-TB" “Bản sao đã lưu trữ”. Lưu trữ bản gốc ngày 6 tháng 10 năm 2008. Truy cập ngày 16 tháng 12 năm 2022.Quản lý CS1: bot: trạng thái URL ban đầu không rõ (liên kết)
- ^ “Extensively Drug-Resistant Tuberculosis (XDR TB)”. Centers for Disease Control and Prevention (CDC). 4 tháng 5 năm 2016. Truy cập ngày 30 tháng 1 năm 2017.
- ^ World Health Organization (2006). "Frequently asked questions – XDR-TB" “Bản sao đã lưu trữ”. Lưu trữ bản gốc ngày 6 tháng 10 năm 2008. Truy cập ngày 16 tháng 12 năm 2022.Quản lý CS1: bot: trạng thái URL ban đầu không rõ (liên kết)
- ^ Richter, Elvira; Rüsch-Gerdes, Sabine; Hillemann, Doris (2009). “Drug-susceptibility testing in TB: Current status and future prospects”. Expert Review of Respiratory Medicine. 3 (5): 497–510. doi:10.1586/ers.09.45. PMID 20477339.
- ^ "Missouri Department of Health & Senior Services." Drug Susceptibility Testing (DST). N.p., n.d. Jan. 2014.<http://health.mo.gov/lab/dst.php>
- ^ Salazar-Austin N, Ordonez AA, Hsu AJ, và đồng nghiệp (2015). “Extensively drug-resistant tuberculosis in a young child after travel to India”. The Lancet Infectious Diseases. 15 (12): 1485–1491. doi:10.1016/S1473-3099(15)00356-4. PMC 4843989. PMID 26607130.
- ^ Jason Beaubien (4 tháng 6 năm 2013). “Moldova Grapples With Whether To Isolate TB Patients”. Special Series: Tuberculosis Returns With A Deadly Twist. NPR. Truy cập ngày 29 tháng 1 năm 2015.
- ^ Center for Disease Control (2006). “Emergence of Mycobacterium tuberculosis with extensive resistance to second-line drug—Worldwide, 2000–2004”. MMWR Weekly. 55 (11): 301–305.
- ^ Keshavjee, S; Gelmanova, I; Farmer, P; Mishustin, S; Strelis, A; Andreev, Y; Pasechnikov, A; Atwood, S; và đồng nghiệp (2008). “Treatment of extensively drug-resistant tuberculosis in Tomsk, Russia: a retrospective cohort study”. The Lancet. 372 (9647): 1403–9. doi:10.1016/S0140-6736(08)61204-0. PMID 18723218.
- ^ “Global tuberculosis report”. World Health Organization (WHO). 28 tháng 2 năm 2019. Truy cập ngày 18 tháng 8 năm 2019.
- ^ Lange, Christoph; Chesov, Dumitru; Furin, Jennifer; Udwadia, Zarir; Dheda, Keertan (2018). “Revising the definition of extensively drug-resistant tuberculosis”. The Lancet Respiratory Medicine. 6 (12): 893–895. doi:10.1016/s2213-2600(18)30428-4. ISSN 2213-2600. PMID 30420247.
- ^ Collaborative Group for the Meta-Analysis of Individual Patient Data in MDR-TB treatment–2017; Ahmad, Nafees; Ahuja, Shama D (8 tháng 9 năm 2018). “Treatment correlates of successful outcomes in pulmonary multidrug-resistant tuberculosis: an individual patient data meta-analysis”. Lancet. 392 (10150): 821–834. doi:10.1016/S0140-6736(18)31644-1. ISSN 1474-547X. PMC 6463280. PMID 30215381.
- ^ “Nix-TB”. TB Alliance. 19 tháng 7 năm 2015.
- ^ Cohen, Jon (2017). “Simpler, safer treatment hailed as 'breakthrough' against drug-resistant TB”. Science. doi:10.1126/science.aal0769.
- ^ Flor de Lima, Bárbara; Tavares, Margarida (22 tháng 7 năm 2013). “Risk factors for extensively drug-resistant tuberculosis: a review”. The Clinical Respiratory Journal. 8 (1): 11–23. doi:10.1111/crj.12044. ISSN 1752-6981. PMID 23875862.
- ^ Velayati, Ali Akbar; Masjedi, Mohammad Reza; Farnia, Parissa; Tabarsi, Payam; Ghanavi, Jalladein; Ziazarifi, Abol Hassan; Hoffner, Sven Eric (2009). “Emergence of New Forms of Totally Drug-Resistant Tuberculosis Bacilli”. Chest. 136 (2): 420–425. doi:10.1378/chest.08-2427. PMID 19349380.
- ^ Shah, N. Sarita; Pratt, R.; Armstrong, L.; Robison, V.; Castro, K. G.; Cegielski, J. P. (2008). “Extensively Drug-Resistant Tuberculosis in the United States, 1993-2007”. JAMA. 300 (18): 2153–2160. doi:10.1001/jama.300.18.2153. PMID 19001626.
- ^ Murase, Yoshiro; Maeda, Shinji; Yamada, Hiroyuki; Ohkado, Akihiro; Chikamatsu, Kinuyo; Mizuno, Kazue; Kato, Seiya; Mitarai, Satoshi (2010). “Clonal Expansion of Multidrug-Resistant and Extensively Drug-Resistant Tuberculosis, Japan”. Emerging Infectious Diseases. 16 (6): 948–954. doi:10.3201/eid1606.091844. PMC 3086214. PMID 20507745.
- ^ Alexander, Paul E; De, Prithwish (30 tháng 1 năm 2017). “The emergence of extensively drug-resistant tuberculosis (TB): TB/HIV coinfection, multidrug-resistant TB and the resulting public health threat from extensively drug-resistant TB, globally and in Canada”. The Canadian Journal of Infectious Diseases & Medical Microbiology. 18 (5): 289–291. doi:10.1155/2007/986794. ISSN 1712-9532. PMC 2533560. PMID 18923728.
Liên kết ngoài[sửa | sửa mã nguồn]
- World Health Organization Stop TB Department
- Stop TB Partnership
- The Global Plan to Stop TB
- Advocacy to Control TB Internationally - ACTION
- International Standards of TB Care
- Video: Drug-Resistant TB in Russia Lưu trữ 2011-06-05 tại Wayback Machine July 24, 2007, Woodrow Wilson Center event featuring Salmaan Keshavjee and Murray Feshbach
- XDRTB.org: Spread the Story. Stop the Disease. (photo documentary of XDR-TB by James Nachtwey)
- TB Drug Resistance Mutation Database
- British Red Cross helps combat TB
- The Strange, Isolated Life of a Tuberculosis Patient in the 21st Century
- Population Services International Lưu trữ 2019-08-23 tại Wayback Machine.
