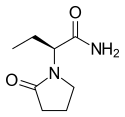
Levetiracetam
Bài viết này là một bản dịch thô từ ngôn ngữ khác. |
| |||
| Dữ liệu lâm sàng | |||
|---|---|---|---|
| Phát âm | /lɛvɪtɪˈræsɪtæm/ | ||
| Tên thương mại | Keppra, Elepsia, other | ||
| AHFS/Drugs.com | Chuyên khảo | ||
| MedlinePlus | a699059 | ||
| Giấy phép |
| ||
| Danh mục cho thai kỳ | |||
| Dược đồ sử dụng | By mouth, intravenous | ||
| Mã ATC | |||
| Tình trạng pháp lý | |||
| Tình trạng pháp lý | |||
| Dữ liệu dược động học | |||
| Sinh khả dụng | ~100% | ||
| Liên kết protein huyết tương | <10% | ||
| Chuyển hóa dược phẩm | Enzymatic hydrolysis of acetamide group | ||
| Chu kỳ bán rã sinh học | 6–8 hrs | ||
| Bài tiết | Urinary | ||
| Các định danh | |||
Tên IUPAC
| |||
| Số đăng ký CAS | |||
| PubChem CID | |||
| IUPHAR/BPS | |||
| DrugBank | |||
| ChemSpider | |||
| Định danh thành phần duy nhất | |||
| KEGG | |||
| ChEBI | |||
| ChEMBL | |||
| ECHA InfoCard | 100.121.571 | ||
| Dữ liệu hóa lý | |||
| Công thức hóa học | C8H14N2O2 | ||
| Khối lượng phân tử | 170.209 g/mol | ||
| Mẫu 3D (Jmol) | |||
SMILES
| |||
Định danh hóa học quốc tế
| |||
| (kiểm chứng) | |||
Levetiracetam, được bán dưới tên thương mại Keppra, là một loại thuốc dùng để điều trị bệnh động kinh.[1] Nó được sử dụng để khởi phát một phần, co giật cơ hoặc tonic-clonic.[2] Nó được dùng bằng đường uống dưới dạng thuốc phóng thích ngay lập tức hoặc kéo dài hoặc tiêm vào tĩnh mạch.
Các tác dụng phụ thường gặp bao gồm buồn ngủ, chóng mặt, cảm thấy mệt mỏi và hung hăng. Các tác dụng phụ nghiêm trọng có thể bao gồm rối loạn tâm thần, tự tử và phản ứng dị ứng như hội chứng Stevens-Johnson và sốc phản vệ. Không rõ liệu sử dụng có an toàn trong thai kỳ hay không nhưng có vẻ ổn khi cho con bú.[3] Đây là S-enantiomer của etiracetam.[4] Cách thức hoạt động không rõ ràng.
Levetiracetam đã được chấp thuận cho sử dụng y tế tại Hoa Kỳ vào năm 1999.[1] Nó có sẵn như là một loại thuốc gốc.[5] Một tháng cung cấp ở Vương quốc Anh tiêu tốn của NHS khoảng 19,31 bảng mỗi tháng tính đến năm 2019.[5] Tại Hoa Kỳ, chi phí bán buôn của số tiền này là khoảng 4,50 đô la Mỹ.[6] Năm 2016, đây là loại thuốc được kê đơn nhiều thứ 89 tại Hoa Kỳ với hơn 8 triệu đơn thuốc.[7]
Sử dụng trong y tế[sửa | sửa mã nguồn]
Động kinh khu trú[sửa | sửa mã nguồn]
Levetiracetam có hiệu quả như điều trị bằng thuốc đơn cho bệnh động kinh khu trú mới được chẩn đoán ở người lớn.[8] Nó làm giảm co giật khu trú từ 50% trở lên dưới dạng thuốc bổ sung.
Động kinh một phần phức tạp[sửa | sửa mã nguồn]
Levetiracetam có hiệu quả như điều trị bổ sung cho bệnh động kinh một phần (khu trú).[9]
Động kinh tổng quát[sửa | sửa mã nguồn]
Levetiracetam có hiệu quả trong điều trị động kinh tonic-clonic tổng quát.[10] Nó đã được chấp thuận ở Hoa Kỳ dưới dạng điều trị bổ sung cho co giật cơ và tonic-clonic[11]. Levetiracetam đã được chấp thuận tại Liên minh Châu Âu như là một phương pháp điều trị đơn trị liệu cho bệnh động kinh trong trường hợp co giật một phần, hoặc như một liệu pháp bổ trợ cho co giật một phần, cơ tim và thuốc bổ.[12]
Levetiracetam đôi khi được sử dụng ngoài nhãn để điều trị bệnh động kinh
Phòng chống động kinh[sửa | sửa mã nguồn]
Dựa trên bằng chứng chất lượng thấp, levetiracetam có hiệu quả tương đương với phenytoin trong phòng ngừa co giật sớm sau chấn thương sọ não.[13] Nó có thể có hiệu quả để ngăn ngừa các cơn động kinh liên quan đến xuất huyết dưới nhện.[14]
Khác[sửa | sửa mã nguồn]
Levetiracetam đã không được tìm thấy là hữu ích để điều trị đau thần kinh,[15] cũng như để điều trị các chứng run cơ bản.[16] Levetiracetam không được tìm thấy là hữu ích để điều trị bệnh tự kỷ,[17][18] nhưng là một phương pháp điều trị hiệu quả cho các cơn động kinh một phần, cơ tim hoặc thuốc bổ liên quan đến rối loạn phổ tự kỷ.[19]
Nhóm đặc biệt[sửa | sửa mã nguồn]
Levetiracetam là một loại thuốc C thai kỳ. Các nghiên cứu trên chuột cái mang thai đã cho thấy những bất thường về xương của thai nhi khi được sử dụng liều levetiracetam tối đa ở người trong suốt thai kỳ và cho con bú.[14]
Các nghiên cứu đã được thực hiện để tìm kiếm các tác dụng phụ gia tăng ở người cao tuổi so với bệnh nhân trẻ tuổi. Một nghiên cứu như vậy được công bố trong Nghiên cứu Động kinh cho thấy không có sự gia tăng đáng kể về tỷ lệ mắc các triệu chứng bất lợi của bệnh nhân trẻ hoặc người già bị rối loạn hệ thần kinh trung ương (CNS)
Levetiracetam có thể được sử dụng một cách an toàn ở trẻ em trên 4 tuổi. Tuy nhiên, vẫn chưa xác định được liệu nó có thể được sử dụng an toàn cho trẻ em dưới 4 tuổi hay không [20]
Tác dụng phụ[sửa | sửa mã nguồn]
Các tác dụng phụ phổ biến nhất của điều trị levetiracetam bao gồm các tác dụng CNS như buồn ngủ, giảm năng lượng, đau đầu, chóng mặt, thay đổi tâm trạng và khó khăn trong việc phối hợp. Những tác dụng phụ này được thấy rõ nhất trong tháng đầu điều trị. Khoảng 4% bệnh nhân bỏ các thử nghiệm lâm sàng trước khi phê duyệt do các tác dụng phụ này.[21]
Khoảng 13% những người dùng levetiracetam gặp các triệu chứng bất lợi về thần kinh, thường là nhẹ. Chúng bao gồm kích động, thù địch, thờ ơ, lo lắng, mất khả năng cảm xúc và trầm cảm. Tác dụng phụ nghiêm trọng về tâm thần nghiêm trọng được đảo ngược khi ngừng thuốc xảy ra trong khoảng 1%. Chúng bao gồm ảo giác, ý nghĩ tự tử hoặc rối loạn tâm thần. Chúng xảy ra chủ yếu trong tháng điều trị đầu tiên, nhưng chúng có thể phát triển bất cứ lúc nào trong quá trình điều trị.[22]
Mặc dù hiếm gặp, hội chứng Stevens-Johnson (SJS) và hoại tử biểu bì độc hại (TEN), xuất hiện dưới dạng phát ban đau đớn với đỏ và phồng rộp và/hoặc bong tróc da, đã được báo cáo ở những bệnh nhân được điều trị bằng levetiracetam.[23] Tỷ lệ mắc bệnh SJS sau khi tiếp xúc với thuốc chống động kinh như levetiracetam là khoảng 1 trên 3.000.[24]
Levetiracetam không nên được sử dụng ở những người trước đây đã cho thấy quá mẫn cảm với levetiracetam hoặc bất kỳ thành phần không hoạt động nào trong máy tính bảng hoặc dung dịch uống. Các phản ứng quá mẫn như vậy bao gồm, nhưng không giới hạn, phát ban không rõ nguyên nhân với đỏ hoặc da phồng rộp, khó thở và căng tức ở ngực hoặc đường thở.[21]
Trong một nghiên cứu, tỷ lệ giảm mật độ khoáng xương của bệnh nhân dùng levetiracetam cao hơn đáng kể so với các thuốc điều trị động kinh khác.[25]
Tự tử[sửa | sửa mã nguồn]
Levetiracetam, cùng với các loại thuốc chống động kinh khác, có thể làm tăng nguy cơ hành vi hoặc suy nghĩ tự tử. Những người dùng levetiracetam nên được theo dõi chặt chẽ các dấu hiệu trầm cảm, suy nghĩ hoặc khuynh hướng tự tử, hoặc bất kỳ trạng thái cảm xúc hoặc hành vi thay đổi nào.[26]
Thận và gan[sửa | sửa mã nguồn]
Suy thận làm giảm tốc độ đào thải levetiracetam khỏi cơ thể. Các cá nhân có chức năng thận giảm có thể yêu cầu điều chỉnh liều. Chức năng thận có thể được ước tính từ tốc độ thanh thải creatinin.[21]
Điều chỉnh liều levetiracetam là không cần thiết trong suy gan.[21]
Tương tác thuốc[sửa | sửa mã nguồn]
Không có tương tác dược động học quan trọng đã được quan sát giữa levetiracetam hoặc chất chuyển hóa chính và thuốc đồng thời của nó.[27] Các dược động học của Levetiracetam là không bị ảnh hưởng bởi phenytoin, phenobarbital, primidone, carbamazepine, valproic acid, lamotrigine, gabapentin, digoxin, ethinylestradiol, hoặc warfarin.[28]
Cơ chế hoạt động[sửa | sửa mã nguồn]
Cơ chế chính xác mà levetiracetam hoạt động để điều trị bệnh động kinh vẫn chưa được biết. Levetiracetam không thể hiện hành động dược lý tương tự như thuốc chống co giật cổ điển. Nó không hít vào các kênh Na + phụ thuộc vào điện áp, không ảnh hưởng đến việc truyền GABAergic và không liên kết với các thụ thể GABAergic hoặc glutamatergic.[29] Tuy nhiên, thuốc liên kết với SV2A,[30] một glycoprotein túi synap, và ức chế các kênh calci trước synap,[31] làm giảm giải phóng chất dẫn truyền thần kinh và hoạt động như một chất điều chế thần kinh. Điều này được cho là cản trở sự dẫn truyền xung động qua các khớp thần kinh.[32]
Dược động học[sửa | sửa mã nguồn]
Hấp thu[sửa | sửa mã nguồn]
Sự hấp thu của viên thuốc levetiracetam và dung dịch uống là nhanh chóng và cơ bản hoàn tất. Sinh khả dụng của levetiracetam gần 100% và ảnh hưởng của thức ăn đến sự hấp thụ là không đáng kể.[21]
Phân phối[sửa | sửa mã nguồn]
Thể tích phân phối của levetiracetam tương tự như tổng lượng nước cơ thể. Levetiracetam liên kết khiêm tốn với protein huyết tương (dưới 10%).[21]
Chuyển hóa[sửa | sửa mã nguồn]
Levetiracetam không trải qua quá trình chuyển hóa rộng rãi, và các chất chuyển hóa được hình thành không hoạt động và không hoạt động dược lý. Chuyển hóa của levetiracetam không phải do enzyme cytochrom P450 của gan, mà thông qua các con đường chuyển hóa khác như thủy phân và hydroxyl hóa.[21]
Bài tiết[sửa | sửa mã nguồn]
Ở những người có chức năng thận bình thường, levetiracetam được đào thải khỏi cơ thể chủ yếu bởi thận với khoảng 66% thuốc ban đầu được truyền không đổi vào nước tiểu. Thời gian bán hủy trong huyết tương của levetiracetam ở người lớn là khoảng 6 đến 8 giờ.[21]
Tương tự[sửa | sửa mã nguồn]
Brivaracetam, một chất tương tự hóa học với levetiracetam, là một dẫn xuất racetam có tính chất tương tự.
Xã hội và văn hoá[sửa | sửa mã nguồn]
Levetiracetam có sẵn dưới dạng thuốc uống phóng thích đều đặn và kéo dài và dưới dạng thuốc tiêm tĩnh mạch.[21][33]
Máy tính bảng phát hành ngay lập tức đã có sẵn dưới dạng chung tại Hoa Kỳ kể từ năm 2008 và ở Anh kể từ năm 2011 [34][35] Bằng sáng chế cho máy tính bảng phát hành mở rộng sẽ hết hạn vào năm 2028.[36]
Phiên bản thương hiệu Keppra được sản xuất bởi UCB Cosmetics Inc. [37]
Vào năm 2015, dạng thuốc viên sủi được in bằng 3d của Aprecia đã được FDA chấp thuận, dưới tên thương mại là Spritam.[38]
Nghiên cứu[sửa | sửa mã nguồn]
Levetiracetam đang được xem xét trong các tình trạng tâm thần và thần kinh như hội chứng Tourette,[39] và rối loạn lo âu.[40] Tuy nhiên, tác dụng phụ nghiêm trọng nhất của nó là hành vi và tỷ lệ rủi ro lợi ích của nó trong các điều kiện này không được hiểu rõ.[40]
Tham khảo[sửa | sửa mã nguồn]
- ^ a b “Levetiracetam Monograph for Professionals”. Drugs.com (bằng tiếng Anh). AHFS. Truy cập ngày 14 tháng 1 năm 2019.
- ^ “Tonic-clonic Seizures”. Epilepsy Foundation (bằng tiếng Anh). Truy cập ngày 30 tháng 10 năm 2021.
- ^ “Levetiracetam Use During Pregnancy”. Drugs.com (bằng tiếng Anh). Truy cập ngày 5 tháng 3 năm 2019.
- ^ Cavanna, Andrea E. (2018). Behavioural Neurology of Anti-Epileptic Drugs: A Practical Guide (bằng tiếng Anh). Oxford University Press. tr. 17. ISBN 9780198791577.
- ^ a b British national formulary: BNF 76 (ấn bản 76). Pharmaceutical Press. 2018. tr. 319. ISBN 9780857113382.
- ^ “NADAC as of 2019-02-27”. Centers for Medicare and Medicaid Services (bằng tiếng Anh). Bản gốc lưu trữ ngày 6 tháng 3 năm 2019. Truy cập ngày 3 tháng 3 năm 2019.
- ^ “The Top 300 of 2019”. clincalc.com. Truy cập ngày 22 tháng 12 năm 2018.
- ^ Lattanzi S, Zaccara G, Giovannelli F, Grillo E, Nardone R, Silvestrini M, Trinka E, Brigo F (tháng 1 năm 2019). “Antiepileptic monotherapy in newly diagnosed focal epilepsy. A network meta-analysis”. Acta Neurol. Scand. 139 (1): 33–41. doi:10.1111/ane.13025. PMID 30194755.
- ^ Slater J, Chung S, Huynh L, Duh MS, Gorin B, McMicken C, Ziemann A, Isojarvi J (tháng 7 năm 2018). “Efficacy of antiepileptic drugs in the adjunctive treatment of refractory partial-onset seizures: Meta-analysis of pivotal trials”. Epilepsy Res. 143: 120–129. doi:10.1016/j.eplepsyres.2017.10.004. PMID 29784458.
- ^ Nevitt SJ, Sudell M, Weston J, Tudur Smith C, Marson AG (tháng 12 năm 2017). “Antiepileptic drug monotherapy for epilepsy: a network meta-analysis of individual participant data”. Cochrane Database Syst Rev. 12: CD011412. doi:10.1002/14651858.CD011412.pub3. PMID 29243813.
- ^ “Tonic-clonic Seizures”. Epilepsy Foundation (bằng tiếng Anh). Truy cập ngày 30 tháng 10 năm 2021.
- ^ BNF 59. BMA & RPSGB. 2010.
- ^ Khan NR, VanLandingham MA, Fierst TM, Hymel C, Hoes K, Evans LT, Mayer R, Barker F, Klimo P (tháng 12 năm 2016). “Should Levetiracetam or Phenytoin Be Used for Posttraumatic Seizure Prophylaxis? A Systematic Review of the Literature and Meta-analysis”. Neurosurgery. 79 (6): 775–782. doi:10.1227/NEU.0000000000001445. PMID 27749510.
- ^ Shah, Dharmen; Husain, Aatif M. (2009). “Utility of levetiracetam in patients with subarachnoid hemorrhage”. Seizure. 18 (10): 676–9. doi:10.1016/j.seizure.2009.09.003. PMID 19864168.
- ^ Crawford-Faucher, A; Huijon, R. M. (2015). “The Role of Levetiracetam in Treating Chronic Neuropathic Pain Symptoms”. American Family Physician. 92 (1): 23–4. PMID 26132123.
- ^ Zesiewicz, T. A.; Elble, R. J.; Louis, E. D.; Gronseth, G. S.; Ondo, W. G.; Dewey, R. B.; Okun, M. S.; Sullivan, K. L.; Weiner, W. J. (2011). “Evidence-based guideline update: Treatment of essential tremor: Report of the Quality Standards Subcommittee of the American Academy of Neurology”. Neurology. 77 (19): 1752–5. doi:10.1212/WNL.0b013e318236f0fd. PMC 3208950. PMID 22013182.
- ^ Volkmar, Fred; Siegel, Matthew; Woodbury-Smith, Marc; King, Bryan; McCracken, James; State, Matthew (2014). “Practice Parameter for the Assessment and Treatment of Children and Adolescents with Autism Spectrum Disorder”. Journal of the American Academy of Child & Adolescent Psychiatry. 53 (2): 237–57. doi:10.1016/j.jaac.2013.10.013. PMID 24472258.
- ^ Hirota, Tomoya; Veenstra-Vanderweele, Jeremy; Hollander, Eric; Kishi, Taro (2013). “Antiepileptic Medications in Autism Spectrum Disorder: A Systematic Review and Meta-Analysis”. Journal of Autism and Developmental Disorders. 44 (4): 948–57. doi:10.1007/s10803-013-1952-2. PMID 24077782.
- ^ Frye, Richard; Rossignol, Daniel; Casanova, Manuel F.; Brown, Gregory L.; Martin, Victoria; Edelson, Stephen; Coben, Robert; Lewine, Jeffrey; Slattery, John C. (2013). “A review of traditional and novel treatments for seizures in autism spectrum disorder: Findings from a systematic review and expert panel”. Frontiers in Public Health. 1: 31. doi:10.3389/fpubh.2013.00031. PMC 3859980. PMID 24350200.
- ^ “Advancements in the Treatment of Epilepsy” (PDF). harvard.edu. ngày 1 tháng 1 năm 2008. Truy cập ngày 8 tháng 7 năm 2017.
- ^ a b c d e f g h i “Keppra (levetiracetam) Prescribing Information” (PDF).
- ^ Gambardella, Antonio (2008). “Monotherapy for partial epilepsy: Focus on levetiracetam”. Neuropsychiatric Disease and Treatment. 4 (1): 33–8. doi:10.2147/NDT.S1655. PMC 2515905. PMID 18728811.
- ^ Zou, Li-Ping; Ding, Chang-Hong; Song, Zhen-Jiang; Li, Xiao-Feng (2012). “Stevens–Johnson syndrome induced by levetiracetam”. Seizure. 21 (10): 823–5. doi:10.1016/j.seizure.2012.09.005. PMID 23036769.
- ^ Griebel, May L. (1998). “Acute Management of Hypersensitivity Reactions and Seizures”. Epilepsia. 39: S17–21. doi:10.1111/j.1528-1157.1998.tb01680.x. PMID 9798757.
- ^ Beniczky, Simona Alexandra; Viken, Janina; Jensen, Lars Thorbjørn; Andersen, Noémi Becser (2012). “Bone mineral density in adult patients treated with various antiepileptic drugs”. Seizure. 21 (6): 471–2. doi:10.1016/j.seizure.2012.04.002. PMID 22541979.
- ^ “DailyMed - KEPPRA- levetiracetam tablet”. dailymed.nlm.nih.gov. Truy cập ngày 4 tháng 11 năm 2015.
- ^ Browne, T. R.; Szabo, G. K.; Leppik, I. E.; Josephs, E.; Paz, J.; Baltes, E.; Jensen, C. M. (2000). “Absence of Pharmacokinetic Drug Interaction of Levetiracetam with Phenytoin in Patients with Epilepsy Determined by New Technique”. The Journal of Clinical Pharmacology. 40 (6): 590–5. doi:10.1002/j.1552-4604.2000.tb05984.x. PMID 10868309.
- ^ Gidal, Barry E.; Baltès, Eugène; Otoul, Christian; Perucca, Emilio (2005). “Effect of levetiracetam on the pharmacokinetics of adjunctive antiepileptic drugs: A pooled analysis of data from randomized clinical trials”. Epilepsy Research. 64 (1–2): 1–11. doi:10.1016/j.eplepsyres.2005.01.005. PMID 15823510.
- ^ Deshpande LS, Delorenzo RJ (2014). “Mechanisms of levetiracetam in the control of status epilepticus and epilepsy”. Front Neurol. 5: 11. doi:10.3389/fneur.2014.00011. PMC 3907711. PMID 24550884.
- ^ Lynch BA, Lambeng N, Nocka K, và đồng nghiệp (tháng 6 năm 2004). “The synaptic vesicle protein SV2A is the binding site for the antiepileptic drug levetiracetam”. Proc Natl Acad Sci USA. 101 (26): 9861–6. Bibcode:2004PNAS..101.9861L. doi:10.1073/pnas.0308208101. PMC 470764. PMID 15210974.
- ^ Vogl C, Mochida S, Wolff C, và đồng nghiệp (tháng 8 năm 2012). “The Synaptic Vesicle Glycoprotein 2A Ligand Levetiracetam Inhibits Presynaptic Ca2+ Channels through an Intracellular Pathway”. Mol. Pharmacol. 82 (2): 199–208. doi:10.1124/mol.111.076687. PMID 22554805.
- ^ Rogawski, MA (tháng 6 năm 2006). “Diverse mechanisms of antiepileptic drugs in the development pipeline”. Epilepsy Research. 69 (3): 273–94. doi:10.1016/j.eplepsyres.2006.02.004. PMC 1562526. PMID 16621450.
- ^ “Levetiracetam Injection Prescribing Information” (PDF).
- ^ Mbizvo, Gashirai K; Dixon, Pete; Hutton, Jane L; Marson, Anthony G (2012). “Levetiracetam add-on for drug-resistant focal epilepsy: An updated Cochrane Review”. Cochrane Database of Systematic Reviews (9): CD001901. doi:10.1002/14651858.cd001901.pub2. PMID 22972056.
- ^ Branch Website Management. “Patent Terms Extended Under 35 USC §156”. www.uspto.gov. Truy cập ngày 5 tháng 11 năm 2015.
- ^ Webber, Keith (ngày 12 tháng 9 năm 2011). “FDA Access Data” (PDF). ANDA 091291. Department of Health and Human Services. Truy cập ngày 4 tháng 11 năm 2015.
- ^ “Products | UCB”. www.ucb-usa.com. Bản gốc lưu trữ ngày 25 tháng 9 năm 2017. Truy cập ngày 5 tháng 11 năm 2015.
- ^ “FDA approves the first 3D-printed drug product | KurzweilAI”. www.kurzweilai.net. ngày 13 tháng 10 năm 2015. Truy cập ngày 14 tháng 10 năm 2015.
- ^ Martínez-Granero, M. A.; García-Pérez, A; Montañes, F (2010). “Levetiracetam as an alternative therapy for Tourette syndrome”. Neuropsychiatric Disease and Treatment. 6: 309–16. PMC 2898169. PMID 20628631.
- ^ a b Farooq MU, Bhatt A, Majid A, Gupta R, Khasnis A, Kassab MY (2009). “Levetiracetam for managing neurologic and psychiatric disorders”. Am J Health Syst Pharm. 66 (6): 541–61. doi:10.2146/ajhp070607. PMID 19265183.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
Liên kết ngoài[sửa | sửa mã nguồn]
- Thông tin người tiêu dùng Levetiracetam tại Thư viện Y khoa Quốc gia Hoa Kỳ MedlinePlus
- Nhãn Keppra (levetiracetam) Tháng 4 năm 2009. Trung tâm đánh giá và nghiên cứu thuốc, Cục quản lý thực phẩm và dược phẩm Hoa Kỳ. Truy cập ngày 29 tháng 7 năm 2011.