Khác biệt giữa bản sửa đổi của “Kali hydroxide”
Nội dung được xóa Nội dung được thêm vào
n →Tham khảo: replaced: {{tham khảo}} → {{tham khảo|2}} |
|||
| Dòng 75: | Dòng 75: | ||
'''Kali hiđroxit''' (công thức hóa học: KOH) là một hiđroxit kiềm mạnh có tính ăn mòn, tên thông dụng là potash ăn da. Nó là một chất rắn kết tinh màu trắng, ưa ẩm. Nó hòa tan trong nước. Phần lớn các ứng dụng của chất này do độ phản ứng của nó đối với [[axít|axit]] và tính ăn mòn. Năm 2005, ước tính toàn cầu sản xuất 700.000-800.000 tấn hợp chất này, ước tính sản lượng hàng năm của [[Natri hiđroxit|NaOH]] cao gấp 100 lần KOH<ref name=Ullmann>H. Schultz, G. Bauer, E. Schachl, F. Hagedorn, P. Schmittinger “Potassium Compounds” in Ullmann’s Encyclopedia of Industrial Chemistry, 2005, Wiley-VCH, Weinheim. {{DOI|10.1002/14356007.a22_039}}</ref>. KOH là tiền chất của phần lớn xà phòng lỏng và mềm cũng như các hóa chất có chứa kali khác. |
'''Kali hiđroxit''' (công thức hóa học: KOH) là một hiđroxit kiềm mạnh có tính ăn mòn, tên thông dụng là potash ăn da. Nó là một chất rắn kết tinh màu trắng, ưa ẩm. Nó hòa tan trong nước. Phần lớn các ứng dụng của chất này do độ phản ứng của nó đối với [[axít|axit]] và tính ăn mòn. Năm 2005, ước tính toàn cầu sản xuất 700.000-800.000 tấn hợp chất này, ước tính sản lượng hàng năm của [[Natri hiđroxit|NaOH]] cao gấp 100 lần KOH<ref name=Ullmann>H. Schultz, G. Bauer, E. Schachl, F. Hagedorn, P. Schmittinger “Potassium Compounds” in Ullmann’s Encyclopedia of Industrial Chemistry, 2005, Wiley-VCH, Weinheim. {{DOI|10.1002/14356007.a22_039}}</ref>. KOH là tiền chất của phần lớn xà phòng lỏng và mềm cũng như các hóa chất có chứa kali khác. |
||
==Tham khảo== |
==Tham khảo== |
||
{{tham khảo}} |
{{tham khảo|2}} |
||
{{sơ khai hóa học}} |
{{sơ khai hóa học}} |
||
Phiên bản lúc 15:25, ngày 10 tháng 12 năm 2013
| Potassium hydroxide | |
|---|---|
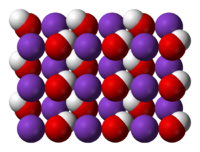 crystal structure of KOH | |
| Danh pháp IUPAC | Potassium hydroxide |
| Tên khác | Caustic potash Potash lye Potassia Potassium hydrate |
| Nhận dạng | |
| Số CAS | |
| PubChem | |
| Số EINECS | |
| ChEBI | |
| Số RTECS | TT2100000 |
| Ảnh Jmol-3D | ảnh |
| SMILES | đầy đủ
|
| InChI | đầy đủ
|
| UNII | |
| Thuộc tính | |
| Công thức phân tử | KOH |
| Khối lượng mol | 56.1056 g/mol |
| Bề ngoài | white solid, deliquescent |
| Mùi | odorless |
| Khối lượng riêng | 2.044 g/cm3[1] |
| Điểm nóng chảy | 406 °C (679 K; 763 °F) |
| Điểm sôi | 1.327 °C (1.600 K; 2.421 °F) |
| Độ hòa tan trong nước | 97 g/100 mL (0 °C) 121 g/100 mL (25 °C) 178 g/100 mL (100 °C)[1] |
| Độ hòa tan | soluble in alcohol, glycerol insoluble in ether, liquid ammonia |
| Độ axit (pKa) | 13.5 (0.1 M) |
| Chiết suất (nD) | 1.409 |
| Cấu trúc | |
| Cấu trúc tinh thể | rhombohedral |
| Nhiệt hóa học | |
| Enthalpy hình thành ΔfH | −425 kJ·mol−1[2] |
| Entropy mol tiêu chuẩn S | 79 J·mol−1·K−1[2] |
| Các nguy hiểm | |
| MSDS | ICSC 0357 |
| Phân loại của EU | Corrosive (C) Harmful (Xn) |
| Chỉ mục EU | 019-002-00-8 |
| NFPA 704 |
|
| Chỉ dẫn R | R22, R35 |
| Chỉ dẫn S | (S1/2), S26, S36/37/39, S45 |
| Điểm bắt lửa | Non-flammable |
| LD50 | 273 mg/kg (rat, oral) |
| Các hợp chất liên quan | |
| Anion khác | Potassium hydrosulfide Potassium amide |
| Cation khác | Lithium hydroxide Sodium hydroxide Rubidium hydroxide Caesium hydroxide |
| Hợp chất liên quan | Potassium oxide |
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |
Kali hiđroxit (công thức hóa học: KOH) là một hiđroxit kiềm mạnh có tính ăn mòn, tên thông dụng là potash ăn da. Nó là một chất rắn kết tinh màu trắng, ưa ẩm. Nó hòa tan trong nước. Phần lớn các ứng dụng của chất này do độ phản ứng của nó đối với axit và tính ăn mòn. Năm 2005, ước tính toàn cầu sản xuất 700.000-800.000 tấn hợp chất này, ước tính sản lượng hàng năm của NaOH cao gấp 100 lần KOH[3]. KOH là tiền chất của phần lớn xà phòng lỏng và mềm cũng như các hóa chất có chứa kali khác.
Tham khảo
- ^ a b Lide, D. R. biên tập (2005). CRC Handbook of Chemistry and Physics (ấn bản 86). Boca Raton (FL): CRC Press. tr. 4-80. ISBN 0-8493-0486-5.
- ^ a b Zumdahl, Steven S. (2009). Chemical Principles 6th Ed. Houghton Mifflin Company. tr. A22. ISBN 0-618-94690-X.
- ^ H. Schultz, G. Bauer, E. Schachl, F. Hagedorn, P. Schmittinger “Potassium Compounds” in Ullmann’s Encyclopedia of Industrial Chemistry, 2005, Wiley-VCH, Weinheim. doi:10.1002/14356007.a22_039

