Khác biệt giữa bản sửa đổi của “Phân lớp (vỏ nguyên tử)”
Nội dung được xóa Nội dung được thêm vào
Không có tóm lược sửa đổi Thẻ: Soạn thảo trực quan Sửa đổi di động Sửa đổi từ trang di động |
|||
| Dòng 1: | Dòng 1: | ||
[[Tập tin:Periodic table blocks spdf (32 column).svg|400px|right|thumb|alt=Blocks in the periodic table]] |
[[Tập tin:Periodic table blocks spdf (32 column).svg|400px|right|thumb|alt=Blocks in the periodic table]] |
||
'''Phân lớp electron''' trong [[bảng tuần hoàn]] các nguyên tố hóa học là một tập hợp các [[Nhóm (bảng tuần hoàn)|nhóm]] lân cận nhau.<ref>Charles Janet, ''La classification hélicoïdale des éléments chimiques'', Beauvais, 1928</ref> Các electron năng |
'''Phân lớp electron''' trong [[bảng tuần hoàn]] các nguyên tố hóa học là một tập hợp các [[Nhóm (bảng tuần hoàn)|nhóm]] lân cận nhau.<ref>Charles Janet, ''La classification hélicoïdale des éléments chimiques'', Beauvais, 1928</ref> Các electron năng lượng cao nhất tương ứng trong một nguyên tố trong cùng một phân lớp thì thuộc cùng một kiểm [[obitan nguyên tử]]. Mỗi phân lớp được đặt tên theo tính chất của orbitan của nó. Do đó, các phân lớp bao gồm: |
||
* phân lớp |
* phân lớp '''S''' |
||
* phân lớp |
* phân lớp '''P''' |
||
* phân lớp |
* phân lớp '''D''' |
||
* phân lớp |
* phân lớp '''F''' |
||
* phân lớp |
* phân lớp '''G''' (giả thiết) |
||
Tên phân lớp (s, p, d, f và g) xuất phát từ ký hiệu quang phổ của [[obitan nguyên tử]] tương ứng: '''s'''harp, '''p'''rincipal, '''d'''iffuse và '''f'''undamental, và cuối cùng g theo sau ký hiệu f trong bảng chữ cái. |
Tên phân lớp (s, p, d, f và g) xuất phát từ ký hiệu quang phổ của [[obitan nguyên tử]] tương ứng: '''s'''harp, '''p'''rincipal, '''d'''iffuse và '''f'''undamental, và cuối cùng g theo sau ký hiệu f trong bảng chữ cái. |
||
Phiên bản lúc 14:19, ngày 21 tháng 8 năm 2019
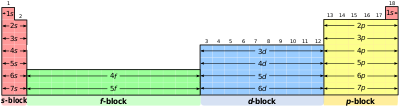
Phân lớp electron trong bảng tuần hoàn các nguyên tố hóa học là một tập hợp các nhóm lân cận nhau.[1] Các electron năng lượng cao nhất tương ứng trong một nguyên tố trong cùng một phân lớp thì thuộc cùng một kiểm obitan nguyên tử. Mỗi phân lớp được đặt tên theo tính chất của orbitan của nó. Do đó, các phân lớp bao gồm:
- phân lớp S
- phân lớp P
- phân lớp D
- phân lớp F
- phân lớp G (giả thiết)
Tên phân lớp (s, p, d, f và g) xuất phát từ ký hiệu quang phổ của obitan nguyên tử tương ứng: sharp, principal, diffuse và fundamental, và cuối cùng g theo sau ký hiệu f trong bảng chữ cái.
Tham khảo
- ^ Charles Janet, La classification hélicoïdale des éléments chimiques, Beauvais, 1928
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | |||||||||||||||
| 1 | H | He | ||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | ||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | ||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |
