Fluticasone/salmeterol
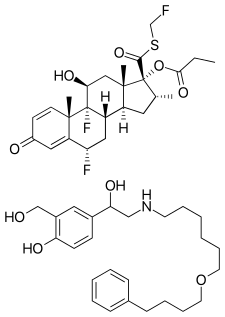 Fluticasone propionate (top) and salmeterol (bottom) | |
| Kết hợp của | |
|---|---|
| Fluticasone propionate | Glucocorticoid |
| Salmeterol | Long-acting β2 agonist (LABA) |
| Dữ liệu lâm sàng | |
| Tên thương mại | Advair, Seretide, others |
| AHFS/Drugs.com | Thông tin thuốc chuyên nghiệp FDA |
| MedlinePlus | a699063 |
| Danh mục cho thai kỳ | |
| Dược đồ sử dụng | Inhalation |
| Mã ATC | |
| Tình trạng pháp lý | |
| Tình trạng pháp lý | |
| Các định danh | |
| PubChem CID | |
| ChemSpider | |
| (kiểm chứng) | |
Flnomasone/salmeterol, được bán dưới tên thương hiệu Advair trong số những loại khác, là một loại thuốc kết hợp có chứa flnomasone propionate và salmeterol.[1] Nó được sử dụng trong quản lý hen và bệnh phổi tắc nghẽn mạn tính (COPD). Nó được sử dụng bằng cách hít thuốc vào phổi.
Các tác dụng phụ thường gặp bao gồm tưa miệng, đau đầu và ho.[2] Tác dụng phụ nghiêm trọng có thể bao gồm hen suyễn nặng hơn, sốc phản vệ, co giật và các vấn đề về tim. An toàn trong thai kỳ và cho con bú là không rõ ràng.[3] Flnomasone, một corticosteroid, hoạt động bằng cách giảm viêm trong khi salmeterol, một chất chủ vận beta-adrenoceptor tác dụng dài (LABA), hoạt động bằng cách kích hoạt thụ thể adrenergic beta-2.
Sự kết hợp đã được chấp thuận cho sử dụng y tế tại Hoa Kỳ vào năm 2000.[2] Một phiên bản gốc đã được phê duyệt tại Hoa Kỳ vào năm 2019.[4] Một nguồn cung cấp hai tháng tại Vương quốc Anh tiêu tốn cho Dịch vụ Y tế Quốc gia khoảng 35 bảng mỗi tháng kể từ năm 2019.[1] Tại Hoa Kỳ, chi phí bán buôn của số tiền này là khoảng 89 USD.[5] Năm 2016, đây là loại thuốc được kê đơn nhiều thứ 62 tại Hoa Kỳ, với hơn 12 triệu đơn thuốc.[6]
Sử dụng trong y tế[sửa | sửa mã nguồn]
Flnomasone, một corticosteroid, là thành phần chống viêm của sự kết hợp làm giảm viêm trong phổi. Điều này dẫn đến việc cải thiện hơi thở. Salmeterol, một LABA, điều trị co thắt đường thở. Sự kết hợp của cả hai có nghĩa là được sử dụng như một liệu pháp duy trì và không phải là một liệu pháp cứu hộ cho các triệu chứng đột ngột.
Tác dụng phụ[sửa | sửa mã nguồn]
Các tác dụng phụ phổ biến của sự kết hợp này là những thuốc riêng lẻ của nó. Ví dụ, việc sử dụng corticosteroid dạng hít có liên quan đến nhiễm nấm miệng, thường được gọi là nhiễm trùng nấm men hoặc bệnh tưa miệng. Súc miệng bằng nước sau khi hít thuốc làm giảm nguy cơ phát triển tình trạng này.
Mặc dù việc sử dụng steroid dạng hít và LABA được khuyến nghị để cải thiện kết quả kiểm soát các triệu chứng hen suyễn,[7] đã lo ngại rằng salmeterol có thể làm tăng nguy cơ tử vong do hen suyễn và nguy cơ bổ sung này không giảm khi bổ sung steroid dạng hít.[8] Các tác dụng phụ khác từ sự kết hợp thuốc này có thể bao gồm tăng huyết áp, thay đổi nhịp tim, nhịp tim không đều, tăng nguy cơ loãng xương, đục thủy tinh thể và tăng nhãn áp.[9] Các nghiên cứu đã chứng minh sự an toàn của flnomasone propionate dạng hít ở trẻ em. Một đánh giá có hệ thống được công bố vào năm 2013 cho thấy không có tác dụng phụ đáng kể nào đối với chức năng của trục thượng thận tuyến yên, sự phát triển và mật độ khoáng xương ở trẻ em hen suyễn khi sử dụng flnomasone trong tối đa ba tháng.[10]
Xã hội và văn hoá[sửa | sửa mã nguồn]
Tương đương gốc[sửa | sửa mã nguồn]
Vào ngày 30 tháng 1 năm 2019, FDA đã cấp cho Mylan NV sự chấp thuận chung đầu tiên cho Advair Diskus.[11]
Khu định cư dân sự[sửa | sửa mã nguồn]
Năm 2012, Advair là một phần của thỏa thuận giải quyết dân sự lớn hơn giữa GlaxoSmithKline (GSK) và Hoa Kỳ, trong đó GSK đồng ý trả 1,043 tỷ đô la; Hoa Kỳ nói rằng GSK đã thúc đẩy việc sử dụng Advair ngoài nhãn hiệu và trả lại tiền cho các chuyên gia chăm sóc sức khỏe để bán loại thuốc này, trong số những người khác.[12]
Tham khảo[sửa | sửa mã nguồn]
- ^ a b British national formulary: BNF 76 (ấn bản 76). Pharmaceutical Press. 2018. tr. 263–264. ISBN 9780857113382.
- ^ a b “Fluticasone and Salmeterol inhalation - FDA prescribing information, side effects and uses”. Drugs.com (bằng tiếng Anh). Truy cập ngày 4 tháng 3 năm 2019.
- ^ “Fluticasone / salmeterol Pregnancy and Breastfeeding Warnings”. Drugs.com (bằng tiếng Anh). Truy cập ngày 3 tháng 3 năm 2019.
- ^ Office of the Commissioner. “Press Announcements - FDA approves first generic Advair Diskus”. www.fda.gov (bằng tiếng Anh). Truy cập ngày 1 tháng 2 năm 2019.
- ^ “NADAC as of 2019-02-27”. Centers for Medicare and Medicaid Services (bằng tiếng Anh). Bản gốc lưu trữ ngày 6 tháng 3 năm 2019. Truy cập ngày 3 tháng 3 năm 2019.
- ^ “The Top 300 of 2019”. clincalc.com. Truy cập ngày 22 tháng 12 năm 2018.
- ^ “Guideline 101: British Guideline on the Management of Asthma”. British Thoracic Society & Scottish Intercollegiate Guidelines Network (SIGN). Bản gốc lưu trữ ngày 18 tháng 4 năm 2015.
- ^ Salpeter SR, Buckley NS, Ormiston TM, Salpeter EE (tháng 6 năm 2006). “Meta-analysis: effect of long-acting beta-agonists on severe asthma exacerbations and asthma-related deaths”. Ann. Intern. Med. 144 (12): 904–12. doi:10.7326/0003-4819-144-12-200606200-00126. PMID 16754916.
- ^ “US fluticasone propionate/Salmeterol label” (PDF). FDA. tháng 4 năm 2016.
- ^ Muley, Prasad; Shah, Monali (2013). “Safety of Inhaled Fluticasone Propionate Therapy for Pediatric Asthma - A Systematic Review”. Current Drug Safety. 8 (3): 186-194. PMID 23859431.
- ^ “FDA approves first generic Advair Diskus”. U.S. Food and Drug Administration.
- ^ “GlaxoSmithKline to Plead Guilty and Pay $3 Billion to Resolve Fraud Allegations and Failure to Report Safety Data”. Department of Justice: Office of Public Affairs. ngày 2 tháng 7 năm 2012.
