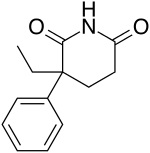
Glutethimide
 | |
 | |
| Dữ liệu lâm sàng | |
|---|---|
| Tên thương mại | Doriden, Elrodorm, Noxyron, others |
| Danh mục cho thai kỳ |
|
| Nguy cơ lệ thuộc | Medium-high |
| Dược đồ sử dụng | By mouth |
| Mã ATC | |
| Tình trạng pháp lý | |
| Tình trạng pháp lý |
|
| Dữ liệu dược động học | |
| Sinh khả dụng | Variable (Tmax = 1–6 hours)[1] |
| Liên kết protein huyết tương | ~50% |
| Chuyển hóa dược phẩm | Extensive Gan |
| Chu kỳ bán rã sinh học | 8–12 hours |
| Bài tiết | Thận |
| Các định danh | |
Tên IUPAC
| |
| Số đăng ký CAS | |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| Định danh thành phần duy nhất | |
| KEGG | |
| ChEMBL | |
| ECHA InfoCard | 100.000.921 |
| Dữ liệu hóa lý | |
| Công thức hóa học | C13H15NO2 |
| Khối lượng phân tử | 217.264 g/mol |
| Mẫu 3D (Jmol) | |
| Điểm nóng chảy | 84 °C (183 °F) |
| Độ hòa tan trong nước | 999 mg/L (30 °C/86 °F) mg/mL (20 °C) |
SMILES
| |
Định danh hóa học quốc tế
| |
| (kiểm chứng) | |
Glutethimide là thuốc an thần thôi miên được Ciba giới thiệu vào năm 1954 như là một thay thế an toàn cho barbiturat để điều trị chứng mất ngủ. Tuy nhiên, trước đó, rõ ràng là glutethimide có khả năng gây nghiện và gây ra các triệu chứng cai tương tự. Doriden là phiên bản thương hiệu. Mức sản xuất hiện tại ở Hoa Kỳ (hạn ngạch hàng năm cho sản xuất do DEA áp đặt là ba gram, đủ cho sáu máy tính bảng Doriden, trong một số năm) chỉ sử dụng trong nghiên cứu quy mô nhỏ. Việc sản xuất thuốc đã bị ngừng ở Mỹ vào năm 1993 và đã ngừng ở một số nước Đông Âu vào năm 2006.

Sử dụng lâu dài[sửa | sửa mã nguồn]
Tác dụng hồi phục sử dụng lâu dài, tương tự như những gì đã thấy khi rút tiền, đã được mô tả một cách ngẫu nhiên ở những bệnh nhân vẫn đang dùng một liều thuốc ổn định. Các triệu chứng bao gồm mê sảng, ảo giác, co giật và sốt.[2]
Sử dụng giải trí[sửa | sửa mã nguồn]
Glutethimide là một chất cảm ứng enzyme CYP2D6. Khi được sử dụng với codeine, (được biết đến trên đường phố là "lượt truy cập", "cibas và codeine", "Dors và 4s"), nó cho phép cơ thể chuyển đổi số lượng cao hơn của codein thành morphin. Tác dụng an thần chung của glutethimide cũng làm tăng thêm tác dụng của sự kết hợp.[3] Nó tạo ra một cơn khoái cảm mãnh liệt, kéo dài tương tự như sử dụng heroin IV. Khá nhiều cái chết đã xảy ra do lạm dụng sự kết hợp này.[4] Hiệu quả này cũng được sử dụng lâm sàng, bao gồm một số nghiên cứu trong những năm 1970 ở nhiều quốc gia sử dụng nó trong các trường hợp được theo dõi cẩn thận như một hình thức điều trị thay thế thuốc chủ vận opioid, ví dụ như một thay thế có thể là một thay thế hữu ích cho methadone.[5][6] Nhu cầu về sự kết hợp này ở Philadelphia, Pittsburgh, Newark, NYC, Boston, Baltimore và các khu vực lân cận của các tiểu bang khác và có lẽ ở những nơi khác, đã dẫn đến sự tổng hợp glutethimide quy mô nhỏ từ năm 1984,[7] :203 một quá trình, giống như tổng hợp methaquater (Quaalude), hơi khó khăn và có nhiều kết quả xấu khi các nhà hóa học kém năng khiếu đang thực hiện hành vi với tiền chất cấp công nghiệp mà không kiểm soát chất lượng đầy đủ. Thực tế là sự tổng hợp clandestine đơn giản hơn các thuốc ức chế dược phẩm đã không còn sử dụng khác như ethchlorvynol, methyprylon hoặc barbiturat lâu đời nhất dường như không chỉ ra mức độ động lực cao xung quanh một loại thuốc độc đáo, giống như methaquater. Việc sản xuất glutethimide đã bị ngừng ở Mỹ vào năm 1993 và ở một số nước Đông Âu, nổi bật nhất là Hungary, năm 2006. Phân tích glutethimide bị tịch thu dường như luôn luôn cho thấy thuốc hoặc kết quả của quá trình tổng hợp đã cố gắng, trong khi đó methaquater có ý nghĩa là trong phần lớn các trường hợp được tìm thấy là trơ, hoặc chứa diphenhydramine hoặc benzodiazepine.
Tình trạng pháp lý[sửa | sửa mã nguồn]
Glutethimide là một loại thuốc thuộc Bảng II theo Công ước về các chất hướng thần. Nó ban đầu là một loại thuốc thuộc Lịch III ở Hoa Kỳ theo Đạo luật về các chất bị kiểm soát, nhưng vào năm 1991, nó đã được nâng cấp lên Bảng II, vài năm sau khi phát hiện ra rằng lạm dụng kết hợp với codeine làm tăng tác dụng của codein và tử vong kết quả từ sự kết hợp.[8][9] Nó có DEA ACSCN là 2550 và hạn ngạch sản xuất năm 2013 là 3 g.
Hóa học[sửa | sửa mã nguồn]
Glutethimide (3-etyl-3-phenylgutarimide) được tổng hợp bằng cách bổ sung 2 phenylbutanenitrile đến Metyl acrylat (phản ứng Michael), và quá trình thủy phân kiềm tiếp theo của nitrile nhóm trong hợp chất thu được vào một amide nhóm, và tạo vòng axit tiếp theo của sản phẩm vào glutethimide mong muốn.[10] Đồng phân (R) có tác dụng khởi phát nhanh hơn và hoạt tính chống co giật mạnh hơn trong mô hình động vật so với đồng phân (S).[11]

Xem thêm[sửa | sửa mã nguồn]
Tham khảo[sửa | sửa mã nguồn]
- ^ Barceloux, Donald G. (2012). Medical Toxicology of Drug Abuse: Synthesized Chemicals and Psychoactive Plants. Hoboken, N.J.: John Wiley & Sons, Inc. tr. 492–493. ISBN 978-0-471-72760-6.
- ^ Cookson, J. C. (1995). “Rebound exacerbation of anxiety during prolonged tranquilizer ingestion”. Journal of the Royal Society of Medicine. 88 (9): 544. PMC 1295346. PMID 7562864.
- ^ “Codeine and glutethimide. Euphoretic, addicting combination”. New York State Journal of Medicine. 75 (1): 97–99. 1975.
- ^ Havier, R. G.; Lin, R. (1985). “Deaths as a result of a combination of codeine and glutethimide”. Journal of Forensic Sciences. 30 (2): 563–6. PMID 3998703.
- ^ Popa, D.; Loghin, F.; Imre, S.; Curea, E. (2003). “The Study of Codeine-Gluthetimide Pharmacokinetic Interaction in Rats”. Journal of Pharmaceutical and Biomedical Analysis. 32 (4–5): 867–877. doi:10.1016/s0731-7085(03)00189-4. PMID 12899973.
- ^ Khajawall, A. M.; Sramek, J. J. Jr.; Simpson, G. M. (1982). “'Loads' Alert”. The Western Journal of Medicine. 137 (2): 166–168. PMC 1274052. PMID 7135952.
- ^ Paul Gahlinger (2003). “Chapter 19. Methaqualone and Glutethimide”. Illegal Drugs: A Complete Guide to Their History, Chemistry, Use, and Abuse.
- ^ Havier, R. G.; Lin, R. (1985). “Deaths as a Result of a Combination of Codeine and Glutethimide”. Journal of Forensic Sciences. 30 (2): 563–566. PMID 3998703.
- ^ Feuer, E.; French, J. (1984). “Descriptive Epidemiology of Mortality in New Jersey due to Combinations of Codeine and Glutethimide”. American Journal of Epidemiology. 119 (2): 202–207. PMID 6695899.
- ^
Tagmann, E.; Sury, E.; Hoffmann, K. (1952). “Über Alkylenimin-Derivate. 2. Mitteilung”. Helvetica Chimica Acta. 35 (5): 1541–1548. doi:10.1002/hlca.19520350516.
Đăng ký phát minh {{{country}}} {{{number}}}, "Verfahren zur Herstellung neuer Dioxopiperidine", trao vào [[{{{gdate}}}]]
Đăng ký phát minh {{{country}}} {{{number}}}, "3-disubstituted dioxopiperidines and the manufacture thereof", trao vào [[{{{gdate}}}]]
Salmon-Legagneur, F.; Neveu, C. (1952). Compt. Rend. 234: 1060.|title=trống hay bị thiếu (trợ giúp)
Salmon-Legagneur, F.; Neveu, C. (1953). Bull. Soc. Chim. France. 70.|title=trống hay bị thiếu (trợ giúp) - ^ Annual Report in Medicinal Chemistry Volume 12 page 13
