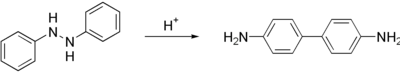Benzidine
| Benzidine | |
|---|---|
 | |
 | |
| Tên khác | Benzidine, di-phenylamine, diphenylamine, 4,4'-bianiline, 4,4'-biphenyldiamine, 1,1'-biphenyl-4,4'-diamine, 4,4'-diaminobiphenyl, p-diaminodiphenyl, p-benzidine |
| Nhận dạng | |
| Số CAS | |
| PubChem | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| Số RTECS | DC9625000 |
| Ảnh Jmol-3D | ảnh |
| SMILES | đầy đủ
|
| InChI | đầy đủ
|
| UNII | |
| Thuộc tính | |
| Công thức phân tử | C12H12N2 |
| Khối lượng mol | 184.24 g/mol |
| Bề ngoài | Bột tinh thể xám-vàng, đỏ-xám hoặc trắng[1] |
| Khối lượng riêng | 1.25 g/cm³ |
| Điểm nóng chảy | 122 đến 125 °C (395 đến 398 K; 252 đến 257 °F) |
| Điểm sôi | 400 °C (673 K; 752 °F) |
| Độ hòa tan trong nước | 0.94 g/100 mL ở 100 °C |
| MagSus | -110.9·10−6 cm³/mol |
| Các hợp chất liên quan | |
| Hợp chất liên quan | biphenyl |
| Các nguy hiểm | |
| Nguy hiểm chính | carcinogenic |
| PEL | occupational carcinogen[1] |
| Ký hiệu GHS |    |
| Báo hiệu GHS | Danger |
| Chỉ dẫn nguy hiểm GHS | H302, H350, H410 |
| Chỉ dẫn phòng ngừa GHS | P201, P202, P264, P270, P273, P281, P301+P312, P308+P313, P330, P391, P405, P501 |
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |
Benzidine (tên thông thường), còn được gọi là 1,1'-biphenyl-4,4'-diamine (tên hệ thống), là một hợp chất hữu cơ có công thức (C6H4NH2)2. Nó là một amin thơm và là một thành phần của một phản ứng xét nghiệm xyanua. Các dẫn xuất liên quan được sử dụng trong sản xuất thuốc nhuộm. Benzidine có liên quan đến các chứng ung thư tuyến tụy và ung thư bàng quang.[2]
Điều chế và tính chất[sửa | sửa mã nguồn]
Benzidine được điều chế theo quy trình hai bước từ nitrobenzene. Đầu tiên, nitrobenzene được chuyển thành 1,2-diphenylhydrazine, thường sử dụng bột sắt làm chất khử. Xử lý hydrazine này bằng acid khoáng tạo ra phản ứng sắp xếp lại thành 4,4'-benzidine. Một lượng nhỏ hơn các đồng phân khác của chất này cũng được hình thành.[3] Quá trình sắp xếp lại benzidine, được tiến hành giữa các phân tử, là một bài toán cổ điển trong hóa học hữu cơ.[4]
Sự chuyển đổi này được mô tả như một phản ứng [5,5] sigmatropic.[5][6]
Về tính chất vật lý, 4,4'-benzidine hòa tan kém trong nước lạnh nhưng có thể được kết tinh lại từ nước nóng, nơi nó kết tinh dưới dạng monohydrat. Nó là loài bazơ, các loài đã được deproto hóa có giá trị Ka 9,3×10−10 và 5,6×10−11. Các dung dịch của nó phản ứng với các chất oxy hóa để tạo ra các dẫn xuất liên quan đến quinone có màu đậm.
Ứng dụng[sửa | sửa mã nguồn]
Việc chuyển hóa benzidine thành muối bis(diazonium) đã từng là một bước không thể thiếu trong quá trình điều chế thuốc nhuộm trực tiếp (không cần chất kết dính). Xử lý muối bis(diazonium) này bằng acid 1-aminonaphthalene-4-sulfonic tạo ra thuốc nhuộm màu đỏ congo phổ biến một thời. Trước đây, benzidine được dùng để xét nghiệm sự tồn tại của máu. Một loại enzyme trong máu gây ra quá trình oxy hóa benzidine tạo thành một dẫn xuất có màu xanh lam đặc trưng. Xét nghiệm đối với cyanide dựa trên khả năng phản ứng tương tự. Các ứng dụng như vậy phần lớn đã được thay thế bằng các phương pháp sử dụng phenolphthalein/hydro peroxide và luminol.
Tham khảo[sửa | sửa mã nguồn]
- ^ a b “NIOSH Pocket Guide to Chemical Hazards #0051”. Viện An toàn và Sức khỏe Nghề nghiệp Quốc gia Hoa Kỳ (NIOSH).
- ^ “Known and Probable Carcinogens”. American Cancer Society. 29 tháng 6 năm 2011. Bản gốc lưu trữ ngày 17 tháng 3 năm 2008. Truy cập ngày 5 tháng 8 năm 2021.
- ^ “Benzidine and Benzidine Derivatives”, Bách khoa toàn thư Ullmann về Hóa chất công nghiệp, Weinheim: Wiley-VCH, 2005
- ^ March, J. (1992). Advanced Organic Chemistry (ấn bản 5). New York: J. Wiley and Sons. ISBN 0-471-60180-2.
- ^ Shine, H. J.; Zmuda, H.; Park, K. H.; Kwart, H.; Horgan, A. G.; Collins, C.; Maxwell, B. E. (1981). “Mechanism of the benzidine rearrangement. Kinetic isotope effects and transition states. Evidence for concerted rearrangement”. Journal of the American Chemical Society. 103 (4): 955–956. doi:10.1021/ja00394a047.
- ^ Shine, H. J.; Zmuda, H.; Park, K. H.; Kwart, H.; Horgan, A. G.; Brechbiel, M. (1982). “Benzidine rearrangements. 16. The use of heavy-atom kinetic isotope effects in solving the mechanism of the acid-catalyzed rearrangement of hydrazobenzene. The concerted pathway to benzidine and the nonconcerted pathway to diphenyline”. Journal of the American Chemical Society. 104 (9): 2501–2509. doi:10.1021/ja00373a028.