Prucalopride
 | |
| Dữ liệu lâm sàng | |
|---|---|
| Tên thương mại | Resolor, Resotran |
| AHFS/Drugs.com | Tên thuốc quốc tế |
| Giấy phép | |
| Danh mục cho thai kỳ |
|
| Dược đồ sử dụng | Oral |
| Mã ATC | |
| Tình trạng pháp lý | |
| Tình trạng pháp lý |
|
| Các định danh | |
Tên IUPAC
| |
| Số đăng ký CAS | |
| PubChem CID | |
| IUPHAR/BPS | |
| ChemSpider | |
| Định danh thành phần duy nhất | |
| KEGG | |
| Dữ liệu hóa lý | |
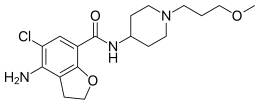
| Công thức hóa học | C18H26ClN3O3 |
| Khối lượng phân tử | 367.870 g/mol |
| Mẫu 3D (Jmol) | |
SMILES
| |
Định danh hóa học quốc tế
| |
| (kiểm chứng) | |
Prucalopride, tên thương hiệu Prudac, trong số những thuốc khác, là một loại thuốc đóng vai trò là chất chủ vận thụ thể 5-HT4 có chọn lọc, có ái lực cao [1] nhằm vào nhu động bị suy yếu liên quan đến táo bón mạn tính, do đó bình thường hóa nhu động ruột.[2][3][4][5][6][7] Prucalopride đã được phê duyệt để sử dụng ở châu Âu vào năm 2009,[8] ở Canada vào năm 2011 [9] và ở Israel vào năm 2014 [10] nhưng chỉ mới được Cục quản lý thực phẩm và dược phẩm phê duyệt gần đây để sử dụng ở Hoa Kỳ. Thuốc cũng đã được thử nghiệm để điều trị tắc nghẽn đường ruột mạn tính.[11][12]
Sử dụng trong y tế[sửa | sửa mã nguồn]
Các biện pháp chính về hiệu quả trong các thử nghiệm lâm sàng là ba hoặc nhiều lần đi tiêu hoàn toàn tự phát mỗi tuần; một biện pháp thứ cấp là tăng ít nhất một lần đi tiêu hoàn toàn tự phát mỗi tuần.[7][13][14] Các biện pháp khác là cải thiện PAC-QOL [15] (chất lượng đo lường cuộc sống) và PAC-SYM [16] (một loạt các triệu chứng phân, bụng và trực tràng liên quan đến táo bón mạn tính). Nhu động ruột không thường xuyên, đầy hơi, căng thẳng, đau bụng và đại tiện không có khả năng di tản có thể là triệu chứng nghiêm trọng, ảnh hưởng đáng kể đến chất lượng cuộc sống.[17][18][19][20][21]
Trong ba thử nghiệm lâm sàng lớn, 12 tuần điều trị với prucalopride 2 và 4 mg/ngày dẫn đến một tỷ lệ cao hơn đáng kể của bệnh nhân đạt đến điểm cuối hiệu quả chính của trung bình ≥3 nhu động ruột hoàn toàn tự phát so với giả dược.[7][13][14] Cũng có cải thiện đáng kể thói quen đại tiện và các triệu chứng liên quan, sự hài lòng của bệnh nhân với thói quen và điều trị ruột, và HR-QOL ở những bệnh nhân bị táo bón mạn tính nghiêm trọng, bao gồm cả những người không được giảm đau bằng các liệu pháp trước đó (> 80% số người tham gia thử nghiệm).[7][13][14] Sự cải thiện sự hài lòng của bệnh nhân với thói quen và điều trị ruột được duy trì trong suốt quá trình điều trị tới 24 tháng; điều trị prucalopride nói chung được dung nạp tốt.[22][23]
Chống chỉ định[sửa | sửa mã nguồn]
Prucalopride chống chỉ định khi có mẫn cảm với hoạt chất hoặc với bất kỳ tá dược nào, suy thận cần lọc máu, thủng ruột hoặc tắc nghẽn do rối loạn cấu trúc hoặc chức năng của thành ruột, tắc ruột, tình trạng viêm nặng của đường ruột như bệnh Crohn, và viêm loét đại tràng và megacolon/megarectum ngộ độc.[24]
Tác dụng phụ[sửa | sửa mã nguồn]
Prucalopride đã được dùng bằng đường uống cho ~ 2700 bệnh nhân bị táo bón mạn tính trong các thử nghiệm lâm sàng có kiểm soát. Các tác dụng phụ được báo cáo thường xuyên nhất là đau đầu và các triệu chứng tiêu hóa (đau bụng, buồn nôn hoặc tiêu chảy). Phản ứng như vậy xảy ra chủ yếu khi bắt đầu điều trị và thường biến mất trong vài ngày sau khi tiếp tục điều trị.[24]
Cơ chế hoạt động[sửa | sửa mã nguồn]
Prucalopride, một chất đầu tiên trong lớp dihydro-benzofuran-carboxamide, là một chất chủ vận thụ thể serotonin có ái lực cao (5-HT4) với các hoạt động enterokinetic.[24] Prucalopride làm thay đổi mô hình vận động của đại tràng thông qua kích thích thụ thể serotonin 5-HT4: nó kích thích các chuyển động khối đại tràng, cung cấp lực đẩy chính cho đại tiện.
Các hiệu ứng quan sát được phát huy thông qua hành động chọn lọc cao trên các thụ thể 5-HT4:[24] prucalopride có ái lực cao hơn 150 lần đối với các thụ thể 5-HT4 so với các thụ thể khác.[1][25] Prucalopride khác với các chất chủ vận 5-HT4 khác như tegaserod và cisapride, ở nồng độ trị liệu cũng tương tác với các thụ thể khác (5-HT1B/D và kênh ether a-go-go K + của tim người tương ứng) và điều này có thể giải thích cho các biến cố tim mạch bất lợi dẫn đến sự hạn chế của các loại thuốc này.[25] Các thử nghiệm lâm sàng đánh giá tác dụng của prucalopride trên khoảng QT và các tác dụng phụ liên quan không chứng minh sự khác biệt đáng kể so với giả dược.[24]
Dược động học[sửa | sửa mã nguồn]
Prucalopride được hấp thu nhanh chóng (Cmax đạt được 2 giờ 3 giờ sau khi 2 mg liều uống) và được phân phối rộng rãi. Trao đổi chất không phải là con đường thải trừ chính. Trong ống nghiệm, sự trao đổi chất ở gan của con người rất chậm và chỉ có một lượng nhỏ chất chuyển hóa được tìm thấy. Một phần lớn hoạt chất được bài tiết dưới dạng không đổi (khoảng 60% liều dùng trong nước tiểu và ít nhất 6% trong phân). Bài tiết qua thận của prucalopride không thay đổi liên quan đến cả quá trình lọc thụ động và bài tiết chủ động. Độ thanh thải trong huyết tương trung bình là 317 ml/phút, thời gian bán hủy của thiết bị đầu cuối là 24 giờ 30 giờ,[26] và đạt trạng thái ổn định trong vòng 3 Lần4. Điều trị một lần mỗi ngày với 2 mg prucalopride, nồng độ trong huyết tương ở trạng thái ổn định dao động giữa giá trị máng và đỉnh là 2,5 và 7 ng/ml, tương ứng.[24]
Dữ liệu in vitro chỉ ra rằng prucalopride có khả năng tương tác thấp và nồng độ điều trị của prucalopride dự kiến sẽ không ảnh hưởng đến chuyển hóa qua trung gian CYP của các sản phẩm thuốc dùng chung.[24]
Sự chấp thuận[sửa | sửa mã nguồn]
Trong Khu vực kinh tế châu Âu, prucalopride ban đầu được chấp thuận để điều trị triệu chứng táo bón mạn tính ở những phụ nữ mà thuốc nhuận tràng không cung cấp cứu trợ đầy đủ.[24] Sau đó, nó đã được Ủy ban châu Âu chấp thuận cho sử dụng ở người lớn - nghĩa là, bao gồm cả bệnh nhân nam - cho cùng một chỉ định.[27]
Tham khảo[sửa | sửa mã nguồn]
- ^ a b Briejer, M. R.; Bosmans, J. P.; Van Daele, P.; Jurzak, M.; Heylen, L.; Leysen, J. E.; Prins, N. H.; Schuurkes, J. A. (2001). “The in vitro pharmacological profile of prucalopride, a novel enterokinetic compound”. European Journal of Pharmacology. 423 (1): 71–83. doi:10.1016/S0014-2999(01)01087-1. PMID 11438309.
- ^ Clinical trial number [1] for "NCT00793247" at ClinicalTrials.gov
- ^ Emmanuel, A. V.; Kamm, M. A.; Roy, A. J.; Kerstens, R.; Vandeplassche, L. (2012). “Randomised clinical trial: The efficacy of prucalopride in patients with chronic intestinal pseudo-obstruction - a double-blind, placebo-controlled, cross-over, multiple n = 1 study”. Alimentary Pharmacology & Therapeutics. 35 (1): 48–55. doi:10.1111/j.1365-2036.2011.04907.x. PMC 3298655. PMID 22061077.
- ^ Smart, C. J.; Ramesh, A. N. (2011). “The successful treatment of acute refractory pseudo-obstruction with Prucalopride”. Colorectal Disease. 14 (8): e508. doi:10.1111/j.1463-1318.2011.02929.x. PMID 22212130.
- ^ Bouras, E. P.; Camilleri, M.; Burton, D. D.; McKinzie, S. (1999). “Selective stimulation of colonic transit by the benzofuran 5HT4 agonist, prucalopride, in healthy humans”. Gut. 44 (5): 682–686. doi:10.1136/gut.44.5.682. PMC 1727485. PMID 10205205.
- ^ Bouras, E. P.; Camilleri, M.; Burton, D. D.; Thomforde, G.; McKinzie, S.; Zinsmeister, A. R. (2001). “Prucalopride accelerates gastrointestinal and colonic transit in patients with constipation without a rectal evacuation disorder”. Gastroenterology. 120 (2): 354–360. doi:10.1053/gast.2001.21166. PMID 11159875.
- ^ a b c d Tack, J.; Van Outryve, M.; Beyens, G.; Kerstens, R.; Vandeplassche, L. (2008). “Prucalopride (Resolor) in the treatment of severe chronic constipation in patients dissatisfied with laxatives”. Gut. 58 (3): 357–365. doi:10.1136/gut.2008.162404. PMID 18987031.
- ^ “European Medicines Agency -EPAR”. Bản gốc lưu trữ ngày 31 tháng 1 năm 2010. Truy cập ngày 22 tháng 8 năm 2019.
- ^ “Health Canada, Notice of Decision for Resotran”. hc-sc.gc.ca. Bản gốc lưu trữ ngày 18 tháng 3 năm 2017. Truy cập ngày 1 tháng 5 năm 2018.
- ^ “Digestive Remedies in Israel”. www.euromonitor.com. Lưu trữ bản gốc ngày 13 tháng 3 năm 2018. Truy cập ngày 1 tháng 5 năm 2018.
- ^ Briejer, M. R.; Prins, N. H.; Schuurkes, J. A. (2001). “Effects of the enterokinetic prucalopride (R093877) on colonic motility in fasted dogs”. Neurogastroenterology and Motility. 13 (5): 465–472. doi:10.1046/j.1365-2982.2001.00280.x. PMID 11696108.
- ^ Oustamanolakis, P.; Tack, J. (2012). “Prucalopride for chronic intestinal pseudo-obstruction”. Alimentary Pharmacology & Therapeutics. 35 (3): 398–9. doi:10.1111/j.1365-2036.2011.04947.x. PMID 22221087.
- ^ a b c Camilleri, M.; Kerstens, R.; Rykx, A.; Vandeplassche, L. (2008). “A Placebo-Controlled Trial of Prucalopride for Severe Chronic Constipation”. New England Journal of Medicine. 358 (22): 2344–2354. doi:10.1056/NEJMoa0800670. PMID 18509121.
- ^ a b c Quigley, E. M. M.; Vandeplassche, L.; Kerstens, R.; Ausma, J. (2009). “Clinical trial: the efficacy, impact on quality of life, and safety and tolerability of prucalopride in severe chronic constipation – a 12-week, randomized, double-blind, placebo-controlled study”. Alimentary Pharmacology & Therapeutics. 29 (3): 315–328. doi:10.1111/j.1365-2036.2008.03884.x. PMID 19035970.
- ^ Marquis, P.; De La Loge, C.; Dubois, D.; McDermott, A.; Chassany, O. (2005). “Development and validation of the Patient Assessment of Constipation Quality of Life questionnaire”. Scandinavian Journal of Gastroenterology. 40 (5): 540–551. doi:10.1080/00365520510012208. PMID 16036506.
- ^ Frank, L.; Kleinman, L.; Farup, C.; Taylor, L.; Miner Jr, P. (1999). “Psychometric validation of a constipation symptom assessment questionnaire”. Scandinavian Journal of Gastroenterology. 34 (9): 870–877. doi:10.1080/003655299750025327. PMID 10522604.
- ^ Johanson, JF; Kralstein, J (2007). “Chronic constipation: a survey of the patient perspective”. Alimentary Pharmacology & Therapeutics. 25 (5): 599–608. doi:10.1111/j.1365-2036.2006.03238.x. PMID 17305761.
- ^ Koch, A.; Voderholzer, W. A.; Klauser, A. G.; Müller-Lissner, S. (1997). “Symptoms in chronic constipation”. Diseases of the Colon and Rectum. 40 (8): 902–906. doi:10.1007/BF02051196. PMID 9269805.
- ^ McCrea, G. L.; Miaskowski, C.; Stotts, N. A.; MacEra, L.; Paul, S. M.; Varma, M. G. (2009). “Gender differences in self-reported constipation characteristics, symptoms, and bowel and dietary habits among patients attending a specialty clinic for constipation”. Gender Medicine. 6 (1): 259–271. doi:10.1016/j.genm.2009.04.007. PMID 19467522.
- ^ Pare, P.; Ferrazzi, S.; Thompson, W. G.; Irvine, E. J.; Rance, L. (2001). “An epidemiological survey of constipation in Canada: definitions, rates, demographics, and predictors of health care seeking”. The American Journal of Gastroenterology. 96 (11): 3130–3137. doi:10.1111/j.1572-0241.2001.05259.x. PMID 11721760.
- ^ Wald, A.; Scarpignato, C.; Kamm, M. A.; Mueller-Lissner, S.; Helfrich, I.; Schuijt, C.; Bubeck, J.; Limoni, C.; Petrini, O. (2007). “The burden of constipation on quality of life: results of a multinational survey”. Alimentary Pharmacology & Therapeutics. 26 (2): 227–236. doi:10.1111/j.1365-2036.2007.03376.x. PMID 17593068.
- ^ Camilleri, M; Beyens, G; Kerstens, R; Vandeplassche, L (2009). “Long-term follow-up of safety and satisfaction with bowel function in response to oral prucalopride in patients with chronic constipation [Abstract]”. Gastroenterology. 136 (Suppl 1): 160. doi:10.1016/s0016-5085(09)60143-8.
- ^ Van Outryve, MJ; Beyens, G; Kerstens, R; Vandeplassche, L (2008). “Long-term follow-up study of oral prucalopride (Resolor) administered to patients with chronic constipation [Abstract T1400]”. Gastroenterology. 134 (4 (suppl 1)): A547. doi:10.1016/s0016-5085(08)62554-8.
- ^ a b c d e f g h SmPC. Summary of product characteristics Resolor (prucalopride) October, 2009: 1-9.
- ^ a b De Maeyer, JH; Lefebvre, RA; Schuurkes, JA (tháng 2 năm 2008). “5-HT(4) receptor agonists: similar but not the same”. Neurogastroenterol Motil. 20 (2): 99–112. doi:10.1111/j.1365-2982.2007.01059.x. PMID 18199093.
- ^ Frampton, J. E. (2009). “Prucalopride”. Drugs. 69 (17): 2463–2476. doi:10.2165/11204000-000000000-00000. PMID 19911858.
- ^ “Shire Receives European Approval to Use Resolor® (prucalopride) in Men for the Symptomatic Treatment of Chronic Constipation”. www.shire.com. Lưu trữ bản gốc ngày 21 tháng 11 năm 2017. Truy cập ngày 1 tháng 5 năm 2018.
