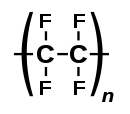
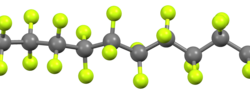
Polytetrafluoroethylen
| Polytetrafluoroethylen | |
|---|---|
 | |
 | |
| Danh pháp IUPAC | poly(1,1,2,2-tetrafluoroethylene)[1] |
| Tên khác | Syncolon, Fluon, Poly(tetrafluoroethene), Poly(difluoromethylene), Poly(tetrafluoroethylene) |
| Nhận dạng | |
| Viết tắt | PTFE |
| Số CAS | |
| KEGG | |
| ChEBI | |
| Thuộc tính | |
| Công thức phân tử | (C2F4)n |
| Khối lượng riêng | 2200 kg/m³ |
| Điểm nóng chảy | 600 K 327 °C |
| Điểm sôi | |
| Độ dẫn nhiệt | 0.25 W/(m·K) |
| Các nguy hiểm | |
| NFPA 704 |
|
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |
Polytetrafluoroethylen là một chất fluoropolymer tổng hợp của tetrafluoroethylene có nhiều ứng dụng công nghiệp. Nhãn hiệu nổi tiếng nhất của công thức dựa trên chất này là Teflon của công ty Chemours[2]. Chemours là một công ty spin-off năm 2015 của DuPont Co,[3] nơi phát hiện ra hợp chất này vào năm 1938.[2]
Lịch sử[sửa | sửa mã nguồn]
Tháng 4 năm 1938, Roy J. Plunkett, lúc ấy đang làm việc ở Phòng thí nghiệm hãng DuPont quyết định thử dùng tetrafluoroethylen làm khí sinh hàn cho máy lạnh. Ông mở van một bình thép chứa khí nén không thấy có khí thoát ra, cân lại thấy khối lượng bình không đổi. "Van không hỏng, khí đi đằng nào", ông bắt đầu cảm thấy tò mò. Ông cưa đôi bình thép và thấy một lớp polyme bám chặt phía trong thành bình, hơ nóng không chảy, trơ với mọi hoá chất mà ông thử. Đó chính là teflon.[4]
Tính chất[sửa | sửa mã nguồn]
- Không bị giòn đi trong không khí lỏng, không mềm đi trong nước đun sôi, không biến đổi trạng thái trong khoảng từ -190 °C đến 300 °C[5]
- Rất bền với các tác nhân hoá học (không tác dụng với dung dịch acid, base đậm đặc, với các tác nhân oxy hoá mạnh (nước cường thủy)
- Có hệ số ma sát rất nhỏ (0,04), độ bền nhiệt cao (tới 400 °C mới bắt đầu thăng hoa), không nóng chảy, phân huỷ chậm
- Cách điện tốt, không chịu ảnh hưởng của điện từ trường[5]
Ứng dụng[sửa | sửa mã nguồn]
Teflon được sử dụng rộng rãi vào nhiều ngành công nghiệp: công nghiệp đông lạnh, công nghiệp hoá học, công nghiệp điện, công nghiệp thực phẩm, công nghiệp y dược,... Cụ thể, teflon được dùng để:
- Chế tạo thiết bị nhiệt độ thấp để chứa đựng không khí lỏng
- Chế tạo các bình phản ứng chịu ăn mòn, vỏ bình acquy, làm tấm lọc
- Chế tạo các lớp vỏ cách điện rất mỏng, chỉ cần 15 micromet là đã có một màng cách điện hoàn hảo
- Chế tạo xương nhân tạo, làm vật liệu tạo sụn cho ngoại khoa
- Chế tạo rađa, vật liệu thông tin cao tần, thiết bị sóng ngắn
- Tráng phủ lên chảo, nồi để chống dính[5]
- Sử dụng làm chất chống ma sát trong ngành cầu đường.
- Sử dụng làm các loại màng chống dính trong ngành bơm công nghiệp như bơm màng đôi hay bơm định lượng chất lỏng...
- Làm chất sơn chống nóng trên các bộ phận xe máy, xe hơi như pô xe để chống phỏng nặng khi va quẹt với cơ thể người và chống gỉ sét.
- Trong công nghệ cao nó được sơn phủ lên một số phương tiện quốc phòng để chống sóng ra đa, chống ma sát làm tăng tốc độ của phương tiện!
- Trong máy móc nó có thể thay thế một số bạc thau đồng trong các lõi trục mô-tơ loại nhỏ.
- Được dùng để làm chỉ nha khoa.
Điều chế[sửa | sửa mã nguồn]
Teflon được sản xuất từ chloroform theo sơ đồ sau
CHCl3 +HF/SbF5> CHF2Cl 700 °C> CF2=CF2 peroxide> (CF2-CF2)n[5]
Tham khảo[sửa | sửa mã nguồn]
- ^ “poly(tetrafluoroethylene) (CHEBI:53251)”. ebi.ac.uk. Truy cập ngày 12 tháng 7 năm 2012.
- ^ a b “Teflon ™| Chemours Teflon™ Nonstick Coatings and Additives”. www.chemours.com. Bản gốc lưu trữ 4 Tháng Ba năm 2016. Truy cập ngày 1 tháng 3 năm 2016.
- ^ “DuPont - DuPont Completes Spin-off of The Chemours Company”. investors.dupont.com. Bản gốc lưu trữ ngày 6 tháng 3 năm 2016. Truy cập ngày 1 tháng 3 năm 2016.
- ^ Hóa học 11 Nâng cao (sách giáo khoa Việt Nam), tr. 183
- ^ a b c d Hóa học 12 (sách giáo khoa Việt Nam), tr. 73

