Hydroni
| Hydroni | |||
|---|---|---|---|
| |||
| |||
| Danh pháp IUPAC | oxoni | ||
| Tên khác | ion hydroni | ||
| Nhận dạng | |||
| Số CAS | |||
| Thuộc tính | |||
| Công thức phân tử | H3O+ | ||
| Khối lượng mol | 19,02322 g/mol | ||
| Điểm nóng chảy | |||
| Điểm sôi | |||
| Độ axit (pKa) | -1,7 | ||
| Các nguy hiểm | |||
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |||
Trong hóa học, hydroni là tên gọi chung của ion nước H3O+, loại ion oxonium được tạo ra bởi sự proton hóa của nước. Đó là ion dương có mặt khi acid Arrhenius hòa tan trong nước, vì các phân tử acid Arrhenius trong dung dịch nhường một proton (ion hydro dương, H+) cho các phân tử nước xung quanh (H2O).
Xác định độ pH[sửa | sửa mã nguồn]
Tỷ lệ giữa các ion hydroni và ion hydroxide quyết định độ pH của dung dịch. Các phân tử trong nước tinh khiết tự động phân ly (nghĩa là: phản ứng với nhau) thành các ion hydroni và hydroxide ở trạng thái cân bằng sau:
Trong nước tinh khiết, có một số lượng bằng nhau các ion hydroxide và hydroni, vì vậy nó trung tính. Ở nhiệt độ 25 ℃, nước có độ pH là 7 (điều này thay đổi khi nhiệt độ thay đổi). Giá trị pH nhỏ hơn 7 chỉ ra dung dịch acid và giá trị pH lớn hơn 7 chỉ ra dung dịch base.
Danh pháp[sửa | sửa mã nguồn]
Theo danh pháp hóa học hữu cơ của IUPAC, ion hydroni nên được gọi là oxoni.[1] Hydroxoni cũng có thể được sử dụng rõ ràng để xác định nó. Một đề xuất dự thảo của IUPAC cũng khuyến nghị sử dụng oxonium và oxyani trong bối cảnh hóa học hữu cơ và vô cơ.
Một ion oxoni là bất kỳ ion nào có catot oxy hóa trị ba. Ví dụ, nhóm hydroxyl được proton hóa là ion oxoni, nhưng không phải là ion hydroni.
Kết cấu[sửa | sửa mã nguồn]
Vì O+
và N có cùng số electron, H3O+ là đẳng lượng với amonia. Như thể hiện trong các hình ảnh trên, H3O+ có dạng hình học phân tử hình chóp tam giác với nguyên tử oxy ở đỉnh của nó. Góc liên kết của H hạng O hạng H là khoảng 113°,[2] và tâm khối lượng rất gần với nguyên tử oxy. Bởi vì cơ sở của kim tự tháp được tạo thành từ ba nguyên tử hydro giống hệt nhau, H3O+.Cấu hình đỉnh đối xứng của phân tử H3O+ sao cho thuộc nhóm điểm C3v. Do tính đối xứng này và thực tế là nó có mômen lưỡng cực, quy tắc chọn xoay là ΔJ = ± 1 và Δ K = 0. Lưỡng cực chuyển tiếp nằm dọc theo c -axis và, vì điện tích âm được định vị gần nguyên tử oxy, nên mômen lưỡng cực chỉ vào đỉnh, vuông góc với mặt phẳng cơ sở.
Acid và tính acid[sửa | sửa mã nguồn]
Hydroni là catot hình thành từ nước với sự có mặt của các ion hydro. Những hydron này không tồn tại ở trạng thái tự do - chúng cực kỳ phản ứng và bị hòa tan bởi nước. Một chất tan có tính acid nói chung là nguồn hydron; tuy nhiên, hydroni tồn tại ngay cả trong nước tinh khiết. Trường hợp đặc biệt này của nước phản ứng với nước để tạo ra các ion hydroni (và hydroxide) thường được gọi là tự ion hóa nước. Các ion hydroni thu được rất ít và tồn tại trong thời gian ngắn. pH là thước đo hoạt động tương đối của các ion hydroni và hydroxide trong dung dịch nước. Trong các dung dịch acid, hydroni hoạt động mạnh hơn, proton dư thừa của nó sẵn sàng cho phản ứng với các base.
Các ion hydroni có tính acid mạnh: ở 25 ℃, pKa của nó là 0.[3] Đây là loài có tính acid nhất có thể tồn tại trong nước (giả sử đủ nước để hòa tan): bất kỳ acid mạnh hơn sẽ làm ion hóa và proton hóa một phân tử nước để tạo thành hydroni. Độ acid của hydroni là tiêu chuẩn ngầm được sử dụng để đánh giá độ bền của acid trong nước: acid mạnh phải là chất cho proton tốt hơn hydroni, nếu không, một phần acid đáng kể sẽ tồn tại ở trạng thái không bị ion hóa (ví dụ: acid yếu). Không giống như hydroni trong các dung dịch trung tính do sự tự phân ly của nước, các ion hydroni trong các dung dịch acid là lâu dài và tập trung, tỷ lệ với sức mạnh của acid hòa tan.
Độ pH ban đầu được hình thành là thước đo nồng độ ion hydro của dung dịch nước.[4] Bây giờ chúng ta biết rằng hầu như tất cả các proton tự do như vậy nhanh chóng phản ứng với nước để tạo thành hydroni; Do đó tính acid của dung dịch nước được đặc trưng chính xác hơn bởi nồng độ hydroni của nó. Trong các tổng hợp hữu cơ, như phản ứng xúc tác acid, ion hydroni (H3O+) có thể được sử dụng thay thế cho nhau với ion H+.
Giải quyết[sửa | sửa mã nguồn]
Các nhà nghiên cứu vẫn chưa mô tả đầy đủ sự hòa tan của ion hydroni trong nước, một phần vì có nhiều ý nghĩa khác nhau của sự hòa tan tồn tại. Một nghiên cứu suy giảm điểm đóng băng đã xác định rằng ion hydrat trong nước lạnh xấp xỉ H
3O+
(H
2O)
6[5], mỗi ion hydroni được hòa tan bởi 6 phân tử nước không thể hòa tan các phân tử chất tan khác.
Một số cấu trúc hydrat hóa khá lớn: H
3O+
(H
2O)
20 kỳ diệu cấu trúc số ion (gọi tắt là kỳ diệu vì sự ổn định tăng của nó đối với các cấu trúc hydrat hóa liên quan đến một số so sánh của các phân tử nước với - đây là một cách sử dụng tương tự của sự kỳ diệu từ như trong vật lý hạt nhân) có thể đặt hydroni bên trong một quanh khối lồng.[6] Tuy nhiên, các mô phỏng động lực học phân tử phương pháp ab initio gần đây đã chỉ ra rằng, trung bình, proton ngậm nước nằm trên bề mặt của cụm H
3O+
(H
2O)
20.[7] Hơn nữa, một số tính năng khác nhau của các mô phỏng này đồng ý với các đối tác thử nghiệm của họ cho thấy một cách giải thích khác về kết quả thử nghiệm.
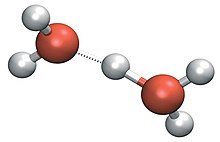
Một tính toán năm 2007 của các enthalpies và năng lượng miễn phí của các trái phiếu khác nhau hydro xung quanh catốt hydroni trong nước proton hóa lỏng[8] ở nhiệt độ phòng và một nghiên cứu của các proton hopping cơ chế sử dụng động lực học phân tử cho thấy rằng các ion hydro trái phiếu Chính phủ xung quanh ion hydroni (được hình thành với ba phối tử nước trong lớp vỏ hòa tan đầu tiên của hydroni) khá mạnh so với các khối nước.
Tham khảo[sửa | sửa mã nguồn]
- ^ “Table 17 Mononuclear parent onium ions”. IUPAC.
- ^ Tang, Jian; Oka, Takeshi (1999). “Infrared spectroscopy of Bản mẫu:H3O+: the v1 fundamental band”. Journal of Molecular Spectroscopy. 196 (1): 120–130. Bibcode:1999JMoSp.196..120T. doi:10.1006/jmsp.1999.7844. PMID 10361062.
- ^ Meister, Erich; Willeke, Martin; Angst, Werner; Togni, Antonio; Walde, Peter (2014). “Confusing Quantitative Descriptions of Brønsted-Lowry Acid-Base Equilibria in Chemistry Textbooks – A Critical Review and Clarifications for Chemical Educators”. Helv. Chim. Acta. 97 (1): 1–31. doi:10.1002/hlca.201300321. Truy cập ngày 20 tháng 3 năm 2017.
- ^ Sorensen, S. P. L. (1909). “Ueber die Messung und die Bedeutung der Wasserstoffionenkonzentration bei enzymatischen Prozessen”. Biochemische Zeitschrift (bằng tiếng Đức). 21: 131–304.
- ^ Zavitsas, A. A. (2001). “Properties of water solutions of electrolytes and nonelectrolytes”. The Journal of Physical Chemistry B. 105 (32): 7805–7815. doi:10.1021/jp011053l.
- ^ Hulthe, G.; Stenhagen, G.; Wennerström, O.; Ottosson, C-H. (1997). “Water cluster studied by electrospray mass spectrometry”. Journal of Chromatography A. 512: 155–165. doi:10.1016/S0021-9673(97)00486-X.
- ^ Iyengar, S. S.; Petersen, M. K.; Burnham, C. J.; Day, T. J. F.; Voth, G. A.; Voth, G. A. (2005). “The Properties of Ion-Water Clusters. I. The Protonated 21-Water Cluster” (PDF). The Journal of Chemical Physics. 123 (8): 084309. Bibcode:2005JChPh.123h4309I. doi:10.1063/1.2007628. PMID 16164293.
- ^ Markovitch, O.; Agmon, N. (2007). “Structure and Energetics of the Hydronium Hydration Shells” (PDF). The Journal of Physical Chemistry A. 111 (12): 2253–6. Bibcode:2007JPCA..111.2253M. doi:10.1021/jp068960g. PMID 17388314. Bản gốc (PDF) lưu trữ ngày 31 tháng 8 năm 2018. Truy cập ngày 12 tháng 2 năm 2019.
Đọc thêm[sửa | sửa mã nguồn]
- Sách giáo khoa hoá học 11, Nhà xuất bản Giáo dục
| Wikimedia Commons có thêm hình ảnh và phương tiện truyền tải về Hydroni. |




