Kênh ion cảm ứng acid
| Acid-sensing sodium channel | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| |||||||||
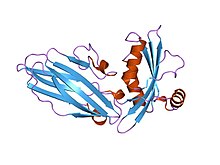
| Structure of acid-sensing ion channel 1.[1] | |||||||||
| Danh pháp | |||||||||
| Ký hiệu | ASC | ||||||||
| Pfam | PF00858 | ||||||||
| InterPro | IPR001873 | ||||||||
| PROSITE | PDOC00926 | ||||||||
| SCOP | 2qts | ||||||||
| TCDB | 1.A.6 | ||||||||
| OPM family | 181 | ||||||||
| OPM protein | 4fz1 | ||||||||
| |||||||||
Các kênh ion cảm ứng axit (ASIC) là các kênh natri không nhạy cảm với điện thế thần kinh được kích hoạt bởi các proton ngoại bào thấm vào Na +. ASIC1 cũng cho thấy độ thấm Ca 2+ thấp.[2] Protein ASIC là một phân họ của siêu họ ENaC / Deg của các kênh ion. Những gen này có các biến thể mối nối mã hóa cho một số đồng phân được đánh dấu bằng hậu tố. Ở động vật có vú, các kênh ion cảm nhận axit (ASIC) được mã hóa bởi năm gen tạo ra các tiểu đơn vị protein ASIC: ASIC1, ASIC2, ASIC3, ASIC4 và ASIC5.[3] Ba trong số các tiểu đơn vị protein này tập hợp lại để tạo thành ASIC, có thể kết hợp thành cả hai kênh đồng âm và dị thể thường thấy ở cả hệ thần kinh trung ương và hệ thần kinh ngoại biên.[2] Tuy nhiên, ASIC phổ biến nhất là ASIC1a và ASIC1a / 2a và ASIC3. ASIC2b tự nó không hoạt động nhưng điều chỉnh hoạt động kênh khi tham gia vào các dị vòng và ASIC4 không có chức năng được biết đến. Trên phạm vi rộng, ASIC là mục tiêu ma túy tiềm năng do có liên quan đến các tình trạng bệnh lý như tổn thương võng mạc, co giật và chấn thương não do thiếu máu cục bộ.[4][4][5][5]
Kết cấu
[sửa | sửa mã nguồn]Mỗi kênh ion cảm nhận axit bao gồm một chuỗi amino acid 500-560, được xây dựng thành một phân đoạn sáu màng tế bào hai hai tiểu đơn vị (TMD1 và TMD2), một amino-carboxyl termini và một miền ngoại bào lớn.[3] Các miền termini amino-carboxyl nội bào rất quan trọng đối với các tương tác và điều chế protein nội bào của kênh, tính thấm của ion và giao phối. Tuy nhiên, gating và cơ học của từng kênh ion cảm nhận axit được xác định bởi sự kết hợp của các tiểu đơn vị ASIC tạo thành cấu trúc của nó.[3]
Pore
[sửa | sửa mã nguồn]Các cơ chế của chức năng lỗ rỗng là cơ bản cho cấu trúc của kênh. Giữa ba tiểu đơn vị ASIC1, một đường hầm kéo dài từ đỉnh của các miền ngoại bào đến tế bào chất của tế bào. Đường hầm trung tâm chạy trực tiếp giữa các đơn vị trimeric, nơi nó có các khu vực hạn chế lớn thay đổi kích thước và hình dạng tùy thuộc vào trạng thái kênh.[3]
Hai miền xuyên màng (TMD1 và TMD2) của mỗi trong ba tiểu đơn vị ASIC chịu trách nhiệm cho lỗ rỗng của kênh. TMD2 chủ yếu liên quan đến lớp lót của lum trong lỗ chân lông và cổng bất hoạt của kênh, khi TMD1 giữ protein trong lớp màng lipid kép của tế bào.[6] TMD1 được kết nối với các tấm của miền ngoại bào uốn cong để mở rộng miền ngoại bào để cho phép ion đi qua kênh.[3] Ở giữa các phân đoạn TMD2 nằm trong bộ lọc chọn lọc tạo thành phần hẹp nhất của lỗ chân lông, chịu trách nhiệm cho phép ASIC cho phép chủ yếu là Na +. Đối với ASIC1, chín dư lượng amino acid, ba phần được đóng góp bởi mỗi tiểu đơn vị ASIC (Gly443, Ala444, Ser445), tạo thành bộ lọc chọn lọc. Biệt danh là "vành đai GAS", cả ba carbonyl oxygens đều có lỗ chân lông, tạo ra một tiềm năng tiêu cực góp phần vào sự dẫn điện của các cation.[3] Dư lượng amino acid cụ thể của aspartate trên lòng bên ngoại bào của TMD2 trong ASIC1 đã được liên kết với độ dẫn Ca 2+ thấp của kênh. Ngoài ra, dư lượng n-termini của vùng xuyên màng cũng cho thấy sự chọn lọc đối với Na +, do các đột biến trong vùng này đã thay đổi chức năng và độ dẫn Na +.[3]
Khu vực ngoại bào
[sửa | sửa mã nguồn]ASIC có một khu vực ngoại bào giống như nắm tay lớn, tiêu thụ hầu hết cấu trúc protein. Trong cấu trúc "giống như nắm tay" của nó có một miền cổ tay, lòng bàn tay, ngón tay, đốt ngón tay, ngón cái và-ball. "Lòng bàn tay" chiếm phần lớn miền ngoại bào, được hình thành bởi bảy tấm,, trong đó phần còn lại của các miền cấu trúc thứ cấp bao gồm các phân đoạn xoắn ốc.[3] Được phân biệt bởi các cấu hình amino acid cụ thể của nó, khu vực ngoại bào là cơ bản cho việc kích hoạt / bất hoạt cùng với gating pH. Vùng vòng β tờ cụ thể giữa miền "lòng bàn tay" và "ngón tay cái" đã cho thấy sự liên quan đến sự truyền tín hiệu từ miền ngoại bào sang vùng xuyên màng, dẫn đến sự thay đổi về hình dạng của ASIC sang trạng thái mở.[3] Tuy nhiên, vẫn chưa có kết luận về việc dư lượng cụ thể nào tương tác với các proton để kích hoạt kênh. Trong năm 2009, các nghiên cứu có thể đã thiết lập mối quan hệ giữa dư lượng thơm Tyr72, Pro287 và Trp288 và proton-gating của ASIC.[3] Những dư lượng này tạo thành một túi axit thể hiện tiềm năng tĩnh điện chịu trách nhiệm cho sự phụ thuộc pH trong kích hoạt và điều chế kênh.[7] Túi này trong miền ngoại bào hoạt động như một dự trữ cho các cation tập trung để hỗ trợ thêm cho dòng Na +. Glycosyl hóa cũng rõ ràng trong khu vực ngoại bào, đóng một vai trò quan trọng trong việc buôn bán kênh đến bề mặt của màng cũng như thiết lập độ nhạy của ASIC với mức độ pH. Bằng chứng thực nghiệm sâu hơn đã chỉ ra rằng Ca 2+ cũng có thể đóng vai trò nòng cốt trong việc điều chỉnh ái lực proton của ASIC giao phối cả trong lỗ chân lông và trên miền ngoại bào.[3]
Chức năng
[sửa | sửa mã nguồn]Vai trò của ASIC là cảm nhận mức độ pH ngoại bào giảm và dẫn đến phản ứng hoặc tín hiệu từ tế bào thần kinh. Phối tử liên kết với vị trí kích hoạt từ lâu đã được cho là độc quyền của các proton; tuy nhiên, các nghiên cứu gần đây đã chỉ ra rằng ASIC4 và ASIC1 có thể được kích hoạt ở mức độ pH bình thường, chỉ ra các loại chất kết dính phối tử khác.[8] Trong điều kiện axit tăng lên, một proton liên kết với kênh trong khu vực ngoại bào, kích hoạt kênh ion để trải qua sự thay đổi về hình dạng do đó mở ra miền xuyên màng 2 (TMD2). Điều này dẫn đến dòng ion natri chảy qua lum của TMD2. Tất cả các ASIC đều đặc biệt thấm vào các ion natri. Biến thể duy nhất là ASIC1a cũng có độ thấm thấp đối với các ion calci. Dòng của các cation này dẫn đến khử cực màng. Các kênh Ca 2+ được kiểm soát điện áp được kích hoạt dẫn đến dòng calci tràn vào tế bào. Điều này gây ra sự khử cực của tế bào thần kinh và một phản ứng kích thích được giải phóng. Trong ASIC1a, Ca 2+ tăng bên trong tế bào là kết quả của việc truyền calci trực tiếp qua kênh.[8]
Sau khi kích hoạt, ASIC có thể tiếp tục kích hoạt vô số protein effector khác nhau và các phân tử tín hiệu dẫn đến các phản ứng khác nhau từ tế bào. Cụ thể, α-Actinin dẫn đến tăng độ nhạy pH và phục hồi giải mẫn cảm. Họ cũng có thể tăng mật độ dòng chảy thông qua kênh.[8] Ngoài ra còn có nhiều kinase protein điều chỉnh chức năng ASIC thông qua quá trình phosphoryl hóa. Chúng bao gồm protein kinase A (PKA) và protein kinase C (PKC). Có nhiều người cho rằng có nhiều cơ quan quản lý hơn, tuy nhiên tác dụng của chúng chưa được kết luận bằng thực nghiệm.[8]
Có một số yếu tố khác có thể đóng một vai trò trong quy định của ASIC. Sự hiện diện của glycans được liên kết N trưởng thành trên bề mặt kênh được cho là cho phép kênh lưu lượng ưu tiên cho ASIC1a. Đây là kết quả từ các vị trí N-glycosyl hóa tăng trên ASIC1a và ASIC2a.[8] Hàm lượng glycerol cao (được biết đến là quá trình trưởng thành protein) trên bề mặt ASIC2 cũng hỗ trợ cho việc điều chỉnh chức năng của các kênh này phụ thuộc vào sự trưởng thành của protein. Người ta cũng đưa ra giả thuyết rằng quá trình oxy hóa đóng một vai trò trong buôn bán.[8]
Vị trí
[sửa | sửa mã nguồn]Hầu hết ASIC được thể hiện trong hệ thống thần kinh. ASIC1, ASIC2, ASIC2b và ASIC4 thường được biểu hiện ở cả hệ thần kinh trung ương và ngoại biên, trong khi ASIC1b và ASIC3 thường chỉ nằm ở ngoại vi.
Trong hệ thống thần kinh ngoại biên, ASIC nằm trong cơ thể tế bào của màng sau synap và các đầu dây thần kinh cảm giác. Ngoài ra, ASIC thường được tìm thấy trong các sợi thần kinh hướng tâm của da, cơ, khớp và nội tạng, nơi chúng được phát hiện có liên quan đến đau, vị giác và chức năng đường tiêu hóa.[6]
Trong hệ thống thần kinh trung ương, ASIC thường được tìm thấy ở sừng phía sau của tủy sống.[4] ASIC1 đặc biệt tập trung ở amygdala, minh họa vai trò của nó trong hành vi lo lắng và ASIC3 đã được tìm thấy trong cơ quan của Corti và hạch xoắn ốc minh họa vai trò của kênh cụ thể này trong nhận thức thính giác và thị giác.[6]
Sinh lý
[sửa | sửa mã nguồn]ASIC là các mục tiêu thuốc tiềm năng để điều trị một loạt các điều kiện liên quan đến cả CNS và PNS.[4][5] Quan tâm đặc biệt đến lĩnh vực đau là ASIC3 nhóm phụ receptor, được thể hiện cụ thể trong nociceptors. Loại phụ này thể hiện dòng điện hai pha khi kích hoạt proton, trong đó dòng Na + ban đầu đi vào ngay sau đó là dòng cation duy trì.
ASIC rất quan trọng trong chức năng võng mạc và cung cấp sự bảo vệ để đáp ứng với ánh sáng. Tính nhạy cảm của tổn thương võng mạc tăng lên sau khi xóa gen ASIC2. Tăng apoptosis xảy ra khi phản ứng với ánh sáng trong gen ASIC2 - / - so với võng mạc loại hoang dã.[8]
Các kênh ASIC1a cũng đóng một vai trò trong việc bảo vệ chống lại hoạt động co giật. Động kinh gây ra tăng, hoạt động thần kinh không kiểm soát trong não giải phóng một lượng lớn các axit có tính axit.[5] Các kênh ASIC1a mở để đáp ứng và đã cho thấy để bảo vệ chống lại các cơn động kinh bằng cách giảm sự tiến triển của chúng. Các nghiên cứu nghiên cứu hiện tượng này đã phát hiện ra rằng việc xóa gen ASIC1a dẫn đến hoạt động co giật được khuếch đại.[8]
Các kênh ASIC1a đặc biệt mở để đáp ứng với pH 5,0-6,9 và góp phần vào bệnh lý của chấn thương não do thiếu máu cục bộ vì sự kích hoạt của chúng gây ra sự gia tăng nhỏ trong tính thấm Ca 2+ và dòng Ca 2+ vào trong. Các kênh ASIC1a cũng tạo điều kiện thuận lợi cho việc kích hoạt các kênh Ca2 + bị kiểm soát điện áp và các kênh thụ thể NMDA khi khử cực ban đầu, góp phần vào sự gia tăng lớn của calci nội bào dẫn đến chết tế bào.[9] Một cơ chế có thể của cái chết tế bào qua trung gian kênh ASIC1a là do sự kích hoạt của các kênh khác, dẫn đến Ca 2+ tăng cao tạo ra các con đường truyền tín hiệu cho quá trình apoptosis và hoại tử trong tế bào.[5] Các nghiên cứu loại bỏ gen cũng như phong tỏa ASIC đã cho thấy giảm tới 60% khối lượng nhồi máu não, cho thấy các kênh ASIC đóng vai trò chính trong sự phát triển của các trạng thái bệnh lý do nhiễm toan và thiếu máu cục bộ gây ra tổn thương thần kinh.[9] Tác động của cả phong tỏa ASIC và NMDA đã được nghiên cứu để xác định vai trò của cả hai kênh trong độc tính Ca 2+ và đánh giá sự đóng góp tương ứng của chúng. Việc sử dụng phong tỏa cho cả hai kênh cung cấp bảo vệ thần kinh lớn hơn so với sử dụng phong tỏa cho chỉ một kênh và phong tỏa ASIC tạo ra hiệu quả kéo dài của phong tỏa NMDA.[9]
Dược lý
[sửa | sửa mã nguồn]Do vai trò của các kênh ion cảm nhận axit trong nhận thức đau và một số quá trình sinh lý bệnh, chúng có ý nghĩa dược lý như là một mục tiêu thuốc để ức chế. Các kênh ion cảm nhận axit được tìm thấy ở cả tế bào thần kinh trung ương và ngoại biên. Điều chế hoạt động ASIC có thể kiểm soát bổ sung các triệu chứng bất lợi về hành vi và cảm xúc của cơn đau mãn tính như lo lắng và trầm cảm.
Các kênh ion cảm ứng axit (ASIC) được quan sát thấy được kích hoạt ở pH dưới ~ 6 với độ biến thiên tùy thuộc vào loại kênh và vị trí của nó. Việc giảm pH có thể là do nhiều lý do bao gồm viêm mô, đột quỵ do thiếu máu cục bộ, tích tụ axit lactic do tăng chuyển hóa tế bào. Kích hoạt kênh này làm tăng tính thấm của các ion natri làm khử cực tế bào và gây ra sự bắn ra một tiềm năng hành động. Các tiềm năng hành động kết quả có thể được điều chỉnh thông qua các chất ức chế phân tử nhỏ.
Amiloride là một ví dụ về chất ức chế ASIC, mặc dù không được coi là có hiệu lực cao do giá trị IC50 trong phạm vi micromol, đã cho phép nghiên cứu về tác dụng ức chế ASIC đối với chứng đau nửa đầu. Trong cơn đau nửa đầu, trầm cảm lan tỏa vỏ não được quan sát gây ra sự mất cân bằng ion và giải phóng các phân tử tích điện có thể kích hoạt ASIC. Thử nghiệm amiloride ở động vật gặm nhấm, cho thấy giảm trầm cảm lan tỏa vỏ não trong cơn đau nửa đầu. Các nghiên cứu cho thấy amiloride hoạt động như một chất ức chế cạnh tranh của các chương ASIC. Việc sử dụng amiloride cũng cho thấy tác dụng phụ ở động vật gặm nhấm do ức chế trao đổi natri / calci. Sự ức chế của các chất trao đổi này phá vỡ cân bằng nội môi calci của tế bào và gây ra mức calci cao trong tế bào, điều này giải thích hiệu quả bảo vệ thần kinh giảm khi sử dụng amiloride. Những phát hiện đã được thông qua do ức chế ASIC bởi amiloride đang hứa hẹn và hỗ trợ tiềm năng điều trị. Tuy nhiên, do thiếu tính đặc hiệu và hiệu lực của amiloride, việc phát triển thuốc hơn nữa về cấu trúc của nó sẽ cần phải được thực hiện trước khi thuốc có thể được phát hành.[9][10]
Một chất ức chế phân tử nhỏ, A-317567, cho thấy tiềm năng điều trị nhiều hơn amiloride với độ đặc hiệu cao hơn đối với các kênh ASIC và tăng hiệu lực. Mặc dù A-317567 cho thấy ít sự chọn lọc đối với các loại kênh ASIC khác nhau, nhưng kết quả in vivo cho thấy các tác dụng phụ nhìn thấy khi sử dụng amiloride được tránh do tính đặc hiệu của A-317567 đối với ASIC. Ngoài ra, A-317567 có khả năng duy trì sự ức chế dòng điện duy trì có thể hứa hẹn đặc biệt trong điều kiện mãn tính qua trung gian nhiễm toan.[9]
Chất ức chế ASICs hiệu quả nhất và được biết đến nhiều nhất là PcTX1. PcTX1 đặc biệt ức chế ASICa và có giá trị IC50 trong phạm vi nano - IC50 nhỏ hơn tất cả các chất ức chế ASIC đã biết khác có trong phạm vi micromol. Ngoài ra, PcTX1 không ức chế các kênh ion bị điện thế khác hoặc các kênh bị phối tử. Cấu trúc của chất ức chế này là 40 amino acid liên kết với các liên kết disulfide. Nó được xác định là độc tố peptide từ loài tarantula Psalmopoeus Cambridge của Nam Mỹ.[9] Khi PcTX1 được sử dụng trong amygdala cơ bản của chuột, các triệu chứng liên quan đến cảm xúc và lo lắng liên quan đến cơn đau đã giảm đáng kể.[11]
Các thuốc chống viêm không steroid (NSAID) thường được sử dụng đã được tìm thấy có vai trò ức chế ASIC góp phần điều chỉnh cơn đau. Cơ chế nổi tiếng về chức năng NSAID là sự ức chế tổng hợp tuyến tiền liệt của họ, một hợp chất gây viêm chủ yếu. Tuy nhiên, các phát hiện cho thấy NSAIDs ibuprofen và aspirin ức chế ASIC với giá trị IC50 tương ứng là 350 cáchM và 260 siêuM. NSAID có khả năng ức chế dòng ASIC trong cơn đau cấp tính, đặc biệt là do viêm mô, và do đó ức chế tín hiệu đến các tế bào thần kinh cảm giác đau.[9]
Bằng cách tiếp tục nghiên cứu về tiềm năng dược lý trong ức chế ASIC, bệnh nhân bị đau mãn tính và các bệnh lý khác nhau liên quan đến nhiễm toan có thể có các lựa chọn điều trị lớn hơn trong tương lai. Ngoài ra, các nghiên cứu khám phá thuốc của ASIC cung cấp kiến thức lớn hơn về chức năng của chính các kênh và ý nghĩa sinh lý của chúng.
Tài liệu tham khảo
[sửa | sửa mã nguồn]- ^ Jasti J, Furukawa H, Gonzales EB, Gouaux E (2007). “Structure of acid-sensing ion channel 1 at 1.9 Å resolution and low pH”. Nature. 449 (7160): 316–322. doi:10.1038/nature06163. PMID 17882215.
- ^ a b Gründer S, Pusch M (tháng 7 năm 2015). “Biophysical properties of acid-sensing ion channels (ASICs)”. Neuropharmacology. 94: 9–18. doi:10.1016/j.neuropharm.2014.12.016. PMID 25585135.
- ^ a b c d e f g h i j k Hanukoglu I (tháng 2 năm 2017). “ASIC and ENaC type sodium channels: conformational states and the structures of the ion selectivity filters”. The FEBS Journal. 284 (4): 525–545. doi:10.1111/febs.13840. PMID 27580245.
- ^ a b c d Sluka KA, Winter OC, Wemmie JA (tháng 9 năm 2009). “Acid-sensing ion channels: A new target for pain and CNS diseases”. Current Opinion in Drug Discovery & Development. 12 (5): 693–704. PMC 3494879. PMID 19736627.
- ^ a b c d e Wang YZ, Xu TL (tháng 12 năm 2011). “Acidosis, acid-sensing ion channels, and neuronal cell death”. Molecular Neurobiology. 44 (3): 350–8. doi:10.1007/s12035-011-8204-2. PMID 21932071.
- ^ a b c Osmakov DI, Andreev YA, Kozlov SA (2014). “Acid-sensing ion channels and their modulators”. Biochemistry. Biokhimiia. 79 (13): 1528–45. doi:10.1134/S0006297914130069. PMID 25749163.
- ^ Sherwood TW, Frey EN, Askwith CC (tháng 10 năm 2012). “Structure and activity of the acid-sensing ion channels”. American Journal of Physiology. Cell Physiology. 303 (7): C699–710. doi:10.1152/ajpcell.00188.2012. PMC 3469599. PMID 22843794.
- ^ a b c d e f g h Zha XM (tháng 1 năm 2013). “Acid-sensing ion channels: trafficking and synaptic function”. Molecular Brain. 6: 1. doi:10.1186/1756-6606-6-1. PMC 3562204. PMID 23281934.
- ^ a b c d e f g Xiong ZG, Pignataro G, Li M, Chang SY, Simon RP (tháng 2 năm 2008). “Acid-sensing ion channels (ASICs) as pharmacological targets for neurodegenerative diseases”. Current Opinion in Pharmacology. Neurosciences. 8 (1): 25–32. doi:10.1016/j.coph.2007.09.001. PMC 2267925. PMID 17945532.
- ^ Baron A, Lingueglia E (tháng 7 năm 2015). “Pharmacology of acid-sensing ion channels - Physiological and therapeutical perspectives”. Neuropharmacology. Acid-Sensing Ion Channels in the Nervous System. 94: 19–35. doi:10.1016/j.neuropharm.2015.01.005. PMID 25613302.
- ^ Aissouni, Youssef; El Guerrab, Abderrahim; Hamieh, Al Mahdy; Ferrier, Jérémy; Chalus, Maryse; Lemaire, Diane; Grégoire, Stéphanie; Etienne, Monique; Eschalier, Alain (ngày 2 tháng 3 năm 2017). “Acid-Sensing Ion Channel 1a in the amygdala is involved in pain and anxiety-related behaviours associated with arthritis”. Scientific Reports. 7: 43617. doi:10.1038/srep43617. ISSN 2045-2322. PMC 5340794. PMID 28321113.
