Quỳ
Bài viết này cần thêm chú thích nguồn gốc để kiểm chứng thông tin. |
| Giấy quỳ (chất chỉ thị pH) | ||
| pH dưới 4,5 | pH trên 8,3 | |
| 4,5 | ⇌ | 8,3 |


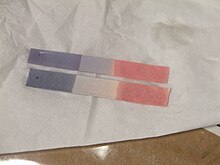
Quỳ là hỗn hợp hòa tan trong nước của các loại thuốc nhuộm khác nhau, được tách từ một số loài địa y (sinh vật hợp lại từ tảo hoặc vi khuẩn lam sống trong các sợi của nhiều loài nấm trong quan hệ hỗ sinh), như Roccella, Dendrographa, Variolaria, Ochrolechia, Parmotrema hay Parmelia spp. Ở dạng nguyên chất nó là một loại bột sẫm màu có mùi hơi giống amonia.[1]
Trong điều kiện pH trung tính thì màu gốc của quỳ chính xác là màu tía (màu thứ cấp, pha trộn của màu đỏ có bước sóng 610-760 nm với màu xanh lam có bước sóng 450-500 nm), tuy nhiên sự phân biệt màu tía với màu tím (màu quang phổ có bước sóng 380-450 nm) là không rõ ràng với mắt người nên trong thực tế người ta gọi nó là quỳ tím.
Nguồn gốc[sửa | sửa mã nguồn]
Quỳ được thầy thuốc người Tây Ban Nha là Arnaldus de Villa Nova (~1240-1311) sử dụng lần đầu tiên vào khoảng năm 1300.[2][3] Từ thế kỷ 16 trở đi, khi thông tin về phương pháp sản xuất quỳ được phổ biến thì thuốc nhuộm màu xanh lam được chiết từ một số loài địa y như Leuconora tartarea và Rocella tinctoria được sản xuất ở quy mô công nghiệp, đặc biệt là tại Hà Lan với các nhãn hiệu Bergmoos và Klippmoos để xuất khẩu. Năm 1704, nó được đặt tên gọi trong tiếng Hà Lan là lakmoes - từ leg (nhỏ giọt) và mus (cháo) trong ngữ hệ Ấn-Âu, phản ánh phương pháp sản xuất nó bằng cách chiết nhỏ giọt địa y nghiền vụn như cháo. Tên gọi là tiền đề cho các tên gọi trong một số ngôn ngữ châu Âu như tiếng Anh litmus, tiếng Đức lackmus, tiếng Nga лакмус.
Năm 1640, các nhà thực vật học mô tả một loại thuốc nhuộm thu được từ loài thực vật có hương thơm với hoa màu tím tía là vòi voi (Heliotropium spp.). Ban đầu các nhà hóa học sử dụng nó làm chất chỉ thị (do trong dung dịch axit nó chuyển thành màu đỏ, còn trong dung dịch kiềm thì nó chuyển thành màu xanh lam). Ban đầu quỳ được dùng chủ yếu để nghiên cứu nước khoáng, nhưng kể từ thập niên 1670 thì các nhà hóa học đã quan tâm tới nó nhiều hơn. Do tại Pháp thì quỳ cô lập từ Heliotropium được các nhà hóa học sử dụng rộng rãi nên một tên gọi khác cho quỳ được chấp nhận tại Pháp là tournesol - theo tên gọi trong tiếng Pháp cho Heliotropium. Muộn hơn thì toàn bộ bột quỳ được sản xuất theo cách thức rẻ tiền hơn là thu từ địa y.
Nguồn tự nhiên[sửa | sửa mã nguồn]

Quỳ có thể sản xuất từ các loài địa y khác nhau. Các thuốc nhuộm này được chiết từ các loài như Roccella tinctoria (bờ tây Nam Mỹ, Cabo Verde, quần đảo Canaria, Madeira, Açores), Roccella fuciformis (Angola và Madagascar), Roccella pygmaea (Algeria), Roccella phycopsis, Lecanora tartarea (Na Uy, Thụy Điển), Variolaria dealbata (Pyrénées, Avernes), Ochrolechia parella (duyên hải tây bắc châu Âu), Parmotrema tinctorum (quần đảo Canaria) và Parmelia. Các nguồn cung cấp quỳ chính hiện nay là Roccella montagnei (Mozambique) và Dendrographa leucophoea (California).[2]
Sản xuất[sửa | sửa mã nguồn]
Trong một thời gian dài, việc sản xuất quỳ là độc quyền và người ta không cung cấp thông tin chi tiết về các phương pháp phân lập nó. Ban đầu, phương pháp sau được sử dụng để thu được bột quỳ:
- Nguyên liệu địa y được nghiền thành bột;
- Bột được ngâm trong dung dịch soda-ammoniac (soda hoặc kali cacbonat + NH4OH) trong 3 tuần và được khuấy đảo liên tục. Nước tiểu được sử dụng thay cho dung dịch amonia (như một nguồn cung cấp ion CO32- và NH4+);
- Sau khi ngâm (chiết) và lên men, màu của hỗn hợp chuyển từ đỏ sang xanh da trời, cặn lắng được tách bỏ;
- Sau khi tách cặn, dịch chiết màu xanh da trời được sấy khô và nghiền. Sản phẩm thu được là hỗn hợp bột của các thuốc nhuộm quỳ và orcein;
- Sau khi chiết bột bằng cồn, dung dịch màu đỏ carmin (đỏ son) được loại bỏ và phần lắng còn lại là quỳ màu xanh lam sẫm;
- Ép khối đối với phần lắng bằng thạch cao hoặc đá phấn để thu được quỳ khô ở dạng dễ nghiền.
Phương pháp hiện đại sản xuất thuốc nhuộm orcein và quỳ, được hai nhà hóa học người Anh (G. Gordon và Cuthbert Gordon) đăng ký bằng sáng chế năm 1758 là như sau:
- Nguyên liệu địa y được nghiền thành bột;
- Bột được trộn với dung dịch huyền phù vôi tôi + kali cacbonat và amoni cacbonat và để lên men trong không khí;
- Sau khoảng 3 tuần lên men, màu của hỗn hợp chuyển từ màu tím hoặc nâu sang màu xanh lam sẫm;
- Hỗn hợp được chia tách bằng sàng, dung dịch tách ra chứa tới 90% orcein và tới 8% các chất quỳ khi quy khô.
- Dung dịch có thể được sử dụng để ép bánh với đá phấn hoặc thạch cao, hoặc cho bay hơi để sau đó chiết rượu thu được orcein.
Hóa học[sửa | sửa mã nguồn]
Hỗn hợp quỳ có số CAS 1393-92-6 và chứa 10-15 thuốc nhuộm khác nhau. Tất cả các thành phần hóa học của quỳ rất có thể là giống như của hỗn hợp có liên quan là orcein (số CAS 1400-62-0), nhưng với các tỷ lệ khác. Trái với orcein, thành phần chủ yếu của quỳ có khối lượng phân tử trung bình khoảng 3.300.[4] Các chất chỉ thị axit-base trên quỳ là do các tính chất của chúng đối với chromophore 7-hydroxyphenoxazon.[5] Một số phân đoạn của quỳ từng được đặt tên gọi riêng, như:[6]
- Erythrolitmin hay Orcein erythrolein (С13H22O6)
- Azolitmin (C9H10NO5)
- Spaniolitmin
- Leucoorcein
- Leucazolitmin.
Azolitmin thể hiện hiệu ứng gần giống như quỳ.[6]
Giấy quỳ[sửa | sửa mã nguồn]
Giấy quỳ là giấy có tẩm dung dịch quỳ trong etanol hoặc nước, được sử dụng trong ngành hóa học để thử, kiểm nghiệm pH. Khi nhúng giấy quỳ vào dung dịch, nếu màu giấy quỳ giữ nguyên màu tía thì dung dịch đó trung tính, nếu ngả sang màu xanh lá thì dung dịch đó mang tính kiềm, nếu chuyển sang màu hồng thì dung dịch đó mang tính axit. Sự thay đổi màu diễn ra ngoài khoảng pH 4,5–8,3 ở 25 °C (77 °F). Các phản ứng không phải là axit base cũng có thể làm đổi màu giấy quỳ. Chẳng hạn, khí clo làm cho giấy quỳ tím đổi thành màu đỏ rồi chuyển thành màu trắng – thuốc nhuộm quỳ bị tẩy trắng,[7] do sự có mặt của các ion hypoclorit (ClO−). Phản ứng này là không thuận nghịch, vì thế quỳ không có vai trò của chất chỉ thị màu trong tình huống này.
Theo nhiều nguồn tham khảo,[cần dẫn nguồn] người ta cho rằng quỳ được tẩm vào giấy để làm chất chỉ thị pH đầu tiên là nhà hóa học người Pháp Gay-Lussac (1778-1850) vào khoảng thế kỷ 19. Nhưng điều này chưa có chứng cứ rõ ràng và chính xác.
Tính chất[sửa | sửa mã nguồn]
Ưu điểm của giấy quỳ chính là sự tiện dụng của nó. Chỉ cần một mẩu giấy quỳ nhỏ, người ta có thể biết dung dịch mình đang sử dụng có tính acid hay base một cách nhanh chóng (chỉ mất vài phần trăm giây), và độ mạnh yếu của tính axit/base (một cách tương đối) dựa vào sự thay đổi đậm nhạt của màu sắc. Ngoài ra, giấy quỳ ẩm (giấy quỳ cho thấm ướt bởi nước cất) còn có thể được ứng dụng để kiểm tra tính axit/base của các loại khí (như H2S, SO3…). Một ưu điểm rõ ràng khác của giấy quỳ nữa là giá thành rẻ của nó so với các chỉ thị pH khác.
Tuy nhiên, giấy quỳ không thể cho biết chính xác độ mạnh yếu axit/base cũng như độ pH của dung dịch cần đo. Thay vào đó, người ta sử dụng các loại chỉ thị pH cao cấp hơn như máy đo pH. Các loại máy đo pH hiện này ngoài chức năng cho biết chính xác độ pH của dung dịch, mà còn cho biết nhiệt độ, độ dẫn điện của dung dịch cần đo
Sản xuất[sửa | sửa mã nguồn]
Để sản xuất giấy quỳ cũng cần nguồn nguyên liệu như sản xuất các loại giấy khác là gỗ, rồi trải qua khâu nghiền, phối trộn bột giấy, qua máy xeo, cán mỏng, sấy,...Điểm khác biệt là ta sẽ cho thêm hoạt chất quỳ vào bột giấy, sau đó sấy khô sẽ có giấy quỳ như thành phẩm.
Công dụng[sửa | sửa mã nguồn]
pH là một thông số quan trọng trong nhiều lĩnh vực khoa học. Các tế bào trong cơ thể sinh vật sống đều có một khoảng pH (pH scale) nhất định, chỉ cần sự thay đổi dù nhỏ giá trị pH của môi trường đều có thể ảnh hưởng nghiêm trọng đến sự sống của chúng. Trong nông nghiệp, pH cũng là thông số cần được chú ý trong canh tác đất trồng. Nếu đất mang tính acid (còn gọi là đất chua, đất nhiễm phèn) sẽ làm ảnh hưởng đến khả năng hấp thu dinh dưỡng của cây trồng, dẫn đến không có giá trị canh tác. Do vậy, trong thực tế, người ta thường phải bón vôi (nguồn cung cấp base) để trung hòa các ion hydro, ion alum (nhôm) trong đất, làm giảm tính acid và tăng pH cho đất.
Địa y[sửa | sửa mã nguồn]
-
Trên cành vân sam.
-
Địa y trên đá tại Vườn bang Custer, Nam Dakota, USA
-
Cây tú cầu
Xem thêm[sửa | sửa mã nguồn]
- Dung dịch Phenolphthalein không màu khi vào dung dịch kiềm sẽ hóa thành màu đỏ hồng
-
Phenolphthalein khi nhỏ acid (pH dưới 0)
-
Phenolphthalein
- Giấy ozon tẩm Kali Iodide KI và hồ tinh bột để nhận biết ozon màu xanh
- Giấy fluoretxein để nhận biết Brom.
- Giấy nghệ để nhận biết Bo màu đỏ
- Giấy quỳ còn được dùng gọi tắt cho giấy dát vàng quỳ để dát lên tranh
Tham khảo[sửa | sửa mã nguồn]
- ^ Manfred Neupert: Lackmus in Römpp Lexikon Chemie (Tiếng Đức.).
- ^ a b Manfred Neupert: Lackmus trong Römpp Lexikon Chemie (tiếng Đức). Tra cứu ngày ngày 4 tháng 4 năm 2019.
- ^ Wissenschaft-Online-Lexika: Eintrag zu Lackmus im Lexikon der Arzneipflanzen und Drogen
- ^ Beecken H.; E-M. Gottschalk; U. v Gizycki; H. Krämer; D. Maassen; H-G. Matthies; H. Musso; C. Rathjen; Ul. Zdhorszky (2003). “Orcein and Litmus”. Biotechnic & Histochemistry. 78 (6): 289–302. doi:10.1080/10520290410001671362.
- ^ H. Musso, C. Rathjen (1959). “Orcein dyes. X. Light absorption and chromophore of litmus”. Chem. Ber. 92 (3): 751–753. doi:10.1002/cber.19590920331.
- ^ a b E.T. Wolf: Vollständige Übersicht der Elementar-analytischen Untersuchungen organischer Substanzen. Tr. 450-453, veröffentlicht 1846, Verlag E. Anton (tiếng Đức)
- ^ UCC - Chlorine
Liên kết ngoài[sửa | sửa mã nguồn]
- How to used Litmus Paper*
 Tư liệu liên quan tới Chất chỉ thị pH tại Wikimedia Commons
Tư liệu liên quan tới Chất chỉ thị pH tại Wikimedia Commons- Litmus (chemistry) tại Encyclopædia Britannica (tiếng Anh)












