Amoni
| Amoni | |||
|---|---|---|---|
| |||
| Danh pháp IUPAC |
Amoni | ||
| Tên hệ thống |
Azani[1] | ||
| Nhận dạng | |||
| Số CAS |
| ||
| PubChem |
| ||
| MeSH |
| ||
| ChEBI |
| ||
| Ảnh Jmol-3D | |||
| SMILES |
List
| ||
| InChI |
1/H3N/h1H3/p+1 | ||
| Thuộc tính | |||
| Công thức phân tử |
NH+ | ||
| Điểm nóng chảy | |||
| Điểm sôi | |||
| Độ axit (pKa) |
9.25 | ||
| Các nguy hiểm | |||
| Cấu trúc | |||
| Hình dạng phân tử |
Tetrahedral | ||
Cation amoni (còn được gọi là azani hoặc amôn, amon) là một ion đa năng tích điện dương với công thức hóa học NH+
4. Nó được hình thành bởi sự khuếch tán amonia (NH
3). Amoni cũng là một tên tổng quát cho amine được proton hóa và các ion amoni bậc bốn (NR+
4), trong đó một hoặc nhiều nguyên tử hydro được thay thế bởi các nhóm hữu cơ (được chỉ ra bởi R).
Muối amoni
[sửa | sửa mã nguồn]
Amoni được tìm thấy trong một loạt các muối như amoni cacbonat, amoni chloride, và amoni nitrat. Hầu hết các muối amoni đơn giản đều hòa tan trong nước. Một ngoại lệ là hexanochloroplatinat amoni. Các muối amoni của nitrat và đặc biệt là perchlorat là chất nổ, trong những trường hợp này amoni là chất khử. Trong một quá trình khác, ion amoni tạo thành một hỗn hợp amalgam. Những loại này được điều chế bằng điện phân của dung dịch amoni bằng catốt thủy ngân.[2] Hợp chất này cuối cùng phân hủy để giải phóng ammonia và hydro.
Cấu trúc và liên kết
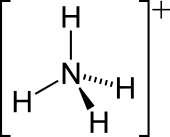
[sửa | sửa mã nguồn]Một cặp electron đơn trên nguyên tử nitơ (N) trong amonia, đại diện như một dòng trên N, tạo thành liên kết với một proton (H+
). Sau đó, tất cả bốn liên kết N-H tương đương, là các liên kết cộng hóa trị cực. Ion có cấu trúc tứ diện và không tương tác với metan và borohydrit. Xét về kích thước, ion cation amoni (rionic = 175 pm) giống với cation caesi (rionic = 183 pm).
Tham khảo
[sửa | sửa mã nguồn]- ^ International Union of Pure and Applied Chemistry (2005). Nomenclature of Inorganic Chemistry (IUPAC Recommendations 2005). Cambridge (UK): RSC–IUPAC. ISBN 0-85404-438-8. pp. 71,105,314. Electronic version.
- ^ “Pseudo-binary compounds”. Bản gốc lưu trữ ngày 27 tháng 7 năm 2020. Truy cập ngày 28 tháng 12 năm 2017.