Amonia
| Amonia | |
|---|---|
 | |
| Tổng quan | |
| Danh pháp IUPAC | Ammonia Azane |
| Tên khác | Azane |
| Công thức phân tử | NH3 |
| Phân tử gam | 17,02982 g/mol |
| Biểu hiện | Chất khí không màu mùi khai |
| Số CAS | [7664-41-7] |
| Thuộc tính | |
| Tỷ trọng và pha | 0,6813 g/l, khí |
| Độ hòa tan trong nước | 89,9 g/100 ml ở 0 ℃ |
| Nhiệt độ nóng chảy | −77,73 °C (−107,91 °F; 195,42 K) |
| Điểm sôi | −33,34 °C (−28,01 °F; 239,81 K) |
| pKa | ≈ 34 |
| pKb | 4,75 |
| Khác | |
| MSDS | MSDS ngoài |
| Các nguy hiểm chính | Chất ăn mòn và chất độc |
| NFPA 704 | |
| Điểm bắt lửa | 11 ℃ |
| Rủi ro/An toàn | R10, R23, R34, R50 S1/2, S16, S36/37/39, S45, S61 |
| Số RTECS | BO0875000 |
| Các hợp chất liên quan | |
| Các hợp chất liên quan | Hiđrazin Axit hydrazoic Hydroxylamin Cloramin |
| Ngoại trừ có thông báo khác, các dữ liệu được lấy ở 25 °C, 100 kPa Thông tin về sự phủ nhận và tham chiếu | |
Amonia (bắt nguồn từ từ tiếng Pháp ammoniac /amɔnjak/),[1] còn được viết là a-mô-ni-ắc,[1] là một hợp chất của nitơ và hydro có công thức hóa học NH3. Là một hydride nhị phân ổn định và hydride pnictogen đơn giản nhất, amonia là một chất khí không màu, có mùi hăng đặc trưng (mùi khai). Nó là một chất thải nitơ phổ biến, đặc biệt là giữa các sinh vật sống dưới nước, và nó góp phần đáng kể vào nhu cầu dinh dưỡng của các sinh vật trên cạn bằng cách đóng vai trò là tiền chất của thực phẩm và phân bón. Thanh, trực tiếp hoặc gián tiếp, cũng là một chất xây dựng để tổng hợp nhiều sản phẩm dược phẩm và được sử dụng trong nhiều sản phẩm tẩy rửa thương mại. Nó chủ yếu được thu thập bằng cách tổng hợp hạ mức của không khí và nước.
Mặc dù khá phổ biến trong tự nhiên – cả trên cạn và ở các hành tinh bên ngoài Hệ Mặt trời - và được sử dụng rộng rãi, amonia vừa có tính ăn mòn vừa nguy hiểm ở dạng đậm đặc. Nó được phân loại là một chất cực kỳ nguy hiểm ở Hoa Kỳ và phải tuân theo các yêu cầu báo cáo nghiêm ngặt bởi các cơ sở sản xuất, lưu trữ hoặc sử dụng nó với khối lượng đáng kể.[2]
Sản lượng amonia công nghiệp toàn cầu năm 2018 là 175 triệu tấn,[3] không có thay đổi đáng kể so với sản lượng công nghiệp toàn cầu năm 2013 là 175 triệu tấn.[4] Amonia công nghiệp được bán dưới dạng rượu amonia (thường là 28% amonia trong nước) hoặc amonia lỏng khan có áp suất hoặc làm lạnh được vận chuyển trong xe bồn hoặc ống trụ.[5]
NH3 sôi ở -33,34 ℃ ở áp suất tiêu chuẩn, do đó chất lỏng phải được bảo quản dưới áp suất hoặc ở nhiệt độ thấp. Amonia gia dụng hoặc amoni hydroxide là một dung dịch NH3 trong nước. Nồng độ của các dung dịch này được đo bằng đơn vị của thang Baumé (khối lượng riêng), với 26 độ Baumé (khoảng 30% (theo trọng lượng) amonia ở 15,5 °C hay 59,9 °F) là sản phẩm thương mại nồng độ cao điển hình của chất này.[6]
Từ nguyên[sửa | sửa mã nguồn]
Pliny, trong Sách XXXI về Lịch sử Tự nhiên của mình, đề cập đến một loại muối được sản xuất ở tỉnh Cyrenaica của La Mã có tên là hammoniacum, được gọi như vậy vì nó nằm gần Đền thờ Jupiter Amun (tiếng Hy Lạp là Ἄμμων Ammon).[7] Tuy nhiên, mô tả của Pliny về muối không phù hợp với các đặc tính của amoni chloride. Theo lời bình luận của Herbert Hoover trong bản dịch tiếng Anh của ông về De re metallica của Georgius Agricola, nó có thể là muối biển thông thường.[8] Trong mọi trường hợp, muối đó cuối cùng đã tạo ra tên cho các hợp chất amonia và amoni.
Xuất hiện trong tự nhiên[sửa | sửa mã nguồn]
Amonia là một chất hóa học được tìm thấy ở dạng vi lượng trong tự nhiên, được sản xuất từ chất động thực vật có nitơ. Amonia và muối amoni cũng được tìm thấy với số lượng nhỏ trong nước mưa, trong khi amoni chloride (sal amonia), và amoni sulfat được tìm thấy ở các vùng có núi lửa; tinh thể Amoni bicarbonat đã được tìm thấy trong phân chim Patagonia.[9] Thận tiết ra amonia để trung hòa acid dư thừa.[10] Các muối amoni được tìm thấy trong các vùng đất màu mỡ và trong nước biển.
Amonia cũng được tìm thấy trên khắp các hành tinh trong hệ Mặt Trời trên sao Hỏa, sao Mộc, sao Thổ, sao Thiên Vương, sao Hải Vương, và Sao Diêm Vương, và những nơi khác: trên, trên các hành tinh nhỏ hơn như Sao Diêm Vương, amonia có thể hoạt động như một chất chống đông mang tính địa chất quan trọng, do hỗn hợp của nước và amonia có thể có nhiệt độ nóng chảy thấp tới 173 K (−100 °C; −148 °F) nếu nồng độ amonia đủ cao và do đó cho phép các thiên thể như vậy giữ lại các đại dương bên trong và địa chất đang hoạt động ở nhiệt độ thấp hơn nhiều so với trường hợp hành tinh chỉ có nước.[11][12] Các chất có chứa amonia, hoặc những chất tương tự với nó, được gọi là amoniaal.
Tính chất vật lý[sửa | sửa mã nguồn]
Amonia là chất khí không màu, có mùi hắc đặc trưng. Nó nhẹ hơn không khí, mật độ của nó gấp 0,589 lần không khí. Nó dễ dàng hóa lỏng do có liên kết hydro mạnh giữa các phân tử; chất lỏng sôi ở −33,3 °C (−27,94 °F), và đóng băng thành tinh thể trắng [9] ở −77,7 °C (−107,86 °F).
Amonia có thể được khử mùi thuận tiện bằng cách cho nó phản ứng với natri bicacbonat hoặc axit axetic. Cả hai phản ứng này đều tạo thành muối amoni không mùi.
- Chất rắn
Đối xứng tinh thể là hình khối, ký hiệu Pearson cP16, nhóm không gian P213 (№. 198), hằng số mạng 0,5125 nm.
- Chất lỏng
Amonia dạng lỏng có khả năng ion hóa mạnh do có chỉ số ε cao là 22. Amonia lỏng có sự thay đổi entanpi của quá trình hóa hơi tiêu chuẩn rất cao (23,35 kJ/mol, cf. nước 40,65 kJ/mol, methan 8,19 kJ/mol, photphin 14,6 kJ/mol) và do đó có thể được sử dụng trong phòng thí nghiệm trong các bình không cách nhiệt mà không cần làm lạnh thêm. Xem amonia lỏng như một dung môi.
- Thuộc tính dung môi
Amonia dễ dàng hòa tan trong nước. Trong dung dịch nước, nó có thể được loại bỏ bằng cách đun sôi. Dung dịch nước của amonia có tính base. Nồng độ tối đa của amonia trong nước (dung dịch bão hòa) có khối lượng riêng là 0,880 g/cm³ và thường được gọi là '880 amonia'.
- Cháy
Amonia không cháy ngay hoặc có khả năng duy trì sự cháy, ngoại trừ trong điều kiện hỗn hợp nhiên liệu-không khí hẹp có 15–25% không khí. Khi trộn với oxy, nó cháy với ngọn lửa màu vàng lục nhạt. Sự bốc cháy xảy ra khi clo được truyền vào amonia, tạo thành nitơ và hydro chloride; nếu clo dư thì nitơ trichloride (NCl3) rất dễ nổ cũng được tạo thành.
- Sự phân hủy
Ở nhiệt độ cao và có mặt chất xúc tác thích hợp, amonia bị phân hủy thành các nguyên tố cấu thành của nó. Sự phân hủy amonia là một quá trình thu nhiệt nhẹ cần 5,5 kcal/mol amonia, và tạo ra khí hydro và nitơ. Amonia cũng có thể được sử dụng như một nguồn hydro cho pin nhiên liệu axit nếu amonia chưa phản ứng có thể được loại bỏ. Các chất xúc tác ruthenium và platinum được cho là hoạt động tích cực nhất, trong khi các chất xúc tác Ni được hỗ trợ thì hoạt động kém hơn.
Cấu trúc[sửa | sửa mã nguồn]
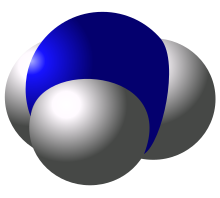
Phân tử amonia có dạng hình chóp tam giác theo dự đoán của thuyết đẩy cặp electron lớp vỏ hóa trị (thuyết VSEPR) với góc liên kết xác định bằng thực nghiệm là 106,7°.[13] Nguyên tử nitơ trung tâm có năm electron lớp ngoài cùng với một electron bổ sung từ mỗi nguyên tử hydro. Điều này tạo ra tổng cộng tám điện tử, hoặc bốn cặp điện tử được sắp xếp theo hình tứ diện. Ba trong số các cặp electron này được sử dụng như các cặp liên kết, chúng để lại một cặp electron duy nhất. Cặp đơn lẻ đẩy mạnh hơn các cặp liên kết, do đó góc liên kết không phải là 109,5°, như mong đợi đối với sắp xếp tứ diện đều, mà là 106,7°.[13] Hình dạng này tạo cho phân tử một momen lưỡng cực và làm cho nó phân cực. Tính phân cực của phân tử, và đặc biệt, khả năng hình thành liên kết hydro của nó, làm cho amonia có thể trộn lẫn với nước rất cao. Cặp đơn độc làm cho amonia trở thành một base, một chất nhận proton. Amonia có tính base vừa phải; Dung dịch nước 1,0 M có pH là 11,6, và nếu thêm axit mạnh vào dung dịch như vậy cho đến khi dung dịch trung tính (pH = 7), 99,4% số phân tử amonia được proton hóa. Nhiệt độ và độ mặn cũng ảnh hưởng đến tỷ lệ NH4+. Sau này có hình dạng của một tứ diện đều và là đẳng điện tử với methan.
Phân tử amonia dễ dàng trải qua quá trình nghịch chuyển nitơ ở nhiệt độ phòng; một phép tương tự hữu ích là một chiếc ô tự quay ra ngoài trong một cơn gió mạnh. Rào cản năng lượng đối với sự nghịch đảo này là 24,7 kJ/mol và tần số cộng hưởng là 23,79 GHz, tương ứng với bức xạ vi sóng có bước sóng 1,260 cm. Sự hấp thụ ở tần số này là phổ vi sóng đầu tiên được quan sát thấy.
Tính lưỡng tính[sửa | sửa mã nguồn]
Một trong những tính chất đặc trưng nhất của amonia là tính base. Amonia được coi là một base yếu. Nó kết hợp với axit để tạo thành muối; do đó với axit clohydric nó tạo thành amoni chloride (sal amonia); với axit nitric tạo thành amoni nitrat, v.v. Amonia khô hoàn toàn sẽ không kết hợp với hydro chloride khô hoàn toàn; độ ẩm là cần thiết để thực hiện phản ứng. [14][15] Như một thí nghiệm mô tả, các chai amonia và axit clohydric đậm đặc đã mở nắp tạo ra các "đám mây" amoni chloride, dường như xuất hiện từ "không có gì" khi muối hình thành nơi hai đám mây phân tử khuếch tán gặp nhau, ở đâu đó giữa hai chai.
Các muối được tạo ra do tác dụng của amonia với axit được gọi là muối amoni và tất cả đều chứa ion amoni (NH4+). Mặc dù amonia được biết đến là một base yếu, nó cũng có thể hoạt động như một axit cực kỳ yếu. Nó là một chất proton và có khả năng hình thành amit (có chứa ion NH2−). Ví dụ, lithi hòa tan trong amonia lỏng để tạo ra dung dịch lithi amit:
Tính chất hóa học[sửa | sửa mã nguồn]
Trong amonia, nitơ có số oxy hóa thấp nhất nên amonia có tính khử. Ví dụ như trong phản ứng hóa học:
Nguyên tử kim loại loại kiềm hoặc nhôm:
Tác dụng với dung dịch muối:
Tính base yếu[sửa | sửa mã nguồn]
Tan trong nước[sửa | sửa mã nguồn]
Theo thuyết Brønsted-Lowry, NH3 khi tan trong nước, một phần nhỏ các phân tử amonia kết hợp với ion H+ của nước tạo thành cation amoni NH4+ và giải phóng anion OH-, lúc này nước sẽ đóng vai trò là axit.
- \]
Ion OH- làm cho dung dịch có tính base, tuy nhiên so với dung dịch kiềm mạnh (thí dụ xút, potat, nước vôi trong...) cùng nồng độ thì nồng độ anion OH- do amonia tạo thành nhỏ hơn nhiều. Do có tính base nên dung dịch amonia làm cho quỳ tím hóa xanh còn dung dịch phenolphtalein từ không màu chuyển thành hồng. Do đó để phát hiện amonia, người ta dùng quỳ tím ẩm để nhận ra khí này.
Tác dụng với axit[sửa | sửa mã nguồn]

Amonia (ở dạng khí cũng như dung dịch) dễ dàng trung hòa axit tạo thành muối amoni. Thí dụ:
hay
Khi đặt hai bình mở nút đựng dung dịch HCl đặc và dung dịch NH3 ở gần nhau thì thấy có "khói" màu trắng tạo nên (hình 1). Do HCl và NH3 là những hợp chất dễ bay hơi nên chúng đã hóa hợp với nhau tạo thành tinh thể muối amoni chloride, chính tinh thể này đã tạo nên hiện tượng "khói".
Phản ứng này được dùng để nhận biết khí amonia.
Tác dụng với dung dịch muối[sửa | sửa mã nguồn]

Dung dịch amonia có khả năng tạo kết tủa nhiều hydroxide kim loại khi tác dụng
Thí dụ trong hình 2, dung dịch amonia đã phản ứng với dung dịch đồng(II) sunfat tạo kết tủa xanh lam:
Khả năng tạo phức[sửa | sửa mã nguồn]
Dung dịch amonia có khả năng tạo phức với rất nhiều hợp chất khó tan của kim loại như Cu, Ag, Ni, Pb, Zn,…
Vì các cation này có orbital trống nên có thể tiếp nhận cặp electron chưa liên kết trong nguyên tử N của NH3.
- (với M = Cu, Zn, Pb,…)
Điều chế[sửa | sửa mã nguồn]
Trong phòng thí nghiệm:
Trong công nghiệp:
Phần lớn NH3 (90%) được sản xuất theo phương thức Haber-Bosch với từ không khí, từ khí Mêtan () và nước.
- (xúc tác Ni, nhiệt độ cao)
(ΔH = –92 kJ/mol)
Phản ứng trên thuận nghịch và tỏa nhiệt, do đó phải có các điều kiện phù hợp để chuyển dịch cân bằng về bên phải theo nguyên lý Le Chatelier. Thực tế, phản ứng này thường được thực hiện ở 450–500 ℃, 200–300 atm, xúc tác là hỗn hợp Fe, Al2O3, K2O,… nhưng hiệu suất chỉ từ 20–25%. Phương thức CaCN2 của Rothe-Frank-Caro:
Phương thức Persek từ nhôm nitride AlN và nước:
Từ NO và H2:
Khử hydro bằng nitơ (tiếng anh: hydrodenitrogenation)
Hiện nay, một số nghiên cứu từ phòng thí nghiệm cho thấy rằng ammonia được sản xuất trực tiếp từ nitơ và nước với sự có mặt của chất xúc tác titan(IV) oxide và tia cực tím:
Ứng dụng[sửa | sửa mã nguồn]
Ứng dụng chủ yếu của amonia là điều chế phân đạm, điều chế axit nitric, là chất sinh hàn, sản xuất hiđrazin N2H4 dùng làm nhiên liệu cho tên lửa. Ngoài ra, dung dịch amonia còn được dùng làm chất tẩy rửa gia dụng. Dạng lỏng của amonia đóng vai trò quan trọng trong phản ứng khử Birch.
Nguy hiểm[sửa | sửa mã nguồn]
Nếu hít nhiều amonia sẽ bị bỏng đường hô hấp (rát cổ họng). Khí amonia gây ức chế thần kinh tạo nên cảm giác khó chịu cáu gắt. Triệu chứng: Ho, đau ngực (nặng), đau thắt ngực, khó thở, thở nhanh, thở khò khè, khó thở, ho ra máu, co giật cùng các biểu hiện:
- Mắt, miệng, họng: Chảy nước mắt và đốt mắt, mù mắt, đau họng nặng, đau miệng, sứt môi .
- Tim mạch: Nhanh, mạch yếu, sốc.
- Thần kinh: Lẫn lộn, đi lại khó khăn, chóng mặt, thiếu sự phối hợp, bồn chồn, ngẩn ngơ.
- Da: Môi xanh lợt màu, bỏng nặng nếu tiếp xúc lâu.
- Dạ dày và đường tiêu hóa: Đau dạ dày nghiệm trọng, nôn.
Tham khảo[sửa | sửa mã nguồn]
- ^ a b Đặng Thái Minh, "Dictionnaire vietnamien - français. Les mots vietnamiens d’origine française", Synergies Pays riverains du Mékong, n° spécial, năm 2011. ISSN: 2107-6758. Trang 49.
- ^ “40 C.F.R.: Appendix A to Part 355—The List of Extremely Hazardous Substances and Their Threshold Planning Quantities” (PDF) . Government Printing Office. Bản gốc (PDF) lưu trữ ngày 25 tháng 2 năm 2012. Truy cập ngày 29 tháng 10 năm 2011. Chú thích journal cần
|journal=(trợ giúp) - ^ “Mineral Commodity Summaries 2020, p. 117 – Nitrogen” (PDF). USGS. 2020. Truy cập ngày 12 tháng 2 năm 2020.
- ^ “Nitrogen (fixed) - ammonia statistics”. USGS. 2017. Truy cập ngày 12 tháng 2 năm 2020.
- ^ R. Norris Shreve; Joseph Brink (1977). Chemical Process Industries (ấn bản 4). tr. 276. ISBN 978-0-07-057145-7. See also Gas carrier and Bottled gas.
- ^ “Ammonium hydroxide physical properties” (PDF). Bản gốc (PDF) lưu trữ ngày 27 tháng 11 năm 2007.
- ^ “Pliny the Elder, The Natural History, Book XXXI, Chapter 39. (7.) - The various kinds of salt; the methods of preparing it, and the remedies derived from it”.
- ^ Hoover, Herbert (1950). Georgius Agricola De Re Metallica - Translated from the first Latin edition of 1556. New York: Dover Publications. tr. 560. ISBN 978-0486600062.
- ^ a b Chisholm 1911, tr. 861.
- ^ Kirschbaum, B; Sica, D; Anderson, F. P. (1999). “Urine electrolytes and the urine anion and osmolar gaps”. The Journal of Laboratory and Clinical Medicine. 133 (6): 597–604. doi:10.1016/S0022-2143(99)90190-7. ISSN 0022-2143. PMID 10360635.
- ^ Shannon, Francis Patrick (1938) Tables of the properties of aqua-ammonia solutions. Part 1 of The Thermodynamics of Absorption Refrigeration. Lehigh University studies. Science and technology series
- ^ An ammonia-water slurry may swirl below Pluto's icy surface. Purdue University (ngày 9 tháng 11 năm 2015)
- ^ a b Haynes, William M. biên tập (2013). CRC Handbook of Chemistry and Physics (ấn bản 94). CRC Press. tr. 9–26. ISBN 9781466571143.
- ^ Chisholm 1911, tr. 862.
- ^ Baker, H. B. (1894). “Influence of moisture on chemical change”. J. Chem. Soc. 65: 611–624. doi:10.1039/CT8946500611.
- Hóa học vô cơ, tập hai, Hoàng Nhâm, Nhà xuất bản giáo dục Việt Nam.
- Sách giáo khoa Hóa học 11 nâng cao, Nhà xuất bản giáo dục Việt Nam.
Liên kết ngoài[sửa | sửa mã nguồn]
| Wikimedia Commons có thêm hình ảnh và phương tiện truyền tải về Amonia. |
- AMONIAC tại Từ điển bách khoa Việt Nam
- Ammonia (chemical compound) tại Encyclopædia Britannica (tiếng Anh)
- CID 222 từ PubChem


![{\displaystyle {\ce {4NH3 + 3O2 ->[500^o C] 2N2 + 6H2O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/24713424b16a6d0cb2f68374c1c5a0f360121f09)
![{\displaystyle {\ce {2NH3 + 2Na ->[350^o C] 2NaNH2 + H2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e34b4c906c4f4889ec830f56054d37a9e6363060)
![{\displaystyle {\ce {2NH3 + 2Al ->[800-900^o C] 2AlN + 3H2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/375054d38ad80d520769fdc6ebd0e7cf606f25bd)






2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/161640ee3e29c23b3c2fc7c5db961cfa230f0cc4)
2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/9db405cbec65824bb3a148c735155fbc976329b4)
![{\displaystyle {\ce {Ag+ + 2NH3 -> [Ag(NH3)2]+}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/6a54fcb6a7a78659b60e2e2e3fccb837b0a11a7c)











![{\displaystyle {\xrightarrow[{\text{UV}}]{{\text{TiO}}_{2}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/19eca1eae28c21ed403c989342041b52e35d1ba6)
