Acid triflic
| Acid triflic | |||
|---|---|---|---|
| |||
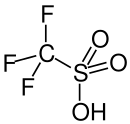 Trifluoromethanesulfonic acid | |||
| Danh pháp IUPAC | Trifluoromethanesulfonic acid | ||
| Tên khác | Triflic acid | ||
| Nhận dạng | |||
| Số CAS | |||
| PubChem | |||
| ChEBI | |||
| Ảnh Jmol-3D | ảnh | ||
| SMILES | đầy đủ
| ||
| InChI | đầy đủ
| ||
| UNII | |||
| Thuộc tính | |||
| Công thức phân tử | CF3SO3H | ||
| Khối lượng mol | 150.07121 g/mol | ||
| Bề ngoài | Chất lỏng không màu | ||
| Khối lượng riêng | 1.696 g/mL | ||
| Điểm nóng chảy | −40 °C (233 K; −40 °F) | ||
| Điểm sôi | 162 °C (435 K; 324 °F) | ||
| Độ hòa tan trong nước | Miscible | ||
| Độ axit (pKa) | -14.7 (±2.0) [1] | ||
| Base liên hợp | Triflate anion | ||
| Các nguy hiểm | |||
| Nguy hiểm chính | Causes severe acid burns | ||
| NFPA 704 |
| ||
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |||

Acid triflic, tên viết tắt của acid trifluoromethanesulfonic, TFMS, TFSA, HOTf hoặc TfOH, là một acid sulfonic có công thức hóa học CF3SO3H. Nó là một trong những acid mạnh nhất được biết đến. Acid triflic được sử dụng chủ yếu trong nghiên cứu làm chất xúc tác cho quá trình este hóa.[2][3] Nó là một chất lỏng hút ẩm, không màu, hơi nhớt và có thể hòa tan trong các dung môi phân cực.
Tổng hợp[sửa | sửa mã nguồn]
Acid trifluoromethanesulfonic được sản xuất công nghiệp bằng phương pháp fluor hóa điện hóa (ECF) của acid methanesulfonic:
- CH3SO3H + 4 HF → CF3SO2F + H2O + 3H2
CF3SO2F thu được bị thủy phân, và muối triflat thu được được proton hóa. Ngoài ra, acid trifluoromethanesulfonic phát sinh bằng cách oxy hóa trifluoromethyl sulfenyl chloride:
- CF3SCl + 2Cl2 + 3H2O → CF3SO3H + 5HCl
Acid triflic được tinh chế bằng cách chưng cất từ anhydride triflic.[3]
Lịch sử[sửa | sửa mã nguồn]
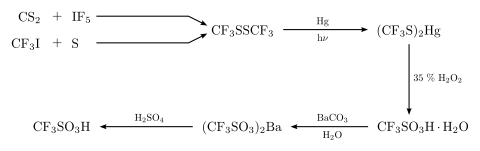
Acid trifluoromethanesulfonic được Robert Haszeldine và Kidd tổng hợp lần đầu tiên vào năm 1954 bằng phản ứng sau:[4]
Tham khảo[sửa | sửa mã nguồn]
- ^ Trummal, A.; Lipping, L.; Kaljurand, I.; Koppel, I. A.; Leito, I. "Acidity of Strong Acids in Water and Dimethyl Sulfoxide" J. Phys. Chem. A. 2016, 120, 3663-3669. doi:10.1021/acs.jpca.6b02253
- ^ Howells, R. D., McCown, J. D. (1977). “Trifluoromethanesulfonic Acid and Derivatives”. Chemical Reviews. 77 (1): 69–92. doi:10.1021/cr60305a005.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- ^ a b Martinez, A. G.; Hanack, M.; Prakash, G. K. S.; Hu, J. (2006). “Trifluoromethanesulfonic Acid”. encyclopedia of Reagents for Organic Synthesis. John Wiley & Sons. doi:10.1002/047084289X.rt246.pub2. ISBN 0-471-93623-5.
|author1=bị thiếu (trợ giúp) - ^ Haszeldine, R. N.; Kidd, J. M. (1954). “Perfluoroalkyl derivatives of sulphur. Part I. Trifluoromethanesulphonic acid”. Journal of the Chemical Society. 1954: 4228–4232. doi:10.1039/JR9540004228.