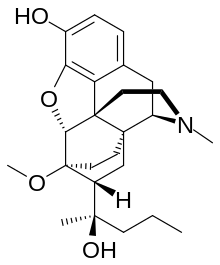
Dihydroetorphine
 | |
| Dữ liệu lâm sàng | |
|---|---|
| Mã ATC |
|
| Tình trạng pháp lý | |
| Tình trạng pháp lý |
|
| Các định danh | |
Tên IUPAC
| |
| Số đăng ký CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| Định danh thành phần duy nhất | |
| ECHA InfoCard | 100.214.784 |
| Dữ liệu hóa lý | |
| Công thức hóa học | C25H35NO4 |
| Khối lượng phân tử | 413.5497 g/mol |
| Mẫu 3D (Jmol) | |
SMILES
| |
Định danh hóa học quốc tế
| |
| (kiểm chứng) | |
Dihydroetorphin được phát triển bởi KW Bentley tại McFarlan-Smith vào những năm 1960 [1] và là thuốc giảm đau opioid mạnh,[2] được sử dụng chủ yếu ở Trung Quốc. Nó là một dẫn xuất của etioine opioid nổi tiếng hơn, được sử dụng như một loại thuốc giảm đau thú y và thuốc gây mê rất mạnh, chủ yếu để gây mê các động vật lớn như voi, hươu cao cổ và tê giác.
Dihydroetorphin là một opioid bán tổng hợp, được sử dụng chủ yếu như một loại thuốc giảm đau mạnh cho con người.[3] Nó mạnh hơn vài nghìn lần so với morphin (từ 1000x đến 12000x mạnh hơn tùy thuộc vào phương pháp nào được sử dụng để so sánh),[1] mặc dù nó được hấp thu kém khi dùng đường uống. Dạng dihydroetorphine dưới lưỡi được sử dụng ở Trung Quốc với liều khác nhau từ 20 đến 40 mg lặp đi lặp lại mỗi 3-4 giờ, và được báo cáo gây giảm đau mạnh mẽ và tác dụng phụ tương đối nhẹ so với opioid khác, mặc dù tất cả các tác dụng phụ opioid thông thường như chóng mặt, an thần, buồn nôn, táo bón và suy hô hấp có thể xảy ra. Các bản vá xuyên da của dihydroetorphin cũng đã được phát triển.[4]
Dihydroetorphin được coi là ít gây nghiện hơn so với nhiều loại thuốc phiện khác, và đôi khi cũng được sử dụng ở Trung Quốc như một loại thuốc duy trì thay thế cho người nghiện opioid,[5] theo cách tương tự như cách sử dụng thuốc buprenorphin liên quan ở các quốc gia phương tây.[6][7] Nó có lẽ được kiểm soát dưới dạng "este, ether, muối..." của etorine ở Hoa Kỳ theo Đạo luật về các chất bị kiểm soát năm 1970 và/hoặc các mảnh của bộ xương carbon morphine đặt nó theo "quy tắc morphin" và/hoặc hành động tương tự năm 1986; nó không có ACSCN riêng.[8] Quy định ở nơi khác có thể khác nhau nhưng có thể tương tự như đối với các chất chủ vận opioid mạnh khác.
Xem thêm[sửa | sửa mã nguồn]
Tham khảo[sửa | sửa mã nguồn]
- ^ a b Bentley, K. W.; Hardy, D. G. (1967). “Novel analgesics and molecular rearrangements in the morphine-thebaine group. 3. Alcohols of the 6,14-endo-ethenotetrahydrooripavine series and derived analogs of N-allylnormorphine and -norcodeine”. Journal of the American Chemical Society. 89 (13): 3281–3292. doi:10.1021/ja00989a032. PMID 6042764.
- ^ Martin, T. J.; Hairston, C. T.; Lutz, P. O.; Harris, L. S.; Porreca, F. (1998). “Anti-allodynic actions of intravenous opioids in the nerve injured rat: Potential utility of heroin and dihydroetorphine against neuropathic pain”. European Journal of Pharmacology. 357 (1): 25–32. doi:10.1016/S0014-2999(98)00531-7. PMID 9788770.
- ^ Lewis, J. W.; Husbands, S. M. (2004). “The orvinols and related opioids--high affinity ligands with diverse efficacy profiles”. Current Pharmaceutical Design. 10 (7): 717–732. doi:10.2174/1381612043453027. PMID 15032698.
- ^ Ohmori, S.; Morimoto, Y. (2002). “Dihydroetorphine: a potent analgesic: pharmacology, toxicology, pharmacokinetics, and clinical effects”. CNS Drug Reviews. 8 (4): 391–404. doi:10.1111/j.1527-3458.2002.tb00236.x. PMID 12481194.
- ^ Bo-Yi, Q. (1996). “Advances in dihydroetorphine: From analgesia to detoxification”. Drug Development Research. 39 (2): 131–134. doi:10.1002/(SICI)1098-2299(199610)39:2<131::AID-DDR3>3.0.CO;2-Q. Bản gốc lưu trữ ngày 25 tháng 5 năm 2013. Truy cập ngày 17 tháng 8 năm 2019.
- ^ Gerak, L. R.; Gauthier, C. R.; France, C. R. (2003). “Discriminative stimulus and antinociceptive effects of dihydroetorphine in rhesus monkeys”. Psychopharmacology. 166 (4): 351–359. doi:10.1007/s00213-002-1268-y. PMID 12601499.
- ^ Husbands, S. M.; Lewis, J. W. (2003). “Opioid ligands having delayed long-term antagonist activity: potential pharmacotherapies for opioid abuse”. Mini Reviews in Medicinal Chemistry. 3 (2): 137–144. doi:10.2174/1389557033405395. PMID 12570846.
- ^ “Bản sao đã lưu trữ”. Bản gốc lưu trữ ngày 2 tháng 3 năm 2016. Truy cập ngày 17 tháng 8 năm 2019.
