Chu kỳ tế bào

Chu kỳ tế bào, hay chu kỳ phân bào, là một vòng tuần hoàn các sự kiện xảy ra trong một tế bào từ lần phân bào này cho đến lần kế tiếp, trong đó bộ máy di truyền và các thành phần của tế bào được nhân đôi và sau đó tế bào phân chia làm hai tế bào con. Ở các sinh vật đơn bào (nấm men, vi khuẩn,...) một cá thể sau khi trải qua chu kỳ phân bào tạo ra hai cá thể mới; còn ở các sinh vật đa bào thì chu kỳ tế bào là một quá trình tối quan trọng để một hợp tử phát triển thành một cơ thể hoàn chỉnh và để cơ thể bổ sung số lượng tế bào thay cho số đã chết.[1]
Trong các tế bào nhân sơ, chu kỳ tế bào trải qua một quá trình mang tên là trực phân. Trong các tế bào nhân chuẩn chu kỳ tế bào bao gồm hai giai đoạn: giai đoạn thứ nhất kỳ trung gian lúc tế bào phát triển, tích lũy vật chất và nhân đôi DNA; giai đoạn thứ hai là nguyên phân (mitosis - M), lúc này tế bào thực thi quá trình phân chia thành hai tế bào con. Nhìn chung, chi tiết của chu trình tế bào thay đổi tùy loại tế bào và tùy sinh vật, tuy nhiên chúng có cùng những điểm chung nhất định và có cùng mục tiêu là truyền đạt lại toàn bộ và chính xác thông tin di truyền của chúng cho các tế bào con. Chính vì vậy bộ DNA của tế bào mẹ phải được nhân đôi một cách chính xác và phải được chia đồng đều cho các tế bào con để mỗi tế bào con đều nhận được bộ DNA y hệt tế bào mẹ.[1][2]
Các giai đoạn trong chu kỳ tế bào[sửa | sửa mã nguồn]
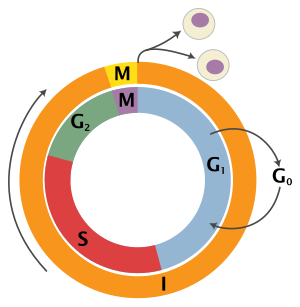
Chu kỳ tế bào có thể được chia thành các pha sau: G1, S [Gc 1], G2 (các pha G1, S, G2 được gộp lại thành kỳ trung gian[3][4]) và pha nguyên phân, hay pha M [Gc 2]. Bản thân pha M bao gồm hai quá trình liên quan chặt chẽ với nhau: quá trình nguyên phân trong đó nhiễm sắc thể của tế bào mẹ được chia tách ra làm hai phần bằng nhau, và quá trình phân chia tế bào chất (cytokinesis) trong đó tế bào chất của tế bào mẹ tách làm hai phần bằng nhau và hình thành hai tế bào con. Việc kích hoạt mỗi pha phụ thuộc vào sự tiến triển đúng cách của pha trước. Tế bào nếu có chu kỳ bị tạm thời ngưng trệ hay bị đảo ngược thì được xem như lâm vào một trạng thái tĩnh lặng gọi là pha G0.
| Trạng thái | Pha | Pha (viết tắt) | Mô tả |
|---|---|---|---|
| tĩnh lặng/ lão hóa |
Gap 0 (khoảng cách 0) |
G0 | Trong pha này tế bào không tham gia vào chu kỳ và ngưng phân chia. |
| Kỳ trung gian | Gap 1 (khoảng cách 1) |
G1 | Trong pha này tế bào tăng kích thước. Điểm kiểm soát G1 điều khiển các cơ chế giúp cho tế bào chuẩn bị đầy đủ mọi thứ trong G1 rồi mới tiến tới pha S. |
| Tổng hợp (synthesis) |
S | Sự nhân đôi DNA và nhiễm sắc thể (NST) xảy ra trong pha này. | |
| Gap 2 (khoảng cách 2) |
G2 | Trong pha G2 tế bào tiếp tục sinh trưởng. Điểm kiểm soát G2 điều khiển các cơ chế giúp cho tế bào chuẩn bị đầy đủ mọi thứ trong G2 rồi mới tiến tới phân chia trong nguyên phân. | |
| Phân bào | Nguyên phân (mitosis) |
M | Tế bào ngừng sinh trưởng và toàn bộ năng lượng được tập trung vào việc phân chia tế bào thành hai tế bào con một cách có quy củ. Ở giữa giai đoạn nguyên phân có một điểm kiểm soát ở kỳ giữa nhằm đảm bảo tế bào đã sẵn sàng hoàn tất quá trình phân bào. |
Sau khi quá trình phân bào kết thúc, các tế bào con tiếp tục kỳ trung gian của một chu kỳ tế bào mới cho riêng mình. Mặc dù thông thường các giai đoạn của kỳ trung gian không được phân biệt rõ ràng bằng các đặc điểm hình thái, mỗi kỳ hay pha của chu kỳ tế bào đều có những quá trình hóa sinh đặc trưng để chuẩn bị cho sự phân chia của tế bào.
Thời gian hoàn tất một chu kỳ tế bào tùy thuộc vào loại tế bào cũng như tùy sinh vật. Đối với người, các tế bào đang có tốc độ sinh sản nhanh hoàn tất một chu kỳ trong vòng 24 tiếng đồng hồ trong khi đối với các tế bào nấm men sinh sản nhanh thì thời gian này chỉ là 90 phút. Trong đó thì thời gian dùng để sinh trưởng và phát triển các bào quan dài hơn nhiều so với thời gian dùng để sao chép DNA và phân chia tế bào chất - ví dụ như trong tế bào người pha nguyên phân chỉ tốn từ 30 phút đến 1 giờ so với một chu kỳ đầy đủ là 24 giờ.[3][4]
Pha G0[sửa | sửa mã nguồn]
Thuật ngữ "hậu nguyên phân" hay "thời kỳ sau nguyên phân" (post-mitotic) thỉnh thoảng được dùng để ám chỉ pha G0 cũng như trạng thái suy lão của tế bào. Các tế bào không phân chia trong các sinh vật đa bào nhân chuẩn thường chuyển từ trạng thái của pha G1 sang trạng thái tĩnh lặng của pha G0 và có thể duy trì trạng thái tĩnh lặng này suốt một thời gian dài, thậm chí là vĩnh viễn[3] (ví dụ tế bào cơ, tế bào thần kinh hay tế bào của mô thủy tinh thể). Đây là điều phổ biến xảy ra trong các tế bào đã hoàn toàn biệt hóa. Trạng thái tĩnh lặng của tế bào xuất hiện khi DNA của chúng bị hư hỏng hay thoái hóa, điều này khiến tế bào không sinh sản được[Gc 3], hoặc giả khi các điều kiện ngoại bào tỏ ra không ủng hộ sự phân bào hay không có tín hiệu kích thích sự tiếp tục của chu kỳ tế bào[3]. Các tế bào ở trạng thái G0 cũng có thể phục hồi khả năng phân bào và quay trở về chu kỳ tế bào; quá trình này được cơ thể điều thiết nhằm đảm bảo sự sinh sản của tế bào nằm trong tầm kiểm soát.[6]
Kỳ trung gian[sửa | sửa mã nguồn]
Trước khi sự phân bào diễn ra, tế bào cần tích lũy các chất dinh dưỡng để chuẩn bị cho sự phân bào. Tất cả việc này diễn ra trong kỳ trung gian. Kỳ trung gian gồm có 3 pha: G1, S, và G2.
Pha G1[sửa | sửa mã nguồn]
Pha G1 - hay còn được gọi là pha sinh trưởng - là giai đoạn đầu tiên của kỳ trung gian, nó bắt đầu khi sự phân bào kết thúc cho đến khi sự sinh tổng hợp DNA bắt đầu xảy ra. Trong khi hoạt động sinh tổng hợp ở quá trình phân bào diễn ra khá chậm, trong pha G1 chúng tăng tốc rất nhanh chóng. Trong pha này nhiều enzyme đã được sản sinh nhằm phục vụ cho các hoạt động diễn ra trong pha S kế tiếp - phần lớn chúng là enzyme xúc tác quá trình tự nhân đôi DNA. Thời gian tiến hành pha G1 thay đổi nhiều tùy theo loài và tùy theo các loại tế bào trong cùng loài.[7] Trong giai đoạn này, kích thước tế bào tăng lên và tế bào tăng cường cung cấp protein cũng như tăng số lượng các bào quan khác (ti thể, ribosome). Ở người, pha này kéo dài chừng 5-6 tiếng đồng hồ.[4]
Pha S[sửa | sửa mã nguồn]
Tiếp theo pha G1 là pha S, bắt đầu khi sự sinh tổng hợp DNA xảy ra và kết thúc khi tất cả các nhiễm sắc thể đều được sao chép - lúc này mỗi nhiễm sắc thể bao hàm hai nhiễm sắc tử chị em. Vì vậy trong pha này, hàm lượng DNA trong tế bào được nhân đôi mặc dù số bội thể của tế bào không thay đổi. Tốc độ phiên mã RNA và sinh tổng hợp protein phải nói là cực kì chậm trong pha này. Tuy nhiên sự sinh tổng hợp histone thì vẫn mau lẹ - thực chất quá trình sinh tổng hợp histone chủ yếu diễn ra trong pha này.[8][9][10]
Pha G2[sửa | sửa mã nguồn]
Sau khi pha S kết thúc, tế bào sẽ chuyển sang pha G2 - pha này kéo dài cho đến khi quá trình nguyên phân bắt đầu. Sự sinh tổng hợp lại diễn ra mạnh ở pha này, trong đó chủ yếu là sự hình thành các sợi thoi hay vi quản vốn cần thiết cho quá trình nguyên phân. Việc ức chế sinh tổng hợp protein trong pha này sẽ khiến tế bào không thể nào bước vào quá trình nguyên phân được.
Pha nguyên phân[sửa | sửa mã nguồn]
Pha nguyên phân, hay còn gọi là pha M, là một pha ngắn bao hàm sự phân bào có tơ (karyokinesis). Pha nguyên phân có thể được chia là nhiều kỳ, lần lượt xếp theo thứ tự thời gian như sau:
- kỳ đầu hay tiền kỳ
- kỳ giữa hay trung kỳ
- kỳ sau hay hậu kỳ
- kỳ cuối hay mạt kỳ
- kỳ phân chia tế bào chất (cytokinesis)[Gc 4]
Nguyên phân là một quá trình mà trong đó tế bào nhân chuẩn chia tách nhiễm sắc thể trong nhân của nó thành hai phần giống hệt nhau để từ đó hình thành nên hai nhân cho hai tế bào con.[11] Ngay sau quá trình nguyên phân là quá trình phân chia tế bào chất (cytokinesis), trong đó nhân tế bào, tế bào chất, bào quan và màng tế bào được phân chia làm hai phần gần giống nhau để hình thành nên hai tế bào con gần giống nhau. Cả hai quá trình này được gộp lại thành pha nguyên phân hay pha M (mitotic phase) - trong đó sự phân bào diễn ra để tế bào mẹ phân chia thành hai tế bào con gần như giống hệt nhau và giống hệt tế bào mẹ. Quá trình này chiếm 10 phần trăm của chu kỳ tế bào; đối với người như đã nói pha nguyên phân chỉ chiếm từ 30 phút đến 1 giờ so với cả chu kỳ là 24 giờ.
Nguyên phân chỉ xảy ra trong các sinh vật nhân chuẩn, tuy nhiên tùy theo loài mà quá trình nguyên phân diễn ra khác nhau. Ví dụ như các động vật trải qua một quá trình nguyên phân "mở" trong đó màng nhân bị phân giải trước khi nhiễm sắc thể bị chia tách, trong khi đó các loại nấm như Aspergillus nidulans và nấm men Saccharomyces cerevisiae trải qua một quá trình nguyên phân "đóng" - tức sự phân chia diễn ra trong một nhân tế bào toàn vẹn.[12] Các sinh vật nhân sơ phân bào theo quá trình trực phân vì chúng không có nhân thật sự.
Quá trình nguyên phân phải nói là khá phức tạp và được điều tiết một cách chặt chẽ. Quá trình nguyên phân được chia thành nhiều kỳ - như đã nói ở trên và chúng tương ứng với sự kết thúc của một nhóm hoạt động trong tế bào cũng như sự khởi phát của một nhóm kế tiếp. Trong quá trình nguyên phân, các cặp nhiễm sắc thể xoắn chặt lại và trở nên co đặc, chúng bám vào các sợi thoi để các sợi thoi này kéo các nhiễm sắc tử chị em về hai phía đối nghịch nhau trong tế bào. Cuối cùng, toàn bộ tế bào mẹ chia làm hai tế bào con trong kỳ phân chia tế bào chất.[13]
Vì việc phân chia tế bào chất thường tiến hành chung với nguyên phân, thuật ngữ "nguyên phân" thường được dùng chung lẫn lộn với "pha nguyên phân" hay "pha M". Tuy nhiên có nhiều loại tế bào tiến hành nguyên phân và phân chia tế bào chất riêng rẽ với nhau, hình thành các tế bào với trong đó mỗi tế bào có nhiều nhân. Hiện tượng này phổ biến nhất trong các loại nấm và nấm nhầy, và cũng xảy ra trong một số nhóm sinh vật khác. Ngay cả trong động vật, phân chia tế bào chất và nguyên phân cũng có thể được tiến hành độc lập với nhau, ví dụ như trong một số giai đoạn phát triển phôi của ruồi dấm Drosophila melanogaster.[14] Những sai hổng xảy ra trong quá trình nguyên phân có thể khiến tế bào bị giết chết bởi sự chết tế bào được lập trình (tiêu biểu là chết rụng tế bào) hay biến nó thành tế bào ung thư.
Điều tiết chu kỳ tế bào sinh vật nhân chuẩn[sửa | sửa mã nguồn]
Việc điều tiết chu kỳ tế bào bao hàm các quá trình có vai trò tối quan trọng trong sự tồn vong của tế bào, bao gồm các quá trình nhận diện và sửa chữa những sai hổng trong bộ máy di truyền cũng như ngăn chặn sự phân bào vô tội vạ. Các sự kiện ở cấp độ phân tử điều kiển chu kỳ tế bào được sắp xếp có quy củ, theo thứ tự và có định hướng; điều này có nghĩa là mỗi quá trình tiến hành một cách liên tục, kế tiếp nhau và một chiều - bản thân chu kỳ tế bào nói chung không thể đảo ngược được.
Vai trò của cyclin và CDK[sửa | sửa mã nguồn]
Hai loại then chốt trong số các chất điều tiết chu kỳ tế bào là, cyclin và kinase phụ thuộc vào cyclin (cyclin-dependent kinase - CDK); chúng quyết định tiến trình của tế bào xuyên suốt chu kỳ của nó.[15] Leland H. Hartwell, R. Timothy Hunt, và Paul M. Nurse nhận được Giải Nobel Y học năm 2001 vì công lao của họ tìm ra được các nhân tố này.[16] Nhiều gien mã hóa cho cyclin và CDK được bảo tồn trong tất cả các sinh vật nhân chuẩn, tuy nhiên những sinh vật có cấu tạo phức tạp hơn thì có một cơ chế điều tiết chu kỳ tế bào tinh vi hơn và bao hàm nhiều thành phần tham gia hơn. Nhiều gien liên quan tới cơ chế này được nhận diện ở nấm men, nhất là loài Saccharomyces cerevisiae;[17] ở đây danh pháp di truyền học ở nấm men khiến nhiều gien như vậy mang cái tên cdc (viết tắt của chữ tiếng Anh "cell division cycle", có nghĩa là "chu trình phân bào") và một mã số theo sau nó, tỉ như cdc25 hay cdc20.
CDK là một enzyme loại kinase có vai trò phosphorylat hóa một số protein đích nhằm bất hoạt hay hoạt hóa chúng, nhờ đó điều tiết hay kích thích các sự kiện quan trọng trong chu kỳ tế bào và sắp xếp lại các cơ sở vật chất giúp tế bào chuyển sang pha tiếp theo của chu kỳ. Tuy nhiên, như cái tên đã đề cập, chúng chỉ được hoạt hóa khi được cyclin bám vào và hình thành một phức hợp dị nhị tụ. Các tổ hợp cyclin-CDK như thế này quyết định các protein đích ở phía dưới của chuỗi phản ứng. CDK chủ yếu biểu hiện trong các tế bào mà cyclin đã được sinh tổng hợp ở một số giai đoạn nhất định của chu kỳ tế bào nhằm phản ứng lại nhiều loại tín hiệu khác nhau ở cấp độ phân tử. Ở đây, hàm lượng CDK không thay đổi trong suốt chu kỳ tế bào, nhưng cyclin thì có, chúng được tổng hợp và phân giải một cách tuần hoàn - chính vì thế hoạt tính của CDK tăng và giảm trong suốt chu kỳ tế bào, điều này dẫn đến sự biến thiên theo chu kỳ của các phản ứng phosphoryl hóa do enzyme này gây ra.[18][19]
Phân loại[sửa | sửa mã nguồn]
Về phân loại, có bốn lớp cyclin chính, mỗi lớp cyclin sẽ hoạt hóa CDK ở một giai đoạn khác nhau. Tương ứng với các lớp cyclin này sẽ có các CDK khác nhau phù hợp với chúng.[18]
- Cyclin G1/S hoạt hóa CDK ở giai đoạn cuối của pha G1 và giúp tế bào vượt qua điểm giới hạn và tiến vào chu kỳ tế bào. Hàm lượng Cyclin này suy giảm vào pha S.
- Cyclin G1 có vai trò điều tiết hoạt tính của G1/S nói trên.
- Cyclin S hoạt hóa Cdk ngay sau khi tế bào vượt qua điểm giới hạn và qua đó giúp kích thích quá trình tự nhân đôi DNA. Cyclin S sẽ giảm dần vào pha nguyên phân mặc dù chúng vẫn có vai trò điều tiết một số hoạt động vào đầu pha này.
- Cyclin M hoạt hóa những CDK giúp tế bào tiến vào quá trình nguyên phân tại điểm kiểm soát G2/M. Chúng bị phân giải vào giai đoạn giữa của nguyên phân.
Một cách phân loại khác gộp lớp G1/S và lớp G1 thành nhóm G1 và hai lớp còn lại thành nhóm B. Tất cả các cyclin nhóm B mang một chuỗi amino acid gọi là "hộp phá hủy" (destruction box), chuỗi amino acid này được enzyme APC ubiquitin ligase nhận diện và vì vậy chúng được điều tiết bởi enzyme này; trong khi đó các cyclin nhóm G1 thì không có.[20]
Trong tế bào nấm men như Saccharomyces pombe và Saccharomyces cerevisae, tế bào chỉ sản xuất một loại CDK duy nhất. Tuy nhiên, các tế bào của động vật có xương sống có bốn loại CDK khác nhau (CDK 1,2,4,6). Mỗi phức hợp cyclin-CDK phosphoryl hóa một nhóm protein khác nhau và vì vậy chúng kích thích các loại hoạt động khác nhau trong tế bào, bản thân một loại phức hợp cũng có hiệu quả hoạt tính khác nhau tùy thời điểm trong chu kỳ.[18][20][21]
| Phức hợp Cyclin-CDK | Động vật có xương sống | Nấm men | ||
|---|---|---|---|---|
| Cyclin | CDK | Cyclin | CDK | |
| G1-CDK | Cyclin D1,D2,D3[Gc 5] | CDK4, CDK6 | Cln3 | CDK1 |
| G1/S-CDK | Cyclin E | CDK2 | Cln1, 2 | CDK1 |
| S-CDK | Cyclin A | CDK2, CDK1 | Clb5, 6 | CDK1 |
| M-CDK | Cyclin B | CDK1 | Clb1, 2, 3, 4 | CDK1 |
Nguồn:[21]
Các hoạt động đặc trưng của phức hợp cyclin-CDK[sửa | sửa mã nguồn]
Cyclin D là cyclin đầu tiên được sinh tổng hợp trong chu kỳ tế bào, nhằm phản ứng lại các tín hiệu ngoại bào tỉ như các nhân tố sinh trưởng. Cyclin D bám vào các CDK4 sẵn có, hình thành nên các phức hợp cyclin D-CDK4. Phức hợp cyclin D-CDK4 sẽ phosphorylat hóa các protein nhạy cảm với khối u ác tính ở mắt (Rb - Retinoblastoma protein). Các Rb bị phosphorylat hóa sẽ tách khỏi protein E2F và không thể ức chế E2F được nữa. E2F được hoạt hóa sẽ kích thích sự phiên mã của nhiều gien khác nhau nhằm sản sinh ra cyclin E, cyclin A, DNA polymerase, thymidin kinase,... và cả bản thân E2F.[22] Cyclin E mới sản sinh ra sẽ bám vào các CDK2, hình thành phức hợp cyclin E-CDK2, phức này sẽ thúc đẩy tế bào tiến từ pha G1 vào pha S (chuyển tiếp G1/S). Cyclin B cùng với cdc2 (ở động vật có vú là CDK1) hình thành nên phức hợp cyclin B-cdc2 có chức năng khơi mào quá trình chuyển tiếp G2/M.[23] Việc hoạt hóa phức hợp Cyclin B-cdc2 dẫn tới sự đổ vỡ của cấu trúc màng nhân sự mở đầu của kỳ đầu trong nguyên phân; và cuối cùng phức này bị bất hoạt sẽ khiến tế bào kết thúc quá trình nguyên phân.[19]
Điều tiết hoạt tính của CDK[sửa | sửa mã nguồn]
- Hàm lượng cyclin
Như đã nói, vì cyclin là nhân tố giúp hoạt hóa CDK (và bản thân hàm lượng CDK được giữ ổn định trong suốt chu kỳ tế bào) nên chính hàm lượng cyclin là nhân tố quyết định chủ đạo đối với hoạt tính của CDK. Tất nhiên, ngoài cyclin, tế bào còn có một số cơ chế khác nhằm tinh chỉnh hoạt tính của CDK ở một số giai đoạn nhất định.[18][21]
- Phosphorylat hóa CDK
Việc phosphorylat hóa CDK - do enzyme kinase Wee1 thực thi - sẽ diễn ra tại một cặp amino acid ở phần trên của vị trí hoạt động của CDK, qua đó ức chế hoạt tính của phức hợp cyclin-CDK. Việc phosphorylst hóa này chủ yếu nhằm vào CDK1 và diễn ra trước pha nguyên phân. Các gốc phosphat bị gắn vào CDK sau đó sẽ được enzyme phosphatase Cdc25 gỡ bỏ nhằm trả lại hoạt tính cho phức hợp cyclin-CDK. Cdc25 cũng chủ yếu tác động vào CDK1 khi pha nguyên phân bắt đầu xảy ra. Nói cách khác, cơ chế điều tiết của Wee1 và Cdc25 đóng vai trò quan trọng trong việc kiểm soát hoạt tính của cyclin M-CDK tại pha nguyên phân.[21][24]
- Bám vào phức hợp cyclin-CDK hay CDK
Một số protein mang tên là protein ức chế CDK (CDK inhibitor protein - CKI) tham gia vào việc điều tiết hoạt động của CDK bằng cách bám vào CDK và có thể cả cyclin, thay đổi cấu trúc không gian ba chiều tại vùng hoạt tính của nó và qua đó ức chế hoạt tính của phức hợp cyclin-CDK.[25]
Ở các động vật có vú, có thể nêu lên hai họ CKI trong nhóm này: cip/kip (protein tương tác CDK/protein ức chế kinase - CDK interacting protein/Kinase inhibitory protein) và INK4a/ARF (Inhibitor of Kinase 4/Alternative Reading Frame).
- Họ cip/kip bao hàm các protein p21CIP, p27KIP2 và p57KIP2. Chúng chặn chu kỳ tế bào ở pha G1 bằng cách bám vào và bất hoạt phức hợp cyclin D-CDK1; vì vậy chúng phải bị phân giải trước khi sự tự nhân đôi DNA diễn ra. Họ này cũng có thể bám vào các phức hợp cyclin-CDK khác trong chu kỳ tế bào của động vật có vú.
- Họ INK4a/ARF bao hàm vài loại protein nhỏ và có mối quan hệ gần với nhau, chúng tương tác với các CDK 4 và 6 để ngăn chận các CDK này bám vào cyclin và vì vậy cũng ức chế luôn hoạt tính của CDK.[26]
| cip/kip | |
|---|---|
| p21 | Có khả năng bám vào tất cả các phức hợp cyclin/CDK trong động vật có vú.[27] Phản ứng lại các sai hỏng, tổn thương về DNA bằng cách bất hoạt các phức hợp G1-CDK và S-CDK.[24][26] Gien mã hóa chúng được kích hoạt bởi p53. |
| p27 | Có vai trò mờ nhạt trong việc điều tiết sự phân bào.[26] Được hoạt hóa bởi nhân tố sinh trưởng biến đổi β (Transforming Growth Factor β -TGF β), một chất ức chế sinh trưởng.[28][29] |
| p57 | Bất hoạt các phức hợp G1/S-CDK và S-CDK trong pha G1 và nhờ đó giúp tế bào thoát khỏi chu kỳ và tiến tới biệt hóa. CDK 2 có thể phosphoryl hóa p57 và khiến chúng bị "đánh dấu" ubiquitin hóa bởi enzyme SCF.[24][26] |
| INKa/ARF | |
| p16 | Một chất ức chế khối u, chúng thường bị đột biến và bất hoạt trong các tế bào ung thư. Bất hoạt phức hợp G1-CDK trong pha G1.[24][26] |
| p14 | Bất hoạt protein MDM2, nhờ đó ngăn chặn sự phân giải của p53.[30] |
Các chất ức chế cdc25 được tổng hợp có thể hữu dụng trong việc chặn chu kỳ tế bào và vì vậy chúng được dùng để chống ung thư.[31]
Điều tiết bằng quá trình phân giải protein[sửa | sửa mã nguồn]
Khác với các giai đoạn khác, việc kích hoạt quá trình chuyển tiếp từ kỳ giữa sang kỳ cuối của nguyên phân được thực thi bởi quá trình phân giải protein.[25] Chúng sẽ bị "đánh dấu" bởi quá trình ubiquitin hóa, tức bị gắn các nhánh ubiquitin để các tiêu thể nhận diện và phân giải. Ưu điểm của cách điều tiết này nằm ở chỗ quá trình phân giải là một chiều, nhờ đó chu kỳ tế bào tiển triển mà không bị đảo ngược tại các thời điểm tối quan trọng[32].
Trong quá trình này, có thể kể đến vai trò của hai tác nhân quan trọng:
- Phức hợp xúc tiến kỳ sau hay thể chu kỳ (Anaphase-promoting complex/cyclosome - APC/C), một enzyme họ ligase ubiquitin; enzyme này chủ yếu ubiquitin hóa vào các tác nhân điều tiết liên quan tới việc thoát khỏi pha nguyên phân. Một mục tiêu quan trọng của APC/C là securin, một protein bảo hộ các liên kết giữa hai nhiễm sắc tử chị em. Mục tiêu quan trọng khác là các cyclin lớp S và lớp M; tiêu trừ chúng sẽ giúp bất hoạt phần lớn số CDK trong chu kỳ và nhờ đó các chất bị CDK phosphorylat hóa sẽ bị khử phosphat trong kỳ sau - việc này nhằm điều cần thiết cho việc hoàn tất nguyên phân và phân chia tế bào chất (như tháo xoắn nhiễm sắc thể, tái hình thành màng nhân,...). APC/C được hoạt hóa vào giai đoạn giữa của nguyên phân và hoạt động cho đến cuối pha G1 của chu kỳ sau, khi cyclin G1-S được hoạt hóa. Cách hoạt hóa APC/C là gắn các tiểu đơn vị thích hợp vào nó, tỉ như Cdc20 sẽ hoạt hóa APC/C tại thời điểm chuyển tiếp kỳ giữa-kỳ sau còn được tiểu đơn vị Cdh1 sẽ duy trì hoạt tính của nó từ cuối nguyên phân cho tới cuối pha G1.[33]
- Phức hợp bao hàm Skp, Cullin, hộp F hay phức hợp SCF cũng là một ligase ubiquitin. Nó ubiquitin hóa các tác nhân điều tiết ở cuối pha G1, ví dụ như các kinase ức chế cyclin CIK (tỉ như p27 ở động vật có vú và Sic1 ở nấm men), nhờ đó mà quá trình hoạt hóa cyclin S-CDK và sao chép DNA được kích hoạt. Ở đây, khác với APC/C, việc ubiquitin hóa của SCF chỉ được thực thi khi protein đích của nó bị cyclin G1-CDK phosphoryl hóa để hộp F của SCF nhận diện - sự khác biệt này có thể là do APC/C phải đảm nhận việc phosphoryl hóa nhiều loại tác nhân hơn so với SCF. Đồng thời, hoạt tính của SCF cũng được giữ nguyên suốt chu kỳ và hoạt động của nó được điều tiết gián tiếp bởi việc protein đích của nó được phosphoryl hóa hay không.[32]
Mạng lưới điều tiết phiên mã[sửa | sửa mã nguồn]
Có những bằng chứng cho thấy một mạng lưới phiên mã bán tự động đã hoạt động phối hợp với bộ máy CDK-cyclin nhằm điều tiết chu kỳ tế bào. Một số nghiên cứu về biểu hiện gien trong nấm men Saccharomyces cerevisiae đã nhận dạng khoảng 800 - 1200 gien có biểu hiện thay đổi xuyên suốt trong chu kỳ tế bào;[17][34][35] chúng được phiên mã ở mức độ cao trong một số giai đoạn của chu kỳ tế bào và ở mức độ thấp trong các giai đoạn còn lại. Trong khi bộ của các gien được nhận diện thay đổi theo các phương pháp điện toán và các tiêu chuẩn dùng để nhận dạng chúng, các nghiên cứu đều chỉ ra rằng phần lớn các gien của nấm men được điều tiết theo thời gian.[36]
Nhiều gien biểu hiện theo giai đoạn được thúc đẩy, dẫn hướng bởi các nhân tố phiên mã, các nhân tố này cũng được biểu hiện một cách định kì. Một bảng về các thí nghiệm gỡ bỏ đơn gien nhận diện được 48 nhân tố phiên mã (chiếm 20 phần trăm số nhân tố phiên mã không thiết yếu) cho thấy chu kỳ tế bào bị sai kém.[37] Các nghiên cứu về bộ gien sử dụng các công nghệ năng suất cao đã nhận dạng được các nhân tố phiên mã bám vào các vùng gien khởi động của bộ gien nấm men, và lập nên một sự tương quan giữa các phát hiện trên với các kiểu biểu hiện theo thời gian đã cho phép nhận diện các nhân tố phiên mã thúc đẩy các biểu hiện gien đặc trưng của từng pha chu kỳ.[34][38] Sự biểu hiện của các nhân tố phiên mã của pha sau đã được xúc tiến bởi các nhân tố phiên mã đặc trưng của pha trước, và các mô hình điện toán đã cho thấy một mạng lưới CDK độc lập của các nhân tố phiên mã đó là đủ để tạo nên một dao động ổn định trong biểu hiện gien.[35][39]
Các bằng chứng có từ các thí nghiệm cũng cho rằng biểu hiện gien có thể dao động theo các giai đoạn trong quá trình phân bào của các tế bào kiểu tự nhiên độc lập với bộ máy CDK-cyclin. Orlando và các đồng sự sử dụng các microarray để đo đạc sự biểu hiện của một bộ 1.271 gien đã được nhận diện định kỳ trong các tế bào bình thường cũng như các tế bào đột biến không có cyclin trong pha S và pha nguyên phân (clb1,2,3,4,5,6). Trong 1.271 gien đó, 882 tiếp tục biểu hiện trong các tế bào thiếu cyclin và cả tế bào bình thường mặc dù chu kỳ của các tế bào thiếu cyclin bị ngừng lại ở giai đoạn cuối pha G1 đầu pha S. 833 gien khác trong số đó biểu hiện khác nhau giữa các tế bào bình thường và các tế bào đột biến, cho thấy rằng các gien này được điều tiết trực tiếp hay gián tiếp bởi bộ máy CDK-cyclin. Một số gien biểu hiện trong cả hai loại tế bào thì cũng biểu hiện ở mức độ khác ở các tế bào đột biến so với tế bào bình thường. Điều này gợi ý rằng trong khi mạng lưới phiên mã có thể dao động độc lập với dao động của CDK-cyclin, chúng bắt cặp với CDK-cyclin theo phương cách để cả hai cùng tham gia vào việc đảm bảo sự chính xác về thời gian của các sự kiện xảy ra trong chu kỳ tế bào.[35] Một số hoạt động điều tiết khác bao gồm phosphoryl hóa, một phương pháp điều chỉnh hậu dịch mã, của các nhân tố phiên mã của chu kỳ tế bào bởi Cdk1 có thể thay đổi vị trí hay hoạt tính của các nhân tố phiên mã nhằm kiểm soát chặt chẽ sự chính xác về thời gian của các gien đích (Ubersax 2003; Sidorova 1995; White 2009).[37][40][41]
Trong khi phiên mã dao động đóng một vai trò quan trọng trong chu kỳ tế bào của nấm men, bộ máy CDK-cyclin hoạt động độc lập trong các chu kỳ của các tế bào trong thời kỳ sớm của phôi. Trước sự chuyển tiếp phôi nang giữa sự phiên mã ở hợp tử không xảy ra và tất cả các protein cần thiết, ví dụ như cyclin kiểu B, được dịch mã từ các RNA thông tin cung cấp từ người mẹ.[42]
Điểm kiểm soát chu kỳ tế bào[sửa | sửa mã nguồn]
Điểm kiểm soát chu kỳ tế bào được tế bào sử dụng nhằm giám sát và điều tiết diễn biến chu kỳ tế bào.[43] Điểm kiểm soát có vai trò ngăn chặn chu kỳ tế bào tại một số điểm nhất định, nhờ đó tế bào có thể kiểm định lại một số diễn biến và quá trình cần thiết và sửa chữa những chỗ sai hỏng của DNA. Tế bào không thể thực hiện pha kế tiếp của chu kỳ cho đến khi nó thỏa mãn các yêu cầu mà điểm kiểm soát đặt ra.
Một số điểm kiểm soát được thiết kế để đảm bảo các DNA bị sai hỏng hay thiếu sót sẽ không được truyền cho các tế bào con cháu. Hai điểm kiểm soát như vậy tồn tại là điểm kiểm soát G1/S và điểm kiểm soát G2/M. Sự chuyển tiếp G1/S là một bước hạn chế bởi tỉ lệ trong chu kỳ tế bào và cũng được biết đến với cái tên điểm giới hạn (trong tế bào động vật) hay điểm bắt đầu (trong nấm men).[19][44] Một mô hình về phản ứng của chu kỳ tế bào trước các sai hổng của DNA đã được đề xuất, mang tên là điểm kiểm soát sau nhân đôi DNA.
Protein p53 đóng một vai trò quan trọng trong việc khơi mào các cơ chế kiểm soát chu kỳ tế bào ở cả hai điểm kiểm soát G1/S và G2/M.
Vai trò trong việc hình thành khối u[sửa | sửa mã nguồn]
Những bất thường trong việc điều hòa chu kỳ tế bào có thể dẫn tới việc hình thành các khối u. Như đã nói, một số gien như các gien ức chế chu kỳ tế bào (RB, p53...) khi bị đột biến có thể khiến tế bào sinh sản vô tội vạ và hình thành khối u. Mặc dù chu kỳ tế bào khối u bằng hay dài hơn tế bào bình thường, trong các khối u tỉ lệ tế bào trong trạng thái sẵn sàng phân bào so với các tế bào ở trạng thái pha G0 cao hơn nhiều so với các tế bào bình thường; trong khi đó các tế bào bị chết rụng hay già lão vẫn không thay đổi. Chính vì thế mà tính tổng cộng thì số tế bào khối u sẽ từ từ tăng dần lên.
Những tế bào đang trải qua chu kỳ một cách tích cực là mục tiêu trong các liệu pháp chữa bệnh ung thư vì các DNA của chúng bộc lộ tương đối rõ rệt trong quá trình phân bào và vì vậy chúng dễ bị tổn thương bởi các loại thuốc hay tia bức xạ. Việc này được tận dụng tối đa trong việc điều trị ung thư bởi một phương pháp mang tên là debulking, lúc này một số lớn các tế bào khối u bị loại bỏ và điều này khiến một số lớn tế bào khối u còn trong pha G0 bị chuyển sang pha G1 (do dinh dưỡng, ôxi, nhân tố sinh trưởng,... dồi dào hơn vì các tế bào giảm đi). Các tế bào này nhanh chóng bị tiêu diệt bởi tia bức xạ hay thuốc ngay khi mới chớm thực thi chu kỳ tế bào.[19] Nhìn chung, các tế bào dễ bị tổn thương nhất vào cuối pha M và vào pha G2, còn sức chống chịu đối với bức xạ cao nhất ở cuối pha S. Đối với những tế bào có chu kỳ dài và pha G1 dài, chúng cũng có sức kháng cự tốt ở cuối pha G1. Kiểu đề kháng này liên quan đến mức độ các hợp chất sulfhydryl trong tế bào. Sulfhydryl có tác dụng kháng bức xạ và có mức độ cao nhất ở pha S và thấp nhất ở gần pha nguyên phân.
Tế bào động vật có vú có chu kỳ ngắn nhất trong môi trường nuôi cấy là tế bào ung thư biểu mô ruột - với chu kỳ kéo dài từ 9 đến 10 giờ. Còn tế bào gốc trong da chuột có thể có chu kỳ kéo dài đến 200 giờ. Những sự khác biệt này chủ yếu do khác biệt về thời gian ở pha G1, còn các pha M và S thì ít thay đổi.
Đồng bộ hóa mẻ cấy tế bào[sửa | sửa mã nguồn]
Một số phương pháp có thể dùng để đồng bộ hóa các tế bào trong cùng mẻ cấy bằng cách tạm thời chặn chu kỳ tế bào ở một pha nào đó. Ví dụ như serum starvation[45] và cho tế bào tiếp xúc với thymidine hay aphidicolin[46] sẽ chặn chu kỳ tế bào ở pha G1, mitotic shake-off, xử lý với colchicine[47] và nocodazole[48] chặn chu kỳ tế bào ở pha nguyên phân; và xử lý với 5-fluorodeoxyuridine chặn ở pha S.
Xem thêm[sửa | sửa mã nguồn]
- Mô hình toán học chu kỳ tế bào
- Phân tích chu kỳ tế bào
- Nguyên phân
- Giảm phân
- Kỳ trung gian
- Phương pháp chụp X quang—Dùng để xác định thời gian của mỗi pha trong chu kỳ.
- Yếu tố khai mào hóa sinh của chu kỳ tế bào
- Cdc25
Chú thích[sửa | sửa mã nguồn]
Cước chú[sửa | sửa mã nguồn]
- ^ S là viết tắt của synthesis, có nghĩa là "tổng hợp".
- ^ M là viết tắt của mitosis, có nghĩa là "nguyên phân".
- ^ Các tế bào như vậy cũng có thể lựa chọn tự hủy diệt chúng thông qua các quá trình chết tế bào được lập trình, ví dụ như chết rụng tế bào.
- ^ Thật ra, nói cho chính xác thì phân chia tế bào chất KHÔNG PHẢI là một phần của nguyên phân. Tuy nhiên giai đoạn này xảy ra ngay sau nguyên phân, lúc đó tế bào mẹ trải qua quá trình chính thức tách thành hai tế bào con.
- ^ Tùy loại tế bào mà hàm lượng D1, D2 hay D3 khác nhau.[20]
Nguồn dẫn[sửa | sửa mã nguồn]
- ^ a b Albert, trang 1053
- ^ Lodish, chương 21, trang 1
- ^ a b c d Albert, trang 1055
- ^ a b c Lodish, chương 21, trang 2
- ^ Cooper GM (2000). “Chapter 14: The Eukaryotic Cell Cycle”. The cell: a molecular approach (ấn bản 2). Washington, D.C: ASM Press. ISBN 0-87893-106-6.
- ^ Lodish, chương 21, trang 3
- ^ Smith JA, Martin L (1973). “Do cells cycle?”. Proc. Natl. Acad. Sci. U.S.A. 70 (4): 1263–7. doi:10.1073/pnas.70.4.1263. PMC 433472. PMID 4515625.
- ^ Wu RS, Bonner WM (1981). “Separation of basal histone synthesis from S-phase histone synthesis in dividing cells”. Cell. 27 (2 Pt 1): 321–30. doi:10.1016/0092-8674(81)90415-3. PMID 7199388.
- ^ Nelson DM, Ye X, Hall C, Santos H, Ma T, Kao GD, Yen TJ, Harper JW, Adams PD (2002). “Coupling of DNA synthesis and histone synthesis in S phase independent of cyclin/cdk2 activity”. Mol. Cell. Biol. 22 (21): 7459–72. doi:10.1128/MCB.22.21.7459-7472.2002. PMC 135676. PMID 12370293.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- ^ Cameron IL, Greulich RC (1963). “Evidence for an essentially constant duration of DNA synthesis in renewing epithelia of the adult mouse”. J. Cell Biol. 18: 31–40. doi:10.1083/jcb.18.1.31. PMC 2106275. PMID 14018040.
- ^ Rubenstein, Irwin, and Susan M. Wick. "Cell." World Book Online Reference Center. 2008. ngày 12 tháng 1 năm 2008 <http://www.worldbookonline.com/wb/Article?id=ar102240 Lưu trữ 2011-05-30 tại Wayback Machine>
- ^ De Souza CP, Osmani SA (2007). “Mitosis, not just open or closed”. Eukaryotic Cell. 6 (9): 1521–7. doi:10.1128/EC.00178-07. PMC 2043359. PMID 17660363.
- ^ Anthea Maton & Hopkins, Jean Johnson, Susan LaHart, David, Quon Warner, David, Wright, Jill D (1997). Cells: Building Blocks of Life. New Jersey: Prentice Hall. tr. 70–4. ISBN 0-13423476-6.Quản lý CS1: sử dụng tham số tác giả (liên kết)
- ^ Lilly M, Duronio R (2005). “New insights into cell cycle control from the Drosophila endocycle”. Oncogene. 24 (17): 2765–75. doi:10.1038/sj.onc.1208610. PMID 15838513.
- ^ Nigg EA (1995). “Cyclin-dependent protein kinases: key regulators of the eukaryotic cell cycle”. Bioessays. 17 (6): 471–80. doi:10.1002/bies.950170603. PMID 7575488.
- ^ “Press release”. Nobelprize.org.
- ^ a b Spellman PT, Sherlock G, Zhang MQ, Iyer VR, Anders K, Eisen MB, Brown PO, Botstein D, Futcher B (1998). “Comprehensive identification of cell cycle-regulated genes of the yeast Saccharomyces cerevisiae by microarray hybridization”. Mol. Biol. Cell. 9 (12): 3273–97. PMC 25624. PMID 9843569.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- ^ a b c d Albert, trang 1062
- ^ a b c d Robbins and Cotran (2004). Pathological Basis of Disease. Kumar, Abbas, Fausto. Elsevier. ISBN 81-8147-528-3.
- ^ a b c Lodish, chương 21, trang 31
- ^ a b c d Albert, trang 1063
- ^ Lodish, chương 21, trang 33
- ^ Norbury C (1995). “Cdc2 protein kinase (vertebrates)”. Trong Hardie, D. Grahame; Hanks, Steven (biên tập). Protein kinase factsBook. Boston: Academic Press. tr. 184. ISBN 0-12-324719-5.Quản lý CS1: nhiều tên: danh sách biên tập viên (liên kết)
- ^ a b c d Albert, trang 1066
- ^ a b Albert, trang 1064
- ^ a b c d e Lodish, chương 21, trang 34
- ^ Lodish, chương 21, trang 37.
- ^ Toyoshima H, Hunter T (1994). “p27, a novel inhibitor of G1 cyclin-Cdk protein kinase activity, is related to p21”. Cell. 78 (1): 67–74. doi:10.1016/0092-8674(94)90573-8. PMID 8033213.
|ngày truy cập=cần|url=(trợ giúp) - ^ Klopfleisch R, Schütze M, Gruber AD. (2009). “Downregulation of transforming growth factor β (TGFβ) and latent TGFβ binding protein (LTBP)-4 expression in late stage canine mammary tumours”. Veterinary Journal. 186 (3): 379–84. doi:10.1016/j.tvjl.2009.09.014. PMID 19836277.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- ^ MeSH Tumor+Suppressor+Protein+p14ARF
- ^ “Presentation on CDC25 PHOSPHATASES: A Potential Target for Novel Anticancer Agents”. Bản gốc lưu trữ ngày 3 tháng 3 năm 2016. Truy cập ngày 4 tháng 6 năm 2011.
- ^ a b Lodish, chương 21, trang 26
- ^ Lodish, chương 21, trang 4
- ^ a b Pramila T, Wu W, Miles S, Breeden L (2006). “The Forkhead transcription factor Hcm1 regulates chromosome segregation genes and fills the S-phase gap in the transcriptional circuitry of the cell cycle”. Genes Dev. 20 (20): 2266–227. doi:10.1101/gad.1450606. PMC 1553209. PMID 16912276.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- ^ a b c Orlando DA, Lin CY, Bernard A, Wang JY, Socolar JES, Iversen ES, Hartemink AJ, Haase SB (2008). “Global control of cell-cycle transcription by coupled CDK and network oscillators”. Nature. 453 (453): 944–947. doi:10.1038/nature06955.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- ^ de Lichtenberg U, Jensen LJ, Fausbøll A, Jensen TS, Bork P, Brunak S (2005). “Comparison of computational methods for the identification of cell cycle-regulated genes”. Bioinformatics. 21 (7): 1164–1171. doi:10.1093/bioinformatics/bti093. PMID 15513999.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- ^ a b White MA, Riles L, Cohen BA (2009). “A systematic screen for transcriptional regulators of the yeast cell cycle”. Genetics. 181 (2): 435–46. doi:10.1534/genetics.108.098145. PMC 2644938. PMID 19033152.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- ^ Lee T (2002). “Transcriptional Regulatory Networks in Saccharomyces cerevisiae”. Science. 298 (5594): 799–804. doi:10.1126/science.1075090. PMID 12399584.
- ^ Simon I (2001). “Serial Regulation of Transcriptional Regulators in the Yeast Cell Cycle”. Cell. 106 (6): 697–708. doi:10.1016/S0092-8674(01)00494-9. PMID 11572776.[liên kết hỏng]
- ^ Sidorova JM, Mikesell GE, Breeden LL (1995). “Cell cycle-regulated phosphorylation of Swi6 controls its nuclear localization”. Mol Biol Cell. 6 (12): 1641–1658. doi:10.1038/nature02062. PMC 301322. PMID 8590795.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- ^ Ubersax J (2003). “Targets of the cyclin-dependent kinase Cdk1”. Nature. 425 (6960): 859–864. Bibcode:2003Natur.425..859U. doi:10.1038/nature02062. PMC 301322. PMID 14574415.
- ^ Morgan DO (2007). “2-3”. The Cell Cycle: Principles of Control. London: New Science Press. tr. 18. ISBN 0=9539181-2-2 Kiểm tra giá trị
|isbn=: ký tự không hợp lệ (trợ giúp). - ^ Stephen J. Elledge (ngày 6 tháng 12 năm 1996). “Cell Cycle Checkpoints: Preventing an Identity Crisis”. Science. 274 (5293): 1664–1672. doi:10.1126/science.274.5293.1664. PMID 8939848.
- ^ Lodish, chương 20, trang 31
- ^ Kues WA, Anger M, Carnwath JW, Paul D, Motlik J, Niemann H (2000). “Cell cycle synchronization of porcine fetal fibroblasts: effects of serum deprivation and reversible cell cycle inhibitors”. Biol. Reprod. 62 (2): 412–9. doi:10.1095/biolreprod62.2.412. PMID 10642581.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- ^ Pedrali-Noy G, Spadari S, Miller-Faurès A, Miller AO, Kruppa J, Koch G (1980). “Synchronization of HeLa cell cultures by inhibition of DNA polymerase alpha with aphidicolin”. Nucleic Acids Res. 8 (2): 377–87. doi:10.1093/nar/8.2.377. PMC 327273. PMID 6775308.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- ^ Prather RS, Boquest AC, Day BN (1999). “Cell cycle analysis of cultured porcine mammary cells”. Cloning. 1 (1): 17–24. doi:10.1089/15204559950020067. PMID 16218827.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- ^ Samaké S, Smith LC (1997). “Synchronization of cell division in eight-cell bovine embryos produced in vitro: effects of aphidicolin”. Theriogenology. 48 (6): 969–76. doi:10.1016/S0093-691X(97)00323-3. PMID 16728186.
Tham khảo[sửa | sửa mã nguồn]
- Morgan DO (2007). The Cell Cycle: Principles of Control. London: Published by New Science Press in association with Oxford University Press. ISBN 0-87893-508-8.
- Bruce Alberts (2008). “17”. Molecular Biology of the Cell. Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts, Peter Walter . Garland Science, Taylor & Francis Group. ISBN 978-0-8153-4106-2.
- Krieger M, Scott MP; Matsudaira PT, Lodish HF, Darnell JE, Zipursky L, Kaiser C; Berk A (2004). Molecular cell biology. New York: W.H. Freeman and CO. ISBN 0-7167-4366-3.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- Watson JD, Baker TA, Bell SP, Gann A, Levine M, Losick R (2004). “Chapter 7”. Molecular biology of the gene (ấn bản 5). San Francisco: Pearson/Benjamin Cummings. ISBN 0-8053-4642-2.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- Harvey Lodish (2003). “22”. Molecular Cell Biology. Arnold Berk, Paul Matsudaira, Chris A. Kaiser, Monty Krieger, Matthew P. Scott, Lawrence Zipursky, James Darnell . ISBN 0716743663.
Liên kết ngoài[sửa | sửa mã nguồn]
| Wikimedia Commons có thêm hình ảnh và phương tiện truyền tải về Chu kỳ tế bào. |
 Bài viết này có sử dụng các nguồn liệu từ Science Primer phát hành tại NCBI, vì đây là một tác phẩm của chính quyền liên bang Hoa Kỳ nên nó thuộc phạm vi công cộng [1].
Bài viết này có sử dụng các nguồn liệu từ Science Primer phát hành tại NCBI, vì đây là một tác phẩm của chính quyền liên bang Hoa Kỳ nên nó thuộc phạm vi công cộng [1].- Cell Cycle and Cytokinesis - The Virtual Library of Biochemistry and Cell Biology Lưu trữ 2005-09-23 tại Wayback Machine
- Transcriptional program of the cell cycle: high-resolution timing
- Cell cycle and metabolic cycle regulated transcription in yeast
- Cell Cycle Animation Lưu trữ 2012-06-25 tại Wayback Machine 1Lec.com
- Cell Cycle and Cytokinesis - The Virtual Library of Biochemistry and Cell Biology Lưu trữ 2005-09-23 tại Wayback Machine
- Cell Cycle
- Cell Cycle Portal
- Fucci:Using GFP to visualize the cell-cycle
- Science Creative Quarterly's overview of the cell cycle
- Cells alive
- CCO Lưu trữ 2019-02-15 tại Wayback Machine The Cell-Cycle Ontology
- KEGG - Human Cell Cycle Lưu trữ 2008-11-03 tại Wayback Machine
- Cell cycle modeling Lưu trữ 2007-07-28 tại Wayback Machine
- Drosophila Cell Cycle Genes - The Interactive Fly
