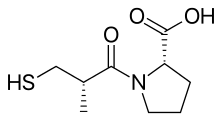
Captopril
 | |
 | |
| Dữ liệu lâm sàng | |
|---|---|
| Phát âm | /ˈkæptəprɪl/ |
| Tên thương mại | Capoten, others |
| AHFS/Drugs.com | Chuyên khảo |
| MedlinePlus | a682823 |
| Danh mục cho thai kỳ | |
| Dược đồ sử dụng | BY mouth |
| Mã ATC | |
| Tình trạng pháp lý | |
| Tình trạng pháp lý |
|
| Dữ liệu dược động học | |
| Sinh khả dụng | 70–75% |
| Chuyển hóa dược phẩm | Gan |
| Chu kỳ bán rã sinh học | 1.9 hours |
| Bài tiết | Thận |
| Các định danh | |
Tên IUPAC
| |
| Số đăng ký CAS | |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| Định danh thành phần duy nhất | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| Phối tử ngân hàng dữ liệu protein | |
| ECHA InfoCard | 100.057.806 |
| Dữ liệu hóa lý | |
| Công thức hóa học | C9H15NO3S |
| Khối lượng phân tử | 217.29 g/mol |
| Mẫu 3D (Jmol) | |
SMILES
| |
Định danh hóa học quốc tế
| |
| (kiểm chứng) | |
Captopril, được bán dưới tên thương hiệu Capoten trong số các tên khác, là một chất ức chế men chuyển angiotensin (ACE) được sử dụng để điều trị tăng huyết áp và một số loại suy tim sung huyết.
Nó đã được cấp bằng sáng chế vào năm 1976 và được chấp thuận cho sử dụng y tế vào năm 1980.[1]
Sử dụng trong y tế[sửa | sửa mã nguồn]

Công dụng chính của Captopril dựa trên sự giãn mạch và ức chế một số hoạt động chức năng thận. Những lợi ích này được thấy rõ nhất ở: 1) Tăng huyết áp 2) Các bệnh về tim như suy tim sung huyết và sau nhồi máu cơ tim 3) Bảo tồn chức năng thận trong bệnh thận đái tháo đường.
Ngoài ra, nó đã cho thấy các đặc tính nâng cao tâm trạng ở một số bệnh nhân. Điều này phù hợp với quan sát rằng các mô hình sàng lọc động vật chỉ ra hoạt động chống trầm cảm giả định cho hợp chất này, mặc dù một nghiên cứu đã cho kết quả âm tính. Các thử nghiệm lâm sàng chính thức ở bệnh nhân trầm cảm chưa được báo cáo.[3]
Nó cũng đã được điều tra để sử dụng trong điều trị ung thư.[4] Captopril stereoisomers cũng đã được báo cáo để ức chế một số kim β—lactamase.[5]
Tác dụng phụ[sửa | sửa mã nguồn]
Tác dụng bất lợi của captopril bao gồm ho do tăng nồng độ bradykinin trong huyết tương, phù mạch, mất bạch cầu hạt, protein niệu, tăng kali máu, thay đổi vị giác, gây quái thai, hạ huyết áp, suy thận cấp và giảm bạch cầu.[6] Ngoại trừ hạ huyết áp tư thế, xảy ra do chế độ tác dụng ngắn và nhanh của captopril, hầu hết các tác dụng phụ được đề cập là phổ biến đối với tất cả các thuốc ức chế men chuyển. Trong số này, ho là tác dụng phụ phổ biến nhất. Tăng kali máu có thể xảy ra, đặc biệt là nếu được sử dụng với các loại thuốc khác làm tăng nồng độ kali trong máu, chẳng hạn như thuốc lợi tiểu tiết kiệm kali. Các tác dụng phụ khác là:
Hồ sơ phản ứng có hại của thuốc (ADR) của captopril tương tự như các thuốc ức chế men chuyển khác, với ho là ADR phổ biến nhất.[7] Tuy nhiên, captopril cũng thường liên quan đến phát ban và rối loạn vị giác (kim loại hoặc mất vị giác), được cho là do chất gây nghiện thiol độc đáo.[8]
Captopril cũng có một hồ sơ dược động học tương đối kém. Thời gian bán hủy ngắn cần hai hoặc ba lần mỗi ngày, điều này có thể làm giảm sự tuân thủ của bệnh nhân.
Quá liều[sửa | sửa mã nguồn]
Captopril (như các thuốc ức chế men chuyển khác) quá liều có thể được điều trị bằng naloxone.[9][10][11]
Lịch sử[sửa | sửa mã nguồn]
Nó đã được cấp bằng sáng chế vào năm 1976 và được chấp thuận cho sử dụng y tế vào năm 1980.[1] Nó là chất ức chế men chuyển đầu tiên được phát triển và được coi là một bước đột phá cả vì cơ chế hoạt động của nó và cũng vì quá trình phát triển.[12] Captopril được phát hiện và phát triển tại ER Squibb & Sons Dược phẩm dựa trên các khái niệm được tiên phong bởi người đoạt giải Nobel Sir John Vane và hiện được bán bởi Bristol-Myers Squibb.[13]
Captopril được phát triển vào năm 1975 bởi ba nhà nghiên cứu tại công ty dược phẩm Squibb (nay là Bristol-Myers Squibb): Miguel Ondetti, Bernard Rubin và David Cushman. Squibb nộp đơn xin bảo hộ bằng sáng chế của Hoa Kỳ về thuốc vào tháng 2 năm 1976 và Bằng sáng chế Hoa Kỳ 4.046.889 đã được cấp vào tháng 9/2017.
Sự phát triển của captopril là một trong những thành công sớm nhất của khái niệm cách mạng về thiết kế thuốc dựa trên phối tử. Hệ thống renin-angiotensin-aldosterone đã được nghiên cứu rộng rãi vào giữa thế kỷ 20, và hệ thống này đưa ra một số mục tiêu cơ hội trong việc phát triển các phương pháp điều trị mới cho bệnh tăng huyết áp. Hai mục tiêu đầu tiên đã được thử là renin và ACE. Captopril là đỉnh cao của những nỗ lực của các phòng thí nghiệm của Squibb để phát triển một chất ức chế men chuyển.
Ondetti, Cushman và các đồng nghiệp được xây dựng dựa trên công trình đã được thực hiện vào những năm 1960 bởi một nhóm các nhà nghiên cứu do John Vane đứng đầu tại Đại học Phẫu thuật Hoàng gia Anh. Bước đột phá đầu tiên được thực hiện bởi Kevin KF Ng [14][15][16] vào năm 1967, khi ông tìm thấy sự chuyển đổi angiotensin I thành angiotensin II diễn ra trong tuần hoàn phổi thay vì trong huyết tương. Ngược lại, Sergio Ferreira [17] tìm thấy bradykinin biến mất trong quá trình lưu thông qua tuần hoàn phổi. Sự chuyển đổi angiotensin I thành angiotensin II và sự bất hoạt của bradykinin được cho là qua trung gian của cùng một loại enzyme.
Năm 1970, sử dụng yếu tố làm tăng bradykinin (BPF) do Sergio Ferreira cung cấp,[18] Ng và Vane đã tìm thấy sự chuyển đổi angiotensin I thành angiotensin II bị ức chế trong quá trình lưu thông qua phổi. BPF sau đó đã được tìm thấy là một peptide trong nọc độc của viper lancehead (Bothrops jararaca), là một chất ức chế sản phẩm được thu thập của chanh của enzyme chuyển đổi. Captopril đã được phát triển từ peptide này sau khi nó được tìm thấy thông qua sửa đổi dựa trên QSAR rằng nửa sulfhydryl cuối cùng của peptide cung cấp khả năng ức chế men chuyển cao.[19][19]
Captopril đã được FDA chấp thuận vào ngày 6 tháng 4 năm 1981. Thuốc đã trở thành một loại thuốc chung ở Mỹ vào tháng 2 năm 1996, khi loại trừ thị trường được tổ chức bởi Bristol-Myers Squibb cho captopril hết hạn.
Sự phát triển của captopril đã được tuyên bố là một ví dụ của 'biopiracy' (thương mại hóa các loại thuốc truyền thống), vì không có lợi ích nào được truyền lại cho bộ lạc Brazil bản địa, người đầu tiên sử dụng nọc độc pit viper như một chất độc đầu mũi tên.[20]
Tổng hợp hóa học[sửa | sửa mã nguồn]
Một tổng hợp hóa học của captopril bằng cách xử lý L-proline với (2S)-3-acetylthio-2-methylpropanoyl chloride trong điều kiện cơ bản (NaOH), sau đó là aminolysis của nhóm acetyl bảo vệ để làm lộ ra thiol tự do của thuốc, được mô tả trong hình bên phải [21]
| Captopril tổng hợp 1 | Captopril tổng hợp 2 |
|---|---|
 |
 |
Quy trình 2 lấy ra bằng sáng chế US4105776. Xem ví dụ 28, 29a và 36.
Dược động học[sửa | sửa mã nguồn]
Không giống như phần lớn các thuốc ức chế men chuyển, captopril không được dùng dưới dạng prodrug (loại duy nhất khác là lisinopril).[26] Khoảng 70% captopril dùng đường uống được hấp thụ. Sinh khả dụng bị giảm do sự hiện diện của thức ăn trong dạ dày. Nó được chuyển hóa một phần và bài tiết một phần không đổi qua nước tiểu.[27]
Xem thêm[sửa | sửa mã nguồn]
- Thử thách Captopril
- Thử nghiệm ức chế Captopril
Tham khảo[sửa | sửa mã nguồn]
- ^ a b Fischer, Jnos; Ganellin, C. Robin (2006). Analogue-based Drug Discovery (bằng tiếng Anh). John Wiley & Sons. tr. 467. ISBN 9783527607495.
- ^ Akif, M.; Georgiadis, D.; Mahajan, A.; Dive, V.; Sturrock, E. D.; Isaac, R. E.; Acharya, K. R. (2010). “High-Resolution Crystal Structures of Drosophila melanogaster Angiotensin-Converting Enzyme in Complex with Novel Inhibitors and Antihypertensive Drugs”. Journal of Molecular Biology. 400 (3): 502–517. doi:10.1016/j.jmb.2010.05.024. PMID 20488190.
- ^ Novel Pharmacological Approaches to the Treatment of Depression
- ^ Attoub S; Gaben AM; Al-Salam S; và đồng nghiệp (tháng 9 năm 2008). “Captopril as a potential inhibitor of lung tumor growth and metastasis”. Ann. N. Y. Acad. Sci. 1138: 65–72. doi:10.1196/annals.1414.011. PMID 18837885. Bản gốc lưu trữ ngày 5 tháng 1 năm 2013.
- ^ Brem, Jürgen; van Berkel, Sander S.; Zollman, David; Lee, Sook Y.; Gileadi, Opher; McHugh, Peter J.; Walsh, Timothy R.; McDonough, Michael A.; Schofield, Christopher J. (ngày 31 tháng 12 năm 2015). “Structural Basis of Metallo-β-Lactamase Inhibition by Captopril Stereoisomers”. Antimicrobial Agents and Chemotherapy. 60 (1): 142–150. doi:10.1128/AAC.01335-15. ISSN 0066-4804. PMC 4704194. PMID 26482303.[liên kết hỏng]
- ^ “Captopril (ACE inhibitor): side effects”. lifehugger. ngày 9 tháng 7 năm 2008. Bản gốc lưu trữ ngày 14 tháng 8 năm 2009. Truy cập ngày 2 tháng 5 năm 2009.
- ^ Rossi S, editor. Australian Medicines Handbook 2006. Adelaide: Australian Medicines Handbook; 2006.
- ^ Atkinson, AB; Robertson, JI (1979). “Captopril in the treatment of clinical hypertension and cardiac failure”. Lancet. 2 (8147): 836–9. doi:10.1016/S0140-6736(79)92186-X. PMID 90928.
- ^ Goldfrank's toxicologic emergencies, Lewis R. Goldfrank, Neal Flomenbaum, page 953.
- ^ Meyler's Side Effects of Analgesics and Anti-inflammatory Drugs, Jeffrey K. Aronson, page 120.
- ^ Ajayi, A A (1985). “Effect of naloxone on the actions of captopril”. Clin Pharmacol Ther. 38 (5): 560–565. doi:10.1038/clpt.1985.224. PMID 2996820.
- ^ “Chronicals of Drug Discovery, vol. 2”. Journal of Pharmaceutical Sciences. 74: 1029–1030. doi:10.1002/jps.2600740942.
- ^ Bryan, Jenny (2009). “From snake venom to ACE inhibitor the discovery and rise of captopril”. Pharmaceutical Journal. Truy cập ngày 8 tháng 1 năm 2015.
- ^ Ng, KKF; Vane, JR (1967). “Conversion of angiotensin I to angiotensin II”. Nature. 216: 762–766. doi:10.1038/216762a0. PMID 4294626.
- ^ Ng, KKF; Vane, JR (1968). “Fate of angiotensin I in the circulation”. Nature. 218: 144–150. doi:10.1038/218144a0. PMID 4296306.
- ^ Ng, KKF; Vane, JR (1970). “Some properties of angiotensin converting enzyme in the lung in vivo”. Nature. 225: 1142–1144. doi:10.1038/2251142b0. PMID 4313869.
- ^ Ferreira, SH; Vane, JR (1967). “The disappearance of bradykinin and eledoisin in the circulation and vascular beds of the cat”. Br. J. Pharmacol. Chemother. 30: 417–424. doi:10.1111/j.1476-5381.1967.tb02148.x. PMC 1557274.
- ^ Smith CG, Vane JR (tháng 5 năm 2003). “The discovery of captopril”. FASEB J. 17 (8): 788–9. doi:10.1096/fj.03-0093life. PMID 12724335.
- ^ a b Patlak M (tháng 3 năm 2004). “From viper's venom to drug design: treating hypertension”. FASEB J. 18 (3): 421. doi:10.1096/fj.03-1398bkt. PMID 15003987.
- ^ “Ellsworth B., Brazil to step up crackdown on "biopiracy" in 2011, Ruters, Dec. 22, 2010”. Bản gốc lưu trữ ngày 7 tháng 9 năm 2012. Truy cập ngày 29 tháng 6 năm 2019.
- ^ Shimazaki, M.; Hasegawa, J.; Kan, K.; Nomura, K.; Nose, Y.; Kondo, H.; Ohashi, T.; Watanabe, K. (1982). “Synthesis of captopril starting from an optically active.BETA.-hydroxy acid”. Chem. Pharm. Bull. 30 (9): 3139–3146. doi:10.1248/cpb.30.3139.
- ^ M. A. Ondetti, D. W. Cushman, Đăng ký phát minh {{{country}}} {{{number}}}, "{{{title}}}", trao vào [[{{{gdate}}}]]; eidem, Bằng sáng chế Hoa Kỳ số 4.046.889 and Bằng sáng chế Hoa Kỳ số 4.105.776 (1977, 1977, 1978 all to Squibb).
- ^ Ondetti, M.; Rubin, B; Cushman, D. (1977). “Design of specific inhibitors of angiotensin-converting enzyme: New class of orally active antihypertensive agents”. Science. 196 (4288): 441–4. doi:10.1126/science.191908. PMID 191908.
- ^ Cushman, D. W.; Cheung, H. S.; Sabo, E. F.; Ondetti, M. A. (1977). “Design of potent competitive inhibitors of angiotensin-converting enzyme. Carboxyalkanoyl and mercaptoalkanoyl amino acids”. Biochemistry. 16 (25): 5484–91. doi:10.1021/bi00644a014. PMID 200262.
- ^ Nam, Doo H.; Lee, Choon S.; Ryu, Dewey D. Y. (1984). “An improved synthesis of captopril”. Journal of Pharmaceutical Sciences. 73 (12): 1843–4. doi:10.1002/jps.2600731251. PMID 6396401.
- ^ Brown, NJ; Vaughan, DE (1998). “Angiotensin-converting enzyme inhibitors”. Circulation. 97 (14): 1411–20. doi:10.1161/01.cir.97.14.1411. PMID 9577953.
- ^ Duchin, KL; McKinstry, DN; Cohen, AI; Migdalof, BH (1988). “Pharmacokinetics of captopril in healthy subjects and in patients with cardiovascular diseases”. Clinical Pharmacokinetics. 14 (4): 241–59. doi:10.2165/00003088-198814040-00002. PMID 3292102.
