Vinylacetylen
Bài viết này hiện đang được thành viên NgocAnMaster (thảo luận · đóng góp) cho là bài chất lượng kém vì lý do: Dịch máy |
Bài viết này có thể cần được viết lại toàn bộ để thỏa mãn tiêu chuẩn chất lượng của Wikipedia. (2024-7-18) |
| Vinylacetylen | |
|---|---|
 | |
 | |
 | |
| Tên khác | Butenyne, normal isomer 3-Butene-1-yne, Vinyl acetylene |
| Nhận dạng | |
| Số CAS | |
| PubChem | |
| ChEBI | |
| Ảnh Jmol-3D | ảnh |
| SMILES | đầy đủ
|
| InChI | đầy đủ
|
| UNII | |
| Thuộc tính | |
| Công thức phân tử | C4H4 |
| Khối lượng mol | 52.07456 g/mol |
| Bề ngoài | colourless gas |
| Điểm nóng chảy | |
| Điểm sôi | 0 đến 6 °C (273 đến 279 K; 32 đến 43 °F) |
| Độ hòa tan trong nước | low |
| Các nguy hiểm | |
| Nguy hiểm chính | flammable |
| NFPA 704 |
|
| Điểm bắt lửa | < |
| [1] | |
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |
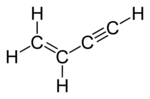
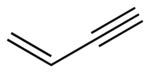
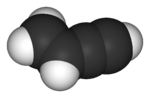
Vinylacetylen là hydrocarbon có công thức hóa học là C4H4. Chất khí không màu này từng được sử trong công nghiệp polyme. Nó chứa cả liên kết đôi C=C(alken) và liên kết ba C≡C (alkyn). Nó là một enyn đơn giản nhất. Vinylacetylene cực kỳ nguy hiểm vì nó có thể tự phát nổ (nổ mà không có sự có mặt của không khí) khi nồng độ lên tới 30% nhất là ở áp suất cao,như áp suất trong các nhà máy hóa chất xử lý hydrocarbon C4. vụ nổ như vậy xảy ra tại nhà máy Union Carbide ở thành phố Texas vào năm 1969.
Tổng hợp[sửa | sửa mã nguồn]
Vinylacetylene tạo ra lần đầu bởi phản ứng khử Hofmann of the related quaternary ammonium salt:[2]
- [(CH3)3NCH2CH=CHCH2N(CH3)3]I2 → 2 [(CH3)3NH]I + HC≡C-CH=CH2
Nó thường được tạo ra bởi phản ứng đề hydrohalogen hóa của 1,3-dichloro-2-butene.[3]
Nó còn tạo từ phản ứng dime hóa của acetylen với sự xúc tác của đồng(I) clorua.[4]
Đề hydro hóa 1,3-butadiene cũng là một cách.
Ứng dụng thực tế[sửa | sửa mã nguồn]
Trong một thời gian, vinylacetylen được dùng để tổng hợp cloropren, một thành phần của cao su tổng hợp Neopren.
Tại đây, acetylen dime hóa tạo thành but 1 en 3 yn. Chất này cộng HCI tạo ra cloropren
- H2C=CH-C≡CH + HCl → H2ClC-CH=C=CH2
- H2ClC-CH=C=CH2 → H2C=CH-CCl=CH2
- ^ “New Environment Inc. - NFPA Chemicals”.
- ^ Willstätter, Richard; Wirth, Theodor (1913). “Über Vinyl-acetylen”. Berichte der Deutschen Chemischen Gesellschaft. 46: 535–538. doi:10.1002/cber.19130460172.
- ^ G. F. Hennion, Charles C. Price, Thomas F. McKeon, Jr. (1958). “Monovinylacetylene”. Organic Syntheses. 38: 70. doi:10.15227/orgsyn.038.0070.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- ^ Trotuş, Ioan-Teodor; Zimmermann, Tobias; Schüth, Ferdi (2014). “Catalytic Reactions of Acetylene: A Feedstock for the Chemical Industry Revisited”. Chemical Reviews. 114 (3): 1761–1782. doi:10.1021/cr400357r. PMID 24228942.

