Sulfide
| Sulfide | |
|---|---|
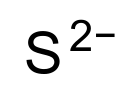 Công thức của sulfide | |
 | |
| Tên hệ thống | Sulfanediide[1] (substitutive) Sulfide(2−)[1] (additive) |
| Nhận dạng | |
| Số CAS | |
| PubChem | |
| ChEBI | |
| Ảnh Jmol-3D | ảnh |
| SMILES | đầy đủ
|
| Thuộc tính | |
| Công thức phân tử | S2− |
| Điểm nóng chảy | |
| Điểm sôi | |
| Acid liên hợp | Bisulfide |
| Các hợp chất liên quan | |
| Anion khác | telluride |
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |
Sulfide (tên hệ thống sulfanedide và sulfide(2−)) là một anion vô cơ của lưu huỳnh với công thức hóa học là S2− hoặc một hợp chất chứa một hoặc nhiều ion S2−. Nó góp phần làm cho muối sulfide không có màu. Nó được phân loại là một base mạnh, thậm chí dung dịch pha loãng muối như natri sulfide (Na2S) là chất có tính ăn mòn và có thể làm tổn thương da. Sulfide là anion lưu huỳnh dơn giản nhất.
Danh pháp[sửa | sửa mã nguồn]
Tính chất hóa học[sửa | sửa mã nguồn]
Nó đã được xác nhận rằng ion sulfide, S2− không tồn tại ngay cả trong dung dịch kiềm-nước đậm đặc của Na2S.[2] Do đó, phản ứng phân ly
- SH− (nước) → S2− + H+
không xảy ra trong dung dịch nước ở bất kỳ nồng độ sulfide nào. Các ion sulfide, S2− được báo cáo là không phát hiện được ở nồng độ lên tới 5 M NaOH.[3] Tuy nhiên, ion sulfide có thể được tạo ra khi một chất rắn được hình thành. Ví dụ cadmi sulfide kết tủa trong nhóm 2 của phân tích định tính.
- H2S (g) + Cd2+ (aq) + 2OH− → CdS↓ (s) + 2H2O
Phản ứng hóa học[sửa | sửa mã nguồn]
Khi xử lý với một acid tiêu chuẩn, sulfide chuyển đổi thành hydro sulfide (H2S) và một muối kim loại. Quá trình oxy hóa sulfide tạo ra lưu huỳnh hoặc sulfat. Sulfide kim loại phản ứng với phi kim bao gồm Iod, brom, và clo tạo thành lưu huỳnh và muối kim loại.
- 8 MgS + 8 I2 → S8 + 8 MgI2
Lưu huỳnh cũng có thể được điều chế từ sulfide và một chất oxy hóa thích hợp.
Dẫn xuất kim loại[sửa | sửa mã nguồn]
Các dung dịch nước của các cation kim loại chuyển tiếp phản ứng với các nguồn sulfide (H2S, NaHS, Na2S) tạo thành các kết tủa sulfide rắn. Các sulfide vô cơ này thường có độ tan rất thấp trong nước và nhiều loại có liên quan đến các khoáng chất có cùng thành phần (xem bên dưới). Một số ví dụ thường gặp là màu vàng sáng loại CdS hay "cadmi vàng". Màu xỉn đen hình thành trên bạc là Ag2S. Các loại này đôi khi được gọi là muối. Trong thực tế, liên kết trong các sulfide kim loại chuyển tiếp có tính cộng hóa trị cao, điều này làm tăng tính chất bán dẫn của chúng, do đó nó liên quan đến các màu đậm. Một số có ứng dụng thực tế như sắc tố, trong các tế bào năng lượng mặt trời, và như chất xúc tác. Nấm Aspergillus niger đóng một vai trò trong việc hòa tan các sulfide kim loại nặng.[4]
Địa chất[sửa | sửa mã nguồn]
Nhiều quặng kim loại quan trọng là sulfide.[5] Các ví dụ phổ biến là: argentite (bạc sulfide), chu sa (thủy ngân), galen (chì sulfide), molypdenit (molypden sulfide), pentlandit (niken sulfide), realgar (asen sulfide), và stibnite (antimon), sphalerit (kẽm sulfide), và pyrit (sắt(II) disulfide), và chalcopyrit (sắt-đồng sulfide).
Ăn mòn gây ra bởi sulfide[sửa | sửa mã nguồn]
Sulfide tự do hòa tan (H2S, HS− và S2−) là những chất ăn mòn mạnh với nhiều kim loại như thép, thép không gỉ và đồng. Sulfide có trong dung dịch nước gây sự ăn mòn dưới ứng suất (SCC) của thép. Ăn mòn là một mối quan tâm lớn trong nhiều ngành công nghiệp chế biến sulfide: các nhà máy mỏ sulfide, giếng dầu sâu, đường ống vận chuyển dầu, nhà máy giấy Kraft.
Ăn mòn bởi vi sinh vật (MIC) hay ăn mòn sulfide sinh học cũng được gây ra bởi vi khuẩn khử sulfat, chúng tạo ra sulfide thoát ra trong không khí và bị oxy hóa trong acid sulfuric bởi vi khuẩn oxy hóa lưu huỳnh. Acid sulfuric sinh học phản ứng với các vật liệu trong hệ thống thoát nước và thường gây ra tổn thất hàng loạt, nứt các ống thoát nước và cuối cùng là sự phá vỡ về cấu trúc. Loại suy thoái này là một quá trình nghiêm trọng ảnh hưởng đến hệ thống thoát nước trên toàn thế giới và dẫn đến chi phí phục hồi rất cao.
Quá trình oxy hóa sulfide cũng có thể tạo thành thiosulfat - một chất trung gian chịu trách nhiệm cho các vấn đề nghiêm trọng của rỗ ăn mòn thép và thép không gỉ trong khi môi trường cũng được acid hóa bởi việc tạo ra acid sulfuric khi quá trình oxy hóa được tăng cường.
Hóa học hữu cơ[sửa | sửa mã nguồn]
Trong hóa học hữu cơ, "sulfide" thường được đề cập đến liên kết C–S–C, mặc dù thuật ngữ thioete ít mơ hồ hơn. Ví dụ, thioete dimetyl sulfide là CH3–S–CH3. Polyphenylene sulfide (xem bên dưới) có công thức đơn giản nhất (công thức thực nghiệm) là C6H4S.Thỉnh thoảng, thuật ngữ sulfide đề cập đến các phân tử chứ nhóm chức –SH. Ví dụ, metyl sulfide có thể có nghĩa là CH3–SH. Mô tả ưu tiên cho các hợp chất chứa SH là thiol hoặc mercaptan, ví dụ, metanthiol, or metyl mercaptan.
Disulfide[sửa | sửa mã nguồn]
Sự nhầm lẫn phát sinh từ các ý nghĩa khác nhau của thuật ngữ "disulfide". Molypden disulfide (MoS2) bao gồm các gốc sulfide khác biệt, kết hợp với molypden ở trạng thái oxy hóa chính thức +4 (tức là, Mo4+ và hai S2−). Sắt disulfide (pyrit, FeS2) mặt khác bao gồm S2−
2,hoặc dianion −S–S−, kết hợp với sắt hóa trị II ở trạng thái oxy hóa chính thức +2 (ion sắt: Fe2+). Dimetyldisulfide có liên kết hóa học CH3–S–S–CH3, trong khi cacbon disulfide không có liên kết S–S, mà là S=C=S (phân tử luyến tính tương tự như CO2). Thông thường trong hóa học lưu huỳnh và hóa sinh, thuật ngữ disulfide thường được gán tương tự lưu huỳnh của liên kết peroxide –O–O–. Liên kết disulfide (–S–S–) đóng một vai trò quan trọng trong cấu tạo của protein và trong hoạt động xúc tác của các enzym.
Ví dụ[sửa | sửa mã nguồn]
| Công thức | Độ nóng chảy (°C) | Điểm sôi (°C) | Số CAS | |
|---|---|---|---|---|
| H2S | Hydro sulfide là một loại khí rất độc và ăn mòn được đặc trưng bởi mùi của "trứng thối". | −85,7 | −60,2 | 7783-06-4 |
| CdS | Cadmi sulfide có thể được sử dụng trong các tế bào ánh sáng điện tử. | 1750 | 1306-23-6 | |
| Calci polysulfide ("vôi lưu huỳnh") là một thuốc diệt nấm truyền thống trong làm vườn. | ||||
| CS2 | Carbon disulfide đôi khi được sử dụng như một dung môi trong hóa học công nghiệp. | −111,6 | 46 | 75-15-0 |
| PbS | Chì sulfide được sử dụng trong các cảm biến hồng ngoại. | 1114 | 1314-87-0 | |
| MoS2 | Molypden disulfide, khoáng vật molypdenit, được sử dụng làm chất xúc tác để loại bỏ lưu huỳnh khỏi nhiên liệu hóa thạch; cũng như chất bôi trơn cho các yêu cầu nhiệt độ cao và áp suất cao. | 1317-33-5 | ||
| Cl–CH2CH2–S–CH2CH2–Cl | Lưu huỳnh mù tạt (khí mù tạt) là một sulfide hữu cơ (thioete) đã được sử dụng như một vũ khí hóa học trong Chiến tranh thế giới thứ nhất, chloride trên phân tử hoạt động như một nhóm rời khi có sự hiện diện của nước và tạo thành một thioete-alcohol và HCl. | 13–14 | 217 | 505-60-2 |
| Ag2S | Bạc sulfide được hình thành trên tiếp điểm điện bạc hoạt động trong bầu không khí nhiều hydro sulfide. | 21548-73-2 | ||
| Na2S | Natri sulfide là một hóa chất công nghiệp quan trọng, được sử dụng trong sản xuất giấy Kraft, thuốc nhuộm, thuộc da, dầu mỏ, xử lý ô nhiễm kim loại nặng và các loại khác. | 920 | 1180 | 1313-82-2 |
| ZnS | Kẽm sulfide được sử dụng cho thấu kính và các thiết bị quang học khác trong thành phần hồng ngoại của phổ điện từ. Kẽm sulfide pha tạp với bạc được sử dụng trong máy dò hạt alpha trong khi kẽm sulfide với đồng có ứng dụng trong phát quang dải cho chiếu sáng khẩn cấp và mặt đồng hồ sáng. | 1185 | 1314-98-3 | |
| MeS | Một số sulfide kim loại được sử dụng làm chất màu trong nghệ thuật, mặc dù việc sử dụng chúng đã giảm một phần do độc tính của chúng. Chất màu sulfide bao gồm cadmi, thủy ngân và asen. | |||
| C6H4S | Polyphenylen sulfide là một loại polymer thường được gọi là "Sulfar". Các đơn phân lặp lại của nó được liên kết với nhau bằng liên kết sulfide (thioether). | 26125-40-6 25212-74-2 | ||
| SeS2 | Seleni disulfide là một thuốc kháng nấm được sử dụng trong các chế phẩm chống gàu, chẳng hạn như Selsun Blue. Sự hiện diện của selen có độc tính cao trong các sản phẩm chăm sóc sức khỏe và mỹ phẩm thể hiện mối quan tâm về sức khỏe và môi trường nói chung. | <100 | 7488-56-4 | |
| FeS2 | Mạng tinh thể pyrit được tạo thành từ sắt disulfide, trong đó sắt có hóa trị hai và có ion sắt là (Fe2+). | 600 | 1317-66-4 |
Điều chế[sửa | sửa mã nguồn]
Các hợp chất sulfide có thể được điều chế theo nhiều cách khác nhau:[6]
- Hóa hợp trực tiếp các nguyên tố:
- Ví dụ: Fe(r) + S(r) → FeS(r)
- Khử sulfat:
- Ví dụ: MgSO4(r) + 4C(r) → MgS(r) + 4CO(k)
- Tạo kết tủa một sulfide không tan:
- Ví dụ: M2+ + H2S(k) → MS(r) + 2H+(l)
An toàn[sửa | sửa mã nguồn]
Nhiều sulfide kim loại không hòa tan trong nước nên chúng có thể không độc hại lắm. Một số sulfide kim loại, khi tiếp xúc với một acid khoáng mạnh, bao gồm acid dịch vị, sẽ giải phóng hydro sulfide độc hại.
Sulfide hữu cơ rất dễ cháy. Khi một sulfide cháy nó tạo ra khí lưu huỳnh dioxide (SO2).
Hydro sulfide, một số muối của nó, và hầu như tất cả các sulfide hữu cơ có mùi hôi mạnh và thối; sinh khối thối rữa giải phóng chúng.
Tài liệu tham khảo[sửa | sửa mã nguồn]
- ^ a b “sulfide(2−) (CHEBI:15138)”. Chemical Entities of Biological Interest (ChEBI). UK: European Bioinformatics Institute.
- ^ May, P.M.; Batka, D.; Hefter, G.; Könignberger, E.; Rowland, D. (2018). “Goodbye to S2-”. Chem. Comm. doi:10.1039/c8cc00187a.
- ^ Meyer, B; Ward, K; Koshlap, K; Peter, L (1983). “Second dissociation constant of hydrogen sulfide”. Inorganic Chemistry. 22: 2345. doi:10.1021/ic00158a027.
- ^ Harbhajan Singh. Mycoremediation: Fungal Bioremediation. tr. 509.
- ^ Vaughan, D. J.; Craig, J. R. "Mineral chemistry of metal sulfides" Cambridge University Press, Cambridge: 1978. ISBN 0-521-21489-0.
- ^ Atkins; Shriver (2010). Inorganic Chemistry (ấn bản 5). New York: W. H. Freeman & Co. tr. 413.
