Acid propionic
| Acid propionic | |
|---|---|
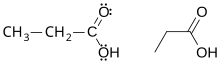 Cấu trúc phân tử của acid propionic | |
| Tổng quan | |
| Danh pháp IUPAC | Acid propanoic |
| Tên khác | Acid ethancarboxylic |
| Công thức phân tử | C3H6O2 |
| Phân tử gam | 74,08 g/mol |
| Biểu hiện | Chất lỏng không màu |
| Số CAS | [79-09-4] |
| Thuộc tính | |
| Tỷ trọng và pha | 0,99 g/cm³, lỏng |
| Độ hòa tan trong nước | Có thể trộn lẫn |
| Nhiệt độ nóng chảy | -21 °C (252 K) |
| Điểm sôi | 141 °C (414 K) |
| pKa | 4,88 |
| Độ nhớt | 10 mPa.s |
| Khác | |
| MSDS | MSDS ngoài |
| Các nguy hiểm chính | Chất ăn mòn (C) |
| NFPA 704 | |
| Điểm bắt lửa | 54°C |
| Rủi ro/An toàn | R: 34 S: 1/2, 23, 36, 45 |
| Số RTECS | UE5950000 |
| Dữ liệu hóa chất bổ sung | |
| Cấu trúc & thuộc tính | n εr, v.v. |
| Dữ liệu nhiệt động lực | Các trạng thái rắn, lỏng, khí |
| Dữ liệu quang phổ | UV, IR, NMR, MS |
| Các hợp chất liên quan | |
| Các hợp chất tương tự | Acid acetic Acid butyric |
| Các hợp chất liên quan | Propionat natri 1-Propanol Propionalđêhit Metyl propionat |
| Ngoại trừ có thông báo khác, các dữ liệu được lấy ở 25 °C, 100 kPa Thông tin về sự phủ nhận và tham chiếu | |
Acid propionic (danh pháp khoa học acid propanoic) là một acid carboxylic có nguồn gốc tự nhiên với công thức hóa học CH3CH2COOH. Ở trạng thái tinh khiết và trong điều kiện thông thường, acid propionic là một chất lỏng không màu có tính ăn mòn và mùi hăng.
Lịch sử
[sửa | sửa mã nguồn]Acid propionic lần đầu tiên được Johann Gottlieb miêu tả năm 1844. Ông là người đã tìm thấy nó trong số các sản phẩm phân hủy của đường. Trong khoảng thời gian vài năm sau đó, các nhà hóa học khác cũng tạo ra acid propionic theo các cách khác nhau, nhưng không có ai trong số họ nhận ra rằng họ đã tạo ra cùng một hợp chất. Năm 1847, nhà hóa học người Pháp là Jean-Baptiste Dumas đã chứng minh được tất cả các acid trên đây chỉ là một hợp chất và ông gọi nó là acid propionic, lấy theo tiếng Hy Lạp protos = "đầu tiên" và pion = "béo", do nó là acid với công thức tổng quát H(CH2)nCOOH nhỏ nhất có các tính chất của một acid béo, chẳng hạn như sự tạo ra một lớp váng mỡ khi bị kết tủa bởi muối và có muối với kali có tính chất giống xà phòng.
Tính chất
[sửa | sửa mã nguồn]Acid propionic có các tính chất vật lý trung gian giữa các tính chất của các acid carboxylic nhỏ hơn như acid formic và acid acetic, với các acid béo lớn hơn. Nó hòa tan trong nước nhưng có thể bị loại ra khỏi nước bằng cách cho thêm muối. Giống như acid acetic và acid formic, dạng khí của nó vi phạm nghiêm trọng định luật khí lý tưởng do nó không chứa các phân tử acid propionic riêng rẽ mà lại có các cặp liên kết hydro giữa các phân tử. Nó cũng có sự bắt cặp này khi ở trạng thái lỏng.
Về mặt hóa học, acid propionic thể hiện các tính chất chung của acid carboxylic, và tương tự như phần lớn các acid carboxylic khác, nó tạo ra các hợp chất amide, ester, anhydride và chloride. Nó cũng có thể tham gia phản ứng halogen hóa pha alpha với brom khi có mặt PBr3 làm chất xúc tác (phản ứng HVZ) để tạo ra CH3CHBrCOOH.
Sản xuất
[sửa | sửa mã nguồn]Trong công nghiệp, acid propionic thông thường được sản xuất từ phản ứng oxy hóa của propionaldehit bằng không khí. Khi có mặt các xúc tác như cobalt, mangan sắt, phản ứng này diễn ra nhanh chóng thậm chí ở nhiệt độ vừa phải. Thông thường sản xuất công nghiệp được thực hiện ở 40-50 °C, được viết dưới phương trình hóa học sau:
Một lượng lớn acid propionic đã từng được sản xuất như là phụ phẩm của việc sản xuất acid acetic, nhưng ngày nay thì nó chỉ là một nguồn rất nhỏ trong sản xuất acid propionic. Nhà sản xuất nay là BASF, với công suất khoảng 80 ktpa.
Acid propionic cũng được tạo ra theo phương pháp sinh học từ sự phân hủy do trao đổi chất của các acid béo chứa số lẻ các nguyên tử carbon, cũng như từ sự phân hủy của một số amino acid. Các vi khuẩn thuộc chi Propionibacterium cũng tạo ra acid propionic như là sản phẩm cuối cùng trong hoạt động trao đổi chất kỵ khí của chúng. Các vi khuẩn này ađược tìm thấy rất phổ biến trong dạ dày của các động vật nhai lại, và hoạt động của chúng là một phần nguyên nhân tạo ra mùi vị của cả phó mát Thụy Sĩ và mồ hôi.
Sử dụng
[sửa | sửa mã nguồn]Acid propionic ngăn cản sự phát triển của mốc và một số vi khuẩn. Do vậy, phần lớn acid propionic được sản xuất để sử dụng làm chất bảo quản cho cả thực phẩm dành cho con người cũng như thức ăn dành cho gia súc. Đối với thức ăn cho gia súc, nó được sử dụng hoặc là trực tiếp hoặc dưới dạng muối amoni. Đối với thực phẩm dành cho con người, đặc biệt là bánh mì và các sản phẩm nướng khác, nó được dùng dưới dạng các muối natri hay calci. Việc sử dụng tương tự cũng diễn ra đối với một số bột chống nấm chân loại cũ.
Acid propionic cũng là một hóa chất trung gian có ích. Nó có thể sử dụng để thay đổi các sợi cellulose tổng hợp. Nó cũng được dùng để sản xuất một số thuốc trừ sâu và dược phẩm. Các este của acid propionic đôi khi được dùng làm dung môi hay các chất tạo mùi nhân tạo.
An toàn
[sửa | sửa mã nguồn]Nguy hiểm chính từ acid propionic là bỏng hóa chất có thể sinh ra do tiếp xúc với acid đậm đặc. Trong các nghiên cứu trên động vật trong phòng thí nghiệm, hiệu ứng nguy hiểm nghiêm trọng duy nhất gắn liền với phơi nhiễm kinh niên đối với một lượng nhỏ acid propionic là các vết loét thực quản và dạ dày do tiêu thụ chất có tính ăn mòn này. Người ta chưa quan sát thấy các hiệu ứng độc hại, dị biến gen, ung thư hay sinh sản nào. Trong cơ thể, acid propionic bị oxy hóa nhanh chóng và bị thải ra khỏi cơ thể trong dạng carbon dioxide theo chu trình Krebs và nó không tạo ra sự tích lũy sinh học.
