Chuỗi vận chuyển điện tử
Các chú thích trong bài hoặc đoạn này phải hoàn chỉnh hơn để có thể được kiểm chứng. |
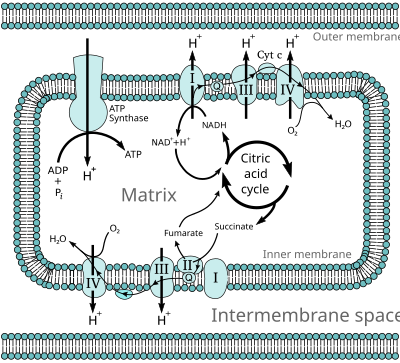

Chuỗi vận chuyển điện tử (tiếng Anh: electron transport chain (ETC)) kết hợp sự chuyển giữa vật cho điện tử (ví dụ như NADH) và một vật nhận điện tử (ví dụ ôxi) đến sự trung chuyển của proton H+ qua lớp màng sinh chất. Kết quả là một độ chênh thế điện hóa học được tạo ra, năng lượng tích chứa trong thế này được ATP synthase chuyển thành hóa năng[1] dưới dạng adenosine triphosphate (ATP). Chuỗi vận chuyển điện tử là một cơ chế cấp độ tế bào và được dùng để sản sinh năng lượng từ ánh sáng mặt trời trong quang hợp và từ các phản ứng oxy hóa khử, ví dụ như từ phản ứng oxy hóa các chất đường (xem thêm hô hấp tế bào).
Ở lục lạp, dưới tác động của ánh sáng nước bị phân giải thành ôxi và NADP+ chuyển thành NADPH với việc ion H+ được chuyển qua màng lục lạp. Ở ti thể, ôxi được chuyển đổi thành nước, NADH thành NAD+ và succinate thành fumarate, nhờ đó tạo nên một độ chênh về thế proton. Mặc dù một số loài vi khuẩn có thực thi chuỗi vận chuyển điện tử với những yếu tố giống như trong ti thể và lạp thể, những loại khác sử dụng các vật nhận và cho điện tử khác với các cơ quan trên. Cả chuỗi vận chuyển điện tử quang hợp và hô hấp đều là nơi xảy ra sự rò rỉ điện tử quá sớm tới ôxi, điều này hình thành superoxide và dẫn đến kết quả là sự gia tăng ứng kích oxy hóa.
Nhìn chung[sửa | sửa mã nguồn]
Chuỗi vận chuyển điện tử bao gồm những phản ứng oxy hóa khử xảy ra ở những khoảng không gian khác nhau, trong đó điện tử (electron) được chuyển từ một phân tử cho điện tử tới một phân tử nhận điện tử. Năng lượng cơ bản thúc đẩy các phản ứng này là năng lượng tự do Gibbs của tác chất và sản phẩm. Năng lượng tự do Gibbs là năng lượng có sẵn ("tự do") để làm việc. Bất cứ phản ứng nào làm giảm tổng năng lượng tự do Gibbs của một hệ thống sẽ tự động phát sinh. Sự chuyển điện tử bắt đầu từ một chất cho điện tử tới một chất nhận điện tử.
ATP synthase, một enzyme có cấu trúc được bảo tồn cao, được cung cấp năng lượng bởi một thế điện hóa proton xuyên màng, đó là kết quả của một loạt các phản ứng oxy hóa khử.[2][Gc 1] Chức năng của chuỗi vận chuyển điện tử là tạo ra thế điện hóa đó.[3][Gc 2] Thế điện hóa xuyên màng có thể kích hoạt sự vận chuyển các nguyên tử xuyên qua màng sinh chất. Nó cũng có thể kích hoạt các hoạt động cơ học như hoạt động xoay của tiên mao hay sản xuất ATP nhằm cung cấp năng lượng cho các hoạt động của tế bào. Một lượng nhỏ ATP có sẵn ở sự phosphorylate hóa cấp độ chất nền, ví dụ như sự thủy phân glycogen. Trong phần lớn các cơ thể sống, đại bộ phận ATP được sản sinh ra từ chuỗi vận chuyển điện tử, trong khi một số nhỏ sản sinh ATP từ việc lên men.[cần dẫn nguồn]
Chuỗi vận chuyển điện tử trong ti thể[sửa | sửa mã nguồn]
Phần lớn các tế bào nhân chuẩn bao hàm ti thể với chức năng sản sinh ATP thông qua chu trình Krebs, sự oxy hóa axít béo, và sự oxy hóa amino acid. Ở lớp màng trong của ti thể, điện tử (electron) từ NADH và succinate đi qua chuỗi vận chuyển điện tử tới ôxi - lúc này ôxi sẽ bị khử thành nước. Chuỗi vận chuyển điện tử bao hàm một chuỗi hơn 15 vật cho và vật nhận điện tử[4] mang tính enzyme. Mỗi vật cho điện tử đi đưa các điện tử đến các vật nhận mang ái lực nhiều hơn với điện tử, vật nhận này lại tiếp tục chuyển điện tử đến một vật nhận sau nó; cuối cùng điện tử được chuyển đến cho ôxi, vật nhận có ái lực lớn nhất và cũng là vật nhận cuối cùng trong chuỗi vận chuyển điện tử.[5] Việc chuyển điện tử như vậy giải phóng một năng lượng dùng để tạo nên thế proton (giữa hai không gian ti thể ngăn cách bởi màng ti thể) bằng cách bơm proton vào khoảng không giữa hai màng ti thể, tạo nên một trạng thái nhiệt động lực học mang một điện thế để thực thi các hoạt động. Ở đây, trong khi việc oxy hóa kiểu "đốt cháy" giải phóng phần nhiều năng lượng dưới dạng nhiệt, sự oxy hóa sinh học ở ti thể giải phóng phần lớn năng lượng này ở dạng mà cơ thể có thể sử dụng được, việc này nhờ có những phương tiện cần thiết trong chuỗi vận chuyển điện tử.[5]
Tuy nhiên, một phần nhỏ các điện tử có thể không kinh qua đầy đủ tất cả các vật cho/vật nhận mà chạy thẳng tới ôxi, hình thành nên các superoxide mang gốc tự do, một loại phân tử có hoạt tính hóa học cực mạnh có thể gây ra ứng kích oxy hóa và là một trong những yếu tô gây ra lão hóa cùng một số bệnh tật khác.
Các vật mang oxy hóa khử ti thể[sửa | sửa mã nguồn]
Năng lượng sinh ra từ sự chuyển các điện tử (mũi tên đen) theo chuỗi vận chuyển điện tử được dùng để bơm proton (mũi tên đỏ) từ chất nền ti thể vào không gian giữa lớp màng kép của ti thể. Việc này khiến tính axít và độ dương điện của chất nền ti thể giảm xuống, tạo ra một sự chênh pH và thế điện màng sinh chất giữa hai môi trường ngăn cách bởi lớp màng ti thể, hai sự chênh lệch này tạo nên một thế proton điện hóa giữa hai không gian đó, gọi là ΔΨ. Thế điện hóa này thực thi một lực vận động proton có độ lớn vào khoảng 180-190mV nhằm kéo proton H+ về chất nền.[Gc 3] Các proton này đi xuyên qua enzyme ATP synthease (gọi tắt ATP-ase) và giúp nó sản sinh ATP từ adenosine diphosphate (ADP) và phosphate vô cơ.
Phần lớn các protein tham gia vào chuỗi vận chuyển điện tử được phân thành các phức hợp enzyme hô hấp chính.[6] Phức hợp I (NADH coenzyme Q reductase) nhận điện tử từ vật mang của chu trình Krebs (nicotinamide adenine dinucleotide - NADH) và chuyển chúng sang coenzyme Q (ubiquinone, viết tắt UQ). UQ cũng nhận điện tử từ phức hợp II (succinate dehydrogenase). Sau đó UQ chuyển điện tử sang phức hợp III (phức hợp cytochrome bc1), phức hợp III lại đưa điện tử sang cytochrome c (viết tắt cyt c). Cyt c đưa điện tử sang phức hợp IV (cytochrome c oxidase), phức hợp IV sẽ dùng điện tử và các proton H+ để khử ôxi thành nước.
4 phức hợp gắn trên màng sinh chất đã được nhận diện trong ti thể. Mỗi phức hợp này là một cấu trúc cực kỳ phức tạp nằm trong lớp nội màng của ti thể. Ba phức hợp là các bơm proton. Các phức hợp được liên kết bằng lực hút tĩnh điện bởi các vật mang điện tử tan trong chất béo. Nhìn chung chuỗi vận chuyển điện tử được mô tả như sau:
NADH → Phức hợp I → Q → Phức hợp III → Cytochrome c → Phức hợp IV → O2
↑
Phức hợp II
Phức hợp I[sửa | sửa mã nguồn]
Ở Phức hợp I (NADH-CoQ Reductase, NADH dehydrogenase[7] hay NADH:ubiquinone oxidoreductase; EC 1.6.5.3) hai điện tử nằm trong 1 cặp (ion hydride) được lấy đi từ NADH. Do phần lớn các vật mang chỉ có thể mang một điện tử, Flavin mononucleotide (FMN) của phức hợp I đóng vai trò như một vật mang trung gian: FMN có thể chứa cả hai điện tử lấy từ NADH nhưng chỉ có thể nhận một điện tử trong một lần nhận và chuyển từng điện tử một vào nhân FeS của phức hợp I.[8][9] Từng điện tử đó cũng được chuyển lần lượt sang một vật mang điện tử tan trong chất béo mang tên ubiquinone (Q), nó khử vật mang này thành ubiquinol (QH2).[Gc 4] QH có thể chuyển động tự do lẫn trong màng sinh chất, và phức hợp I chuyển 4 proton (H+) xuyên qua màng sinh chất[8], điều này tạo ra một thế proton.
Phản ứng tổng quát do phức hợp I xúc tác:
NADH + CoQ + 2H+ → NAD+ + H+ + CoQH2[9]
Chu trình của điện tử diễn ra ở phức hợp I như sau:
NADH bị oxy hóa thành NAD+, bằng cách khử Flavin mononucleotide thành FMNH2 trong một bước hai điện tử. FMNH2 bị oxy hóa trong hai bước một điện tử thông qua một chất trung gian semiquinone. Mỗi điện tử được chuyển từ FMNH2 tới cụm sắt-lưu huỳnh, và từ cụm này tới ubiquinone (Q). Sự chuyển đổi vị trí của điện tử đầu tiên dẫn đến kết quả trong dạng gốc tự do semiquinone của Q, và sự chuyển điện tử thứ hai khử dạng semiquinone trở thành dạng ubiquinol QH2. Trong quá trình đó, 4 proton H+ đã được chuyển đổi vị trí từ chất nền ti thể sang khoảng không giữa hai màng ti thể, tạo nên một thế proton giúp enzyme ATP synthease sản sinh ATP bằng phản ứng phosphorylate oxy hóa.
Phức hợp I là một trong 4 vị trí mà điện tử sẽ bị rò rỉ tới ôxi và sản sinh ra các superoxide độc hại.[cần dẫn nguồn]
Phức hợp II[sửa | sửa mã nguồn]
Phức hợp II (Succinate - CoQ Reductase) có thành phần chính là succinate dehydrogenase (EC 1.3.5.1). Enzyme này sẽ nhận riêng một số điện tử và sau đó cũng sẽ chuyển chúng vào quinone (Q), số điện tử này có nguồn gốc từ succinate và được chuyển tới Q thông qua FAD. Như FMN, FAD cũng có thể nhận một hoặc hai điện tử nhưng chúng chỉ chuyển từng điện tử một vào nhân FeS của phức hợp II, đến lượt mình nhân FeS sẽ chuyển các điện tử đó vào Q.[8] Phản ứng tổng quát xảy ra dưới sự xúc tác của phức hợp II là:
Succinate + CoQ → Fumarate + CoQH2[9]
Phản ứng khử succinate thành fumarate tuy có năng lượng tự do Gibbs (ΔG) mang giá trị âm, nhưng năng lượng do nó tỏa ra không đủ để bơm proton từ chất nền ti thể sang khoảng không giữa hai lớp màng. Vì vậy trái với các phức hợp I, III và IV, không có proton nào được bơm qua phức hợp II.[8][9]
Phức hợp II bao gồm 4 đơn vị con: SDHA, SDHB, SDHC và SDHD. Một số vật cho điện tử (như axít béo và glycerol 3-phosphate) cũng mang điện tử vào Q thông qua FAD.
Coenzyme Q[sửa | sửa mã nguồn]
Coenzyme Q (ubiquinone) là một loại quinone có đuôi hydrocarbon dài. Đuôi này giúp cho các phân tử CoQ có thể khuếch tán dễ dàng trong lớp màng lipid của ti thể. Cả dạng khử (quinol) và dạng oxy hóa (quinone) của Q có thể di chuyển dễ dàng trong lớp màng lipid. Mỗi lượt coenzyme Q lấy một điện tử từ phức hợp I hoặc II và phân tán vào trong lớp màng ti thể cho đến khi va chạm với phức hợp III - lúc đó điện tử lại được chuyển cho phức hợp III.[8] Chính sự khuếch tán của CoQ cùng với Cytochrome C trong lớp màng ti thể đã đóng vai trò quan trọng trong việc luân chuyển các điện tử đến các phức hợp kế nhau trong chuỗi vận chuyển điện tử.[Gc 5]
Phức hợp III[sửa | sửa mã nguồn]
Ở Phức hợp III (Coenzyme Q - Cytochrome c Reductase hay phức hợp cytochrome b-c1[7]; EC 1.10.2.2) CoQH2 chuyển hai điện tử của nó cho phức hợp để trở lại dạng oxy hóa CoQ, đồng thời hai proton được chuyển vào khoảng không giữa hai màng ti thể, tạo nên một phần thế proton. Ở bên trong phức hợp, điện tử sau khi rời CoQ sẽ đến nhân FeS, sau đó đến một trong ba loại cytochrome (bL, bH, c1) rồi chuyển sang cytochrome c, một phân tử ngoại biên tan trong nước khuếch tán ở trong khoảng không giữa hai màng ti thể.[10]
Phản ứng tổng quát do phức hợp 3 xúc tác như sau:
2Cytochrome c3+ + CoQH2-> 2Cytochrome c2+ + CoQ + 2H+[10]
Tổng cộng cứ mỗi cặp điện tử chạy qua phức hợp III thì có 2 proton được phức hợp 3 bơm vào khoảng không giữa hai màng ti thể.[10]
Khi việc chuyển điện tử bị biến đổi (bởi một thế màng sinh chất cao hay một chất ức chế hô hấp như antimycin A), điện tử có thể bị rò rỉ tại phức hợp III và chúng sẽ tham gia hình thành nên superoxide.
Cytochrome C[sửa | sửa mã nguồn]
Cytochrome C là một phân tử protein lưu động có vai trò như vật mang điện tử. Cytochrome C nằm ở mặt ngoài của màng trong ti thể, tiếp xúc với khoảng không giữa hai lớp màng và có nhiệm vụ chuyển điện tử từ phức hợp III sang phức hợp IV.[11] Như đã nói, chính sự khuếch tán của Cytochrome C cũng như của CoQ trong lớp màng ti thể đã đóng vai trò quan trọng trong việc luân chuyển các điện tử đến các phức hợp kế nhau trong chuỗi vận chuyển điện tử.[10]
Phức hợp IV[sửa | sửa mã nguồn]
Trong Phức hợp IV (cytochrome c oxidase; EC 1.9.3.1), cytochrome c chuyển điện tử của nó - mỗi lần chuyển có một phân tử cyt c chuyển một điện tử - cho phức hợp này; đầu tiên điện tử sẽ đi vào một cặp ion đồng (Cua2+), tiếp đó chuyển sang cytochrome a, rồi sang một phức hợp chứa ion đồng Cub2+, tiếp theo sang cytochrome a3 và cuối cùng là phân tử ôxi - vật nhận điện tử cuối cùng - để sản sinh ra nước.[10]
Phản ứng tổng quát do phức hợp IV xúc tác:
2Cyt c2+ + 2H+ + 1/2O2 → 2Cyt c3+ + H2O
Ứng với mỗi cặp điện tử được chuyển tới phức hợp IV, có 2 proton được phức hợp này bơm vào khoảng không giữa hai màng ti thể.[10]
Bắt cặp với sự phosphorylate oxy hóa[sửa | sửa mã nguồn]
Như đã nói, chuỗi vận chuyển điện tử gây ra một sự chênh lệch thế điện hóa proton giữa hai môi trường ngăn cách bởi lớp màng trong ti thể. Điều này khiến các proton di chuyển ngược lại từ khoảng không giữa hai lớp màng ti thể về với chất nền để xóa bỏ chênh lệch đó. Dòng proton này di chuyển vào chất nền qua một kênh ưa nước do ATP synthase tạo ra và kích hoạt quá trình sản sinh ATP; ở đây năng lượng của thể proton đã được chuyển sang dự trữ trong các phân tử ATP. Như vậy việc bắt cặp giữa sự phosphorylate oxy hóa với thế điện hóa proton là yêu cầu tiên quyết để sản sinh ATP.
Tuy nhiên trong một số trường hợp, năng lượng dự trữ trong sự chênh lệch thế proton không được dùng cho việc sinh tổng hợp ATP bởi sự hiện diện của tác nhân tách cặp như 2-4 dinitrophenol (DNP). Chúng bắt lấy các proton ở khoảng không giữa hai lớp màng rồi đem thả proton trở lại chất nền ti thể mà không qua ATP synthase. Như vậy proton lực vận động proton coi như bị triệt tiêu và mặc dù chuỗi vận chuyển điện tử vẫn hoạt động nhưng không có ATP nào được tạo ra. Ở đây năng lượng trong thế proton được chuyển hóa hoàn toàn sang nhiệt năng, điều xảy ra trong các mô mỡ nâu nơi có chức năng cung cấp nhiệt cho cơ thể. Quá trình điều tiết hô hấp cũng bị triệt tiêu dưới sự hiện diện của các protein này dẫn tới hoạt động của chuỗi vận chuyển điện tử diễn ra với tốc độ tối đa.[12][13][14]
Sự điều tiết hoạt động của chuỗi vận chuyển điện tử[sửa | sửa mã nguồn]
Hoạt động của chuỗi vận chuyển điện tử ở ti thể còn được điều tiết bởi một ảnh hưởng mang tính ức chế của thế điện hóa proton. Ví dụ khi áp đặt một thế điện hóa cao xuyên qua lớp nội màng ti thể, chuỗi vận chuyển điện tử có thể bị ức chế hoặc thậm chí điện tử di chuyển theo chiều ngược lại. Các nghiên cứu cho thấy sự điều tiết này nhằm duy trì một trạng thái cân bằng giữa sự chênh lệch năng lượng tự do của động thái bơm proton liên quan tới chuỗi vận chuyển điện tử và động thái chuyển điện tử; tức là độ lớn của thế proton ảnh hưởng đến tốc độ và hướng hoạt động của chuỗi vận chuyển điện tử. Nguyên do là khi chênh lệch thế proton đạt một mức độ quá lớn thì năng lượng cần thiết để bơm proton ra khỏi chất nền cũng đạt một mức độ khổng lồ đến mức việc oxy hóa NAD, FADH2 cùng hoạt động của chuỗi vận chuyển điện tử bị đình trệ; lúc này ti thể không đào đâu ra được một lượng năng lượng lớn như thế.[12][14]
Nồng độ ATP,ADP và phosphate vô cơ cũng ảnh hưởng gián tiếp đến hoạt động của chuỗi vận chuyển điện tử thông qua sự ảnh hưởng đến hoạt động của ATP synthase. Khi việc sử dụng ATP tăng cao làm giảm tỉ lệ ATP:ADP, ATP synthase bắt đầu tăng cường hoạt động sinh tổng hợp ATP và cho nhiều proton đi qua nó hơn. Điều này làm giảm thế điện hóa và kích thích tốc độ hoạt động của chuỗi vận chuyển điện tử. Nếu nồng độ ADP giảm đến mức quá thấp thì thế điện hóa proton không thể bị tiêu biến qua quá trình sinh tổng hợp ATP từ ADP và chuỗi vận chuyển điện tử bị đình lại.[12][14]
Như đã nói ở trên, các protein tách cặp đã khiến thế proton cùng lực vận động proton liên tục bị tiêu biến đi nhanh chóng mà không cần đến sự hoạt động của ATP synthase. Sự sụp đổ của thế proton khiến các cơ chế điều tiết nói trên cũng bị triệt tiêu và chuỗi vận chuyển điện tử được tự do hoạt động hết công suất của nó bất chấp nồng độ ADP hay ATP.[12][14]
Chuỗi vận chuyển điện tử trong quá trình quang hợp[sửa | sửa mã nguồn]
Trong sự phosphorylate oxy hóa, điện tử được chuyển từ một vật cho điện tử có mức năng lượng cao (ví dụ NADH) đến một vật nhận điện tử (ví dụ O2) thông qua một chuỗi vận chuyển điện tử. Trong sự phosphorylate quang hóa, năng lượng ánh sáng mặt trời để "chế tạo" một vật cho điện tử có mức năng lượng cao cùng một vật nhận tương ứng. Điện tử được chuyển từ vật cho sang vật nhận thông qua một chuỗi vận chuyển điện tử khác.
Các chuỗi vận chuyển điện tử trong quang hợp có nhiều điểm giống nhau với chuỗi vận chuyển điện tử oxy hóa của quá trình hô hấp. Chúng dùng các vật mang lưu động, tan trong chất béo (các quinone) và các vật mang lưu động tan trong nước (các cytochrome...). Chúng cũng bao gồm một bơm proton. Một điều đáng chú ý khác là các bơm proton trong tất cả các chuỗi vận chuyển điện tử quang hợp đều giống như phức hợp số 3 của ti thể.
Các chuỗi vận chuyển điện tử trong quang hợp sẽ được đề cập kỹ hơn trong các bài sự phosphorylate quang hóa, quang hợp, trung tâm phản ứng quang hợp và phản ứng phụ thuộc vào ánh sáng.
Kết quả[sửa | sửa mã nguồn]
Chuỗi vận chuyển điện tử là các phản ứng oxy hóa khử trong đó các điện tử được chuyển tử một vật cho đến một vật nhận. Sự chuyển điện tử đi kèm với sự thay đổi vị trí của proton xuyên qua màng sinh chất, tạo ra một thế proton. Thế proton được dùng để tạo năng lượng cho các hoạt động cần thiết.
Sự đi đôi của các phản ứng sinh hóa thuận lợi và không thuận lợi (về mặt nhiệt động lực học) bởi các đại phân tử sinh học là một ví dụ của tính chất mới phát sinh – một tính chất không thể được dự đoán, và thậm chí kiến thức đầy đủ về hệ địa hóa học cổ sơ từ chỗ mà những đại phân tử đó tiến hóa.[nghiên cứu chưa công bố?] Nó là một câu hỏi mở về việc những tính chất như vật xuất hiện một cách tình cơ hay chúng xuất hiện như là một kết quả tất yếu của quá trình tiến hóa xảy ra trong các hệ thống sinh địa hóa học lớn, theo các định luật cơ bản của vật lý.[cần dẫn nguồn]
Chú thích[sửa | sửa mã nguồn]
Ghi chú[sửa | sửa mã nguồn]
- ^ Karp discusses ATP gradient: "These three protein complexes [I, II, and IV] are often described as proton pumps. The translocation of protons by these electron-transporting complexes establishes the proton gradient that drives ATP synthesis."(194)
- ^ Harper's Illustrated Biochemistry explaining the function of the complexes of the transport chain: "Each of the respiratory chain complexes I, II, and IV... acts as a proton pump...creating an electrochemical potential difference across the [mitochondrial inner] membrane."(96)
- ^ Trong đó thế điện màng sinh chất đóng góp 160-180mV và độ chênh pH đóng góp 0,3 đến 0,5 đơn vị pH (1 đơn vị pH tương đương 60mV)[5][6]
- ^ Q có thể mang một hoặc 2 điện tử tựa như FMN.[8]
- ^ Các phức hợp trong chuỗi chuyển điện tử chuyển động về phía bên trong lớp màng trong ti thể; đồng thời số lượng của mỗi loại không bằng nhau và chúng không hình thành các liên kết bền chặt với nhau. Tất cả các yếu tố này ngăn cản sự chuyển điện tử trực tiếp từ mỗi phức hợp sang phức hợp kế tiếp và chính CoQ cùng Cyt C đã đảm nhận vai trò trung chuyển điện tử giữa chúng.[10]
Nguồn dẫn[sửa | sửa mã nguồn]
- ^ Hóa năng (hay còn được gọi là hóa sinh) là một lĩnh vực trong ngành hóa học nghiên cứu về quá trình chuyển đổi năng lượng trong các hệ thống sống và các quá trình sinh học khác. Nó tập trung vào việc tìm hiểu và giải thích cách các hợp chất hóa học trong cơ thể sinh vật được tạo ra, phân hủy và sử dụng năng lượng. Trong các quá trình hóa năng, các chất hóa học tham gia vào các phản ứng hóa học để tạo ra hoặc tiêu thụ năng lượng. Các quá trình này diễn ra trong các cơ quan, tế bào và các cấu trúc tế bào của sinh vật, và đóng vai trò quan trọng trong việc duy trì sự sống và hoạt động của chúng. Hóa năng cũng nghiên cứu về cách các chất dẫn truyền năng lượng, chẳng hạn như các chất điện giải và các hợp chất hữu cơ, trong các quá trình sinh học. Các nghiên cứu về hóa năng đóng vai trò quan trọng trong việc hiểu cơ chế hoạt động của các quá trình sinh học và phát triển các ứng dụng trong lĩnh vực y học, công nghệ sinh học và năng lượng tái tạo.
- ^ Karp, Gerald (2008). Cell and Molecular Biology (5th edition). Hoboken, NJ: John Wiley & Sons. tr. 194. ISBN 10-0-470-04217-6 Kiểm tra giá trị
|isbn=: số con số (trợ giúp). - ^ Robert K. Murray & Daryl K. Granner, Peter A. Mayes, Victor W. Rodwell (2003). Harper's Illustrated Biochemistry. New York, NY: Lange Medical Books/ MgGraw Hill. tr. 96. ISBN 0-07-121766-5.Quản lý CS1: sử dụng tham số tác giả (liên kết)
- ^ Bruce et al., trang 819
- ^ a b c Bruce et al., trang 820
- ^ a b Bruce et al., trang 821
- ^ a b Albert et al., trang 832
- ^ a b c d e f Gajera, Patel, Golakiya, trang 314
- ^ a b c d Lodish et al., trang 320
- ^ a b c d e f g Lodish et al., trang 321
- ^ Gajera, Patel, Golakiya, trang 315
- ^ a b c d Lodish et al., trang 330
- ^ Albert et al., trang 836
- ^ a b c d Albert et al., trang 837
Xem thêm[sửa | sửa mã nguồn]
Tham khảo[sửa | sửa mã nguồn]
- Bruce Alberts (2008). Molecular Biology of the Cell. Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts, Peter Walter . Garland Science, Taylor & Francis Group. ISBN 978-0-8153-4106-2.
- Harvey Lodish (2003). Molecular Cell Biology. Arnold Berk, Paul Matsudaira, Chris A. Kaiser, Monty Krieger, Matthew P. Scott, Lawrence Zipursky, James Darnell . ISBN 0716743663.
- H. P. Gajera, S. V. Patel, B. A. Golakiya (2008). Fundamentals of Biochemistry: A Textbook . International Book Distributing Co. (Publishing Division). ISBN 978-81-8189-165-5.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- Fenchel T (2006). Bacterial Biogeochemistry: The Ecophysiology of Mineral Cycling. King GM, Blackburn TH . Elsevier. ISBN 978-0121034559.
- Lengeler JW (1999). Biology of the Prokaryotes. Drews G; Schlegel HG (editors). Blackwell Science. ISBN 978-0632053575.
- Nelson DL (2005). Lehninger Principles of Biochemistry. Cox MM (ấn bản 4). W. H. Freeman. ISBN 978-0716743392.
- Nicholls DG (2002). Bioenergetics 3. Ferguson SJ. Academic Press. ISBN 978-0125181211.
- Stumm W (1996). Aquatic Chemistry. Morgan JJ (ấn bản 3). John Wiley & Sons. ISBN 978-0471511854.
- Thauer RK (1977). Jungermann K; Decker K. “Energy conservation in chemotrophic anaerobic bacteria”. Bacteriol Rev. 41 (1): 100–80. PMC 413997. PMID 860983.
- White D. (1999). The Physiology and Biochemistry of Prokaryotes (ấn bản 2). Oxford University Press. ISBN 978-0195125795.
- Voet D (2004). Biochemistry. Voet JG (ấn bản 3). John Wiley & Sons. ISBN 978-0471586517.
- Kim HS.; Patel, K; Muldoon-Jacobs, K; Bisht, KS; Aykin-Burns, N; Pennington, JD; Van Der Meer, R; Nguyen, P; Savage, J (2010). “SIRT3 is a mitochondria-localized tumor suppressor required for maintenance of mitochondrial integrity and metabolism during stress”. Cancer Cell. 17 (1): 41–52. doi:10.1016/j.ccr.2009.11.023. PMID 20129246.
Liên kết ngoài[sửa | sửa mã nguồn]
- MeSH Electron+Transport+Chain+Complex+Proteins
- UMich Orientation of Proteins in Membranes families/superfamily-3 - Complexes with cytochrome b-like domains
- UMich Orientation of Proteins in Membranes families/superfamily-4 - Bacterial and mitochondrial cytochrome c oxidases
- UMich Orientation of Proteins in Membranes families/superfamily-2 - Photosynthetic reaction centers and photosystems
- UMich Orientation of Proteins in Membranes families/superfamily-78 - Cytochrome c family
- UMich Orientation of Proteins in Membranes families/superfamily-101 - Cupredoxins
- UMich Orientation of Proteins in Membranes protein/pdbid-1e6e - Adrenodoxin reductase
- UMich Orientation of Proteins in Membranes families/superfamily-130 - Electron transfer flavoproteins
Bản mẫu:Cellular respiration Bản mẫu:Electron transport chain
Bài viết này có một danh sách các nguồn tham khảo, nhưng vẫn chưa đáp ứng khả năng kiểm chứng được bởi thân bài vẫn còn thiếu các chú thích trong hàng. (November 2008) |
Cảnh báo: Từ khóa xếp mặc định “Chuỗi_vận_chuyển_điện_tử” ghi đè từ khóa trước, “Electron Transport Chain”.
