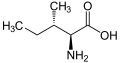
Isoleucin
| L-Isoleucine | |||
|---|---|---|---|
| |||
| Danh pháp IUPAC | Isoleucine | ||
| Tên khác | 2-Amino-3-methylpentanoic acid | ||
| Nhận dạng | |||
| Số CAS | |||
| PubChem | |||
| DrugBank | DB00167 | ||
| KEGG | |||
| ChEBI | |||
| Ảnh Jmol-3D | ảnh | ||
| SMILES | đầy đủ
| ||
| InChI | đầy đủ
| ||
| UNII | |||
| Thuộc tính | |||
| Điểm nóng chảy | |||
| Điểm sôi | |||
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |||
Isoleucine (viết tắt là Ile hoặc I)[1] là một α-amino acid với công thức hóa học HO2CCH(NH2)CH(CH3)CH2CH3. Nó là một amino acid thiết yếu, nghĩa là cơ thể người không tự tổng hợp được và phải lấy từ thức ăn. Codon của nó là AUU, AUC và AUA.
Do có nhánh hydrocarbon, isoleucine được xếp vào nhóm amino acid kị nước. Cùng với threonine, isoleucine là một trong hai amino acid thường gặp có mạch nhánh đối xứng. Có bốn đồng phân lập thể có thể gặp của isoleucine, trong đó có hai đồng phân không đối quang của L-isoleucine. Tuy nhiên, trong thiên thiên isoleucine tồn tại dưới dạng đồng phân đối quang, acid (2S,3S)-2-amino-3-metylpentanoic.
Sinh tổng hợp[sửa | sửa mã nguồn]
Do là một amino acid thiết yếu, isoleucine không được tổng hợp ở cơ thể động vật, do đó phải được lấy từ thức ăn, thường là protein. Ở các loài thực vật và vi sinh, nó được tổng hợp qua nhiều giai đoạn, từ axit pyruvic và alpha-cetoglutarate. Các enzym tham gia vào quá trình này gồm:[2]
- Acetolactate synthase (hay còn được gọi là acetohydroxy acid synthase)
- Acetohydroxy acid isomeroreductase
- Dihydroxyacid dehydratase
- Valine aminotransferase
Chuyển hóa[sửa | sửa mã nguồn]
Isoleucine vừa là một amino acid sinh đường và là một amino acid sinh ceton. Sau phản ứng chuyển amin với alpha-cetoglutarate, khung cacbon có thể được chuyển hóa thành Succinyl CoA, và được đưa vào chu trình Krebs để bị oxy hóa, hoặc chuyển thành oxaloaxetat cho sự sinh đường mới (sinh đường). Nó cũng có thể được chuyển hóa thành Acetyl CoA và được đưa vào chu trình Krebs bằng cách kết hợp với oxaloacetate để tạo thành citrate. Ở các loài động vật có vú Acetyl CoA không thể được chuyển hóa ngược lại thành cacbohydrate nhưng có thể được dùng để tổng hợp các thể ceton hoặc các acid béo (sinh ceton).
Biotin, còn được gọi là Vitamin B7 hoặc Vitamin H, là thành phần không thể thiếu trong chuyển hóa đầy đủ của isoleucine (và leucine). Nếu cơ thể thiếu biotin, isoleucine và leucine sẽ không được chuyển hóa hoàn toàn [3]. Điều này có thể dẫn tới nhiều vấn đề sinh lý (như trương lực cơ, sự tổng hợp protein, chuyển hóa lipid và acid béo) và các vấn đề về nhận thức do sự tích tụ sản phẩm chuyển hóa của isoleucine là hydroxyisovalerate. Toan huyết isovaleric là một ví dụ về rối loạn chuyển hóa.[cần dẫn nguồn]
Nguồn cung cấp[sửa | sửa mã nguồn]
Mặc dù không được tổng hợp, isoleucine được dự trữ nhiều trong cơ thể động vật. Các thực phẩm giàu isoleucine gồm trứng, đậu nành, rong biển, gà tây, gà, cừu, pho mát, cá.[4]
Các đồng phân của isoleucine[sửa | sửa mã nguồn]
  |
| L-isoleucine (2S,3S) và D-isoleucine (2R,3R) |
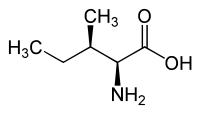  |
| L-allo-isoleucine (2S,3R) và D-allo-isoleucine (2R,3S) |
Tổng hợp[sửa | sửa mã nguồn]
Isoleucine có thể được tổng hợp qua nhiều bước, từ 2-bromobutane và diethylmalonate.[5] Sự tổng hợp isoleucine được báo cáo lần đầu vào năm 1905.[6]
Nhà học học người Đức Felix Ehrlich đã khám phá ra isoleucine trong hemoglobin vào năm 1903.
Tham khảo[sửa | sửa mã nguồn]
- ^ IUPAC-IUBMB Joint Commission on Biochemical Nomenclature. “Nomenclature and Symbolism for Amino Acids and Peptides”. Recommendations on Organic & Biochemical Nomenclature, Symbols & Terminology etc. Truy cập ngày 17 tháng 5 năm 2007.
- ^ Nelson, D. L.; Cox, M. M. "Lehninger, Principles of Biochemistry" 3rd Ed. Worth Publishing: New York, 2000. ISBN 1-57259-153-6.
- ^ “Genova Diagnostics”. Bản gốc lưu trữ ngày 19 tháng 10 năm 2013. Truy cập 25 tháng 9 năm 2015.
- ^ [1], List is in order of highest to lowest of per 200 Calorie serving of the food, not volume or weight.
- ^ “dl-Isoleucine”. Organic Syntheses. 1955.; Collective Volume, 3, tr. 495
- ^ Bouveault and Locquin, Compt. rend., 141, 115 (1905).