Điện thế hoạt động

Trong sinh lý học thần kinh, điện thế hoạt động (cũng được gọi là xung động thần kinh hay gai) được định nghĩa là sóng xung điện lan truyền dọc theo nhiều loại màng tế bào.[1][2]:72 Hiện tượng này đã được nghiên cứu rất kỹ trên màng sợi trục thần kinh, đồng thời quan sát thấy ở các tế bào có tính hưng phấn, dễ bị kích thích chẳng hạn như các tế bào cơ tim, tế bào nội tiết hay thậm chí là cả những tế bào thực vật.[2]:134[2]:263[2]:708 Màng sợi trục có giá trị điện thế nghỉ khoảng −70 milivôn (mV),[3]:720[4] và hầu như hằng định theo thời gian. Tuy nhiên, cũng có một số loại tế bào nhất định vận hành một cách linh động, hiệu điện thế màng được tạo ra bởi sự phân bố khác biệt giữa các ion của chúng không thực sự "nghỉ" mà dao động theo thời gian.[5]:1070 Giá trị âm của điện thế tĩnh đã nói lên rằng bên trong màng tế bào luôn có điện thế âm so với bên ngoài, và số lượng các điện tích âm trong màng cũng vượt trội hơn so với số lượng các điện tích dương bên ngoài màng tế bào.[6]:57 Khi các kích thích đã đủ khả năng làm hưng phấn màng, theo đó khởi tạo điện thế hoạt động; quá trình này diễn ra không cố định tại một điểm mà sẽ lan truyền ra các cấu trúc nơron lân cận như hiệu ứng "domino".[7] Thời gian điện thế động tiến hành cực nhanh ước tính khoảng 1 miligiây, tức gấp 100 lần thời gian một cái chớp mắt.[6]:82 Sau khi chu kỳ của điện thế hoạt động hoàn thành, màng tế bào tái phân lập trạng thái phân cực cũ, lúc này tương ứng giá trị điện thế trở về mức −70 milivôn. Xung động thần kinh di chuyển dọc theo sợi trục với tốc độ khoảng 100 m/s (225 dặm mỗi giờ).[3]:27 Khi những tế bào thần kinh được cho là có thể dài đến 1 mét hoặc hơn, chính tốc độ dẫn truyền nhanh này hỗ trợ cho những nơron thần kinh liên lạc thông tin với nhau một cách có hiệu quả. Điện thế hoạt động là cơ sở điện hóa cho các quá trình xử lý thông tin trong hệ thần kinh, bước đầu tiến tới hình thành nhận thức và tư duy.[8]:55

Tại vị trí màng tế bào, điện thế hoạt động sẽ được tạo ra khi các kích thích đủ mạnh để gây ra hiện tượng khử cực, tức là khi giá trị điện thế nghỉ đã đạt ngưỡng hưng phấn cần thiết là −55 mV.[9]:55 Quá trình khử cực sẽ làm "mở khóa" các kênh nhạy cảm với điện thế (voltage-sensitive channels), điều này cho phép dòng ion mang điện tích dương di chuyển vào trong sợi trục (axon), như vậy sự khử cực xuyên màng sẽ càng được tăng cường hơn nữa.[10] Thông qua đó sự phóng điện hình thành, khởi động vòng điều hòa ngược dương tính[11] một cách đột ngột và nhanh chóng khiến cho điện tích bên trong màng càng trở nên dương hơn. Sau sự tăng nhanh về biên độ điện thế, nhiều sự kiện phối hợp nhau nhằm thiết lập mức điện thế trở về trạng thái nghỉ: trong đó có các kênh chịu trách nhiệm cho việc lưu thông các ion vào bên trong màng bị bất hoạt, trong khi các kênh nhạy cảm với điện thế khác hoạt động tích cực tống các ion ra ngoài màng phục vụ cho sự cân bằng điện tích lúc chưa bị khử cực.[12][13][14][15] Điện thế hoạt động tuân theo cơ chế điều hòa ngược dương tính, cũng tức là nguyên lý tất cả hoặc không (all-or-none); quá trình điện thế hoạt động sẽ không chỉ giới hạn và một khi nó đã xảy ra sẽ làm cho tất cả các nơron liên đới với nó cùng chạy quá trình như vậy.[16][17][18][19] Đối với nơron và tại bất kỳ điểm nào trên sợi trục, một điện thế hoạt động điển hình kéo dài khoảng vài phần nghìn giây.[3]:26 Sự lan truyền của điện thế hoạt động qua các điểm sẽ làm cho các kênh ion đi vào trạng thái không cân bằng, các kênh sẽ khó bị mở ra hơn, và như vậy ức chế sự tạo thêm các điện thế hoạt động khác khi sợi trục vẫn còn trong giai đoạn trơ (refractory).[20]

Các ion chính yếu trong việc tạo ra điện thế hoạt động này là những cation Na+[21] và K+; Khi ion Na+ đi vào bên trong tế bào, và ion K+ đi ra, cứ như thế trong một chu kỳ của điện thế hoạt động cũng như đưa sự chênh lệch nồng độ của các ion về trạng thái cũ.[22] Có tương đối ít ion vượt màng tế bào để cảm ứng mạnh điện thế hoạt động. Vì lẽ đó, tiến trình trao đổi những ion trong quá trình điện thế hoạt động không tạo ra những thay đổi đáng kể nào đối với nồng độ những ion nội bào và ngoại bào. Sự hiện diện của các bơm Na⁺/K⁺-ATPase (được hoạt hóa liên tục thực hiện việc duy trì điện thế nghỉ)[3]:397 và các kênh vận chuyển ion khác (ion transporters) đóng vai trò quan trọng giúp đẩy các ion ra ngoài màng và duy trì nồng độ ion trở lại bình thường.[23] Các cation calci và anion chloride đặc biệt liên quan đến các dạng điện thế hoạt động khác, chẳng hạn như là điện thế hoạt động cơ tim[24][25][26][27] và điện thế hoạt động quan sát ở tảo xanh đơn bào Acetabularia.[28][29]


Điện thế hoạt động lan truyền theo sợi trục mà không có bất kỳ sự suy giảm nào về biên độ, bởi vì tín hiệu thần kinh được tái tạo ngay tại mỗi điểm màng.[30] Xung động thần kinh xảy ra tại một điểm sẽ làm tăng vọt điện thế ở các điểm kế cận, tiếp tục quá trình khử cực và sản sinh một điện thế hoạt động mới ở đó. Trên thực tế, điện thế hoạt động không có lan truyền dọc theo sợi trục, mà đó chính là sự tái tạo lại điện thế hoạt động liên tục thành chuỗi đi từ điểm khởi sinh sang các điểm kế tiếp.[31]:55–58 Đối với những nơron không có bao myelin, điện thế hoạt động lan truyền sang các vùng lân cận mà không bị trở ngại, tuy nhiên đối với các nơron có bao myelin, điện thế hoạt động thực hiện những "bước nhảy" qua các bao myelin này khi những bao này đóng vai trò như những chất cách điện, chính vì vậy làm cho quá trình dẫn truyền xung động thần kinh nhanh hơn và hiệu quả hơn.[32][33][34][35] Cấu trúc sợi trục thần kinh thường có sự phân nhánh,[36] và điện thế hoạt động thường lan truyền theo các nhánh đến tận các cúc tận cùng, tại đó xung động thần kinh không còn nữa, mà thay vào đó sự phóng thích các chất dẫn truyền thần kinh diễn ra ngay tại các khớp synap.[37][38][39] Những hóa chất dẫn truyền nội sinh này gắn kết với các thụ thể ở màng tế bào sau synap.[40][41][42][43] Các thụ thể này chính là thụ thể kênh ion phối tử (LGIC) hay còn gọi là thụ thể của các chất dẫn truyền thần kinh, không như các kênh ion nằm trên màng sợi trục; về tổng thể các kênh LGIC sẽ mở ra sau khi chất dẫn truyền đã gắn vào nó, trong khi những thay đổi điện thế không tác động đáng kể lắm đến những kênh này.[44][45] Các kênh liên kết thụ thể trải qua sự hoạt hóa và kích hoạt khử cực màng sau synap (trong trường hợp các kênh kích thích), hay chống lại khử cực (được biết với hiện tượng siêu phân cực, đối với các kênh ức chế). Nếu như quá trình khử cực đủ mạnh, điều này khiến cho chu kỳ điện thế hoạt động lại tiếp tục diễn ra ở màng sau synap.[46][47][48][49]
Hệ điện ly và cơ chế lý sinh của điện thế hoạt động[sửa | sửa mã nguồn]
Ion và các lực thúc đẩy sự chuyển động[sửa | sửa mã nguồn]

Khái niệm điện sinh vật đã bao hàm cả điện thế tĩnh và điện thế hoạt động.[50]:129–135 Cơ chế sinh học lý giải cho hiện tượng điện "sống" đã được khám phá và làm sáng tỏ,[51][52][53][54][55][56] trong đó các ion là nguyên nhân chính trong việc tạo ra vô số dòng điện mang tín hiệu truyền tải thông tin qua lại giữa các cấu trúc.[57]:9 Sự tương tác qua lại của các cation mang điện tích dương và các anion mang điện tích âm đã quyết định nên tính chất của dòng điện. Các cation quan trọng nhất nắm giữ vai trò then chốt cho sự tồn tại của điện thế hoạt động, bao gồm có natri (Na+) và kali (K+),[58]:140–141 cả hai đều là các cation đơn hóa trị mang một điện tích dương. Điện thế hoạt động cũng đồng thời liên quan đến ion calci (Ca2+),[58]:153–154 là cation hóa trị 2 và tương ứng mang hai điện tích dương. Đáng chú ý, anion chloride (Cl−) đóng vai trò chủ yếu tạo ra điện thế hoạt động đối với một số loại tảo,[29] nhưng nhìn chung không có gây ra sự thay đổi đáng kể nào lên trên dạng điện thế hoạt động ở hầu hết các loài động vật.[59]:483
Dòng ion chuyển động xuyên màng tế bào chịu tác động bởi hai lực: đó chính là lực khuếch tán do gradient nồng độ chi phối và lực điện trường.[57]:10–13 Quá trình khuếch tán cho phép các ion lưu thông theo hai chiều đi từ nơi có nồng độ cao đến nơi có nồng độ thấp.[60][61][62] Lực điện trường cũng có sự chi phối đến các ion khi có sự phân cực màng, tức là các ion dương có xu hướng rời môi trường cũ để đến phía âm, ngược lại ion âm dịch chuyển về môi trường dương hơn.[63][64][65][66][67][68][69] Theo định nghĩa, người ta xem tổng lực điện trường tại một điểm màng tế bào tương đương với giá trị điện thế Vm tại điểm đó. Như thế đối với các vùng có đường kính 1 µm và chứa duy chỉ một vài kênh ion (trong sinh lý học thần kinh, người ta dùng thuật ngữ "patch" để mô tả những vùng như vậy),[70]:279 dòng chảy của các hạt mang điện qua vùng này sẽ tạo ra dòng điện cho vùng đó; và tổng dòng điện được tính là tổng dòng chảy của từng ion riêng biệt. Khi sử dụng những định nghĩa liên quan đến điện thế và dòng ion, ta có thể mô hình hóa cấu trúc màng tế bào và dịch sinh vật như là mạch điện tương đương.[71] Cụ thể hơn, vùng "patch" có điện dung C và điện dẫn g (tính thấm chọn lọc màng); theo như định luật Ohm, cường độ dòng điện I của mỗi loại ion có liên quan đến điện thế xuyên màng qua phương trình I = g Vm. Tập hợp các ion với hệ số thấm nhất định, sự chuyển dời của các hạt điện tích dừng lại cũng là lúc mà điện thế đạt trạng thái cân bằng E; chính dòng chảy tự nhiên của các ion sẽ làm cho giá trị điện thế màng Vm tiến gần đến giá trị cân bằng E.[72]:279 Điều này diễn ra tuân theo những điều kiện nhất định, đó chính là khi màng đạt trạng thái cân bằng nhiệt động lực học, và chỉ thấm đối với một loại ion riêng biệt.[31][73][74]:41
Màng tế bào[sửa | sửa mã nguồn]

Màng tế bào đóng vai trò như là tụ điện, và kiến trúc của nó sẽ quyết định sự biến đổi cực nhanh của điện thế màng đáp ứng với những thay đổi trong sự phân bố các ion ở hai bên màng. Lớp màng bao quanh tế bào gần như không thấm đối với tất cả mọi loại ion,[75] vì vậy tế bào phải có cơ chế tiến hóa để vận chuyển ion xuyên màng. Hệ tiến hóa này bao gồm hai cơ chế: cơ chế vận chuyển thụ động với sự hiện diện của các lỗ thủng (tức các kênh), thứ hai là cơ chế vận chuyển chủ động với các bơm ion sử dụng nguồn năng lượng adenosine triphosphate (ATP) để hoạt động, cơ chế thứ hai này không tuân theo định luật khuếch tán Fick thứ nhất và nguyên lý thứ hai của nhiệt động lực học.[57]:9–10[76][77][78]:528 Các bơm ion được vận hành một cách liên tục không gián đoạn miễn là các ion vẫn còn (và cả ATP). Ngược lại, những kênh ion mở hay đóng tùy thuộc vào tín hiệu đến từ môi trường ngoài. Hai cơ chế này có vai trò hỗ trợ lẫn nhau; các bơm ion thực hiện việc tạo ra sự chênh lệch về nồng độ ion xuyên màng, trong khi các kênh ion mang nhiệm vụ dẫn truyền tín hiệu điện. Có thể ví dụ rằng, các bơm ion đóng vai trò như bộ ắc quy thông qua đó cho phép mạch điện vô tuyến (là các kênh ion) truyền đi các tín hiệu.[31]:42
Các kênh ion[sửa | sửa mã nguồn]

Các kênh ion có bản chất là các protein xuyên màng (integral membrane proteins) mà qua đó ion mới có thể đi qua màng được. Hầu hết các kênh chỉ đặc hiệu cho mỗi loại ion nhất định; trong khi đó trường hợp một kênh ion cho qua nhiều loại ion rất hiếm.[79] Chẳng hạn như, dù rằng ion kali và natri có cùng điện tích và chỉ hơi sai khác về bán kính, các kênh kali cho phép ion K+ đi qua rất dễ dàng, ngược lại số lượng ion Na+ vượt qua rất ít ỏi. Tại vị trí những lỗ thủng nơi mà các ion băng qua, nơi đó quá nhỏ khiến cho các ion phải đi một mình và theo hàng một.[80] Các kênh hoặc ở trạng thái mở hoàn toàn, hoặc là ở trạng thái đóng hoàn toàn. Khi kênh đã mở ra, dòng ion tuân theo cơ chế thụ động, tức là, với tốc độ vận chuyển được xác định bởi điện thế màng Vm và sự chênh lệch nồng độ giữa hai phía màng.[72]:33–37 Dấu hiệu cho thấy một điện thế hoạt động đã hình thành chính là nhiều kênh ion khác nhau được mở và đóng tại các thời điểm khác nhau.[58]:132

Một kênh có thể có nhiều trạng thái khác nhau (tương ứng với sự khác nhau về cấu hình không gian protein), nhưng mỗi trạng thái như vậy có thể mở hoặc đóng. Nhìn chung, trạng thái đóng là trạng thái trong đó các lỗ có hiện tượng co lại—làm cho các ion không thể vượt qua được—hoặc là những phần độc lập cấu thành protein sẽ thắt lỗ lại. Chẳng hạn, kênh natri phụ thuộc điện thế khi trải qua sự bất hoạt, một phần cấu trúc nhỏ trong phân tử protein dao động và tiến hành "phong ấn" lỗ thủng thông thương dòng chảy ion đi vào và đi ra đó.[81] Sự bất hoạt này sẽ ngừng lại dòng chảy của ion natri và đồng thời đóng vai trò then chốt trong quá trình điện thế hoạt động.[82][83][84]
Các kênh ion có thể được phân loại theo cách chúng đáp ứng với môi trường.[85] Ví dụ cụ thể, các kênh ion có liên quan đến điện thế hoạt động là các kênh nhạy cảm với điện thế; và kênh sẽ mở và đóng phù hợp với sự thay đổi về điện thế xuyên màng. Các kênh ion phối tử cũng là kênh quan trọng; những kênh ion này sẽ mở ra và đóng lại phụ thuộc vào sự hiện diện của phối tử, chẳng hạn như các chất dẫn truyền thần kinh. Trong khi đối với những kênh ion khác—vị trí tại những nơron cảm giác—thì việc mở và đóng phụ thuộc vào nhiều kích thích khác, như ánh sáng, nhiệt độ hay áp suất.[86][87][88][89][90][91][92][93][94]
Bơm ion[sửa | sửa mã nguồn]

Dòng chảy của các ion tức các hạt mang điện sẽ xác định nên sự khác biệt về nồng độ các ion ở hai bên màng, cũng như quyết định sự diễn ra của chu kỳ điện thế hoạt động. Chính các kênh vận chuyển ion thiết lập sự khác biệt này, chúng là những protein xuyên màng và thực hiện cơ chế vận chuyển chủ động, sử dụng nguồn năng lượng tế bào (ATP) để bơm ion chống lại gradient nồng độ.[95] Như thế những bơm ion sẽ lấy đi các ion từ phía màng bất kỳ (làm giảm nồng độ các ion ở đó) và giải phóng cho phía còn lại (làm tăng nồng độ các ion ở đó). Loại bơm ion mà vai trò của nó hết sức mật thiết với điện thế hoạt động đó chính là bơm Na⁺/K⁺-ATPase (còn gọi là bơm Na–K),[96][97][98][99] vận chuyển ba ion Na+ ra ngoài màng và đưa hai ion K+ vào trong.[100][101] Do đó, nồng độ ion K+ bên trong tế bào nơron cao gấp 20 lần so với bên ngoài, trong khi đó nồng độ ion Na+ bên ngoài màng lại cao gấp 9 lần so với bên trong.[102][103] Tương tự, các ion khác cũng có sự khác nhau về nồng độ phân bổ phía trong và ngoài màng, chẳng hạn như calci, chloride và magnesi.[103]

Các bơm ion ảnh hưởng đến quá trình điện thế hoạt động chỉ khi chúng tổ chức lại tỷ lệ ion tương đối giữa trong và ngoài màng tế bào. Điện thế hoạt động chủ yếu xảy ra phụ thuộc vào sự mở và đóng của các kênh ion, không phải hoạt động của các bơm ion. Nếu như các bơm ion không vận hành được do sự thiếu hụt nguồn năng lượng cung cấp, hoặc là đưa vào chất ức chế ouabain, màng sợi trục vẫn có thể "bắn" từ 100,000 đến 1,000,000 điện thế hoạt động trước khi biên độ bắt đầu có sự suy giảm đáng kể.[95] Hơn nữa, các bơm ion không đóng vai trò quan trọng nào trong giai đoạn tăng tái phân cực màng (repolarization) sau khi diễn ra điện thế hoạt động.[58]:140–141[72]:33–35
Điện thế nghỉ[sửa | sửa mã nguồn]
Mỗi loại ion đều có một giá trị điện thế nghịch đảo E—cũng được gọi là điện thế cân bằng—khi mà chuyển động vào và ra khỏi màng đã hoàn toàn dừng lại; lực điện trường do các ion tạo ra sẽ chống lại lực thúc đẩy bởi sự chênh lệch nồng độ xuyên màng (tức gradient nồng độ). Qua phương trình Nernst ta có thể tính được giá trị điện thế cân bằng:[31]:41[58]:133–134[59]:478–480, 596–597[72]:33–35[104]
Trong phương trình này, n là hóa trị của chính ion đó (chẳng hạn, đối với K+ là +1, Ca2+ là +2, Cl− là −1), T là nhiệt độ tuyệt đối K, R là hằng số khí lý tưởng, F là hằng số Faraday, cũng được xem là điện tích của 1 mol electron. Các số liệu tính ra được chỉ mang tính minh họa, phù hợp với mức sinh lý của cơ thể, giá trị điện thế cân bằng kali EK là −75 mV, trong khi giá trị điện thế cân bằng của natri ENa là +55mV. Vì sự khác biệt này, điện năng sẽ không được tạo thành khi tổng cường độ dòng chảy các ion natri và kali bằng không, điều này cũng có nghĩa rằng là màng tế bào phải có tính thấm riêng biệt đối với các ion để tạo ra được một hiệu điện thế xuyên màng.
Tuy nhiên, giá trị điện thế màng Em được tạo ra khi sự chuyển động của tất cả các ion xuyên màng bằng không; các cơ chế chính xác của việc tạo ra điện thế tĩnh này đã được mô hình hóa qua phương trình Goldman dưới đây:[31]:43[58]:138–140[59]:480[72]:35–37[105]
Trong đó ba ion đơn hóa trị kali (K+), natri (Na+), và chloride (Cl−) có vai trò cực kỳ quan trọng đối với điện thế hoạt động. Vì là anion, nên nồng độ chloride nội bào sẽ là tử thức, và nồng độ chloride ngoại bào sẽ là mẫu thức, ngược lại so với cation. Nếu ion calci cũng được xét đến, công thức tính ra giá trị điện thế cân bằng sẽ phức tạp hơn nhiều.[106]

Điện thế màng Vm không cần thiết phải bằng giá trị cân bằng Em. Tuy nhiên, vì Vm có thể biến đổi nhanh chóng khi chỉ có vài ion vượt màng và làm thay đổi trật tự phân cực màng, giá trị Vm có thể tiến gần sát giá trị Em. Trong quá trình điện thế hoạt động, sự thay đổi về biên độ điện thế màng Vm có thể xấp xỉ khoảng 100 mV, trong khi đó bên trong sợi trục nồng độ ion thay đổi chỉ cỡ 1 phần 10 triệu;[58]:135–136 chính vì thế, khi vô số các điện thế hoạt động đã được phóng ra với số lượng từ 100,000 đến 1,000,000 xung, chu kỳ của các điện thế hoạt động này phải diễn ra cực nhanh trước khi các bơm ion được hoạt hóa nhằm đưa tỷ lệ về nồng độ ion phân bố ở hai bên màng trở lại mức tiêu chuẩn bình thường.[95]
Điện thế cân bằng Em dưới ngưỡng bình thường, với điều kiện không có các kích thích được gọi là điện thế nghỉ Vnghỉ, với giá trị điển hình khoảng −70 mV.[58]:131 Tính thấm của màng đối với ion kali vượt trội hơn so với các ion khác; và điều này cũng nhất quán với phương trình Goldman, khi giá trị điện thế nghỉ gần bằng giá trị điện thế cân bằng kali EK.[58]:134[59]:478–480[21] Tuy nhiên, trong giai đoạn giữa của chu kỳ điện thế hoạt động, tính thấm của ion natri áp đảo hơn, khiến cho giá trị Em tăng lên đến +45 mV, tiến gần đến giá trị điện thế cân bằng của natri ENa.[58]:135[59]:480–481[21]
Giải phẫu học nơron thần kinh[sửa | sửa mã nguồn]
Nhiều tế bào khác nhau ngoài tế bào thần kinh cũng có thể thực hiện quá trình điện thế hoạt động, chẳng hạn như tế bào thực vật, tế bào cơ, và những tế bào chuyên biệt cấu tạo nên trái tim (tại đó diễn ra điện thế hoạt động cơ tim).[24] Tuy nhiên, tế bào dễ bị kích thích chính và chủ yếu đó chính là nơron, được xem là tế bào có cơ chế tạo ra điện thế hoạt động đơn giản nhất.

Hầu hết các nơron thần kinh đều có sự phân nhánh tỏa ra từ thân tế bào (neurites),[58]:11[107][108][109][110] được chia làm hai loại đó là sợi nhánh (dendrites) và sợi trục (axon). Đa số các nơron chỉ có một sợi trục, nhưng có rất nhiều sợi nhánh;[58]:14 tại vị trí bắt đầu của sợi trục có một mỏm lồi hình nón được gọi là tiểu đồi sợi trục (axon hillock).[58]:19, 25[111]:22 Tiểu đồi sợi trục là vùng khởi động (trigger zone) trong đó điện thế hoạt động luôn luôn xuất phát từ vùng này, và lan truyền dọc theo sợi trục; rất hiếm trường hợp điện thế hoạt động xảy ra tại sợi nhánh.[58]:11 Một sợi trục điển hình chia tiếp thành nhiều nhánh nhỏ giống như cây phân nhánh; và kết thúc tận cùng tại những cúc tận cùng (synaptic knobs). Những cúc tận cùng này chính là nơi mà kết cấu synap hình thành với cấu trúc sợi nhánh từ các tế bào thần kinh kế cận khác (hay những tế bào có thể kích thích khác); thông qua đó cho phép quá trình truyền tin giữa các tế bào diễn ra dưới dạng các xung động thần kinh.[58]:29–49[112][113][114][115][116]
Đối với một số loài động vật (và hầu hết các loài động vật có xương sống), trên sợi trục có những phân đoạn được bao bọc bởi loại vỏ gồm nhiều lớp lipid và protein gọi là bao myelin,[58]:58–61 do các tế bào thần kinh đệm sinh ra, có chức năng làm tăng tốc độ dẫn truyền xung điện thần kinh dọc theo sợi trục.[58]:157–164[32][117] Đối với hệ thần kinh ngoại biên, các tế bào Schwann đóng vai trò quan trọng trong việc tạo ra các bao myelin bằng cách quấn xoắn ốc nhiều lần quanh sợi trục, tạo lớp lipid dày ngăn chặn sự xâm nhập và thoát của các ion trong phạm vi sợi trục. Trong đó, nhiều lớp màng tế bào (khoảng 100 lớp) bọc quanh sợi trục hình thành nên bao myelin, và phần tế bào chất và nhân tế bào Schwann bị đẩy ra ở lớp ngoài cùng. Dòng chảy ion đi vào và đi ra sợi trục chỉ có thể diễn ra được tại khoảng trống giữa vỏ myelin được gọi là eo Ranvier.[58][118]:58–61[119] Chính vì thế, điện thế hoạt động sẽ "nhảy vọt" từ eo Ranvier này đến eo Ranvier kế cận; đối với những sợi trục mà không có sự myelin hóa, điện thế hoạt động lan truyền theo sợi trục một cách liên tục mà không có sự gián đoạn nào.[120]:25–31
Các giai đoạn biến đổi của điện thế hoạt động[sửa | sửa mã nguồn]

Quá trình điện thế hoạt động được xác định bởi hai hệ quả phối hợp nhau.[120]:127–128 Thứ nhất, các kênh ion nhạy cảm với điện thế sẽ mở và đóng tùy thuộc vào những thay đổi về điện thế màng Vm, như thế làm thay đổi tính thấm màng đối với các ion.[31]:65 Tuy nhiên, theo phương trình Goldman, sự biến đổi về tính thấm các ion cũng sẽ gây ra tác động ngược lại với điện thế cân bằng Em, cũng như đối với điện thế màng Vm.[105] Sự tương tác hai chiều này giữa Vm và những kênh ion sẽ xây dựng vòng điều hòa ngược dương tính, điều này vô cùng quan trọng trong giai đoạn tăng khử cực (rising phase) của điện thế hoạt động.[31]:49–55[58]:141, 150–151[59]:483[72]:89[120]:127 Điều này thực sự không diễn ra một cách thuận lợi, bởi vì kênh ion có thể có "cánh cổng" bên trong chống lại những biến đổi mà điện thế màng Vm gây ra, hoặc là cản trở tốc độ lưu hành của dòng ion vào nội bào.[31]:69[58]:149–150[72]:84–85[120]:152–158[121][1][22] Chẳng hạn, dẫu rằng giá trị Vm tăng lên sẽ khiến cho các cổng của kênh natri nhạy cảm điện thế mở ra, nhưng nó cũng đồng thời làm cho "cánh cổng bất hoạt" của kênh đóng lại một cách rất chậm.[58]:147–148[120]:128 Như vậy, khi điện thế màng Vm tăng đột biến và những cánh cổng hoạt hóa kênh natri bắt đầu mở ra (activation gate), nhưng sau đó dòng chảy ion Na+ cũng bị chặn lại là kết quả của sự đóng lại chậm các cánh cổng bất hoạt (inactivation gate).

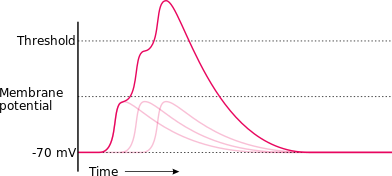
Một chu kỳ của điện thế hoạt động có thể được chia ra thành bốn giai đoạn: giai đoạn tăng khử cực (rising phase), giai đoạn tăng tái phân cực hay giai đoạn giảm khử cực (falling phase), giai đoạn cực hóa (hay siêu phân cực, undershoot phase), và giai đoạn trơ (refractory period). Tính thấm màng tế bào đối với ion kali lớn hơn nhiều so với các ion khác, khiến cho giá trị điện thế nghỉ tiến dần đến giá trị EK.[31]:45[58]:134[59]:478–480 Hiện tượng khử cực đủ mạnh (làm tăng giá trị Vm) sẽ đẩy các cánh cổng của kênh natri nhạy cảm với điện thế; tăng cường tính thấm ion natri đưa giá trị Vm tiến tới giá trị điện thế cân bằng của natri ENa là +55mV. Biên độ điện thế càng tăng cao càng thúc đẩy nhiều kênh natri mở ra hơn, điều này tương đương giá trị Vm sẽ càng tiến đến giá trị ENa. Cơ chế điều hòa ngược dương tính này sẽ tiếp tục vận hành cho đến khi các kênh natri hoàn toàn mở ra và giá trị điện thế nghỉ Vm cũng tiến gần đến giá trị cân bằng ENa.[31]:46[58]:140–141, 150–151[59]:480–481, 483–484[72]:89–90 Đây là giai đoạn tăng khử cực.[31]:46 Đến điểm giới hạn nhất định, các kênh natri bắt đầu bất hoạt dần, tương ứng tính thấm của màng đối với ion natri giảm xuống, và đưa giá trị Vm trở về mức giá trị điện thế nghỉ ban đầu.[31]:49[58]:147–148[120]:128 Trong khi đó, các kênh kali sẽ mở ra toàn bộ, như thế làm cho giá trị điện thế màng tiến về giá trị điện thế cân bằng kali EK.[31]:55[58]:147–149[120]:126–127[59]:483–484 Đây chính là giai đoạn tăng tái phân cực.[31]:47 Trong khoảng thời gian mà tính thấm của ion kali vẫn còn cao bất thường, điều này sẽ cực hóa điện thế màng, với giá trị vượt xa hơn giá trị điện thế nghỉ bình thường; và đây là giai đoạn siêu phân cực.[31]:55 Những sự kiện cuối cùng của chu kỳ điện thế hoạt động gồm có, đó là khoảng thời gian mà điện thế hoạt động kế tiếp không được tạo ra hay khó có thể tạo ra, được gọi là giai đoạn trơ, và giai đoạn này có thể xảy ra trùng với những giai đoạn khác.[31]:55
Vào năm 1952, giá trị điện thế và cường độ dòng ion của điện thế hoạt động đã được mô hình hóa một cách chính xác bởi Alan Lloyd Hodgkin và Andrew Huxley trong tất cả các giai đoạn.[1][22][121] Năm 1963, họ nhận được Giải Nobel Sinh lý học và Y học nhờ vào những cống hiến của họ.[123] Tuy nhiên, mô hình mà họ đưa ra chỉ xoay quanh hai loại kênh ion nhạy cảm với điện thế, và có nhiều giả định trong đó, cụ thể hơn là các cánh cổng bên trong sẽ mở và đóng một cách độc lập. Trên thực tế, có nhiều loại kênh ion khác nhau,[85] và chúng không chỉ luôn luôn giữ trạng thái ổn định (hoặc mở, hoặc đóng).[124]
Các kích thích ngoại vi và giai đoạn tăng khử cực[sửa | sửa mã nguồn]

Điện thế hoạt động cơ bản bắt đầu diễn ra tại cấu trúc tiểu đồi sợi trục (axon hillock) khi kích thích làm tăng Vm đã đủ mạnh để gây ra khử cực.[120][125][126][127]:49 Trên mẫu mô sinh thiết, là những axon khổng lồ của các loài mực ống Châu Âu, nhà nghiên cứu sinh lý học thần kinh thường kích thích hiện tượng khử cực bằng cách tiêm dung dịch có chứa cation natri vào bên trong tế bào thần kinh; trong cơ thể sinh vật cũng có nhiều nguồn cation natri phong phú trong dịch ngoại bào ở tại những synap hóa học, nơron cảm giác, hay tại tế bào tạo nhịp cơ tim hình thành nên một dạng điện thế hoạt động trong đó ion Ca2+ đóng vai trò chủ đạo được gọi là điện thế tạo nhịp (pacemaker potentials).[128][129][130][131]
Quá trình khử cực sẽ mở các kênh natri và kali tại màng tế bào, và cho phép dòng ion chảy vào và ra khỏi sợi trục. Nếu như khử cực có diễn ra nhưng nhỏ (làm tăng Vm từ −70 mV đến −60 mV), lúc này dòng ion kali đi ra ngoài màng sẽ lấn át dòng ion natri đi vào trong, như vậy màng sẽ tái phân cực lại đưa về giá trị điện thế nghỉ −70 mV.[58]:150–151[59]:484[72]:89–90 Ở bức hình 2 minh họa, ta có thể thấy được rằng các kích thích dưới ngưỡng (failed initiations) không đủ để khởi động nên chu kỳ điện thế hoạt động. Tuy nhiên là, trong trường hợp sự khử cực đã đủ lớn và chạm đến ngưỡng, dòng ion natri đi vào bên trong vượt trội hơn so với dòng ion kali đi ra bên ngoài, cơ chế điều hòa ngược dương tính xảy ra cực nhanh ngoài phạm vi kiểm soát được: đó là càng có nhiều dòng Na+ đi vào bên trong tế bào, giá trị điện thế màng Vm càng tăng cao, điều này khiến cho cường độ dòng Na+ càng được tăng cường.[31]:57[58]:141, 150–151[59]:483[72]:89[120]:127 Sự tăng mạnh và đột ngột về biên độ Vm và tính thấm natri tương ứng với giai đoạn tăng khử cực của chu kỳ điện thế hoạt động.[31]:46
Ngưỡng điện thế cần thiết để gây nên trạng thái chuyển động "out of control" trên hệ sinh vật vi mô là khoảng −45 mV, nhưng việc này phụ thuộc vào hoạt động thần kinh của sợi trục trong thời gian gần. Một khi màng đã vừa mới phóng một xung động thần kinh, nó sẽ không thể phóng thêm một xung động khác ngay lập tức, lý giải cho điều này, đó là vì những kênh ion chưa thể trở về trạng thái bình thường. Khoảng thời gian trong đó không có bất kỳ một điện thế hoạt động mới nào được tạo ra, được gọi là giai đoạn trơ tuyệt đối (absolute refractory period).[132]:105 Khi thời gian "nghỉ" đã được kéo dài, nhưng tất cả các kênh ion vẫn còn chưa hồi phục hết, màng sợi trục có thể tiếp nhận kích thích và theo đó sản sinh một điện thế hoạt động khác, nhưng đó là đối với kích thích khử cực mạnh hơn nhiều (ví dụ đến ngưỡng là −30 mV, chứ không còn là −45 mV). Thời gian mà những nơron khó có thể bắn ra điện thế hoạt động được gọi là giai đoạn trơ tương đối (relative refractory period).[132]:105
Đỉnh điểm của điện thế hoạt động và giai đoạn tăng tái phân cực[sửa | sửa mã nguồn]

Vòng điều hòa ngược dương tính của giai đoạn khử cực sẽ sớm bị phân rã, tạm ngừng lại khi những kênh ion natri đã mở ra tối đa. Khi biên độ của điện thế hoạt động đạt đến giá trị cao nhất, cùng lúc tính thấm natri đã tối đa hóa và giá trị điện thế màng Vm gần bằng với giá trị điện thế cân bằng natri ENa. Tuy nhiên là, mức điện thế năng lượng tăng cao cũng khiến cho các kênh natri dần dần đóng lại một cách chậm rãi, thông qua việc chặn lại các lỗ; kênh natri trở nên bất hoạt.[122]:60[31]:69[58]:147–148[120]:128 Điều này sẽ làm cho tính thấm màng đối với natri giảm xuống, "đạp" giá trị điện thế màng xuống. Cùng lúc đó (khi giá trị điện thế vẫn còn ở mức cao), các kênh kali nhạy cảm với điện thế mở cửa; tính thấm của màng đối với ion kali tăng lên, khi này giá trị điện thế màng Vm sẽ tiến về giá trị cân bằng EK. Những biến đổi phối hợp này về tính thấm natri và kali gây ra sự suy giảm nhanh chóng của điện thế màng Vm, tái phân cực màng và biểu hiện ra "giai đoạn đổ nát" của điện thế hoạt động.[31]:47[58]:147–149, 152[59]:483–484[120]:126–127
Giai đoạn siêu phân cực[sửa | sửa mã nguồn]
Điện thế tăng cao làm mở rất nhiều kênh kali hơn bình thường (mức điện thế nghỉ), và những kênh này vẫn không đóng lại ngay cả khi trạng thái tĩnh của điện thế màng đã được thiết lập. Tính thấm ion kali tăng cao thất thường và không ổn định, khiến cho giá trị điện thế màng Vm tiến tới rất sát với giá trị điện thế cân bằng kali EK. Vì thế đây là giai đoạn cực hóa (âm), hay siêu phân cực theo ngôn ngữ chuyên môn, duy trì cho đến khi tính thấm màng đối với ion kali trở về giá trị bình thường.[31]:47[58]:152
Giai đoạn trơ[sửa | sửa mã nguồn]
Trong chu kỳ điện thế hoạt động, sự mở và đóng của các kênh natri và kali có thể làm chúng rơi vào trạng thái "trơ", có nghĩa rằng là chúng sẽ không thể mở ra được nữa cho đến khi hồi phục.[31]:55[58]:151[72]:4–5[120]:19–20 Trong giai đoạn trơ tuyệt đối, có rất nhiều kênh ion bị trơ khi đó không có điện thế hoạt động mới nào được phóng ra. Tiến trình khôi phục các chức năng của vô số kênh gắn trên màng (khử bất hoạt) diễn ra đáng kể khi màng sợi trục vẫn còn giữ trạng thái cực hóa trong khoảng thời gian nhất định. Trong giai đoạn trơ tương đối, các kênh hồi phục với mức độ đủ để có thể hình thành điện thế hoạt động, nhưng với điều kiện kích thích đó mạnh hơn so với các kích thích trước. Hiện tượng trơ của các tế bào thần kinh đảm bảo rằng là điện thế hoạt động chỉ lan truyền một hướng dọc theo sợi trục.[31]:57
Sự kiện khởi đầu, lan truyền và hoàn thành chu kỳ điện thế hoạt động[sửa | sửa mã nguồn]

Vùng tiểu đồi sợi trục đóng vai trò quan trọng trong sự phát sinh các điện thế hoạt động khi có sự khử cực màng và điện thế đã tăng lên đủ đạt ngưỡng. Khi điện thế màng tăng lên, cả hai kênh ion natri và kali đều bắt đầu mở ra, làm tăng lưu lượng dòng chảy natri và cân bằng dòng chảy kali. Đối với bất kỳ sự tăng biên độ điện thế nhỏ nào, dòng chảy kali sẽ thắng dòng chảy natri và giá trị điện thế trở về mức nghỉ là −70 mV.[58]:150–151[72]:89–90[59]:484 Tuy nhiên, nếu như điện thế tăng quá ngưỡng tới hạn (critical threshold), điển hình là cao hơn giá trị nghỉ 15 mV, dòng chảy natri lúc này chiếm ưu thế và chu kỳ điều hòa ngược dương tính (runaway condition) diễn ra; lúc này tế bào thần kinh phóng ra xung động thần kinh.[31]:57[58]:141, 150–151[59]:483[72]:89[120]:127 Khi quá trình điện thế hoạt động này đã diễn ra truyền dọc theo sợi trục liên tục không gián đoạn;[59]:484 khi một phạm vi màng (patch) đã bị khử cực với sự xuất hiện của điện thế hoạt động, những vùng kế cận cũng bị khử cực và đánh bật ra những điện thế hoạt động mới ở đó. Thực tế, điện thế hoạt động được tân tạo trong mỗi phân vùng màng; và năng lượng xung điện tỏa ra bắt nguồn từ sự sai biệt cục bộ về nồng độ ion xuyên màng, chứ không phải là quá trình khử cực gây ra. Sợi trục chính có thể phân nhánh bên (axon collateral), không thể nhầm lẫn với cấu trúc telodendron, tức là các tận cùng sợi trục. Các nhánh bên chính có thể phân tiếp cho ra các nhánh bên phụ, rất hiếm các trường hợp điện thế hoạt động lan truyền dừng lại tại các điểm phân nhánh (branch point), thay vào đó gắn liền với sự suy giảm về biên độ do màng sợi trục rơi vào giai đoạn trơ. Đối với những xung động thần kinh phức tạp ("spikelet", tức các xung con), sự lan truyền của điện thế động có thể dừng lại tại các điểm như thế.[58]:209 Điện thế hoạt động đi đến vị trí kết thúc sợi trục sẽ kích hoạt sự giải phóng của các hóa chất dẫn truyền thần kinh vào synap, kết hợp với các điện thế hoạt động khác từ những nơron khác nhằm thúc đẩy một điện thế hoạt động mới ngay tại màng sau synap của tế bào thần kinh hay tế bào cơ.[3][133][134][135][136][137]:39, 535
Sự kiện khởi đầu[sửa | sửa mã nguồn]
Trước khi đề cập đến quá trình lan nhanh và mạnh của điện thế hoạt động và kết thúc tại những cúc tận cùng, việc hiểu rõ các cách thức khởi tạo nên điện thế hoạt động tại tiểu đồi sợi trục là quan trọng, bởi vì chính những quá trình điện động cơ sở này là nền tảng cho các quá trình sinh hóa khác.[3]:67, 135, 183, 519, 527, 561, 951, Điều kiện thiết yếu đó là giá trị điện thế màng tại tiểu đồi sợi trục trên ngưỡng để có thể gây ra làn sóng hưng phấn; hiện tượng khử cực này có thể diễn ra được theo nhiều cơ chế khác nhau.[3]:24
Quá trình truyền động các hóa chất thần kinh[sửa | sửa mã nguồn]

Điện thế hoạt động khởi động được hầu hết là nhờ điện thế kích thích sau synap (excitatory postsynaptic potentials, EPSP) được phóng bởi các nơron trước synap.[3]:1157–[58]:177–240[59]:490–499[120]:47–68 Trong đó EPSP có được phụ thuộc vào sự phóng thích của những phân tử truyền đạt thần kinh bởi nơron trước synap, các phân tử này sẽ gắn vào các thụ thể tại màng sau synap.[138][139][140][141][142][143] Sự gắn kết của các phân tử sẽ làm mở nhiều loại kênh ion khác nhau, kéo theo sự thay đổi tính thấm màng tế bào diễn ra cục bộ tại màng sau synap, gây ra biến đổi điện thế màng như đã nói ở trên. Nếu như quá trình liên kết tại các khớp thần kinh làm tăng điện thế (khử cực màng), đây là synap kích thích;[144][145][146] và ngược lại nếu làm giảm điện thế (siêu phân cực màng), đây là synap ức chế.[31][147][148][149][150][151]:107[57]:361 Dẫu cho giá trị điện thế tăng hay giảm, những thay đổi về điện này sẽ lan truyền những vùng lân cận một cách thụ động, điều này đã được làm rõ và mô tả chính xác trong phương trình điện thần kinh (cable equation),[57]:66 trong đó những dây thần kinh được ví như những dây cáp dẫn điện qua lại giữa vô số vùng khác nhau của cơ thể, và đặc tính của tế bào thần kinh, sợi trục, sợi nhánh, thân thần kinh sẽ tác động đến khả năng lan truyền và vận tốc của điện thế hoạt động. Cụ thể hơn, kích thích điện hay điện thế khởi sinh (do sự gắn vào của các phân tử dẫn truyền thần kinh) sẽ bị phân rã theo cấp số mũ theo không gian (khoảng cách synap) và thời gian.[57]:68–71[2]:11 Tập hợp một phần xung điện hưng phấn EPSP có thể lan đến tiểu đồi sợi trục và (trong trường hợp hiếm) khử cực màng đủ để khởi tạo điện thế hoạt động.[122] Điện thế khởi sinh (graded potential) là nền tảng cho sự khai sinh của điện thế hoạt động, và chống lại nguyên tắc tất cả hoặc không, cường độ của nó phụ thuộc vào độ mạnh của kích thích.[152]:31[153] Điện thế khởi sinh càng vượt ngưỡng bao nhiêu, tần số của điện thế hoạt động càng mạnh bấy nhiêu.[152]:32 Sự tham gia của nhiều xung kích thích đến từ các synap cần phải phối hợp đồng thời trong cùng một thời gian (cộng hưởng kích thích) để có thể phóng ra "gai" mới.[152]:228 Tuy nhưng, những ảnh hưởng chung này có thể bị cản trở bởi tác động phản kháng của những điện thế ức chế sau synap (inhibitory postsynaptic potentials).[152]:222
Quá trình dẫn truyền tín hiệu thần kinh cũng có thể xảy ra đối với các synap điện với tốc độ nhanh hơn nhiều so với các synap hóa học, và hai chiều do sự kết nối trực tiếp giữa các tế bào kích thích.[111]:33 Tuy rằng, có các kênh chỉnh lưu có chức năng đảm bảo rằng điện thế hoạt động chỉ truyền đi theo một chiều qua các synap như vậy.[152][154]:180
Điện thế hoạt động tại các nơron cảm giác[sửa | sửa mã nguồn]

Ở những nơron cảm giác, các kích thích ngoại vi chẳng hạn như là áp suất, nhiệt độ, ánh sáng, hay âm thanh đều gắn liền với sự đóng và mở các cổng kênh ion, và như vậy làm thay đổi tính thấm màng đối với những ion đặc thù và cả giá trị điện thế.[58]:49–56, 76–93, 247–255[59]:535–580[120]:69–79 Những chuyển đổi phát sinh dòng điện này có thể là kích thích (khử cực) hoặc ức chế (siêu phân cực) và, trong một số nơron cảm giác, tích hợp các kích thích và ức chế có thể cho ra quá trình khử cực tại tiểu đồi sợi trục và khởi động chu kỳ điện thế hoạt động. Lấy tế bào thần kinh khứu giác (ORN) và tiểu thể Meissner (Meissner's corpuscles) ở người làm ví dụ, chúng đặc biệt quan trọng đối với sự nhận cảm về mùi và cảm giác thân thể.[155][156][157][158][159][160][161][162][163][164][165] Tuy rằng, không phải tất cả các nơron cảm giác đều chuyển đổi tín hiệu ngoài thành các điện thế hoạt động; bởi do một số loại nơron thậm chí không có cả sợi trục![58]:53, 122–124 Thay vào đó, chúng có thể tiếp nhận các tín hiệu kích thích và trực tiếp gây nên sự phóng thích của các hóa chất dẫn truyền,[2]:245 hay hình thành ra điện thế khởi sinh (hay còn gọi là điện thế tầng, graded potentials),[2]:237 và một trong hai đều có thể kích thích các tế bào thần kinh khác phóng ra điện thế hoạt động. Cụ thể hơn, trong tai người, có các tế bào có lông tác động đến sự mở và đóng của các kênh nhạy cảm với sự biến đổi về cơ học (mechanosensitive channels) dưới sự hiện diện của các sóng âm thanh thu được.[166][167][168][169][170][171][172][173] Tiếp theo đó, là sự giải phóng các phân tử truyền đạt thần kinh.[2]:245 Tương tự, đối với hệ võng mạc người, tế bào nhận cảm ánh sáng (tức tế bào nón và tế bào que, photoreceptor cell) là lớp ngoài cùng của võng mạc, cùng với hai lớp trong (các tế bào lưỡng cực và tế bào thần kinh trung gian amacrine) không sản sinh ra các điện thế hoạt động;[174]:292–295[175][176] chỉ có lớp thứ ba, đó là các tế bào hạch tạo ra (ganglion cells) điện thế hoạt động và xung điện lan theo sợi thần kinh thị giác.[177][178][179]
Điện thế tạo nhịp[sửa | sửa mã nguồn]

Điện thế hoạt động diễn ra là kết quả của các kích thích ngoại vi, thông qua sự truyền đạt các phân tử thần kinh và các nơron cảm giác. Tuy nhiên, một số tế bào có thể kích thích nhưng không cần kích thích để phóng điện: chúng khử cực vùng tiểu đồi sợi trục một cách tự phát và bắn điện thế hoạt động với một tốc độ đều đặn, giống như đồng hồ sinh học.[72]:115–132 Dạng điện thế của những tế bào như thế được gọi là điện thế tạo nhịp.[58]:152–153 Các tế bào tạo nhịp cơ tim thuộc khu vực nút xoang nhĩ (sinoatrial node) ở tim là ví dụ điển hình.[180] Mặc dù rằng những điện thế tạo nhịp được tạo ra một cách tự nhiên, nhưng nó có thể bị điều chỉnh bởi các kích thích ngoài; chẳng hạn như, nhịp tim có thể bị thay đổi do các tác động dược lý và những tín hiệu đến từ sợi dây thần kinh giao cảm và phó giao cảm.[58]:444–445 Các kích thích ngoài không ảnh hưởng đến sự đồng bộ của các xung, nhưng đơn thuần là thay đổi thời gian.[58]:152–153 Trong một số trường hợp, sự điều hòa về tần số xung có thể rất phức tạp, dẫn đến các loại điện thế hoạt động khác nhau, chẳng hạn như sự đốt cháy của tế bào thần kinh và hiện tượng bùng nổ điện thế hoạt động (burst firing).[181][182][183][184]
Lan truyền[sửa | sửa mã nguồn]
Điện thế hoạt động sẽ truyền dọc theo sợi trục tương tự như sự di chuyển của sóng.[185] Dòng ion đi vào bên trong màng tại một điểm trên sợi trục trong điện thế hoạt động có khuynh hướng lan ra và khử cực những phân màng kế cận. Nếu như khử cực mức độ đủ mạnh sẽ gây ra quá trình điện thế hoạt động ở những khu vực "láng giềng" đó. Cơ chế nền tảng này đã được Alan Lloyd Hodgkin chứng minh vào năm 1937. Bằng thực nghiệm cố gắng phá vỡ chu kỳ điện thế hoạt động sau khi dùng khối ebonite có bọc lớp cao su mỏng để tạo áp lực hay làm lạnh tế bào thần kinh, ông đã chứng minh rằng điện thế hoạt động đến vùng cản điện (phạm vi nhỏ) sẽ dừng lại, nhưng các vùng sau đó nữa có sự tăng tính hưng phấn đi kèm với sự giảm ngưỡng kích thích đến 90%, như thế có thể phóng tiếp điện thế hoạt động mới ở đó.[186]
Một khi điện thế hoạt động đã diễn ra tại điểm màng trong đó rất ít sự hiện diện của các kênh ion, thì màng cần có khoảng thời gian hồi phục nhất định trước khi một điện thế hoạt động mới được tạo ra. Trong mức độ phân tử, giai đoạn trơ tuyệt đối này tương đương với khoảng thời gian cần thiết cho sự trở lại trạng thái cũ của những kênh ion xuyên màng.[187] Dẫu cho điều này sẽ giới hạn lại tần số phóng (frequency of firing),[188] chính giai đoạn trơ tuyệt đối bảo đảm cho điện thế hoạt động chỉ di chuyển một chiều theo sợi trục.[122]:53 Trong trường hợp kích thích tại đoạn giữa sợi trục, dòng ion dương đi vào bên trong màng có thể "tịnh tiến" theo hai hướng.[189] Tuy nhiên, chỉ phần màng không bị kích thích mới có thể đáp ứng bằng cách phóng điện thế hoạt động; và cũng không thể tái kích thích đối với phần màng vừa mới tạo xung điện cho đến khi "giới hạn trơ" không còn. Điện thế hoạt động lan truyền từ tiểu đồi sợi trục cho đến tận các cúc tận cùng, đây được gọi là lối dẫn truyền thuận chiều (orthodromic conduction). Sự dẫn truyền theo hướng ngược lại—được gọi là dẫn truyền ngược chiều—là rất hiếm.[190] Mặc dù rằng là, nếu như thí nghiệm làm kích thích tại phần giữa sợi trục, và toàn bộ sợi trục còn "tươi", tức là chưa bị kích thích; thì kết quả là sẽ có hai điện thế hoạt động được tạo ra, lần lượt di chuyển đến tiểu đồi sợi trục và các cúc tận cùng.
Bao myelin và dẫn truyền bước nhảy[sửa | sửa mã nguồn]

Có những tế bào thần kinh mà sợi trục của nó được bao bọc bởi myelin, với thành phần lipid là vật chất cách điện có chức năng tăng cường vận tốc điện thế hoạt động và khai thác năng lượng một cách hiệu quả.[191] Những sợi trục được myelin hóa bởi các tế bào thần kinh đệm (nơ-rô-gli), như tế bào Schwann và các tế bào ít nhánh (oligodendrocytes).[192] Khoảng trống giữa các bao myelin được gọi là eo Ranvier.
Bao myelin có tác dụng ngăn chặn sự chuyển động vào và ra của những ion khỏi sợi trục. Quá trình myelin hóa được tìm thấy chủ yếu ở động vật có xương sống, nhưng có ngoại lệ đối với một số loài không có xương sống, chẳng hạn như loài tôm.[193] Tuy nhiên, sự myelin hóa không phải diễn ra ở tất cả các nơron. Và cho dù phương thức dẫn truyền là bước nhảy hay thông thường, nhìn chung vận tốc trung bình của điện thế hoạt động nằm trong khoảng từ 1 m/s cho đến hơn 100 m/s, và tỷ lệ thuận với đường kính của sợi trục.[194]
Điện thế hoạt động không thể truyền theo những phần đã myelin hóa của sợi trục, vì rằng tại đó không có ion nào có thể di chuyển qua màng được. Thay vào đó, điện thế hoạt động thực hiện những "bước nhảy" (saltatory conduction) từ eo Ranvier này sang eo Ranvier khác, về khía cạnh tổ chức các phân tử trong những eo này, đặc biệt mật độ các kênh Na+ nhạy cảm với điện thế (voltage-gated Na+ channels) rất đậm đặc (tạo điều kiện thuận lợi cho sự dẫn truyền "nhảy cóc"). Cơ chế dẫn truyền bước nhảy đã được giả thuyết bởi Ralph Lillie vào năm 1925,[195] tuy nhưng nhiều năm sau đó các bằng chứng thực nghiệm mới được đưa ra bởi Ichiji Tasaki[196] và Taiji Takeuchi,[197] Alan Hodgkin và Robert Stämpfli.[198] Ngược lại, ở những sợi trục không có bao myelin, điện thế hoạt động sẽ được kích hoạt tại vị trí màng bất kỳ và truyền liên tục theo sợi trục giống như sóng cơ học.
Sự hiện diện của cấu trúc vỏ myelin đã tạo ra hai thuận lợi quan trọng: đó là sự tăng vọt về tốc độ và hiệu quả năng lượng. Đối với sợi trục myelin hóa có đường kính lớn hơn 1 micrômét (đường kính sợi trục tối thiểu), sự tăng cường về vận tốc điện thế hoạt động sẽ gấp 10 lần.[199] Ngược lại, các sợi có bao myelin nhỏ hơn các sợi không myelin khi chúng đều truyền tải tín hiệu điện với cùng một vận tốc như nhau. Chẳng hạn như là, điện thế hoạt động di chuyển với vận tốc là 25 m/s ở cả sợi trục ếch (có myelin) và sợi trục mực ống khổng lồ (không có myelin), nhưng sợi trục ếch có đường kính nhỏ hơn gấp 30 lần và diện tích mặt cắt ngang (cross-sectional area) nhỏ hơn gấp 100 lần. Hơn nữa, vì dòng chảy của các hạt mang điện chỉ giới hạn ở vùng eo Ranvier, hiện tượng "rò rỉ" ion xuyên màng rất ít xảy ra, điều này giúp giảm thiểu sự thất thoát của năng lượng chuyển hóa. Sự tiết kiệm này có ý nghĩa quan trọng về mặt chọn lọc tự nhiên, do hệ thần kinh người sử dụng xấp xỉ khoảng 20% năng lượng chuyển hóa của cơ thể.[199]

Chiều dài của những đoạn myelin hóa trong sợi trục đóng vai trò quan trọng, quyết định nên sự hiện hành của thuộc tính nhảy cóc đối với tế bào thần kinh. Để tối ưu hóa vận tốc của điện thế hoạt động, độ dài của các đoạn myelin nên đạt giá trị tối đa để tín hiệu điện truyền đi qua các eo Ranvier không bị suy giảm. Về bản chất, những phần myelin hóa nhìn chung được mở rộng ra tọa thành ít nhất hai eo (hay "nốt") đủ để dẫn truyền tín hiệu điện một cách thụ động, và biên độ được duy trì đủ để gây ra một điện thế hoạt động khác tại eo thứ hai hay thứ ba. Vì vậy, hệ số an toàn (safety factor) của cơ cấu dẫn truyền bước nhảy vẫn cao, cho phép sự lan truyền diễn ra bình thường qua những cầu nối như vậy trong trường hợp chấn thương thần kinh. Tuy nhiên, điện thế hoạt động có thể kết thúc sớm tại những vị trí có hệ số an toàn thấp, hay thậm chí ở những nơron không có bao myelin; ví dụ như tại điểm phân nhánh của sợi trục, nơi mà sợi trục phân chia làm hai.[202]
Một số bệnh làm thoái hóa bao myelin và đánh mất khả năng dẫn truyền bước nhảy, như thế vận tốc của điện thế hoạt động sẽ bị giảm xuống.[203] Điển hình nhất là căn bệnh đa xơ cứng (hay còn gọi là xơ cứng rải rác, multiple sclerosis), trong đó lớp vỏ myelin bị phá hủy và kéo theo sự tổn hại về chức năng vận động phối hợp.[204][205][206][207][208][209]
Lý thuyết điện thần kinh[sửa | sửa mã nguồn]

Bằng việc đưa ra lý thuyết điện thần kinh (cable theory, hay còn gọi là lý thuyết dây "cáp" điện sinh vật),[210] người ta đã có thể định lượng được dòng điện sống được tạo ra trong cấu trúc sợi trục và cả sự vận động (dynamics) của nó. Ngoài ra, các mô hình phức tạp hơn cũng ra đời, chẳng hạn như là mô hình từng phần (compartmental model).[211] Lý thuyết cáp điện đã được phát triển từ năm 1855 bởi Lord Kelvin qua việc mô hình tuyến cáp điện tín xuyên Đại Tây Dương, vào năm 1946 Hodgkin và Rushton đã nghiên cứu ra được những điểm tương đồng của dây cáp với tế bào thần kinh.[a] Trong lý thuyết điện thần kinh cơ bản, cấu trúc thần kinh được cho là có khả năng dẫn truyền điện năng một cách thụ động (tức là các Electrotonic potentials, hay còn gọi là điện thế khởi sinh, trong đó "thụ động" mang ý nghĩa sự thay đổi về điện thế không gây ra các biến đổi trên tính thấm màng), các sợi nhánh đã được cấu trúc hóa lại với hình dạng là dây cáp dẫn điện hình trụ tuyệt đối, tất cả đã được mô tả qua phương trình vi phân từng phần:[210]
Trong đó V(x, t) là điện thế xuyên màng tại thời gian t và vị trí x dọc theo chiều dài tế bào thần kinh, và trong đó đại lượng λ và τ đặc trưng cho sự phân rã của điện thế khởi sinh theo không gian và thời gian (λ và τ cũng được coi là các hằng số sinh học phụ thuộc đặc tính của nơron). Theo như sơ đồ mạch điện, những đại lượng này có thể được xác định từ điện trở (resistances) và điện dung (capacitances) trên mỗi độ dài đơn vị.[212]

Thước đo không gian và thời gian này được dùng để hiểu sự phụ thuộc của tốc độ xung thần kinh vào đường kính của nơron trên những sợi không myelin hóa. Chẳng hạn, chu kỳ τ sẽ tăng lên cùng với điện trở màng rm và điện dung màng cm. Khi điện dung tăng, để tạo ra được một dòng điện xuyên màng cần phải có nhiều hạt điện tích vận chuyển qua màng (theo như phương trình q=CV); khi điện trở tăng, có ít điện tích được vận chuyển trong mỗi đơn vị thời gian, làm cho quá trình cân bằng diễn ra chậm hơn. Tương tự, nếu như giá trị trở nội tại ri (internal resistance) của sợi trục trên mỗi độ dài đơn vị được cho là giảm so với sợi trục khác (đồng nghĩa với việc bán kính của sợi trục đó lớn hơn), lúc này hằng số λ tăng lên; tức là tương đương với khả năng mà xung điện thế đi được sẽ càng xa tính từ điểm phát sinh và như thế vận tốc của xung động cũng tăng. Nếu như điện trở màng rm tăng, thì xác suất "rò rỉ" dòng hạt mang điện qua màng sẽ thấp đi, như vậy khiến cho λ sẽ càng lớn, tăng cường tốc độ xung thần kinh. Một cách ẩn dụ, dòng điện được phóng vào mỏm thần kinh tức sợi nhánh được ví như ném hòn đá tảng vào hồ nước, làn sóng nước càng ra xa sẽ càng nhỏ dần.
Hằng số không gian λ đóng vai trò quan trọng giúp đo lường được giới hạn phân rã của xung điện động trong một phạm vi nhất định. Giả sử rằng một xung điện thế EPSP trong trạng thái ổn định đi được một khoảng cách λ trong hệ thống thần kinh thì tương ứng nó sẽ có sự suy giảm về biên độ khoảng 1/e hay 37% giá trị ban đầu, chỉ trong trường hợp dây thần kinh hình trụ dài vô tận (infinite) hay bán vô tận (semi-infinite). Không gian mà EPSP đi được và những điều kiện giới hạn, cũng như là sự hiện diện của các cấu tạo nhánh rất phức tạp, kích thước hạn hẹp của dây thần kinh, là những vấn đề quan trọng để tính ra được các tham số chính xác của hiện tượng tắt dần dao động điện trong trạng thái ổn định.
Hằng số thời gian τ được định nghĩa là giá trị quy ước cho sự suy giảm về biên độ điện thế theo thời gian, τ là khoảng thời gian ước tính sự phân rã của xung điện động, trải qua τ giá trị điện thế suy giảm 1/e tức là 37% giá trị ban đầu và chỉ xét trong trường hợp đẳng điện và các tế bào đều phân cực đồng đều.
Điện thế hoạt động hoàn thành[sửa | sửa mã nguồn]
Synap hóa học[sửa | sửa mã nguồn]

Điện thế hoạt động khi lan truyền đến các cúc tận cùng sẽ gây ra sự giải phóng các chất dẫn truyền thần kinh vào khe synap.[b] Những phân tử dẫn truyền thần kinh với kích thước nhỏ làm mở ra các kênh ion tại màng tế bào sau synap; hầu hết các cúc tận cùng của một nơron chỉ phóng thích cùng một loại hóa chất dẫn truyền đặc thù. Khi điện thế hoạt động đến màng tế bào trước synap, tại đó có các kênh calci nhạy cảm với điện thế (voltage-sensitive calcium channels) sẽ được kích hoạt; dòng chảy của ion calci đi vào bên trong tế bào khiến cho những bọc synap chứa chất dẫn truyền thần kinh di chuyển hướng về màng tế bào, kết quả là cơ chế xuất bào diễn ra với sự hòa nhập của bọc synap với màng sinh chất, đưa một loạt các lượng tử vào khe synap.[c] Quá trình phức tạp này chịu tác động ức chế của các độc tố thần kinh (neurotoxins) tetanospasmin (độc chất uốn ván) và botulinum.[d]
Synap điện[sửa | sửa mã nguồn]
Một số synap không cần đến "phân tử môi giới" truyền đạt tín hiệu thần kinh, thay vào đó tế bào trước và sau synap kết nối với nhau qua những cầu nối bào tương.[e] Khi điện thế hoạt động đi đến được synap, dòng ion đi vào trong tế bào trước synap có thể vượt màng ngăn của hai tế bào và di chuyển vào tế bào sau synap thông qua các lỗ thông tạo bởi 6 phân tử connexin.[f] Chính vì thế, điện thế hoạt động có thể trực tiếp kích thích tế bào sau synap. Synap điện cho phép truyền tin nhanh hơn bởi vì nó không cần sự khuếch tán chậm của các hóa chất thần kinh vào trong khe synap. Nhờ những đặc tính của synap điện, cụ thể trong trường hợp đáp ứng nhanh và khi sự phối hợp về thời gian là quan trọng, chẳng hạn như là phản xạ thoát, cơ quan võng mạc của loài động vật có đốt sống, và tim.
Khớp nối thần kinh cơ[sửa | sửa mã nguồn]
Khớp nối thần kinh cơ là dạng đặc biệt của synap hóa học, trong đó sợi trục của các nơron vận động cho ra các nhánh tận cùng tại sợi cơ.[g] Trong trường hợp như vậy, chất dẫn truyền thần kinh ở đây chính là phân tử acetylcholine, một khi được giải phóng sẽ gắn vào thụ thể acetylcholine là các protein xuyên màng sinh chất (sarcolemma) của tế bào cơ. [h] Tuy nhiên, các phân tử acetylcholine sẽ không liên kết lâu, chúng sẽ sớm bị tách ra và nhanh chóng bị thủy phân bởi tập hợp những enzyme acetylcholinesterase có tại synap. Enzyme này làm giảm kích thích quá mức đến sợi cơ, khiến cho mức độ và thời gian co cơ được điều hòa một cách chính xác. Có một số loại chất độc gây bất hoạt enzyme acetylcholinesterase nhằm mục đích chặn lại cơ chế kiểm soát này, chẳng hạn là các chất độc thần kinh sarin và tabun,[i] và thuốc trừ sâu như diazinon và malathion.[j]
Sự phát triển của điện thế hoạt động theo từng thời kỳ[sửa | sửa mã nguồn]
Khả năng của nơron trong việc tạo ra và lan truyền các điện thế hoạt động được cho là thay đổi theo sự phát triển của hệ thống thần kinh cả trung ương lẫn ngoại vi. Khuynh hướng biến đổi điện thế màng nhiều hay ít là phụ thuộc vào tính trở kháng đầu vào của màng tế bào. Khi một tế bào sinh trưởng, có nhiều kênh được tổng hợp ngay trên màng, điều này khiến cho tính trở kháng đầu vào giảm xuống. Một nơron đã trưởng thành cũng phải trải qua những thay đổi ngắn về điện thế màng khi dòng điện được phóng tại các khớp synap. Các nơron vùng nhân gối ngoài (lateral geniculate nucleus) của loài chồn sương có giá trị hằng số thời gian dài và giá trị điện thế biến thiên giảm tại giai đoạn mới sinh ra (P0) hơn là tại thời điểm 30 ngày tuổi (P30).[213] Hệ quả của sự suy giảm về thời gian điện thế hoạt động đó là các tín hiệu được bảo toàn và vẫn giữ độ chính xác khi đáp ứng với kích thích tần số cao. Những nơron chưa trưởng thành dễ xảy ra hiện tượng ức chế synap hơn là điện thế hóa khi kích thích tần số cao hiện diện.[213]
Trong thời kỳ phát triển sớm của nhiều sinh vật khác nhau, chu kỳ điện thế hoạt động thực tế được khởi động bởi dòng chảy calci hơn là dòng natri. Quá trình động lực học của sự mở và đóng những kênh calci trong giai đoạn phát triển là chậm hơn so với các kênh natri nhạy cảm với điện thế (chuyển tải các điện thế hoạt động trong các nơron trưởng thành). Thời gian mở cổng kênh calci dài có thể dẫn đến các chu kỳ của điện thế hoạt động diễn ra rất chậm so với những nơron trưởng thành.[213] Các tế bào thần kinh thuộc loài ếch Xenopus đã tạo ra được các điện thế hoạt động sơ khai với khoảng thời gian từ 60–90 ms. Trong sự tăng trưởng của sinh vật này, thời gian này giảm 1 ms. Sự suy giảm mạnh này có hai lý do. Thứ nhất, hiện tượng tăng khử cực chịu trách nhiệm chủ yếu bởi các kênh ion natri.[214] Và thứ hai, các kênh kali bắt đầu hoạt động mạnh mẽ và sản sinh ra dòng chảy ion kali ra bên ngoài tế bào gấp 3.5 lần, các kênh này được gọi là bộ máy phân tử chỉnh lưu và cản trở dòng điện (delayed rectifier), và được hoạt hóa trong giai đoạn màng bị khử cực. Sự hoàn thiện của các kênh kali nhạy cảm với điện thế giúp vận chuyển lượng lớn ion K+ ra ngoài màng, thiết lập màng tế bào vào trạng thái nghỉ, và giới hạn dòng ion calci đi vào bên trong tế bào trong điện thế hoạt động.[213]
Để chuyển đổi dạng điện thế hoạt động phụ thuộc Ca2+ sang dạng điện thế hoạt động phụ thuộc Na+, các kênh ion mới cần phải được sinh tổng hợp và gắn vào màng tế bào. Nếu như tế bào thần kinh của những loài Xenopus được nuôi dưỡng trong môi trường có dùng chất ức chế quá trình tổng hợp RNA (hay protein), thì sự chuyển đổi này sẽ bị chặn lại.[215] Thậm chí rằng hoạt động điện của tự thân tế bào có thể đóng vai trò trong việc biểu hiện gen mã hóa kênh protein. Giả sử điện thế hoạt động trong tế bào cơ của loài Xenopus không diễn ra, tương ứng mật độ dòng chảy của ion Na+ và K+ cũng sẽ dừng lại.[216]
Sự phát triển của đặc tính điện thế cũng được thấy ở rất nhiều loài. Cụ thể, người ta nhận thấy rằng là dòng chảy ion Na+ và K+ của loài Xenopus tăng đột ngột sau khi tế bào nơron trải qua giai đoạn cuối cùng của chu kỳ nguyên phân (telophase). Mật độ các kênh Na+ phân bố tại cấu trúc vỏ não chuột tăng gấp 6–10 lần trong vòng hai tuần đầu tiên sau sinh.[213]
Sự lan truyền ngược của điện thế hoạt động[sửa | sửa mã nguồn]

Hiện tượng điện thế hoạt động truyền ngược lại (backpropagating AP) đến sợi nhánh đã được giới khoa học quan sát và nghiên cứu dày công. Trên sợi trục, sự hiện diện của các kênh cổng điện thế Na+ và K+ đã tạo ra hàng loạt các chu kỳ điện thế hoạt động, nhưng tại màng sợi nhánh, ngưỡng kích thích tại nơi đó cao khiến cho tín hiệu điện trước synap không thể gây ra điện thế hoạt động. Thay vào đó, khi thân thần kinh đã khử cực đến một mức độ vừa đủ bằng việc tích hợp các điện thế khởi sinh, mới có thể kích hoạt điện thế hoạt động và lan truyền một chiều dọc theo sợi trục. Tuy nhiên các dữ kiện thực nghiệm đã cho thấy rằng, thân thần kinh cũng có thể khử cực và làm cho khu vực sợi nhánh cũng khử cực theo vì ở đó có các kênh cổng điện thế Na+. Sự lan ngược này có thể ví như làn sóng vang dội lại từ các điện thế hoạt động khởi phát ngay tiểu đồi sợi trục (hay đoạn đầu sợi trục, axon initial segments). Điện thế hoạt động lan theo sợi trục đồng thời tạo ra tín hiệu ngược chiều, đến sợi nhánh hoạt hóa những kênh cổng điện thế Ca2+ dẫn đến sự hình thành của điện thế hoạt động đặc biệt tại đó.
Cần phải lưu ý rằng độ mạnh của điện thế hoạt động ngược thay đổi rất nhiều giữa nhiều loại tế bào nơron khác nhau. Một số loại tế bào nơron không làm thay đổi (hoặc rất ít) biên độ của điện thế hoạt động ngược lan đến cấu trúc cây sợi nhánh, trong khi những tế bào khác, chẳng hạn như tế bào Purkinje trong tiểu não, cản trở điện thế hoạt động rất nhiều và như thế hiện tượng này rất ít diễn ra. Hơn nữa, sự phong phú của các loại tế bào đã thể hiện ra mức độ phân rã biên độ khác nhau trong quá trình lan truyền ngược. Người ta cho rằng là mỗi một loại tế bào nơron chứa số lượng các kênh cổng điện thế riêng biệt cần thiết cho việc dẫn truyền điện thế hoạt động trong sợi nhánh. Tuy nhưng, nhiều kênh K+ loại A tập trung tương đối cao tại mỏm thần kinh đã hạn chế khả năng lan truyền ngược của điện thế hoạt động ngăn chặn vòng điều hòa dương tính diễn ra, không tạo ra được các chu kỳ bất tận và như vậy bảo vệ tế bào khỏi những tổn hại.

Sự lan ngược trở lại của điện thế hoạt động có thể làm giảm ngưỡng kích thích tại sợi nhánh, và ảnh hưởng đến khả năng phóng ra điện thế hoạt động của nơron. Các tín hiệu điện hưng phấn đến từ synap vào nhánh cụm (apical tuft) cộng với các tín hiệu đầu vào của nhánh nền (tức những điện thế hoạt động ngược) sẽ tạo ra hàng loạt các điện thế hoạt động ngắn hạn. Loạt xung điện thế hoạt động (bursting) truyền dọc theo sợi trục chính đến các nơron mục tiêu, tại tận cùng sợi trục người ta đã nhận thấy rằng cơ chế thuận hóa ngắn hạn (short-term facilitation) diễn ra chứng tỏ rằng xung động phối hợp là hiệu quả hơn nhiều so với xung đơn. Những bộ phận nơron tháp (pyramidal neuron) kết nối qua synap với rất nhiều loại tế bào sau synap khác nhau, do đó bằng việc tạo ra loạt khối điện thế hoạt động trong phạm vi thân thần kinh đến sợi nhánh, trong thời gian ngắn khiến cho các kết nối điện giữa nơron tháp với những tế bào đích khác nhau càng thêm hiệu quả.
Điện thế hoạt động ngược cũng có thể mang toàn bộ tín hiệu đầu ra đưa đến vị trí synap kích thích (là nơi nhận tín hiệu đầu vào) và gây ra các đáp ứng cục bộ dài hạn tại đó làm tăng hiệu lực của synap. Những thay đổi như thế được kích hoạt phụ thuộc vào tương quan thời gian giữa điện thế hoạt động trước synap và điện thế hoạt động sau synap, khoảng thời gian vàng là 100 ms xét một cách tương đối. Dựa trên thứ tự xuất hiện chính xác của điện thế hoạt động tại nơron trước synap và điện thế hoạt động ngược của nơron sau synap trong cấu trúc nhánh, hiệu lực synap có thể tăng hoặc giảm sau thời gian vàng đó. Những thay đổi về hiệu lực của synap gây ra bởi những chu kỳ lặp lại gần như trùng hợp của điện thế hoạt động trước synap và điện thế hoạt động sau synap, thể hiện thông qua thuật ngữ tính mềm dẻo phụ thuộc thời gian điện thế hoạt động (STDP). Các thay đổi dài hạn trong tính hiệu lực của synap thường phụ thuộc vào sự tăng cường dòng chảy Ca2+ vào nội bào qua các "chốt" NMDA, ngụ ý rằng sự lan truyền ngược của điện thế hoạt động là một trong những cơ chế kiểm soát khả năng mềm dẻo của synap qua nhiều dòng thác chuyển hóa được vận hành bởi biến đổi tăng về nồng độ Ca2+ bên trong tế bào.
Cơ chế STDP làm tăng hiệu lực synap liên quan đến quá trình lưu thông ion calci vào nội bào qua thụ thể NMDA, người ta quan sát thấy rằng cơ chế này diễn ra khi, có sự xuất hiện đồng thời các EPSP và điện thế hoạt động ngược làm tăng vọt nồng độ ion Ca2+ giới hạn tại vùng đuôi gai dưới dạng hàm trên tuyến tính (supralinear function), điều này đã được chứng minh qua thực nghiệm trên các nơron tháp khu vực CA1 vùng hải mã, nơron tháp vùng vỏ L5, nơron hình sao (stellate neuron) vùng vỏ L4, và nơron trung gian hai cụm (bitufted interneuron) vùng vỏ L2/3. Đối với cấu trúc đuôi gai của nơron hình sao L4, thời gian diễn ra quá trình tổng hợp các tín hiệu calci, gây ra bởi các tác động đồng thời của EPSP và điện thế hoạt động ngược bằng với thời gian khử hoạt các kênh NMDA.
Hiện tượng lan truyền ngược điện thế hoạt động có thể diễn ra trên tất cả các tế bào thần kinh? Thực tế rằng điện thế hoạt động ngược suy giảm về biên độ với mức độ khác nhau trên nhiều loại nơron đặc thù, chẳng hạn như tế bào tháp, tế bào sao, tế bào hai cụm, hiện tượng này đã thúc đẩy cơ chế STDP, và không có gì đáng ngạc nhiên là khả năng ảnh hưởng đến STDP cũng thay đổi trên cùng một loại nơron, phụ thuộc trên vị trí và sự phân bổ chính xác của các synap vào sợi nhánh. Điều này đúng đặc biệt với các tế bào tháp mang nhánh nền và nhánh đỉnh có hình học không gian rất phức tạp. Hơn nữa, xác suất hiện tượng xảy ra tăng lên cùng với tần số của điện thế hoạt động, và phụ thuộc rất lớn vào tín hiệu kích thích đầu vào dưới ngưỡng.

Các chất dẫn truyền thần kinh kinh điển và peptide thần kinh có thể được giải phóng từ cấu trúc sợi nhánh từ nhiều quần thể nơron khác nhau. Chức năng chính nhằm lan truyền tín hiệu ngược trở lại điều chỉnh sự lan truyền các hóa chất qua synap, hoạt động điện tế bào, và trong một số trường hợp làm thay đổi hình thái gốc của tế bào. Điện thế hoạt động ngược cũng thể hiện những vai trò như vậy, cụ thể hơn nó làm sợi nhánh phóng ra chất truyền đạt điều chỉnh lại sự phân biệt về mùi một cách chính xác. Và tương tự, xung thần kinh ngược chiều trong một số nơron trung gian vùng vỏ não mới gây ra sự giải phóng GABA từ sợi nhánh đến các cúc tận cùng của tế bào tháp, và ngược lại trong tế bào tháp sự hiện diện các xung ngược có thể kiểm soát sự phóng thích glutamate và cannabinoid từ sợi nhánh. Hai vòng feedback cục bộ có thể điều phối điện thế hoạt động trong cả hai nơron trung gian và nơron tháp để duy trì hoạt động thần kinh ổn định trong mạch cục bộ ở vỏ não.
Điện thế hoạt động ngược về cơ bản cần thiết cho quá trình ổn định hóa sự hình thành synap sơ khai trong mạch thần kinh đối với não bộ thời kỳ sau sinh, và cả sự phát triển phụ thuộc kinh nghiệm của hệ thần kinh trung ương. Các synap kích thích được tạo chủ yếu trên sợi nhánh, như vậy tín hiệu nối kết giữa sự tăng sinh cấu trúc sợi trục của nơron chiếu đến sợi nhánh của nơron nhận có khả năng liên quan đến tín hiệu điện của các sợi nhánh qua quá trình động học phụ thuộc Ca2+.

Trong giai đoạn đầu đời, các tế bào nơron thường biểu hiện ra những đợt tự phát của điện thế hoạt động cấp độ cao hơn so với người trưởng thành. Những nhà khoa học giả thuyết rằng dạng điện thế hoạt động ngược không chỉ đồng bộ hóa mạng lưới thần kinh đang phát triển qua các khớp synap nhánh-nhánh, mà còn có thể khiến sợi nhánh phóng ra các yếu tố tăng trưởng "hấp dẫn" quá trình tăng sinh sợi trục về phía nó, hay là như tín hiệu kích thích sự phân nhánh bên của sợi trục. Điện thế hoạt động ngược như cung cấp cho sợi nhánh "bản mã thần kinh sao lưu có điều chỉnh" bắt nguồn từ sợi trục và có thể ổn định hóa các kết nối synap ban đầu giữa những tổ hợp nơron trong đó phát động điện cho nhau. Đối với giai đoạn sau sinh, mật độ phân bố của các thụ thể NMDA (trong hệ thần kinh trung ương) điều phối dòng chảy ion tại khe synap nhiều hơn so với người trưởng thành, và vị trí synap kích thích mới hình thành chỉ chứa các thụ thể NMDA, có lẽ rằng là những synap mới này có tính chất điện rất yếu hay thậm chí là không có. Dòng chảy ion calci lưu lượng cao tập trung vào các sợi nhánh qua thụ thể NMDA gắn trên màng sau synap thậm chí vẫn có thể diễn ra trong trường hợp Mg2+ chặn thụ thể NMDA, vì điện thế hoạt động ngược đã kéo Mg2+ ra khỏi vị trí đặc hiệu trong khoảng thời gian ngắn. Về chức năng của điện thế hoạt động ngược trong việc tăng cường độ mạnh cho các mạch thần kinh chuyên biệt qua phối hợp đồng thời các điện thế hoạt động trước và sau synap trong tập hợp nơron thời kỳ phát triển sớm sau sinh hiện vẫn còn đang được nghiên cứu sâu hơn.
Bùng nổ điện thế hoạt động[sửa | sửa mã nguồn]

Sự kiện truyền hàng loạt nhiều điện thế hoạt động, hay các khối điện thế hoạt động (bursting) là sự kiện của nơron phóng ra các cụm (khối) điện thế hoạt động đặc trưng bời sự lặp đi lặp lại. Mỗi một khối xung động như thế tiếp theo sau bằng giai đoạn không hoạt động (quiescence) trước khi khối xung động khác diễn ra. Bùng nổ hai điện thế hoạt động được gọi là nhị xung (doublet), ba điện thế hoạt động gọi là tam xung (triplet), tứ xung (quadruplet), và vân vân. Dạng khối của điện thế hoạt động (phasic activity) được cho là quan trọng đối với sự vận hành của mạch phát sinh điều hòa vận động trung ương, sự liên lạc qua các mật mã thần kinh (neural code), và liên quan đến một số bệnh lý thần kinh chẳng hạn như động kinh, cho đến các chức năng cảm giác, và hành vi có nhận thức. Hầu hết tất cả các nơron đều có thể hình thành vô số khối điện thế hoạt động dưới tác nhân kích thích hay bằng tác động dược lý. Nhiều cụm điện thế hoạt động diễn ra một cách tự động, là do sự tương tác lẫn nhau của dòng chảy ion nhanh chịu trách nhiệm cho hoạt động xung thần kinh, và dòng chảy chậm điều hòa lại trạng thái động học.
Đối với vùng vỏ não mới, có các nơron như sau:
- Các nơron khối nội tại (intrinsically bursting neurons, IB) phần lớn là những nơron tháp phân bố chủ yếu vùng vỏ não L5; khi gặp kích thích điện mạnh, ban đầu chúng phóng ra khối điện thế hoạt động, về sau dần suy giảm trở thành các điện thế hoạt động đơn (tonic activity).
- Các nơron khối chấn động (chattering neurons, CH) hay còn gọi là các tế bào khối nhịp nhanh (FRB) là những nơron tháp thuộc lớp 2-4, và chủ yếu ở lớp thứ 3. Chúng phóng ra các khối điện thế hoạt động với tần số cao khoảng 3-5 xung với khoảng thời gian giữa các xung (interburst period) tương đối ngắn.
Tại hồi hải mã, có các nơron như sau:
- Những nơron khối ngưỡng thấp (low-threshold bursters, LTB) là những nơron tháp vùng CA1, chúng phát ra khối điện thế hoạt động tần số cao đáp ứng với kích thích ngang ngưỡng. Trong nhóm này tồn tại một số nơron phát khối xung tự động.
- Những nơron khối ngưỡng cao (high-threshold bursters, HTB) tương tự nhưng chúng chỉ phóng hàng loạt điện thế hoạt động khi gặp kích thích trên ngưỡng.

Trong cấu trúc đồi thị, có các nơron như sau:
- Các mạch nơron đồi vỏ (thalamocortical neurons, TC) có thể tạo thành những khối xung động thần kinh, biên độ sẽ càng cao khi màng trong trạng thái siêu phân cực mạnh (ức chế), và vì thế cũng được gọi là khối xung động ngưỡng thấp (low-threshold spike). Khi xung EPSP hiện diện rất ít, khiến cho màng đi vào trạng thái cực hóa, trong đó có các kênh Ca2+ loại T trở nên khử bất hoạt (de-inactivation), điện thế hoạt động đơn (tonic mode) chuyển sang điện thế hoạt động khối (burst mode). Dạng điện thế hoạt động khối của mạng lưới nơron đồi vỏ chủ yếu diễn ra trong giai đoạn giấc ngủ sóng chậm.
- Nhóm nơron ức chế vùng nhân lưới đồi thị (reticular thalamic nucleus, RTN) cũng mang khả năng giống với các tế bào nơron đồi vỏ.

Đối với tiểu não chứa các tế bào Purkinje thường có dạng điện thế hoạt động đơn. Tuy nhiên khi tín hiệu synap đầu vào bị chặn, hoạt động của nơron chuyển sang dạng "ba phương thức" trong đó có giai đoạn phóng ra khối điện thế hoạt động. Ngoài ra, phức hợp tiền-Bötzinger là cụm nơron trung gian thuộc trung khu hô hấp trước của cấu trúc hành não. Các nơron này phóng ra các khối điện thế hoạt động theo chu kỳ kiểm soát chức năng hô hấp ở các loài động vật có vú. Một số nơron vùng trung não V phóng ra khối điện thế hoạt động nhịp nhàng, khi khử cực trên ngưỡng thấp. Tế bào nơron khối trước (anterior bursting neuron, AB) trong hạch miệng-dạ dày bắn các khối xung tự động có nhịp điệu. Nơron R15 tại khu vực hạch bụng của loài động vật chân bụng Aplysia Californica, cũng phát ra khối điện thế hoạt động nhịp nhàng một cách tự động. Và các tế bào β đảo tụy hình thành khối xung thần kinh thực hiện việc kiểm soát sự giải phóng của phân tử insulin.
Những cụm điện thế hoạt động được xem như là các đơn vị thông tin thần kinh, và chức năng của nó có ý nghĩa rất nhiều về mặt sinh học bao gồm có:
- Các khối điện thế hoạt động gây ra các đáp ứng trên màng sau synap mạnh hơn (và đáng tin cậy hơn) xung động đơn. Thực tế, điện thế kích thích sau synap (EPSP) với biên độ trên ngưỡng cao là kết quả của các cụm xung này.
- Các khối điện thế hoạt động vượt qua được quá trình dẫn truyền synap thất bại. Thực vậy, đơn xung trước synap có thể không gây ra được các đáp ứng màng sau synap (sự giải phóng các hóa chất dẫn truyền không diễn ra), tuy nhưng "sự bắn phá" của các khối xung thần kinh làm tăng khả năng phóng thích các hóa chất dẫn truyền.
- Các khối điện thế hoạt động thuận hóa sự dẫn truyền thần kinh trong khi đơn xung không thể. Synap với cơ chế thuận hóa ngắn hạn mạnh sẽ kém nhạy với các đơn xung hay thậm chí là những khối xung ngắn, nhưng đối với các khối xung dài thì lại không. Trong khối điện thế hoạt động dài mang tập hợp nhiều xung giúp thuận hóa synap như vậy tác động của vài xung cuối cùng có thể vẫn còn khá mạnh.
- Các khối điện thế hoạt động thúc đẩy cơ chế LTP và vì thế tăng cường thuộc tính mềm dẻo của synap lên rất nhiều, khác biệt rõ rệt với các xung động đơn.
- Các khối điện thế hoạt động có tỷ số tín hiệu trên nhiễu (signal-to-noise ratio) cao hơn đơn xung. Trên thực tế, ngưỡng khối điện thế hoạt động cao hơn ngưỡng điện thế hoạt động đơn, tức là để hình thành khối điện thế hoạt động cần các tín hiệu điện đầu vào mạnh hơn.
- Các khối điện thế hoạt động có thể hỗ trợ cho sự liên lạc thông tin một cách chọn lọc, trong trường hợp tế bào sau synap có những dao động điện thế màng dưới ngưỡng. Những tế bào như thế được coi là nhạy cảm với tần số của tín hiệu. Một số khối điện thế hoạt động cộng hưởng với các dao động và kích động đáp ứng, trong khi những khối xung khác thì không, điều này phụ thuộc vào tần số gian khối điện thế hoạt động (interburst frequency).
- Các khối điện thế hoạt động có thể cộng hưởng với khả năng mềm dẻo synap ngắn hạn, biến synap thành bộ lọc thông dải (band-pass filter). Những synap đã có sự thuận hóa hay ức chế ngắn hạn nhạy cảm nhất đối với những khối điện thế hoạt động có tần số gian khối điện thế hoạt động cộng hưởng nhất định. Các khối xung động khởi động cơ chế thuận hóa với mức độ vừa đủ, trong khi hạn chế với sự ức chế synap, như vậy ảnh hưởng lên màng synap đích được tối ưu hóa.
- Các khối điện thế hoạt động mã hóa cho những tín hiệu cảm giác đầu vào khác nhau không như những xung động đơn. Chẳng hạn, các tế bào nơron trong thùy điện cảm giác đường bên (electrosensory lateral-line lobe) của loài cá điện yếu có thể kích thích mạng lưới hoạt hóa khối xung (network induced-bursts) đáp ứng với tín hiệu tương tác từ môi trường, và phóng ra các điện thế hoạt động đơn khi có tín hiệu con mồi. Trong hệ thống thị giác của đồi thị, tức địa hạt nhân gối ngoài (lateral geniculate nucleus), các tế bào nơron phóng ra khối điện thế hoạt động mã hóa các kích thích phối hợp bao hàm sự ức chế trong khoảng thời gian kéo dài, sau đó là sự hưng phấn. Những sự kiện kích thích như thế thường là thuộc cảnh tượng thiên nhiên.
- Các khối điện thế hoạt động là các mật mã thần kinh chứa nhiều thông tin hơn những xung động đơn khi phân tích thành các đơn vị sự kiện (unitary event). Thông tin nhận được có thể được mã hóa thành chu kỳ khối điện thế hoạt động, hoặc là cơ cấu thời gian chính xác của khối xung, tức là khoảng thời gian cách nhau giữa các xung. Nhìn chung, các khối điện thế hoạt động khả năng cao gây ra tác động mạnh lên trên màng tế bào sau synap hơn các xung đơn, vì lẽ đó sự kiện hình thành cụm điện thế hoạt động là sự kiện tất cả hoặc không, trong khi xung động đơn có thể bị nhiễu.
Tính mềm dẻo phụ thuộc thời gian điện thế hoạt động[sửa | sửa mã nguồn]

Tính mềm dẻo phụ thuộc thời gian điện thế hoạt động (spike-timing-dependent plasticity, STDP) là mô hình khả năng tri thức dựa trên tính bất đối xứng thời gian, trong đó khối lượng synap có sự điều chỉnh lại phụ thuộc vào trật tự thời gian của xung động đến (trước synap) và xung động đi (sau synap). Sự thay đổi về khối lượng synap sẽ xác định synap ở trong trạng thái nào, nếu khối lượng synap tăng lên (thay đổi dương tính), synap đó trong trạng thái LTP, nếu khối lượng synap giảm xuống (thay đổi âm tính), synap đó ở trạng thái LTD. Những thay đổi trên synap đã được xây dựng nên một hàm thời gian tương đối của điện thế hoạt động trước và sau synap; được gọi là hàm STDP hay "cửa sổ học tập" và thay đổi tùy theo những loại synap khác nhau. Hàm STDP thay đổi nhanh qua thời gian tương đối của các xung động thể hiện xác suất mã hóa phụ thuộc thời gian trên phạm vi miligiây.
Hiện tượng STDP trong giới sinh vật[sửa | sửa mã nguồn]
STDP thay đổi rất lớn đối với nhiều loại synap khác nhau và trong nhiều vùng não riêng biệt. Cho dù là như vậy, mô hình STDP cổ điển và tính bất đối xứng thời gian vẫn thể hiện tầm quan trọng hơn hết, được chứng kiến ở loài người và nhiều loài khác như chuột, ếch, châu chấu, chim di vằn, mèo. Đối với những loài động vật có vú, STDP cũng được khám phá trong nhiều vùng não, chẳng hạn như vùng vỏ não trước trán, vỏ não nội khứu, vỏ não cảm giác thân thể, các lớp vỏ não thị giác, cấu tạo hải mã, thể vân, nhân xám ốc tai, và thể hạnh nhân. Tuy nhiên, hoạt động cần thiết cho sự vận hành quá trình STDP thay đổi tùy theo các không gian synap khác nhau. Cụ thể hơn, cửa sổ thời gian cho quá trình LTD và LTP bằng nhau tại những synap kích thích của hồi hải mã, trong khi đó cửa sổ thời gian quá trình LTD rộng hơn nhiều so với quá trình LTP trong nhiều synap vỏ não.
Khoảng thời gian cửa sổ STDP bị đảo ngược lại so với dạng STDP cổ điển đối với một số synap nhất định, như vậy là khoảng thời gian trước- đến-sau sẽ dẫn đến cơ chế LTD, và ngược lại hình thành LTP. Trường hợp này là các synap ức chế của những nơron tháp trong vùng vỏ não mới lớp thứ 2 và lớp thứ 3, tại synap vỏ vân hay thùy điện cảm giác của loài cá mũi voi. Khoảng thời gian cần thiết cho STDP đối với các kết nối giữa những tế bào hình sao có gai trong khu vực vỏ não cảm giác thân thể của loài chuột cũng khác biệt: vì tại đó, có vẻ như synap trải qua quá trình LTD không tuân theo một trật tự thời gian nào. Trong lớp vỏ não mới thứ 5 chứa các nơron tháp, thời gian cần thiết phụ thuộc chủ yếu ở các synap trên cây sợi nhánh: trong khi tín hiệu điện vào synap đầu gần có diễn ra cơ chế STDP cổ điển, thì những synap đầu xa theo quy luật STDP "đảo ngược thời gian". Những xung động đến cũng gây ra các biến đổi LTD và LTP phụ thuộc vào trạng thái tăng khử cực của nhánh đỉnh.
Điện thế hoạt động cơ bản quan trọng cho sự hiện diện của STDP, và STDP thay đổi đáng kể không chỉ với khu vực não và loại synap, mà còn trong tế bào với những bộ phận cấu tạo nhánh khác nhau. Có một câu hỏi mở đó là tính thay đổi này cho mục đích gì. Vì khả năng mềm dẻo của synap là nền tảng cho sự phát triển của mạch thần kinh, điều này ngụ ý rằng quy luật STDP đã tham gia trong giai đoạn phát triển xác định mạch thần kinh chức năng trong não bộ trưởng thành. Nói cách khác, tính đa dạng của STDP rất có thể không phải là sự trùng hợp ngẫu nhiên.
Điện thế hoạt động đối với các loại tế bào khác[sửa | sửa mã nguồn]
Điện thế hoạt động cơ tim[sửa | sửa mã nguồn]

Điện thế hoạt động cơ tim khác với điện thế hoạt động thần kinh, đặc trưng bởi giai đoạn cao nguyên (plateau, hay bình nguyên), trong đó màng tế bào vẫn giữ biên độ điện thế cao trong khoảng thời gian vài trăm miligiây trước khi đến giai đoạn tăng tái phân cực.[k] Giai đoạn cao nguyên này là do sự hoạt động của các kênh calci chậm, các kênh mở ra và dòng ion calci đi vào trong tế bào, duy trì điện thế màng gần đến giá trị điện thế cân bằng ngay cả khi những kênh natri đã trở nên bất hoạt sau đó.
Điện thế hoạt động cơ tim đóng vai trò quan trọng trong sự phối hợp khả năng co cơ tim.[l] Các tế bào cơ tim trong nút xoang nhĩ (sinoatrial node) có chức năng tạo lập điện thế tạo nhịp mang khả năng đồng bộ hóa tim toàn phần. Điện thế hoạt động của những tế bào sinh ra như thế lan truyền tới khu vực nút nhĩ thất (nút AV), và cũng chỉ có con đường này xung động thần kinh mới có thể đi từ tâm nhĩ đến tâm thất. Điện thế hoạt động từ khu vực nút nhĩ thất lan xuống bó His và từ nơi đó tiếp tục rẽ sang các sợi Purkinje.[note 1] Ngược lại, đối với những dạng dị thường của điện thế hoạt động—nguyên do có thể là đột biến bẩm sinh hay là chấn thương—có thể dẫn đến bệnh lý, điển hình là chứng loạn nhịp tim.[m] Có vài loại thuốc chống loạn nhịp tim với cơ chế tác động lên điện thế hoạt động cơ tim, ví dụ như là quinidine, lidocaine, chẹn beta, và verapamil.[n]
Điện thế hoạt động cơ xương[sửa | sửa mã nguồn]
Điện thế hoạt động diễn ra tại tế bào cơ xương (hay cơ vân) tương tự như với dạng điện thế hoạt động xảy ra tại nơron.[217] Điện thế hoạt động là kết quả của quá trình khử cực màng tế bào (màng sợi cơ), điều này khiến cho các kênh natri nhạy cảm với điện thế mở ra; sau đó những kênh này sẽ trở nên bất hoạt và màng tái khử cực lại trở về trạng thái ban đầu khi mà dòng ion kali ra ngoài tế bào. Trước khi chuyển sang điện thế hoạt động, giá trị điện thế nghỉ của cơ xương khoảng −90mV, tức là âm hơn giá trị điện thế nghỉ của nơron. Điện thế hoạt động cơ xương có chu kỳ kéo dài khoảng từ 2–4 ms, thời gian của giai đoạn trơ tuyệt đối là 1–3 ms, và vận tốc dẫn điện dọc theo tế bào cơ là cỡ 5 m/giây. Điện thế hoạt động giải phóng ion calci, cụ thể hơn là hai ion Ca2+ sẽ gắn vào troponin C trên sợi actin, phức hợp troponin-Ca2+ khiến cho protein tropomyosin trượt qua và bộc lộ các vị trí gắn của sợi actin, lúc này hai đầu myosin tiến đến gần và kết chặt với actin, khởi động tiến trình co cơ (hay còn gọi là chu kỳ cầu nối). Điện thế hoạt động cơ xương được kích ứng bởi các điện thế hoạt động của tế bào thần kinh trước synap ngay tại khớp nối thần kinh cơ, nơi này cũng đồng thời được xem là khu vực tác động phổ biến của các chất độc thần kinh.[o]
Điện thế hoạt động đối với tế bào thực vật[sửa | sửa mã nguồn]
Nhiều loại thực vật khác nhau cũng triển khai điện thế hoạt động truyền theo mạch rây (phloem) để phối hợp các hoạt động sinh hóa có hiệu quả. Về khía cạnh sinh lý học của những dòng chuyển động hạt điện tích đã được nghiên cứu rất nhiều trên đối tượng là tảo chẳng hạn như luân tảo (charophyta). Điểm khác nhau chủ yếu giữa thực vật và động vật đó là, chu kỳ điện thế hoạt động của thực vật diễn ra dựa trên các dòng chảy calci và kali, trong khi đó ở động vật, điện thế hoạt động cần có dòng ion kali và natri. Những tín hiệu xung điện này là khả năng của thực vật nhằm tải thông tin nhanh chóng từ các tín hiệu môi trường ví dụ như là nhiệt độ, ánh sáng, tác động cơ học và các tổn thương. Trên thực vật, cấu trúc mạch rây (mạng lưới các tế bào nối kết lẫn nhau) bên trong hệ gân lá có thể được xem là 'dây thần kinh xanh' cho phép truyền đi các điện thế hoạt động gây ra bởi kích thích, và dòng điện thực vật này do các kênh ion đặc hiệu phụ thuộc điện thế đảm nhiệm.
Giới thực vật và giới nấm[p] trong đó bao gồm các sinh vật với những tế bào có thể kích thích và phát sinh ra dòng điện.[q][r][s] Năm 1906, J. C. Bose đã sáng chế ra công cụ rất tài tình, giúp đo lường được điện thế hoạt động trên loài thực vật, mà trước đó hiện tượng điện trên các loài thực vật ăn sâu bọ đã được khám phá ra bởi Burdon-Sanderson và Darwin (nhưng chưa xác thực rõ).[218] Thành công mà Bose mang lại cho giới khoa học đã nhận được sự đánh giá cao từ giới chuyên môn, theo Shepherd (2005): "... ông ấy là người đầu tiên nhận ra được sự tồn tại của các tín hiệu điện có mặt ở khắp nơi giữa những tế bào thực vật, được xem là một trong những chức năng quan trọng giúp phối hợp các đáp ứng với môi trường. Bose đã chứng minh được qua việc đưa ra các chứng cứ xác thực về việc diễn ra quá trình chuyển tải các tín hiệu điện vừa nhanh, vừa truyền đến được những nơi xa, kích thích sự chuyển động của lá trong loài Mimosa pudica (cây trinh nữ) và loài Desmodium gyrans (cây nhảy múa, hay cây điện báo), và đồng thời cho thấy rằng các tế bào thực vật sản sinh ra nhiều xung điện liên tục và lan tỏa cả hệ thống." Ngoài ra, ông cũng đưa ra kết luận rằng hiện tượng điện không chỉ giới hạn ở hai loài thực vật trên, mà còn xảy ra đối với tất cả những loài thực vật. Sự tăng cường dòng ion Ca2+ vào trong chất nguyên sinh sẽ gây ra tác động lực thúc đẩy anion vào trong tế bào. Điều này làm cho ion calci được ví như là "tiền ion" cho sự chuyển động của các ion khác, chẳng hạn như là dòng ion âm chloride vào nội bào, và dòng ion dương kali đi ra, như quan sát thấy ở phần lá của cây đại mạch.[219]
Dòng ion calci khởi đầu vào bên trong màng sẽ khiến tế bào tăng khử cực với mức độ nhỏ, sau đó các kênh cổng ion điện thế mở ra và cho phép dòng ion Cl− đi vào gây nên sự khử cực hoàn toàn và lan truyền sang khu vực lân cận.
Một số loại thực vật (chẳng hạn như loài Dionaea muscipula, được biết đến với cái tên cây bắt ruồi Venus) sử dụng các kênh cổng Na+ để điều khiển sự cử động và về bản chất là "sự tính toán". Cây bắt ruồi Venus được tìm thấy ở những miền đất ẩm cận nhiệt đới thuộc phía Bắc và phía Nam của tiểu bang Carolina.[220] Khi những thành phần dinh dưỡng trong đất không được phong phú, loài cây này dựa vào các bữa ăn khác đó là côn trùng và động vật.[221] Dù đã nghiên cứu trên thực vật, thế nhưng vẫn còn khá mơ hồ về nền tảng phân tử đối với loài cây bắt ruồi nói riêng, và tất cả các loài cây ăn sâu bọ nói chung.[222]
Tuy nhiên, nhiều nghiên cứu đã tìm ra được cơ sở của điện thế hoạt động và cho thấy dòng điện trong loài cây bắt ruồi Venus đã ảnh hưởng đến sự chuyển động nhịp nhàng và chính xác như thế nào. Đầu tiên, người ta nhận ra rằng giá trị điện thế màng trong trạng thái nghỉ của loài cây bắt ruồi Venus là khoảng -120mV, âm hơn giá trị điện thế của tế bào động vật (thường là từ -90mV đến -40mV).[222][223] Chính giá trị điện thế nghỉ của màng càng thấp khiến cho nó dễ bị kích hoạt thành điện thế hoạt động hơn. Vì thế, khi các loài côn trùng nằm trong phạm vi "bẫy" của thực vật, có các lông là các thụ thể nhận cảm cơ học vô cùng nhạy với kích thích từ môi trường, và khi con mồi đã chạm vào lông tương ứng khởi tạo điện thế hoạt động.[222] Điện thế hoạt động diễn ra trong thời gian 1.5 ms.[224] Con mồi càng cố gắng vùng vẫy và trốn thoát, nó sẽ chạm nhiều lông thụ thể hơn, và như thế các chu kỳ điện thế hoạt động được tạo ra liên tục một cách vô hạn (∞ APs). Loài sinh vật này có thể nhớ và ra quyết định, cũng như 'đếm' số lượng các điện thế hoạt động để ước tính kích thước và chất dinh dưỡng của loài côn trùng bị nó làm mồi. Cuối cùng, điện thế hoạt động sẽ làm hoạt hóa dòng ion Ca2+ và làm tích tụ nồng độ ion Ca2+, gây ra làn sóng tín hiệu thứ hai. Bộ máy ion Ca2+ được vận hành sẽ khởi động nên nhiều chu trình sinh hóa khác, có liên quan đến sự sống còn của sinh vật.
Tuy vậy, cây bắt ruồi không đóng lại khi chỉ có một lông được kích thích. Thay vào đó, cần xung động thần kinh đến từ hai hay nhiều lông.[221][222] Nếu chỉ một lông được kích thích, sự hoạt hóa được xem là giả vì không gây những thay đổi đáng kể nào. Hơn nữa, lông thứ hai phải được hoạt hóa trong khoảng thời gian nhất định (0.75 giây - 40 giây) kể từ thời điểm lông thứ nhất đã bị kích thích. Khi lông thứ nhất bị kích thích, có sự tăng lưu lượng ion calci nhưng sau đó giảm xuống chậm. Khi điện thế hoạt động thứ hai được phóng ra trong thời gian hiệu lực, nồng độ ion calci đã đạt đến ngưỡng xác định, lúc này cái bẫy của cây bắt ruồi Venus đóng lại chỉ trong 100 miligiây.
Cùng với giai đoạn sau của điện thế hoạt động, sự giải phóng các ion dương kali ra ngoài màng đã làm giảm áp suất thẩm thấu nội màng (KCl). Trong khi đó, điện thế hoạt động của loài động vật có khuynh hướng cân bằng áp suất thẩm thấu là do dòng chảy ion natri vào bên trong tế bào tương đương với dòng chảy ion kali ra ngoài tế bào thế nên triệt tiêu đi sự thay đổi về tính thẩm thấu bên trong và bên ngoài màng. Đối với tế bào thực vật, sự tương tác của các enzyme điện hóa then chốt và nồng độ ion nội bào ảnh hưởng đến trạng thái thẩm thấu ổn định,[t] điều này cũng ngụ ý rằng trong thời kỳ môi trường muối vẫn đang chịu sự biến đổi, những loài sinh vật thủy tổ đơn bào chung của thực vật và động vật mang khả năng phát sinh ra dòng điện và điều này đã tạo ra hiện tượng thẩm thấu. Hơn thế nữa, chức năng vận chuyển tín hiệu nhanh được thấy ở những tế bào thuộc nhóm động vật đa bào như một sự hoàn thiện chưa từng có trong môi trường thẩm thấu đặc biệt ổn định.[225] Rất có khả năng rằng thuộc tính điện thế hoạt động trong những loài thực vật có mạch phát triển độc lập với dạng điện thế hoạt động của những loài động vật đa bào với tế bào có tính kích thích và tạo ra điện.
Không như giai đoạn tăng khử cực, giai đoạn tăng tái phân cực và giai đoạn siêu phân cực dường như phụ thuộc chủ yếu trên những cation nhưng không phải calci. Để khởi động giai đoạn tăng tái phân cực, tế bào tích cực vận chuyển ion K+ ra bên ngoài qua màng thông qua cơ chế thụ động. Điều này được cho là khác với tế bào nơron là vì trong pha suy giảm điện thế màng không phụ thuộc hoàn toàn vào sự di chuyển của ion K+; trên thực tế, để thực hiện quá trình tăng tái phân cực toàn phần, tế bào thực vật cần năng lượng dưới dạng ATP để hỗ trợ trong việc giải phóng H+ ra ngoài tế bào – qua khai thác chức năng của bơm vận chuyển H+-ATPase.[222][226]
Phân loại điện thế hoạt động và lợi thế tiến hóa[sửa | sửa mã nguồn]
Điện thế hoạt động được thấy ở tất cả sinh vật đa bào, bao gồm có thực vật, động vật không có đốt sống như côn trùng, và các loài có đốt sống như lưỡng cư và động vật hữu nhũ. Động vật thân lỗ dường như là ngành chính của nhóm sinh vật nhân thực đa bào không truyền đi điện thế hoạt động, dù rằng có một số nghiên cứu ám chỉ là những loại sinh vật này cũng có dạng truyền tín hiệu qua các tế bào dưới dạng điện.[u] Điện thế nghỉ, cũng như là quy mô và thời gian của điện thế hoạt động, không thay đổi nhiều theo chu trình tiến hóa, tuy nhưng vận tốc của điện thế hoạt động biến đổi rất nhiều phụ thuộc vào đường kính sợi trục và cơ chế myelin hóa thần kinh.
| Động vật | Loại tế bào | Điện thế nghỉ | Giá trị tăng của ĐTHĐ (mV) | Thời gian của ĐTHĐ (ms) | Tốc độ dẫn truyền (m/s) |
|---|---|---|---|---|---|
| Loài mực ống (Loligo) | Sợi trục khổng lồ | −60 | 120 | 0.75 | 35 |
| Loài giun đất (Lumbricus) | Sợi trục lớn giữa | −70 | 100 | 1.0 | 30 |
| Loài gián (Periplaneta) | Sợi trục lớn | −70 | 80–104 | 0.4 | 10 |
| Loài ếch (Rana) | Sợi trục thần kinh tọa (hông) | −60 đến −80 | 110–130 | 1.0 | 7–30 |
| Loài mèo (Felis) | Thần kinh vận động rễ tủy | −55 đến −80 | 80–110 | 1–1.5 | 30–120 |

Trong cuộc bàn luận khoa học về vấn đề tiến hóa, điện thế hoạt động dường như là có lợi thế tiến hóa. Điện thế hoạt động đặc trưng bởi tính chất nhanh, chuyển phát rất nhiều tín hiệu trong phạm vi dài trong cơ thể sinh vật; với vận tốc dẫn có thể vượt 110 m/giây, bằng một phần ba tốc độ âm thanh. Không một mô nào có thể chiến thắng được mô thần kinh về tốc độ dẫn truyền như vậy xuyên suốt cả toàn bộ cơ thể; có thể làm phép so sánh rằng, một phân tử hormone được mang đi theo dòng máu với tốc độ 8 m/giây trong các động mạch lớn. Ngoài ra, sự dẫn truyền nhanh là giúp ích cho sự phối hợp chặt chẽ các sự kiện cơ học, chẳng hạn như là quá trình co cơ tim. Chức năng thứ hai là các biến đổi điện vi mô gắn liền với cấu tạo phát sinh, và tương ứng với bộ máy xử lý tín hiệu cải tiến qua các thế hệ, theo tiến hóa các giống loài càng hoàn thiện cơ quan thần kinh một cách phong phú, trong đó mạng lưới nơron ngày càng phức tạp hóa, đưa kết cấu không gian lên tới 11 chiều, đưa cách thức xử lý tín hiệu dưới dạng các xung động mã hóa cho các hoạt động tư duy và nhận thức, cảm xúc vượt ngoài khả năng tưởng tượng của con người, song các nhà nghiên cứu họ vẫn có thể tính toán và đưa ra các mô hình toán học với mức độ nhất định. Làn sóng tín hiệu tất cả hoặc không không bị suy giảm theo khoảng cách, chính vì thuận lợi đó, điện thế hoạt động được xem là tương đồng với điện tử số. Sự tích hợp nhiều tín hiệu sợi nhánh đến vùng tiểu đồi sợi trục và tạo ra chuỗi điện thế hoạt động phức tạp là dạng khác của tiến trình xử lý thông tin, trong số đó có mạch thần kinh sinh học đã được khai thác kỹ đó là mạch phát sinh điều hòa vận động trung ương (central pattern generators), và là cơ sở để các nhà khoa học xây dựng nên mạng lưới thần kinh nhân tạo tương tự.[228]
Phương pháp thực nghiệm[sửa | sửa mã nguồn]

Quá trình nghiên cứu điện thế hoạt động cần phải có những phương pháp thực nghiệm với tiến bộ cao. Công trình nghiên cứu khởi xướng từ trước năm 1955 đã xoáy sâu vào ba mục đích chính: tiến hành phân lập các tín hiệu đến từ nơron đơn hay sợi trục đơn, phát triển các phương tiện điện tử nhanh và nhạy, với các điện cực rất nhỏ đủ để ghi lại điện thế bên trong tế bào.
Vấn đề đầu tiên đã được giải quyết khi nghiên cứu trên các sợi trục khổng lồ của chi mực ống Loligo.[v] Những sợi trục này có đường kính rất lớn (xấp xỉ 1 mm, hay nói cách khác là gấp 100 lần kích thước một nơron điển hình) khiến cho chúng có thể nhìn thấy được bằng mắt thường, và như vậy dễ dàng trong việc trích xuất và thao tác trên mô thần kinh.[w][x] Tuy nhiên, sợi trục chi Loligo không thể đại diện cho tất cả các tế bào kích thích, và có nhiều hệ thống khác vận hành cơ chế điện thế hoạt động cũng đã được nghiên cứu và làm rõ.
Vấn đề thứ hai là tập trung vào sự phát triển chủ yếu của kẹp điện thế (voltage clamp),[y] công cụ này cho phép các nhà thí nghiệm thực hiện nghiên cứu hiện tượng điện thế hoạt động gây ra bởi dòng chảy hạt mang điện trong điều kiện nhân tạo, và đã được loại bỏ đáng kể các tín hiệu nhiễu, dòng ion cũng chính là dòng điện IC quan hệ mật thiết với điện dung màng tế bào C.[229] Bởi vì cường độ dòng ion bằng C nhân với đại lượng đặc trưng cho sự thay đổi điện thế màng Vm, dung dịch điện ly cần phải thiết kế sao cho mạch điện có giá trị Vm cố định (tốc độ thay đổi bằng không) bất luận rằng là có dòng chảy ion xuyên màng. Vì lẽ đó, dòng chảy ion cần thiết để duy trì giá trị điện thế màng Vm ở một giá trị ổn định phản ánh trực tiếp dòng chảy ion xuyên màng. Các kỹ thuật ngành điện tử tiên tiến khác bao gồm có lồng Faraday (thiết bị chắn Faraday) và những phương tiện điện tử khác với trở kháng đầu vào cao, như thế giúp cho các phương pháp đo lường không ảnh hưởng đến giá trị điện thế của sinh vật và ghi lại một cách chính xác nhất.[230]

Vấn đề thứ ba đó chính là các điện cực gắn lên trên màng sợi trục ghi lại giá trị điện thế màng phải có kích thước đủ nhỏ để không làm nhiễu đến giá trị (và cả không làm màng tế bào bị tổn thương), khó khăn này đã được tháo gỡ vào năm 1949 khi phát minh ra kỹ thuật vi điện cực nội bào (glass micropipette electrode)[z] với ống mao quản làm bằng thủy tinh, sau đó đã được thông qua và ứng dụng rộng rãi bởi nhiều nhà khoa học..[aa][ab] Phương pháp này đã được phát triển tinh vi đến mức có thể sản xuất ra điện cực với đỉnh của nó nhỏ cỡ khoảng 100 Å (10 nm), cũng như là có trở kháng đầu vào cao.[231] Điện thế hoạt động cũng có thể ghi được với điện cực nhỏ bằng kim loại đặt nhẹ vào tế bào nơron, với bộ vi xử lý (neurochip) có chứa EOSFET có thể tương tác và phát hiện các hoạt động thần kinh, hay là trên phương diện quang học dùng phân tử nhuộm merocyanine 540 nhạy cảm với sự thay đổi về nồng độ Ca2+ hay điện thế.[ac]
Trong khi kỹ thuật vi điện cực nội bào đã giúp đo lường được tổng lượng ion vượt màng thông qua nhiều kênh ion, thì việc nghiên cứu nền tảng điện hóa của duy chỉ một kênh ion đã trở thành thực thi vào năm 1970 với sự phát triển của kỹ thuật kẹp dính mảnh màng (patch clamp), đảm nhiệm bởi Erwin Neher và Bert Sakmann. Vào năm 1991, họ đã nhận được giải Nobel Sinh lý học và Y học nhờ thành tựu này.[lower-Greek 1] Thông qua kỹ thuật kẹp dính mảnh màng này, xác nhận rằng các kênh ion có những trạng thái thấm khác nhau, chẳng hạn như là mở, đóng và bất hoạt.
Chất độc thần kinh[sửa | sửa mã nguồn]


Nhiều chất độc thần kinh, cả dạng tự nhiên hay tổng hợp, đều có cấu tạo chuyên biệt nhằm chặn đứng lại chu kỳ của điện thế hoạt động. Độc tố tetrodotoxin của họ cá nóc và saxitoxin của tảo Gonyaulax (thuộc chi dinoflagellate và là nhóm sinh vật nổi tiếng gây ra hiện tượng "thủy triều đỏ") sẽ ngăn chặn sự hình thành của điện thế hoạt động bằng cách ức chế kênh natri nhạy cảm với điện thế;[ad] tương tự như vậy, độc tố dendrotoxin của loài rắn mamba đen kìm hãm sự hoạt động của kênh kali nhạy cảm với điện thế. Những hóa chất ức chế như thế tác động lên các kênh ion cũng đồng thời phục vụ cho nhiều mục đích nghiên cứu quan trọng, qua đó cho phép các nhà khoa học có thể "dập tắt" những kênh cụ thể tùy ý muốn, vì vậy cô lập được những kênh ion mà chức năng của nó chưa nắm rõ; ngoài ra chúng cũng có thể hữu ích trong việc "thuần khiết" các kênh ion bằng sắc ký ái lực hoặc là trong phân tích nồng độ (các kênh ion). Tuy nhưng, các chất ức chế cũng có thể được chế tạo ra thành những hoạt chất với độc tính cực mạnh hơn nhiều, và có khuynh hướng tận dụng được thành các vũ khí hóa học. Các độc tố thần kinh nhằm mục đích tấn công lên các kênh ion của màng thần kinh loài côn trùng đã được cho là chất trừ sâu có hiệu quả; một ví dụ ở đây là hoạt chất tổng hợp permethrin, với cơ chế kéo dài sự hoạt hóa của kênh natri trong điện thế hoạt động. Những kênh ion trên hệ thần kinh các loài côn trùng khác với kênh ion ở người, trong đó các tác nhân thần kinh chỉ có gây ra một vài tác dụng phụ đối với người (với đương lượng vừa phải, liều cực cao có thể gây ra độc tính gen, trấn áp và phá hủy miễn dịch, hay phát sinh thêm các oncogen) nhưng đối với côn trùng chúng làm tê liệt hệ thống thần kinh. Nhiều loại chất độc thần kinh khác can thiệp vào tác động phóng thích các hóa chất thần kinh của điện thế hoạt động, cụ thể quá trình này diễn ra ngay tại các khớp nối thần kinh cơ.
Lịch sử khám phá hiện tượng điện sinh vật[sửa | sửa mã nguồn]
Vai trò điện sinh học của hệ thống thần kinh trên các đối tượng thí nghiệm động vật lần đầu tiên đã được quan sát thấy ở con ếch bởi Luigi Galvani, người đã tiến hành cuộc nghiên cứu về các thuộc tính điện của thần kinh từ năm 1791 đến năm 1797.[ae] Các giá trị và thành quả thu được từ Galvani đã kích thích Alessandro Volta phát triển ra pin Volta—cũng được xem là loại pin điện đầu tiên trong lịch sử—tạo điều kiện thuận lợi để ông nghiên cứu hiện tượng điện sinh vật (chẳng hạn khả năng phóng ra điện rất mạnh khoảng 600 V của loài cá chình điện) và các đáp ứng sinh lý quan sát được khi dẫn điện áp một chiều qua cơ thể sinh vật.[af]
Vào thế kỷ thứ 19, các nhà khoa học đã nghiên cứu sự truyền động của các tín hiệu điện trong toàn bộ dải thần kinh (tức là, các bó mạch thần kinh) và chứng minh rằng mô thần kinh được làm từ các tế bào, thay vì đó là mạng lưới ống thần kinh kết nối với nhau (reticulum).[232] Carlo Matteucci đã theo dõi những nghiên cứu của Galvani và chứng minh màng tế bào tồn tại một điện thế xuyên màng và có thể sản sinh ra dòng điện một chiều. Tiếp đó, công trình của Matteucci cũng truyền cảm hứng cho nhà sinh lý học người Đức, Emil du Bois-Reymond, và cũng là người khám phá ra điện thế hoạt động vào năm 1843.[233] Vận tốc dẫn truyền của điện thế hoạt động lần đầu tiên được đo lường vào năm 1850 bởi Hermann von Helmholtz, ông là bạn của Bois-Reymond.[234] Để chứng minh mô thần kinh được cấu tạo từ những tế bào rời rạc, vị bác sĩ người Tây Ban Nha Santiago Ramón y Cajal và học trò của ông đã sử dụng kỹ thuật nhuộm mô do Camillo Golgi phát triển để mô tả lại vô số hình dạng khác nhau của những tế bào nơron, họ đã làm công việc này rất chăm chỉ. Nhờ vào những cống hiến của họ, năm 1906 cả Golgi và Ramón y Cajal đều được nhận giải thưởng Nobel Sinh lý học và Y học.[lower-Greek 2] Công trình của họ đã giải quyết được những cuộc tranh cãi lâu dài về khía cạnh giải phẫu thần kinh vào thế kỷ thứ 19; trong đó Golgi vẫn còn tranh luận mô hình mạng lưới hệ thống thần kinh.

Thế kỷ thứ 20 chính là thời đại hoàng kim của lĩnh vực điện sinh lý học. Năm 1902 và năm 1912, Julius Bernstein đã đưa ra giả thuyết rằng điện thế hoạt động là kết quả của sự thay đổi về tính thấm của màng sợi trục đối với các hạt mang điện.[ag][235] Sau đó thì, giả thuyết của Bernstein cũng đã được xác nhận bởi Ken Cole and Howard Curtis, những người này thực nghiệm và thấy rằng tính thấm của màng tế bào tăng lên trong sự kiện điện thế hoạt động.[ah] Năm 1949, Alan Hodgkin và Bernard Katz hoàn thiện hơn nữa cho giả thuyết mà Bernstein đưa ra, đó là tính thấm màng sợi trục có thể khác nhau đối với từng loại ion nhất định; đi sâu vào chi tiết, họ đã chứng minh rằng tính thấm của ion natri đối với điện thế hoạt động là cực kỳ quan trọng.[ai] Tiến độ nghiên cứu này đạt cực điểm vào năm 1952, với sự ra đời của năm bài viết khoa học của Hodgkin, Katz và Andrew Huxley, trong đó họ thực hiện kỹ thuật kẹp điện thế để xác định sự phụ thuộc của tính thấm màng sợi trục đối với các ion natri và kali vào điện thế và thời gian, từ đó họ có khả năng tái xây dựng điện thế hoạt động thông qua mô hình định lượng.[aj] Mô hình toán học mà Hodgkin và Huxley đã đưa ra cũng có tương quan với các kênh ion khác nhau và với các trạng thái khác nhau, bao gồm có "mở", "đóng", và "bất hoạt". Giả thuyết của họ được Erwin Neher và Bert Sakmann xác nhận trong khoảng giữa những năm 1970 và những năm 1980, là những người phát triển kỹ thuật kẹp dính mảnh màng để phát hiện ra sự thay đổi về trạng thái thấm của từng loại kênh ion riêng biệt.[ak] Trong thế kỷ thứ 21, các nhà nghiên cứu dần bắt đầu hiểu rõ cấu trúc nền tảng của những trạng thái thấm và cả tính chọn lọc của kênh cho một số ion đi qua,[al] thông qua cấu trúc tinh thể với độ phân giải nguyên tử,[am] phương pháp đo lường khoảng cách huỳnh quang[an] và phương pháp đông lạnh mẫu thử dùng trong kính hiển vi điện tử (cryo-electron microscopy).[ao]
Julius Bernstein cũng là người đầu tiên đưa ra phương trình Nernst cho điện thế nghỉ xuyên màng; David E. Goldman đã nghiên cứu kỹ hơn về phương trình và tổng quát hóa nó dẫn đến sự thiết lập của phương trình mới mang tên ông vào năm 1943, đó là phương trình Goldman.[ap] Năm 1957, bơm Na⁺/K⁺-ATPase được nhận diện và cơ chế, các chức năng sinh học của nó cũng dần được làm rõ, hình thể kết cấu được xác định một cách rất chính xác qua công nghệ tinh thể học tia X hiển thị cấu trúc với độ phân giải của nguyên tử.[aq][lower-Greek 3][ar][as][at][au] Các bơm ion liên quan cũng đã được khám phá về cấu trúc tinh thể, cho ra cái nhìn toàn diện hơn đối với cách thức những bộ máy phân tử này làm việc như thế nào.[av]
Mô hình định lượng[sửa | sửa mã nguồn]

Các mô hình toán học và khoa học máy tính được xem là cần thiết để hiểu quá trình điện thế hoạt động, và đưa ra được dự đoán dựa vào giá trị hay dữ liệu thực nghiệm, cung cấp độ chính xác cho cuộc khảo nghiệm đối chiếu với lý thuyết. Trong những mô hình như thế, có mô hình Hodgkin–Huxley là quan trọng nhất và cũng chính xác nhất, trong đó điện thế hoạt động được mô tả lại bằng bốn phương trình vi phân thông thường (ODEs).[aw] Dù rằng mô hình Hodgkin–Huxley có thể đơn giản hóa so với màng tế bào thần kinh thực sự,[236] cái phức tạp của nó đã khiến cho nhiều mô hình thậm chí đơn giản hơn nhiều ra đời,[237][ax] chẳng hạn như là mô hình Morris–Lecar[ay] và mô hình FitzHugh–Nagumo,[az] cả hai mô hình đều chỉ có hai phương trình vi phân thường. Các tính chất của mô hình Hodgkin–Huxley và FitzHugh–Nagumo, và mô hình liên quan Bonhoeffer–van der Pol,[ba] đã được nghiên cứu rất chi tiết trong phạm vi toán học,[238][bb] máy tính[239] và công nghệ điện tử.[bc] Nhiều nghiên cứu hiện đại tập trung rất nhiều vào hệ thống tích hợp; bằng việc kết hợp các mô hình điện thế hoạt động với những mô hình khác của hệ thần kinh (chẳng hạn như sợi nhánh và synap), qua đó các nhà nghiên cứu có thể khảo sát sự tính toán và cách thức xử lý của mạng lưới thần kinh (xây dựng các thuật toán nhân tạo phù hợp cho các ứng dụng khác)[240] và các phản xạ đơn giản, ví dụ như phản xạ thoát, và tập hợp hành vi chịu sự kiểm soát của mạch phát sinh điều hòa vận động trung ương.[241][bd]
Xem thêm[sửa | sửa mã nguồn]
Ghi chú[sửa | sửa mã nguồn]
- ^ Chú ý rằng, những sợi Purkinje nhắc đến ở đây là sợi cơ, hoàn toàn không liên quan đến tế bào Purkinje là neuron tìm thấy ở tiểu não.
Tham khảo[sửa | sửa mã nguồn]
Chú thích[sửa | sửa mã nguồn]
- ^ a b c Hodgkin AL, Huxley AF (tháng 8 năm 1952). “A quantitative description of membrane current and its application to conduction and excitation in nerve”. The Journal of Physiology. 117 (4): 500–44. doi:10.1113/jphysiol.1952.sp004764. PMC 1392413. PMID 12991237.
- ^ a b c d e f g h Hille B biên tập (2001). Ion Channels of Excitable Membranes (ấn bản 3). Sunderland, MA: Sinauer Associates.
- ^ a b c d e f g h Squire LR biên tập (2009). Encyclopedia of Neuroscience (Ten Vol. Set) (ấn bản 1). Waltham, MA: Academic Press. ISBN 9780080446172.
- ^ Lewis, Rebecca; Asplin, Katie E.; Bruce, Gareth; Dart, Caroline; Mobasheri, Ali; Barrett-Jolley, Richard (1 tháng 11 năm 2011). “The role of the membrane potential in chondrocyte volume regulation”. Journal of Cellular Physiology. 226 (11): 2979–2986. doi:10.1002/jcp.22646. ISSN 1097-4652. PMC 3229839. PMID 21328349.
- ^ Offermanns S, Rosenthal W biên tập (2009). Encyclopedia of Molecular Pharmacology (ấn bản 2). Berlin Heidelberg: Springer. ISBN 978-3-540-38916-3.
- ^ a b Bear MF, Connors BW, Paradiso MA biên tập (2015). Neuroscience: Exploring the Brain (ấn bản 4). Philadelphia: Lippincott Williams & Wilkins. ISBN 978-0-7817-7817-6.
- ^ “Mysteries of the action potential From 1952 to infinity and beyond?”. line feed character trong
|title=tại ký tự số 34 (trợ giúp) - ^ Trịnh Bỉnh Duy (2006). Sinh Lý Học tập I. Quận Ba Đình, TP Hà Nội: Nhà xuất bản y học.
- ^ Seifter, Julian; Sloane, David; Ratner A, Austin (2005). Concepts in Medical Physiology (ấn bản 1). Philadelphia: Lippincott Williams & Wilkins. ISBN 978-0781744898.
- ^ Lodish H, Berk A, Zipursky SL, Matsudaira P, Baltimore D, Darnell J (2000). “Section 21.3, Molecular Properties of Voltage-Gated Ion Channels”. Molecular Cell Biology (ấn bản 4). New York: Scientific American Books. ISBN 978-0-7167-3136-8.
- ^ Finger, Stanley; Piccolino, Marco (8 tháng 9 năm 2011). The Shocking History of Electric Fishes. OUP USA.
- ^ Hardin J, Bertoni GP, Kleinsmith LJ (tháng 12 năm 2010). Becker's World of the Cell. Benjamin-Cummings Publishing Company. tr. 389. ISBN 978-0-321-71602-6.
- ^ Lentz TL, Erulkar SD (2018). “Nervous System”. Encyclopædia Britannica.
- ^ “Action Potential”. Britannica Academic. Encyclopædia Britannica, Inc. Truy cập ngày 26 tháng 9 năm 2019.
- ^ Kaczmarek LK, Zhang Y (tháng 10 năm 2017). “Kv3 Channels: Enablers of Rapid Firing, Neurotransmitter Release, and Neuronal Endurance”. Physiological Reviews. 97 (4): 1431–1468. doi:10.1152/physrev.00002.2017. PMC 6151494. PMID 28904001.
- ^ Lucas K (tháng 2 năm 1909). “The "all or none" contraction of the amphibian skeletal muscle fibre”. The Journal of Physiology. 38 (2–3): 113–33. doi:10.1113/jphysiol.1909.sp001298. PMC 1533646. PMID 16992966.
- ^ Cannon WB (1922). “Biographical Memoir: Henry Pickering Bowdich”. National Academy of Sciences. 17: 181–96.
- ^ Adrian E (1932). “The activity of nerve fibres”. The Nobel prize Lecture.
- ^ Adrian ED, Zotterman Y (tháng 4 năm 1926). “The impulses produced by sensory nerve-endings: Part II. The response of a Single End-Organ”. The Journal of Physiology. 61 (2): 151–71. doi:10.1113/jphysiol.1926.sp002281. PMC 1514782. PMID 16993780.
- ^ Schmidt, Robert F.; Thews, Gerhard (1983). Human physiology. Springer-Verlag. tr. 725. ISBN 978-3540116691.
- ^ a b c Hodgkin AL, Katz B (tháng 3 năm 1949). “The effect of sodium ions on the electrical activity of giant axon of the squid”. The Journal of Physiology. 108 (1): 37–77. doi:10.1113/jphysiol.1949.sp004310. PMC 1392331. PMID 18128147.
- ^ a b c Hodgkin AL, Huxley AF (tháng 4 năm 1952). “Currents carried by sodium and potassium ions through the membrane of the giant axon of Loligo”. The Journal of Physiology. 116 (4): 449–72. doi:10.1113/jphysiol.1952.sp004717. PMC 1392213. PMID 14946713.
- ^ Purves D, Augustine GJ, Fitzpatrick D, và đồng nghiệp biên tập (2001). “Voltage-Gated Ion Channels”. Neuroscience (ấn bản 2). Sunderland, MA: Sinauer Associates. Truy cập 29 Tháng tám năm 2017. Đã bỏ qua tham số không rõ
|archive- url=(trợ giúp); Đã bỏ qua tham số không rõ|chapter- url=(trợ giúp) - ^ a b Rudy Y (2008). “Molecular basis of cardiac action potential repolarization”. Annals of the New York Academy of Sciences. 1123: 113–8. doi:10.1196/annals.1420.013. PMID 18375583.
- ^ Kurtenbach S, Kurtenbach S, Zoidl G (2014). “Gap junction modulation and its implications for heart function”. Frontiers in Physiology. 5: 82. doi:10.3389/fphys.2014.00082. PMC 3936571. PMID 24578694.
- ^ Becker Daniel E (2006). “Fundamentals of Electrocardiography Interpretation”. Anesthesia Progress. 53 (2): 53–64. doi:10.2344/0003-3006(2006)53[53:foei]2.0.co;2. PMC 1614214. PMID 16863387.
- ^ Santana, Luis F.; Cheng, Edward P.; Lederer, W. Jonathan (1 tháng 12 năm 2010). “How does the shape of the cardiac action potential control calcium signaling and contraction in the heart?”. Journal of Molecular and Cellular Cardiology (bằng tiếng Anh). 49 (6): 901–903. doi:10.1016/j.yjmcc.2010.09.005. PMC 3623268. PMID 20850450.
- ^ Mummert H, Gradmann D (1976). “Voltage dependent potassium fluxes and the significance of action potentials in Acetabularia”. Biochimica et Biophysica Acta (BBA) - Biomembranes. 443 (3): 443–450. doi:10.1016/0005-2736(76)90464-8. PMID 963066.
- ^ a b Mummert H, Gradmann D (1991). “Action potentials in Acetabularia: measurement and simulation of voltage-gated fluxes”. The Journal of Membrane Biology. 124 (3): 265–273. doi:10.1007/BF01994359. PMID 1664861.
- ^ Raghavan M, Fee D, Barkhaus PE (2019). “Generation and propagation of the action potential”. Handbook of Clinical Neurology. 160: 3–22. doi:10.1016/B978-0-444-64032-1.00001-1. PMID 31277855.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y Purves D, Augustine GJ, Fitzpatrick D, và đồng nghiệp biên tập (2018). Neuroscience (ấn bản 6). Sunderland, MA: Sinauer Associates. ISBN 9781605353807.
- ^ a b Bean, Bruce P. (tháng 6 năm 2007). “The action potential in mammalian central neurons”. Nature Reviews Neuroscience. 8 (6): 451–465. doi:10.1038/nrn2148. ISSN 1471-0048. PMID 17514198. S2CID 205503852.
- ^ Carroll, SL (2017). “The Molecular and Morphologic Structures That Make Saltatory Conduction Possible in Peripheral Nerve”. Journal of Neuropathology and Experimental Neurology. 76 (4): 255–257. doi:10.1093/jnen/nlx013. PMID 28340093.
- ^ Keizer J, Smith GD, Ponce-Dawson S, Pearson JE (tháng 8 năm 1998). “Saltatory propagation of Ca2+ waves by Ca2+ sparks”. Biophysical Journal. 75 (2): 595–600. Bibcode:1998BpJ....75..595K. doi:10.1016/S0006-3495(98)77550-2. PMC 1299735. PMID 9675162.
- ^ Dawson SP, Keizer J, Pearson JE (tháng 5 năm 1999). “Fire-diffuse-fire model of dynamics of intracellular calcium waves”. Proceedings of the National Academy of Sciences of the United States of America. 96 (11): 6060–3. Bibcode:1999PNAS...96.6060D. doi:10.1073/pnas.96.11.6060. PMC 26835. PMID 10339541.
- ^ “Axon Terminal”. Medical Dictionary Online. Bản gốc lưu trữ ngày 4 tháng 3 năm 2016. Truy cập ngày 6 tháng 2 năm 2013. Đã bỏ qua tham số không rõ
|archive- url=(trợ giúp) - ^ Llinás R, Steinberg IZ, Walton K (tháng 3 năm 1981). “Relationship between presynaptic calcium current and postsynaptic potential in squid giant synapse”. Biophysical Journal. 33 (3): 323–51. Bibcode:1981BpJ....33..323L. doi:10.1016/S0006-3495(81)84899-0. PMC 1327434. PMID 6261850.
- ^ Rizo, Josep (10 tháng 7 năm 2018). “Mechanism of neurotransmitter release coming into focus”. Protein Science (Review). 27 (8): 1364–1391. doi:10.1002/pro.3445. ISSN 0961-8368. PMC 6153415. PMID 29893445.
Research for three decades and major recent advances have provided crucial insights into how neurotransmitters are released by Ca2+ -triggered synaptic vesicle exocytosis, leading to reconstitution of basic steps that underlie Ca2+ -dependent membrane fusion and yielding a model that assigns defined functions for central components of the release machinery.
- ^ Südhof TC, Rizo J (tháng 12 năm 2011). “Synaptic vesicle exocytosis”. Cold Spring Harbor Perspectives in Biology. 3 (12): a005637. doi:10.1101/cshperspect.a005637. PMC 3225952. PMID 22026965.
- ^ Lodish, H.; Berk, A.; Zipursky, S.L. (2000). Molecular Cell Biology: Section 21.4 Neurotransmitters, Synapses, and Impulse Transmission (ấn bản 4). New York: W. H. Freeman.
- ^ Cherry, Kendra. “What is a Neurotransmitter?”. Bản gốc lưu trữ ngày 4 tháng 3 năm 2016. Truy cập ngày 6 tháng 10 năm 2014.
- ^ “Neuropeptide database”.
- ^ “Neuropeptides. IUPHAR/BPS Guide to pharmacology”.
- ^ “Gene Family: Ligand gated ion channels”. HUGO Gene Nomenclature Committee. Bản gốc lưu trữ ngày 14 tháng 11 năm 2017. Truy cập ngày 7 tháng 9 năm 2021.
- ^ "ligand-gated channel" tại Từ điển Y học Dorland
- ^ Malenka RC, Nestler EJ, Hyman SE (2009). “Chapter 5: Excitatory and Inhibitory Amino Acids”. Trong Sydor A, Brown RY (biên tập). Molecular Neuropharmacology: A Foundation for Clinical Neuroscience (ấn bản 2). New York, USA: McGraw-Hill Medical. tr. 124–125. ISBN 9780071481274.
At membrane potentials more negative than approximately −50 mV, the Mg2+ in the extracellular fluid of the brain virtually abolishes ion flux through NMDA receptor channels, even in the presence of glutamate. ... The NMDA receptor is unique among all neurotransmitter receptors in that its activation requires the simultaneous binding of two different agonists. In addition to the binding of glutamate at the conventional agonist-binding site, the binding of glycine appears to be required for receptor activation. Because neither of these agonists alone can open this ion channel, glutamate and glycine are referred to as coagonists of the NMDA receptor. The physiologic significance of the glycine binding site is unclear because the normal extracellular concentration of glycine is believed to be saturating. However, recent evidence suggests that D-serine may be the endogenous agonist for this site.
- ^ Wu C, Sun D (tháng 4 năm 2015). “GABA receptors in brain development, function, and injury”. Metabolic Brain Disease. 30 (2): 367–79. doi:10.1007/s11011-014-9560-1. PMC 4231020. PMID 24820774.
- ^ Takagi, Hiroshi. "Roles of Ion Channels in EPSP Integration at Neuronal Dendrites." Neuroscience Research, vol. 37, no. 3, 2000, pp. 167–171., doi:10.1016/s0168-0102(00)00120-6.
- ^ Meldrum, BS (tháng 4 năm 2000). “Glutamate as a neurotransmitter in the brain: review of physiology and pathology”. The Journal of Nutrition. 130 (4S Suppl): 1007S–15S. doi:10.1093/jn/130.4.1007s. PMID 10736372.
- ^ Phan Sỹ An (2005). Lý sinh y học. Quận Ba Đình, TP Hà Nội: Nhà xuất bản y học.
- ^ Clarke, Edwin (1987). Nineteenth-century origins of neuroscientific concepts. Jacyna, L. S. Berkeley: University of California Press. ISBN 0-520-05694- 9. OCLC 13456516.
- ^ Pera, Marcello, 1943- (1992). The ambiguous frog : the Galvani-Volta controversy on animal electricity. Tr. Mandelbaum, Jonathan. Princeton, New Jersey: Princeton University Press. ISBN 978-1-4008-6249- 8. OCLC 889251161.
- ^ Piccolino, Marco; Bresadola, Marco (2013). Shocking frogs : Galvani, Volta, and the electric origins of neuroscience. Oxford; New York: Oxford University Press. ISBN 978-0-19-978221-5. OCLC 859536612.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- ^ Bernstein, J (1868). “Ueber den zeitlichen Verlauf der negativen Schwankung des Nervenstroms” [About the time course of the negative fluctuation of the nerve current]. Pflüger, Archiv für die Gesammte Physiologie des Menschen und der Thiere (bằng tiếng Đức). 1 (1): 173–207. doi:10.1007/BF01640316. S2CID 32435163.
- ^ Du Bois- Reymond, Emil (1848). “Untersuchungen über thierische Elektricität” [Investigations on animal electricity]. Annalen der Physik und Chemie (bằng tiếng Đức). 151 (11): 463–4. Bibcode:1848AnP...151..463D. doi:10.1002/andp.18481511120.
- ^ Schuetze, Stephen M (1983). “The discovery of the action potential”. Trends in Neurosciences. 6: 164–8. doi:10.1016/0166-2236(83)90078-4. S2CID 53175297.
- ^ a b c d e f Johnston, Daniel; Samuel Miao-Sin Wu (1994). Foundations of Cellular Neurophysiology (Bradford Books) (ấn bản 1). Cambridge, Massachusetts: the Massachusetts Institute of Technology Press. ISBN 9780262100533.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af ag ah ai aj ak al am an Bullock TH, Orkand R, Grinnell A biên tập (1977). Introduction to Nervous Systems (ấn bản 1). New York: W.H. Freeman & Company. ISBN 0-7167-0030-1.
- ^ a b c d e f g h i j k l m n o p q Schmidt-Nielsen K biên tập (1997). Animal Physiology: Adaptation and Environment (ấn bản 5). Cambridge: Cambridge University Press. ISBN 978-0521570985.
- ^ “5.2 Passive Transport - Biology 2e | OpenStax”. openstax.org (bằng tiếng Anh). Truy cập 2020-12- 06. Kiểm tra giá trị ngày tháng trong:
|access-date=(trợ giúp) - ^ “5.2A: The Role of Passive Transport”. Biology LibreTexts (bằng tiếng Anh). 10 tháng 7 năm 2018. Truy cập ngày 6 tháng 12 năm 2020.
- ^ Skene, Keith R. (2015). “Life's a Gas: A Thermodynamic Theory of Biological Evolution”. Entropy (bằng tiếng Anh). 17 (8): 5522–5548. Bibcode:2015Entrp..17.5522S. doi:10.3390/e17085522.
- ^ Lyklema, J. (1995). Fundamentals of Interface and Colloid Science. 2. tr. 3.208.
- ^ Hunter, R.J. (1989). Foundations of Colloid Science. Oxford University Press.
- ^ Dukhin, S.S.; Derjaguin, B.V. (1974). Electrokinetic Phenomena. J. Wiley and Sons.
- ^ Russel, W.B.; Saville, D.A.; Schowalter, W.R. (1989). Colloidal Dispersions. Cambridge University Press.
- ^ Kruyt, H.R. (1952). Colloid Science. 1, Irreversible systems. Elsevier.
- ^ Dukhin, A.S.; Goetz, P.J. (2017). Characterization of liquids, nano- and micro- particulates and porous bodies using Ultrasound. Elsevier. ISBN 978-0-444-63908-0.
- ^ Anderson, J L (tháng 1 năm 1989). “Colloid Transport by Interfacial Forces”. Annual Review of Fluid Mechanics (bằng tiếng Anh). 21 (1): 61–99. Bibcode:1989AnRFM..21...61A. doi:10.1146/annurev.fl.21.010189.000425. ISSN 0066-4189.
- ^ Pollard TD, Earnshaw WC, Lippincott-Schwartz J, Johnson GT biên tập (2017). Cell Biology (ấn bản 3). Philadelphia, PA: Elsevier. ISBN 978-0-323- 34126-4.
- ^ Finkelstein A, Mauro A (1963). “Equivalent circuits as related to ionic systems”. Biophysical Journal. 3: 215–37.
- ^ a b c d e f g h i j k l m n Junge D biên tập (1981). Nerve and Muscle Excitation (ấn bản 2). Sunderland, MA: Sinauer Associates. ISBN 0-87893-410-3.
- ^ Johns, Paul (1 tháng 1 năm 2014), Johns, Paul (biên tập), “Chapter 6 - Electrical signalling in neurons”, Clinical Neuroscience (bằng tiếng Anh), Churchill Livingstone, tr. 71–80, doi:10.1016/b978-0-443-10321-6.00006-0, ISBN 978-0-443-10321-6, truy cập ngày 28 tháng 12 năm 2020
- ^ Plonsey, Robert; Barr, Roger C. (2007). Bioelectricity: A Quantitative Approach. New York: Springer. tr. 57-64. ISBN 978-0-387-48864-6.
- ^ Lieb WR, Stein WD (1986). “Chapter 2. Simple Diffusion across the Membrane Barrier”. Transport and Diffusion across Cell Membranes. San Diego: Academic Press. tr. 69–112. ISBN 0-12-664661-9.
- ^ Atkins, Peter; de Paula, Julio (2006). Physical Chemistry for the Life Science.
- ^ Conlisk, A. Terrence (2013). Essentials of Micro- and Nanofluidics: With Applications to the Biological and Chemical Sciences. Cambridge University Press. tr. 43. ISBN 9780521881685.
- ^ Berg JM, Tymoczko JL, Stryer L biên tập (2002). Biochemistry, Fifth Edition: International Version (ấn bản 5). New York, NY, United States: W. H. Freeman and Company. ISBN 9780716746843.
- ^ Eisenman G (1961). “On the elementary atomic origin of equilibrium ionic specificity”. Trong A Kleinzeller, A Kotyk (biên tập). Symposium on Membrane Transport and Metabolism. New York: Academic Press. tr. 163–79.
* Eisenman G (1965). “Some elementary factors involved in specific ion permeation”. Proc. 23rd Int. Congr. Physiol. Sci., Tokyo. Amsterdam: Excerta Med. Found. tr. 489–506.
* Diamond JM, Wright EM (1969). “Biological membranes: the physical basis of ion and nonekectrolyte selectivity”. Annual Review of Physiology. 31: 581–646. - ^ Doyle DA, Morais Cabral J, Pfuetzner RA, Kuo A, Gulbis JM, Cohen SL, và đồng nghiệp (1998). “The structure of the potassium channel, molecular basis of K+ conduction and selectivity”. Science. 280: 69–77.
* Zhou Y, Morias-Cabrak JH, Kaufman A, MacKinnon R (2001). “Chemistry of ion coordination and hydration revealed by a K+-Fab complex at 2.0 A resolution”. Nature. 414: 43–48.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
* Jiang Y, Lee A, Chen J, Ruta V, Cadene M, Chait BT, MacKinnon R (2003). “X-ray structure of a voltage-dependent K+ channel”. Nature. 423: 33–41.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết) - ^ Cai SQ, Li W, Sesti F (2007). “Multiple modes of a-type potassium current regulation”. Curr. Pharm. Des. 13 (31): 3178–84. doi:10.2174/138161207782341286. PMID 18045167.
- ^ Armstrong CM (tháng 7 năm 1981). “Sodium channels and gating currents”. Physiological Reviews. 61 (3): 644–83. doi:10.1152/physrev.1981.61.3.644. PMID 6265962.
- ^ Vassilev P, Scheuer T, Catterall WA (tháng 10 năm 1989). “Inhibition of inactivation of single sodium channels by a site-directed antibody”. Proceedings of the National Academy of Sciences of the United States of America. 86 (20): 8147–51. Bibcode:1989PNAS...86.8147V. doi:10.1073/pnas.86.20.8147. PMC 298232. PMID 2554301.
- ^ Bénitah JP, Chen Z, Balser JR, Tomaselli GF, Marbán E (tháng 3 năm 1999). “Molecular dynamics of the sodium channel pore vary with gating: interactions between P-segment motions and inactivation”. The Journal of Neuroscience. 19 (5): 1577–85. doi:10.1523/JNEUROSCI.19-05-01577.1999. PMC 6782169. PMID 10024345.
- ^ a b Goldin AL (2007). “Neuronal Channels and Receptors”. Trong Waxman SG (biên tập). Molecular Neurology. Burlington, MA: Elsevier Academic Press. tr. 43–58. ISBN 978-0-12-369509-3.
- ^ "Engineering Light-Gated Ion Channels" — Biochemistry, 45 (51), 15129 -15141, 2006
- ^ Govorunova, Elena G.; Sineshchekov, Oleg A.; Janz, Roger; Liu, Xiaoqin; Spudich, John L. (7 tháng 8 năm 2015). “Natural light-gated anion channels: A family of microbial rhodopsins for advanced optogenetics”. Science. 349 (6248): 647–650. doi:10.1126/science.aaa7484. ISSN 0036-8075. PMC 4764398. PMID 26113638.
- ^ Nagel, Georg; Brauner, Martin; Liewald, Jana F.; Adeishvili, Nona; Bamberg, Ernst; Gottschalk, Alexander (2005). “Light Activation of Channelrhodopsin-2 in Excitable Cells of Caenorhabditis elegans Triggers Rapid Behavioral Responses”. Current Biology. 15 (24): 2279–2284. doi:10.1016/j.cub.2005.11.032. PMID 16360690.
- ^ Nagel, Georg; Szellas, Tanjef; Huhn, Wolfram; Kateriya, Suneel; Adeishvili, Nona; Berthold, Peter; Ollig, Doris; Hegemann, Peter; Bamberg, Ernst (25 tháng 11 năm 2003). “Channelrhodopsin-2, a directly light-gated cation-selective membrane channel”. Proceedings of the National Academy of Sciences. 100 (24): 13940–13945. doi:10.1073/pnas.1936192100. ISSN 0027-8424. PMC 283525. PMID 14615590.
- ^ Sukharev SI, Martinac B, Arshavsky VY, Kung C (tháng 7 năm 1993). “Two types of mechanosensitive channels in the Escherichia coli cell envelope: solubilization and functional reconstitution”. Biophys. J. 65 (1): 177–83. Bibcode:1993BpJ....65..177S. doi:10.1016/S0006-3495(93)81044-0. PMC 1225713. PMID 7690260.
- ^ Haswell ES, Phillips R, Rees DC (tháng 10 năm 2011). “Mechanosensitive channels: what can they do and how do they do it?”. Structure. 19 (10): 1356–69. doi:10.1016/j.str.2011.09.005. PMC 3203646. PMID 22000509.
- ^ Patel A, Sharif-Naeini R, Folgering JR, Bichet D, Duprat F, Honoré E (tháng 8 năm 2010). “Canonical TRP channels and mechanotransduction: from physiology to disease states”. Pflügers Arch. 460 (3): 571–81. doi:10.1007/s00424-010-0847-8. PMID 20490539. S2CID 22542282.
- ^ Yin J, Kuebler WM (2010). “Mechanotransduction by TRP channels: general concepts and specific role in the vasculature”. Cell Biochem Biophys. 56 (1): 1–18. doi:10.1007/s12013-009-9067-2. PMID 19842065. S2CID 12154460.
- ^ Martinac B (2011). “Bacterial mechanosensitive channels as a paradigm for mechanosensory transduction”. Cell. Physiol. Biochem. 28 (6): 1051–60. doi:10.1159/000335842. PMID 22178995.
- ^ a b c Hodgkin AL, Keynes RD (1955). “Active transport of cations in giant axons from Sepia and Loligo”. J. Physiol. 128: 28–60.
- ^ Active Transport Process Lưu trữ 2012-01-20 tại Wayback Machine. Buzzle.com (2010-05-14). Retrieved on 2011-12-05.
- ^ Lodish H, Berk A, Zipursky SL, et al. Molecular Cell Biology. 4th edition. New York: W. H. Freeman; 2000. Section 15.6, Cotransport by Symporters and Antiporters.
- ^ Lodish H, Berk A, Zipursky SL, et al. Molecular Cell Biology. 4th edition. New York: W. H. Freeman; 2000. Chapter 15, Transport across Cell Membranes.
- ^ Active Transport Lưu trữ tháng 8 24, 2011 tại Wayback Machine. Biologycorner.com. Retrieved on 2011-12-05.
- ^ Caldwell PC, Hodgkin AL, Keynes RD, Shaw TI (1960). “The effects of injecting energy-rich phosphate compounds on the active transport of ions in the giant axons of Loligo”. J. Physiol. 152: 561–90.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- ^ Reese, Jane B.; Urry, Lisa A.; Cain, Michael L.; Wasserman, Steven A.; Minorsky, Peter V.; Jackson, Robert B. (2014). Tenth Edition, Campbell's Biology . United States: Pearson Education Inc. tr. 135. ISBN 978-0-321-77565-8.
- ^ Steinbach HB, Spiegelman S (1943). “The sodium and potassium balance in squid nerve axoplasm”. J. Cell. Comp. Physiol. 22: 187–96.
- ^ a b Hodgkin AL (1951). “The ionic basis of electrical activity in nerve and muscle”. Biol. Rev. 26: 339–409.
- ^ Bernstein J (1902). “Untersuchungen zur Thermodynamik der bioelektrischen Ströme”. Pflüger's Arch. Ges. Physiol. 92: 521–562.
* Bernstein J (1912). Elektrobiologie. Braunschweig: Vieweg und Sohn. - ^ a b Goldman DE (1943). “Potential, impedance and rectification in membranes”. J. Gen. Physiol. 27: 37–60.
- ^ Spangler SG (1972). “Expansion of the constant field equation to include both divalent and monovalent ions”. Ala J Med Sci. 9: 218–23. PMID 5045041.
- ^ Flynn, Kevin C (1 tháng 1 năm 2013). “The cytoskeleton and neurite initiation”. Bioarchitecture. 3 (4): 86–109. doi:10.4161/bioa.26259. ISSN 1949-0992. PMC 4201609. PMID 24002528.
- ^ Valtorta, F.; Leoni, C. (28 tháng 2 năm 1999). “Molecular mechanisms of neurite extension”. Philosophical Transactions of the Royal Society of London. Series B, Biological Sciences. 354 (1381): 387–394. doi:10.1098/rstb.1999.0391. ISSN 0962-8436. PMC 1692490. PMID 10212488.
- ^ Niclou, Simone P.; Franssen, Elske H. P.; Ehlert, Erich M. E.; Taniguchi, Masahiko; Verhaagen, Joost (1 tháng 12 năm 2003). “Meningeal cell-derived semaphorin 3A inhibits neurite outgrowth”. Molecular and Cellular Neurosciences. 24 (4): 902–912. doi:10.1016/s1044-7431(03)00243-4. ISSN 1044-7431. PMID 14697657. S2CID 12637023.
- ^ Luo, Y.; Raible, D.; Raper, J. A. (22 tháng 10 năm 1993). “Collapsin: a protein in brain that induces the collapse and paralysis of neuronal growth cones”. Cell. 75 (2): 217–227. doi:10.1016/0092-8674(93)80064-l. ISSN 0092-8674. PMID 8402908. S2CID 46120825.
- ^ a b GSTS. BS. Trịnh Văn Minh (2017). Giải phẫu người (Tập 3: Hệ thần kinh - Hệ nội tiết). Nhà xuất bản Giáo dục Việt Nam. ISBN 978-604-0-04586-7. Chú thích có tham số trống không rõ:
|1=(trợ giúp) - ^ Foster, M.; Sherrington, C.S. (1897). Textbook of Physiology, volume 3 (ấn bản 7). London: Macmillan. tr. 929.
- ^ Perea, G.; Navarrete, M.; Araque, A. (tháng 8 năm 2009). “Tripartite synapses: astrocytes process and control synaptic information”. Trends in Neurosciences. Cambridge, MA: Cell Press. 32 (8): 421–431. doi:10.1016/j.tins.2009.05.001. PMID 19615761. S2CID 16355401.
- ^ Schacter, Daniel L.; Gilbert, Daniel T.; Wegner, Daniel M. (2011). Psychology (ấn bản 2). New York: Worth Publishers. tr. 80. ISBN 978-1-4292-3719-2. LCCN 2010940234. OCLC 696604625.
- ^ Palay, Sanford (1956). “Synapses in the central nervous system”. J Biophys Biochem Cytol. 2 (4): 193–202. doi:10.1083/jcb.2.4.193. PMC 2229686. PMID 13357542.
- ^ Elias, Lorin J.; Saucier, Deborah M. (2006). Neuropsychology: Clinical and Experimental Foundations. Boston: Pearson/Allyn & Bacon. ISBN 978-0-20534361-4. LCCN 2005051341. OCLC 61131869.
- ^ Stadelmann, Christine; Timmler, Sebastian; Barrantes-Freer, Alonso; Simons, Mikael (1 tháng 7 năm 2019). “Myelin in the Central Nervous System: Structure, Function, and Pathology”. Physiological Reviews. 99 (3): 1381–1431. doi:10.1152/physrev.00031.2018. ISSN 1522-1210. PMID 31066630.
- ^ “Node of Ranvier”. Dictionary.com.
- ^ gxnSalzer J. L. (1997). “Clustering sodium channels at the node of Ranvier: close encounters of the axon-glia kind”. Neuron. 18 (6): 843–846. doi:10.1016/S0896-6273(00)80323-2. PMID 9208851. S2CID 6743084. Bản gốc lưu trữ ngày 18 tháng 12 năm 2007. Truy cập ngày 7 tháng 12 năm 2007.
- ^ a b c d e f g h i j k l m n o Stevens CF (1966). Neurophysiology: A Primer. New York: John Wiley and Sons.LCCN 66-0 – 0
- ^ a b Hodgkin AL, Huxley AF, Katz B (1952). “Measurements of current-voltage relations in the membrane of the giant axon of Loligo”. Journal of Physiology. 116: 424–448. PMID 14946713.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
* Hodgkin AL, Huxley AF (1952). “The components of membrane conductance in the giant axon of Loligo”. J Physiol. 116: 473–496. PMID 14946714.
* Hodgkin AL, Huxley AF (1952). “The dual effect of membrane potential on sodium conductance in the giant axon of Loligo”. J Physiol. 116: 497–506. PMID 14946715. - ^ a b c d Liqun L (2021). “Signaling within Neurons”. Principles of neurobiology (ấn bản 2). Boca Raton, Florida: CRC Press. ISBN 9780815346050.
- ^ The Nobel Prize in Physiology or Medicine 1963.
- ^ Naundorf B, Wolf F, Volgushev M (tháng 4 năm 2006). “Unique features of action potential initiation in cortical neurons” (Letter). Nature. 440: 1060–1063. doi:10.1038/nature04610. Truy cập ngày 27 tháng 3 năm 2008.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- ^ Palay, Sanford L.; Sotelo, Constantino; Peters, Alan; Orkand, Paula M. (1968). “The Axon Hillock and the Initial Segment”. The Journal of Cell Biology. 38 (1): 193–201. doi:10.1083/jcb.38.1.193. PMC 2107452. PMID 5691973.
- ^ Hemmings, Hugh C.; Egan, Talmage D. (6 tháng 12 năm 2012). Pharmacology and Physiology for Anesthesia E-Book: Foundations and Clinical Application (bằng tiếng Anh). Elsevier Health Sciences. ISBN 9781455737932.
- ^ Wollner D, Catterall WA (tháng 11 năm 1986). “Localization of sodium channels in axon hillocks and initial segments of retinal ganglion cells”. Proceedings of the National Academy of Sciences of the United States of America. 83 (21): 8424–28. Bibcode:1986PNAS...83.8424W. doi:10.1073/pnas.83.21.8424. PMC 386941. PMID 2430289.
- ^ Berne, Robert; Matthew Levy; Bruce Koeppen; Bruce Stanton (2004). Physiology. Elsevier Mosby. tr. 276. ISBN 978-0-8243-0348-8.
- ^ Verkerk AO, van Boren MM, Peters RJ, Broekhuis E, Lam K, Coronel R, de Bakker JM, Tan HR (tháng 10 năm 2007). “Pacemaker current (I)f)) in the human sinoatrial node”. Eur Heart J. 28 (1): 2472–8. doi:10.1093/eurheartj/ehm339. PMID 17823213.
- ^ Boron, Walter. F; Emile Boulpaep (2003). Medical Physiology. Elsevier Saunders. tr. 489. ISBN 978-0-7216-0076-5.
- ^ Verkerk AO, van Ginneken AC, Wilders R (tháng 1 năm 2009). “Pacemaker activity of the human sinoatrial node: Role of the hyperpolarization-activated current, I(f)”. Int J Cardiol. 132 (3): 318–36. doi:10.1016/j.ijcard.2008.12.196. PMID 19181406.
- ^ a b Squire LR (2012). “Membrane Potential and Action Potential”. Fundamental neuroscience (ấn bản 4). Waltham, MA: Elsevier Academic Press. ISBN 978-0-12-385870-2.
- ^ Missler M, Südhof TC, Biederer T (2012). “Synaptic cell adhesion”. Cold Spring Harb Perspect Biol. 4 (4): a005694. doi:10.1101/cshperspect.a005694. PMC 3312681. PMID 22278667.
- ^ Craig C. Garner and Kang Shen. Structure and Function of Vertebrate and Invertebrate Active Zones. Structure and Functional Organization of the Synapse. Ed: Johannes Hell and Michael Ehlers. Springer, 2008.
- ^ Zhai R. Grace; Bellen Hugo J. (2004). “The Architecture of the Active Zone in the Presynaptic Nerve Terminal”. Physiology. 19 (5): 262–270. doi:10.1152/physiol.00014.2004. PMID 15381754. S2CID 9609266.
- ^ Phillips GR; và đồng nghiệp (2001). “The presynaptic particle web: ultrastructure, composition, dissolution, and reconstitution”. Neuron. 32 (1): 63–77. doi:10.1016/s0896-6273(01)00450-0. PMID 11604139. S2CID 5996555.
- ^ Siksou; và đồng nghiệp (2007). “Three-Dimensional Architecture of Presynaptic Terminal Cytomatrix”. The Journal of Neuroscience. 27 (26): 6868–6877. doi:10.1523/jneurosci.1773-07.2007. PMC 6672225. PMID 17596435.
- ^ Meldrum BS (tháng 4 năm 2000). rZ8fbQFozhcSICpGPPS0NR2AUWm5GmpntVmXvRk0IAPDI0byFmlizodEnvp4ArjqaaZ_HUVEJL9QPpftMvD9qdWyOWmc_tFUzmxRQYRhx6z8OT7XeYyFwLHxa23_HCtLakmpBplg “Glutamate as a neurotransmitter in the brain: review of physiology and pathology” Kiểm tra giá trị
|url=(trợ giúp) (PDF). The Journal of Nutrition. 130 (4S Suppl): 1007S–15S. doi:10.1093/jn/130.4.1007s. PMID 10736372. - ^ McEntee WJ, Crook TH (1993). “Glutamate: its role in learning, memory, and the aging brain”. Psychopharmacology. 111 (4): 391–401. doi:10.1007/BF02253527. PMID 7870979. S2CID 37400348.
- ^ Okubo Y, Sekiya H, Namiki S, Sakamoto H, Iinuma S, Yamasaki M, Watanabe M, Hirose K, Iino M (tháng 4 năm 2010). “Imaging extrasynaptic glutamate dynamics in the brain”. Proceedings of the National Academy of Sciences of the United States of America. 107 (14): 6526–31. Bibcode:2010PNAS..107.6526O. doi:10.1073/pnas.0913154107. PMC 2851965. PMID 20308566.
- ^ Smith QR (tháng 4 năm 2000). “Transport of glutamate and other amino at the blood-brain barrier”. The Journal of Nutrition. 130 (4S Suppl): 1016S–22S. doi:10.1093/jn/130.4.1016S. PMID 10736373.
- ^ Shigeri Y, Seal RP, Shimamoto K (tháng 7 năm 2004). “Molecular pharmacology of glutamate transporters, EAATs and VGLUTs”. Brain Research. Brain Research Reviews. 45 (3): 250–65. doi:10.1016/j.brainresrev.2004.04.004. PMID 15210307. S2CID 41057787.
- ^ Watkins JC (2000). “l-glutamate as a central neurotransmitter: looking back”. Biochemical Society Transactions. 28 (4): 297–309. doi:10.1042/0300-5127:0280297. PMID 10961913.
- ^ M. Sheng, C. Hoogenraad; Hoogenraad (2006). “The Postsynaptic Architecture of Excitatory Synapses: A More Quantitative View”. Annual Review of Biochemistry. 76: 823–47. doi:10.1146/annurev.biochem.76.060805.160029. PMID 17243894.
- ^ Chua, Kindler; Boykin, Jahn (3 tháng 3 năm 2010). “Architecture of an Excitatory Synapse”. Journal of Cell Science. 123 (6): 819–823. doi:10.1242/jcs.052696. hdl:11858/00-001M-0000-0012-D5F7-3. PMID 20200227.
- ^ Williams, S. Mark; McNamara, James O.; Lamantia, Anthony-Samuel; Katz, Lawrence C.; Fitzpatrick, David; Augustine, George J.; Purves, Dale (2001). “Excitatory and Inhibitory Postsynaptic Potentials”. Sinauer Associates, Inc. Chú thích journal cần
|journal=(trợ giúp) - ^ Coombs JS, Eccles JC, Fatt P (tháng 11 năm 1955). “The specific ionic conductances and the ionic movements across the motoneuronal membrane that produce the inhibitory post-synaptic potential”. The Journal of Physiology. 130 (2): 326–74. doi:10.1113/jphysiol.1955.sp005412. PMC 1363415. PMID 13278905.
- ^ Llinas R, Terzuolo CA (tháng 3 năm 1965). “Mechanisms of Supraspinal Actions Upon Spinal Cord Activities. Reticular Inhibitory Mechanisms Upon Flexor Motoneurons”. Journal of Neurophysiology. 28 (2): 413–22. doi:10.1152/jn.1965.28.2.413. PMID 14283063.
- ^ Thompson SM, Gähwiler BH (tháng 3 năm 1989). “Activity-dependent disinhibition. I. Repetitive stimulation reduces IPSP driving force and conductance in the hippocampus in vitro”. Journal of Neurophysiology. 61 (3): 501–11. doi:10.1152/jn.1989.61.3.501. PMID 2709096.
- ^ Levy M, Koeppen B, Stanton B (2005). Berne & Levy principles of physiology (ấn bản 4). Elsevier Mosby. ISBN 978-0-8089-2321-3.
- ^ Chavas J, Marty A (tháng 3 năm 2003). “Coexistence of excitatory and inhibitory GABA synapses in the cerebellar interneuron network”. The Journal of Neuroscience. 23 (6): 2019–31. doi:10.1523/JNEUROSCI.23-06-02019.2003. PMC 6742031. PMID 12657660.
- ^ a b c d e Kandel ER, Schwartz JH, Jessell TM, Siegelbaum SA, Hudspeth AJ (2013). Principles of Neural Science (ấn bản 5). Manhattan, New York City: McGraw–Hill Companies. ISBN 9780071390118.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- ^ “Medical Definition of GENERATOR POTENTIAL”. Truy cập 24 tháng 7 năm 2023.
- ^ Faber DS, Pereda AE (21 tháng 11 năm 2018). “Two Forms of Electrical Transmission Between Neurons”. Frontiers in Molecular Neuroscience. 11: 427. doi:10.3389/fnmol.2018.00427. PMC 6276723. PMID 30534051.
- ^ Vermeulen, A; Rospars, J. P. (1998). “Dendritic integration in olfactory sensory neurons: A steady-state analysis of how the neuron structure and neuron environment influence the coding of odor intensity”. Journal of Computational Neuroscience. 5 (3): 243–66. doi:10.1023/A:1008826827728. PMID 9663551. S2CID 19598225.
- ^ Saladin, Kenneth (2012). Anatomy & physiology : the unity of form and function (ấn bản 6). McGraw-Hill. tr. 593. ISBN 978-0073378251.
- ^ McEwen, D. P (2008). “Olfactory cilia: our direct neuronal connection to the external world”. Curr. Top. Dev. Biol. Current Topics in Developmental Biology. 85: 333–370. doi:10.1016/S0070-2153(08)00812-0. ISBN 9780123744531. PMID 19147011.
- ^ Bushdid, C.; Magnasco, M. O.; Vosshall, L. B.; Keller, A. (2014). “Humans Can Discriminate More than 1 Trillion Olfactory Stimuli”. Science. 343 (6177): 1370–2. Bibcode:2014Sci...343.1370B. doi:10.1126/science.1249168. PMC 4483192. PMID 24653035.
- ^ Paré, Michel; Joseph E. Mazurkiewicz; Allan M. Smith; Frank L. Rice (15 tháng 9 năm 2001). “The Meissner Corpuscle Revised: A Multiafferented Mechanoreceptor with Nociceptor Immunochemical Properties”. The Journal of Neuroscience. 21 (18): 7236–46. doi:10.1523/JNEUROSCI.21-18-07236.2001. PMC 6763005. PMID 11549734.
- ^ Cauna, Nikolajs; Ross, Leonard L. (1 tháng 10 năm 1960). “The fine structure of Meissner's touch corpuscles of human fingers”. The Journal of Cell Biology. 8 (2): 467–82. doi:10.1083/jcb.8.2.467. PMC 2224947. PMID 13691669.
- ^ Hoffmann, Joscelyn N.; Montag, Anthony G.; Dominy, Nathaniel J. (tháng 11 năm 2004). “Meissner corpuscles and somatosensory acuity: the prehensile appendages of primates and elephants”. The Anatomical Record Part A: Discoveries in Molecular, Cellular, and Evolutionary Biology. 281 (1): 1138–47. doi:10.1002/ar.a.20119. PMID 15470674.
- ^ Martini / Bartholomew (2010) [1995]. Essentials of Anatomy and Physiology 3E. Pearson Benjamin Cummings. Bản gốc lưu trữ ngày 3 tháng 4 năm 2012. Truy cập ngày 22 tháng 9 năm 2021.
- ^ Afifi, Adel K.; Ronald Arly Bergman (2005) [1998]. Functional neuroanatomy: text and atlas. McGraw-Hill Professional. tr. 16. doi:10.1036/0071408126. ISBN 978-0-07-001589-0. 10.1036/0071408126.
- ^ “Nervous system - Touch”. BBC. Truy cập ngày 7 tháng 5 năm 2010.
- ^ Gilman S (2002). “Joint position sense and vibration sense: anatomical organisation and assessment”. Journal of Neurology, Neurosurgery, and Psychiatry. 73 (5): 473–477. doi:10.1136/jnnp.73.5.473. PMC 1738112. PMID 12397137.
- ^ McPherson, Duane (18 tháng 6 năm 2018). “Sensory Hair Cells: An Introduction to Structure and Physiology”. Integrative and Comparative Biology. 58 (2): 282–300. doi:10.1093/icb/icy064. PMC 6104712. PMID 29917041.
- ^ Schlosser, Gerhard (1 tháng 6 năm 2018). “A Short History of Nearly Every Sense—The Evolutionary History of Vertebrate Sensory Cell Types”. Integrative and Comparative Biology. 58 (2): 301–316. doi:10.1093/icb/icy024. PMID 29741623.
- ^ Swalla, Billie (20 tháng 6 năm 2018). “High Time for Hair Cells: An Introduction to the Symposium on Sensory Hair Cells”. Integrative and Comparative Biology. 58 (2): 276–281. doi:10.1093/icb/icy070. PMC 6104703. PMID 30137315.
- ^ Rémy Pujol, Régis Nouvian, Marc Lenoir, "Hair cells (cochlea.eu)
- ^ Müller, U (tháng 10 năm 2008). “Cadherins and mechanotransduction by hair cells”. Current Opinion in Cell Biology. 20 (5): 557–566. doi:10.1016/j.ceb.2008.06.004. PMC 2692626. PMID 18619539.
- ^ Plack, C. J. (2014). The Sense of Hearing. Psychology Press Ltd. ISBN 978-1848725157.
- ^ Kung C. (4 tháng 8 năm 2005). “A possible unifying principle for mechanosensation”. Nature. 436 (7051): 647–654. Bibcode:2005Natur.436..647K. doi:10.1038/nature03896. PMID 16079835. S2CID 4374012.
- ^ Peng, AW.; Salles, FT.; Pan, B.; Ricci, AJ. (2011). “Integrating the biophysical and molecular mechanisms of auditory hair cell mechanotransduction”. Nat Commun. 2: 523. Bibcode:2011NatCo...2..523P. doi:10.1038/ncomms1533. PMC 3418221. PMID 22045002.
- ^ Trịnh Bỉnh Duy (2005). Sinh Lý Học tập II (ấn bản 2). Quận Ba Đình, TP Hà Nội: Nhà xuất bản y học.
- ^ Kevin S. LaBar; Purves, Dale; Elizabeth M. Brannon; Cabeza, Roberto; Huettel, Scott A. (2007). Principles of Cognitive Neuroscience. Sunderland, Mass: Sinauer Associates Inc. tr. 253. ISBN 0-87893-694-7.
- ^ Bloomfield Stewart A.; Dacheux Ramon F. (2001). “Rod Vision: Pathways and Processing in the Mammalian Retina”. Progress in Retinal and Eye Research. 20 (3): 351–384. doi:10.1016/S1350-9462(00)00031-8.
- ^ “Ionic conductances underlying excitability in tonically firing retinal ganglion cells of adult rat”.
- ^ Henne J, Pöttering S, Jeserich G (tháng 12 năm 2000). “Voltage-gated potassium channels in retinal ganglion cells of trout: a combined biophysical, pharmacological, and single-cell RT-PCR approach”. Journal of Neuroscience Research. 62 (5): 629–37. doi:10.1002/1097-4547(20001201)62:5<629::AID-JNR2>3.0.CO;2-X. PMID 11104501.
- ^ Henne J, Jeserich G (tháng 1 năm 2004). “Maturation of spiking activity in trout retinal ganglion cells coincides with upregulation of Kv3.1- and BK-related potassium channels”. Journal of Neuroscience Research. 75 (1): 44–54. doi:10.1002/jnr.10830. PMID 14689447.
- ^ NOBLE D (5 tháng 11 năm 1960). “Cardiac action and pacemaker potentials based on the Hodgkin-Huxley equations”. Nature. 188: 495–497. doi:10.1038/188495b0. PMID 13729365.
- ^ Wagenaar, Daniel; Jerome Pine; Steve M. Potter (7 tháng 2 năm 2006). “An extremely rich repertoire of bursting patterns during the development of cortical cultures”. BMC Neuroscience. 7: 11. doi:10.1186/1471-2202-7-11. PMC 1420316. PMID 16464257.
- ^ Cooper, D (2002). “The significance of action potential bursting in the brain reward circuit”. Neurochemistry International. 41 (5): 333–340. doi:10.1016/S0197-0186(02)00068-2. PMID 12176075. S2CID 22492183.
- ^ Jeffreys, JGR; HL Hass (2 tháng 12 năm 1982). “Synchronized bursting of CA1 hippocampal pyramidal cells in the absence of synaptic transmission”. Letters to Nature. 300 (5891): 448–450. Bibcode:1982Natur.300..448J. doi:10.1038/300448a0. PMID 6292731. S2CID 2767619.
- ^ Smith, JC; HH Ellenberger; K Ballanyi; DW Richter; JL Feldman (tháng 11 năm 1991). “Pre-Botzinger complex: a brainstem region that may generate respiratory rhythm in mammals”. Science. 254 (5032): 726–729. Bibcode:1991Sci...254..726S. doi:10.1126/science.1683005. PMC 3209964. PMID 1683005.
- ^ Bullock, Orkland, and Grinnell, pp. 160–64.
- ^ Hodgkin AL (1937). “Evidence for electrical transmission in nerve, Part I”. Journal of Physiology. 90: 183–210.
* Hodgkin AL (1937). “Evidence for electrical transmission in nerve, Part II”. Journal of Physiology. 90: 211–32. - ^ Stevens, pp. 19–20.
- ^ Stevens, pp. 21–23.
- ^ Bullock, Orkand, and Grinnell, pp. 161–164.
- ^ Bullock, Orkand, and Grinnell, p. 509.
- ^ Zalc B (2006). “The acquisition of myelin: a success story”. Novartis Found. Symp. 276: 15–21, discussion 21–5, 54–7, 275–81. PMID 16805421.
- ^ Simons M, Trotter J (tháng 10 năm 2007). “Wrapping it up: the cell biology of myelination”. Curr. Opin. Neurobiol. 17 (5): 533–40. doi:10.1016/j.conb.2007.08.003. PMID 17923405.
- ^ Xu K, Terakawa S (tháng 8 năm 1999). “Fenestration nodes and the wide submyelinic space form the basis for the unusually fast impulse conduction of shrimp myelinated axons”. J. Exp. Biol. 202 (Pt 15): 1979–89. PMID 10395528. Bản gốc lưu trữ ngày 24 tháng 3 năm 2020. Truy cập ngày 29 tháng 3 năm 2020.
- ^ a b Hursh JB (1939). “Conduction velocity and diameter of nerve fibers”. American Journal of Physiology. 127: 131–39.
- ^ Lillie RS (1925). “Factors affecting transmission and recovery in passive iron nerve model”. J. Gen. Physiol. 7: 473–507. See also Keynes and Aidley, p. 78.
- ^ Tasaki I (1939). “Electro-saltatory transmission of nerve impulse and effect of narcosis upon nerve fiber”. Amer. J. Physiol. 127: 211–27.
- ^ Tasaki I, Takeuchi T (1941). “Der am Ranvierschen Knoten entstehende Aktionsstrom und seine Bedeutung für die Erregungsleitung”. Pflüger's Arch. ges. Physiol. 244: 696–711.
* Tasaki I, Takeuchi T (1942). “Weitere Studien über den Aktionsstrom der markhaltigen Nervenfaser und über die elektrosaltatorische Übertragung des nervenimpulses”. Pflüger's Arch. ges. Physiol. 245: 764–82.
* Tasaki I (1959). J Field, HW Magoun, VC Hall (biên tập). Handbook of Physiology: Neurophysiology . Washington, D.C.: American Physiological Society. tr. 75–121.Quản lý CS1: nhiều tên: danh sách biên tập viên (liên kết) - ^ Huxley A, Stämpfli R (1949). “Evidence for saltatory conduction in peripheral myelinated nerve-fibers”. Journal of Physiology. 108: 315–39.
* Huxley A, Stämpfli R (1949). “Direct determination of membrane resting potential and action potential in single myelinated nerve fibers”. Journal of Physiology. 112: 476–95. - ^ a b Hartline DK, Colman DR (2007). “Rapid conduction and the evolution of giant axons and myelinated fibers”. Curr. Biol. 17 (1): R29–R35. doi:10.1016/j.cub.2006.11.042. PMID 17208176.
- ^ Schmidt-Nielsen, Figure 12.13.
- ^ Rushton WAH (1951). “A theory of the effects of fibre size in the medullated nerve”. Journal of Physiology. 115: 101–22.
- ^ Bullock, Orkland, and Grinnell, p. 163.
- ^ Miller RH, Mi S (2007). “Dissecting demyelination”. Nat. Neurosci. 10 (11): 1351–54. doi:10.1038/nn1995. PMID 17965654.
- ^ Waxman SG (2007). “Multiple Sclerosis as a Neurodegenerative Disease”. Trong Waxman SG (biên tập). Molecular Neurology. Burlington, MA: Elsevier Academic Press. tr. 333–46. ISBN 978-0-12-369509-3.
- ^ Compston A, Coles A (tháng 10 năm 2008). “Multiple sclerosis”. Lancet. 372 (9648): 1502–17. doi:10.1016/S0140-6736(08)61620-7. PMID 18970977. S2CID 195686659.
- ^ Compston A, Coles A (tháng 4 năm 2002). “Multiple sclerosis”. Lancet. 359 (9313): 1221–31. doi:10.1016/S0140-6736(02)08220-X. PMID 11955556. S2CID 14207583.
- ^ Murray ED, Buttner EA, Price BH (2012). Daroff R, Fenichel G, Jankovic J, Mazziotta J (biên tập). Bradley's neurology in clinical practice (ấn bản 6). Philadelphia, PA: Elsevier/Saunders. ISBN 978-1-4377-0434-1.
- ^ Piryonesi SM, Rostampour S, Piryonesi SA (tháng 1 năm 2021). “Predicting falls and injuries in people with multiple sclerosis using machine learning algorithms”. Multiple Sclerosis and Related Disorders. 49: 102740. doi:10.1016/j.msard.2021.102740. PMID 33450500. S2CID 231624230.
- ^ Mazumder R, Murchison C, Bourdette D, Cameron M (25 tháng 9 năm 2014). “Falls in people with multiple sclerosis compared with falls in healthy controls”. PLOS ONE. 9 (9): e107620. Bibcode:2014PLoSO...9j7620M. doi:10.1371/journal.pone.0107620. PMC 4177842. PMID 25254633.
- ^ a b Rall, W in Koch & Segev 1989, Cable Theory for Dendritic Neurons, pp. 9–62.
- ^ Segev I, Fleshman JW, Burke RE (1989). “Compartmental Models of Complex Neurons”. Trong Koch C, Segev I (biên tập). Methods in Neuronal Modeling: From Synapses to Networks. Cambridge, Massachusetts: The MIT Press. tr. 63–96. ISBN 978-0-262-11133-1. LCCN 88008279. OCLC 18384545.
- ^ Purves và đồng nghiệp 2008, tr. 52–53.
- ^ a b c d e Sanes DH, Reh TA (1 tháng 1 năm 2012). Development of the nervous system . Elsevier Academic Press. tr. 211–214. ISBN 9780080923208. OCLC 762720374.
- ^ Partridge D (1991). Calcium Channels: Their Properties, Functions, Regulation, and Clinical relevance. CRC Press. tr. 138–142. ISBN 9780849388071.
- ^ Black I (1984). Cellular and Molecular Biology of Neuronal Development | Ira Black | Springer (bằng tiếng Anh). Springer. tr. 103. ISBN 978-1-4613-2717-2. Lưu trữ bản gốc 17 tháng Bảy năm 2017.
- ^ Pedersen R (1998). Current Topics in Developmental Biology, Volume 39. Elsevier Academic Press. ISBN 9780080584621.
- ^ Ganong 1991, tr. 59–60.
- ^ Tandon, Prakash N (1 tháng 7 năm 2019). “Jagdish Chandra Bose and Plant Neurobiology: Part I” (PDF). Indian Journal of History of Science. 54 (2). doi:10.16943/ijhs/2019/v54i2/49660. ISSN 0019-5235.
- ^ Felle HH, Zimmermann MR (tháng 6 năm 2007). “Systemic signalling in barley through action potentials”. Planta. 226 (1): 203–14. doi:10.1007/s00425-006-0458-y. PMID 17226028. S2CID 5059716.
- ^ Luken JO (tháng 12 năm 2005). “Habitats of Dionaea muscipula (Venus' Fly Trap), Droseraceae, Associated with Carolina Bays”. Southeastern Naturalist (bằng tiếng Anh). 4 (4): 573–584. doi:10.1656/1528-7092(2005)004[0573:HODMVF]2.0.CO;2. ISSN 1528-7092. S2CID 9246114.
- ^ a b Böhm J, Scherzer S, Krol E, Kreuzer I, von Meyer K, Lorey C, và đồng nghiệp (tháng 2 năm 2016). “The Venus Flytrap Dionaea muscipula Counts Prey-Induced Action Potentials to Induce Sodium Uptake”. Current Biology. 26 (3): 286–95. doi:10.1016/j.cub.2015.11.057. PMC 4751343. PMID 26804557.
- ^ a b c d e Hedrich R, Neher E (tháng 3 năm 2018). “Venus Flytrap: How an Excitable, Carnivorous Plant Works”. Trends in Plant Science. 23 (3): 220–234. doi:10.1016/j.tplants.2017.12.004. PMID 29336976.
- ^ Purves D, Augustine GJ, Fitzpatrick D, et al., editors. Neuroscience. 2nd edition. Sunderland (MA): Sinauer Associates; 2001. Electrical Potentials Across Nerve Cell Membranes.Available from:
- ^ Volkov AG, Adesina T, Jovanov E (tháng 5 năm 2007). “Closing of venus flytrap by electrical stimulation of motor cells”. Plant Signaling & Behavior. 2 (3): 139–45. doi:10.4161/psb.2.3.4217. PMC 2634039. PMID 19516982.
- ^ Gradmann, D; Mummert, H in Spanswick, Lucas & Dainty 1980, Plant action potentials, pp. 333–344.
- ^ Opritov, V A, et al. "Direct Coupling of Action Potential Generation in Cells of a Higher Plant (Cucurbita Pepo) with the Operation of an Electrogenic Pump." Russian Journal of Plant Physiology, vol. 49, no. 1, 2002, pp. 142–147.
- ^ Bullock TH, Horridge GA (1965). Structure and Function in the Nervous Systems of Invertebrates. San Francisco: W. H. Freeman. line feed character trong
|title=tại ký tự số 38 (trợ giúp) - ^ Kristan WB (tháng 10 năm 2016). “Early evolution of neurons”. Current Biology. 26 (20): R949–R954. doi:10.1016/j.cub.2016.05.030. PMID 27780067.
- ^ Junge 1981, tr. 63–82.
- ^ Kettenmann & Grantyn 1992.
- ^ Snell, FM in Lavallée, Schanne & Hébert 1969, Some Electrical Properties of Fine-Tipped Pipette Microelectrodes.
- ^ Brazier 1961; McHenry & Garrison 1969; Worden, Swazey & Adelman 1975.
- ^ Finkelstein GW (2013). Emil du Bois-Reymond : neuroscience, self, and society in nineteenth-century Germany. Cambridge, Massachusetts. ISBN 9781461950325. OCLC 864592470.
- ^ Olesko, Kathryn M., and Frederic L. Holmes. "Experiment, Quantification and Discovery: Helmholtz's Early Physiological Researches, 1843-50". In Hermann von Helmholtz and the Foundations of Nineteenth Century Science, ed. David Cahan, 50-108. Berkeley; Los Angeles; London: University of California, 1994.
- ^ Bernstein 1912.
- ^ Baranauskas G, Martina M (tháng 1 năm 2006). “Sodium currents activate without a Hodgkin-and-Huxley-type delay in central mammalian neurons”. The Journal of Neuroscience. 26 (2): 671–84. doi:10.1523/jneurosci.2283-05.2006. PMC 6674426. PMID 16407565.
- ^ Hoppensteadt 1986.
- ^ Sato, S; Fukai, H; Nomura, T; Doi, S in Reeke và đồng nghiệp 2005, Bifurcation Analysis of the Hodgkin-Huxley Equations, pp. 459–478.
- FitzHugh, R in Schwann 1969, Mathematical models of axcitation and propagation in nerve, pp. 12–16.
- Guckenheimer & Holmes 1986, tr. 12–16
- ^ Nelson, ME; Rinzel, J in Bower & Beeman 1995, The Hodgkin-Huxley Model, pp. 29–49.
- Rinzel, J & Ermentrout, GB; in Koch & Segev 1989, Analysis of Neural Excitability and Oscillations, pp. 135–169.
- ^ McCulloch 1988, tr. 19–39, 46–66, 72–141; Anderson & Rosenfeld 1988, tr. 15–41.
- ^ Getting, PA in Koch & Segev 1989, Reconstruction of Small Neural Networks, pp. 171–194.
Bài báo khoa học[sửa | sửa mã nguồn]
- ^ Hodgkin AL, Rushton WA (tháng 12 năm 1946). “The electrical constants of a crustacean nerve fibre”. Proceedings of the Royal Society of Medicine. 134 (873): 444–79. Bibcode:1946RSPSB.133..444H. doi:10.1098/rspb.1946.0024. PMID 20281590.
- ^ Süudhof TC (2008). “Neurotransmitter release”. Pharmacology of Neurotransmitter Release. Handbook of Experimental Pharmacology. 184. tr. 1–21. doi:10.1007/978-3-540-74805-2_1. ISBN 978-3-540-74804-5. PMID 18064409.
- ^ Rusakov DA (tháng 8 năm 2006). “Ca2+-dependent mechanisms of presynaptic control at central synapses”. The Neuroscientist. 12 (4): 317–26. doi:10.1177/1073858405284672. PMC 2684670. PMID 16840708.
- ^ Humeau Y, Doussau F, Grant NJ, Poulain B (tháng 5 năm 2000). “How botulinum and tetanus neurotoxins block neurotransmitter release”. Biochimie. 82 (5): 427–46. doi:10.1016/S0300-9084(00)00216-9. PMID 10865130.
- ^ Zoidl G, Dermietzel R (tháng 11 năm 2002). “On the search for the electrical synapse: a glimpse at the future”. Cell and Tissue Research. 310 (2): 137–42. doi:10.1007/s00441-002-0632-x. PMID 12397368. S2CID 22414506.
- ^ Brink PR, Cronin K, Ramanan SV (tháng 8 năm 1996). “Gap junctions in excitable cells”. Journal of Bioenergetics and Biomembranes. 28 (4): 351–8. doi:10.1007/BF02110111. PMID 8844332. S2CID 46371790.
- ^ Hirsch NP (tháng 7 năm 2007). “Neuromuscular junction in health and disease”. British Journal of Anaesthesia. 99 (1): 132–8. doi:10.1093/bja/aem144. PMID 17573397.
- ^ Hughes BW, Kusner LL, Kaminski HJ (tháng 4 năm 2006). “Molecular architecture of the neuromuscular junction”. Muscle & Nerve. 33 (4): 445–61. doi:10.1002/mus.20440. PMID 16228970. S2CID 1888352.
- ^ Newmark J (tháng 1 năm 2007). “Nerve agents”. The Neurologist. 13 (1): 20–32. doi:10.1097/01.nrl.0000252923.04894.53. PMID 17215724. S2CID 211234081.
- ^ Costa LG (tháng 4 năm 2006). “Current issues in organophosphate toxicology”. Clinica Chimica Acta; International Journal of Clinical Chemistry. 366 (1–2): 1–13. doi:10.1016/j.cca.2005.10.008. PMID 16337171.
- ^ Kléber AG, Rudy Y (tháng 4 năm 2004). “Basic mechanisms of cardiac impulse propagation and associated arrhythmias”. Physiological Reviews. 84 (2): 431–88. doi:10.1152/physrev.00025.2003. PMID 15044680. S2CID 21823003.
- ^ Kléber AG, Rudy Y (tháng 4 năm 2004). “Basic mechanisms of cardiac impulse propagation and associated arrhythmias”. Physiological Reviews. 84 (2): 431–88. doi:10.1152/physrev.00025.2003. PMID 15044680. S2CID 21823003.
- ^ Kléber AG, Rudy Y (tháng 4 năm 2004). “Basic mechanisms of cardiac impulse propagation and associated arrhythmias”. Physiological Reviews. 84 (2): 431–88. doi:10.1152/physrev.00025.2003. PMID 15044680. S2CID 21823003.
- ^ Tamargo J, Caballero R, Delpón E (tháng 1 năm 2004). “Pharmacological approaches in the treatment of atrial fibrillation”. Current Medicinal Chemistry. 11 (1): 13–28. doi:10.2174/0929867043456241. PMID 14754423.
- ^ Newmark J (tháng 1 năm 2007). “Nerve agents”. The Neurologist. 13 (1): 20–32. doi:10.1097/01.nrl.0000252923.04894.53. PMID 17215724. S2CID 211234081.
- ^ Slayman CL, Long WS, Gradmann D (tháng 4 năm 1976). “"Action potentials" in Neurospora crassa, a mycelial fungus”. Biochimica et Biophysica Acta (BBA) - Biomembranes. 426 (4): 732–44. doi:10.1016/0005-2736(76)90138-3. PMID 130926.
- ^ Mummert H, Gradmann D (tháng 12 năm 1991). “Action potentials in Acetabularia: measurement and simulation of voltage-gated fluxes”. The Journal of Membrane Biology. 124 (3): 265–73. doi:10.1007/BF01994359. PMID 1664861. S2CID 22063907.
- ^ Gradmann D (2001). “Models for oscillations in plants”. Aust. J. Plant Physiol. 28 (7): 577–590. doi:10.1071/pp01017.
- ^ Beilby MJ (2007). Action potential in charophytes. International Review of Cytology. 257. tr. 43–82. doi:10.1016/S0074-7696(07)57002-6. ISBN 978-0-12-373701-4. PMID 17280895.
- ^ Gradmann D, Hoffstadt J (tháng 11 năm 1998). “Electrocoupling of ion transporters in plants: interaction with internal ion concentrations”. The Journal of Membrane Biology. 166 (1): 51–9. doi:10.1007/s002329900446. PMID 9784585. S2CID 24190001.
- ^ Leys SP, Mackie GO, Meech RW (tháng 5 năm 1999). “Impulse conduction in a sponge”. The Journal of Experimental Biology. 202 (Pt 9) (9): 1139–50. doi:10.1242/jeb.202.9.1139. PMID 10101111.
- ^ Keynes RD (1989). “The role of giant axons in studies of the nerve impulse”. BioEssays. 10 (2–3): 90–3. doi:10.1002/bies.950100213. PMID 2541698.
- ^ Hodgkin AL, Huxley AF, Katz B (tháng 4 năm 1952). “Measurement of current-voltage relations in the membrane of the giant axon of Loligo”. The Journal of Physiology. 116 (4): 424–48. doi:10.1113/jphysiol.1952.sp004716. PMC 1392219. PMID 14946712.* Hodgkin AL, Huxley AF (tháng 4 năm 1952). “Currents carried by sodium and potassium ions through the membrane of the giant axon of Loligo”. The Journal of Physiology. 116 (4): 449–72. doi:10.1113/jphysiol.1952.sp004717. PMC 1392213. PMID 14946713.
- Hodgkin AL, Huxley AF (tháng 4 năm 1952). “The components of membrane conductance in the giant axon of Loligo”. The Journal of Physiology. 116 (4): 473–96. doi:10.1113/jphysiol.1952.sp004718. PMC 1392209. PMID 14946714.
- Hodgkin AL, Huxley AF (tháng 4 năm 1952). “The dual effect of membrane potential on sodium conductance in the giant axon of Loligo”. The Journal of Physiology. 116 (4): 497–506. doi:10.1113/jphysiol.1952.sp004719. PMC 1392212. PMID 14946715.
- Hodgkin AL, Huxley AF (tháng 8 năm 1952). “A quantitative description of membrane current and its application to conduction and excitation in nerve”. The Journal of Physiology. 117 (4): 500–44. doi:10.1113/jphysiol.1952.sp004764. PMC 1392413. PMID 12991237.
- ^ Meunier C, Segev I (tháng 11 năm 2002). “Playing the devil's advocate: is the Hodgkin-Huxley model useful?”. Trends in Neurosciences. 25 (11): 558–63. doi:10.1016/S0166-2236(02)02278-6. PMID 12392930. S2CID 1355280.
- ^ Cole KS (1949). “Dynamic electrical characteristics of the squid axon membrane”. Arch. Sci. Physiol. 3: 253–8.
- ^ Ling G, Gerard RW (tháng 12 năm 1949). “The normal membrane potential of frog sartorius fibers”. Journal of Cellular and Comparative Physiology. 34 (3): 383–96. doi:10.1002/jcp.1030340304. PMID 15410483.
- ^ Nastuk WL, Hodgkin A (1950). “The electrical activity of single muscle fibers”. Journal of Cellular and Comparative Physiology. 35: 39–73. doi:10.1002/jcp.1030350105.
- ^ Brock LG, Coombs JS, Eccles JC (tháng 8 năm 1952). “The recording of potentials from motoneurones with an intracellular electrode”. The Journal of Physiology. 117 (4): 431–60. doi:10.1113/jphysiol.1952.sp004759. PMC 1392415. PMID 12991232.
- ^ Ross WN, Salzberg BM, Cohen LB, Davila HV (tháng 12 năm 1974). “A large change in dye absorption during the action potential”. Biophysical Journal. 14 (12): 983–6. Bibcode:1974BpJ....14..983R. doi:10.1016/S0006-3495(74)85963-1. PMC 1334592. PMID 4429774.* Grynkiewicz G, Poenie M, Tsien RY (tháng 3 năm 1985). “A new generation of Ca2+ indicators with greatly improved fluorescence properties”. The Journal of Biological Chemistry. 260 (6): 3440–50. doi:10.1016/S0021-9258(19)83641-4. PMID 3838314.
- ^ Milligan JV, Edwards C (tháng 7 năm 1965). “Some factors affecting the time course of the recovery of contracture ability following a potassium contracture in frog striated muscle”. The Journal of General Physiology. 48 (6): 975–83. doi:10.1085/jgp.48.6.975. PMC 2195447. PMID 5855511.* Ritchie JM, Rogart RB (1977). “The binding of saxitoxin and tetrodotoxin to excitable tissue”. Reviews of Physiology, Biochemistry and Pharmacology, Volume 79. Reviews of Physiology, Biochemistry and Pharmacology. 79. tr. 1–50. doi:10.1007/BFb0037088. ISBN 0-387-08326-X. PMID 335473.
- Keynes RD, Ritchie JM (tháng 8 năm 1984). “On the binding of labelled saxitoxin to the squid giant axon”. Proceedings of the Royal Society of London. Series B, Biological Sciences. 222 (1227): 147–53. Bibcode:1984RSPSB.222..147K. doi:10.1098/rspb.1984.0055. PMID 6148754. S2CID 11465181.
- ^ Piccolino M (tháng 10 năm 1997). “Luigi Galvani and animal electricity: two centuries after the foundation of electrophysiology”. Trends in Neurosciences. 20 (10): 443–8. doi:10.1016/S0166-2236(97)01101-6. PMID 9347609. S2CID 23394494.
- ^ Piccolino M (tháng 4 năm 2000). “The bicentennial of the Voltaic battery (1800-2000): the artificial electric organ”. Trends in Neurosciences. 23 (4): 147–51. doi:10.1016/S0166-2236(99)01544-1. PMID 10717671. S2CID 393323.
- ^ Bernstein J (1902). “Untersuchungen zur Thermodynamik der bioelektrischen Ströme”. Pflügers Archiv für die gesamte Physiologie. 92 (10–12): 521–562. doi:10.1007/BF01790181. S2CID 33229139.
- ^ Cole KS, Curtis HJ (tháng 5 năm 1939). “Electric Impedance of the Squid Giant Axon During Activity”. The Journal of General Physiology. 22 (5): 649–70. doi:10.1085/jgp.22.5.649. PMC 2142006. PMID 19873125.
- ^ Hodgkin AL, Katz B (tháng 3 năm 1949). “The effect of sodium ions on the electrical activity of giant axon of the squid”. The Journal of Physiology. 108 (1): 37–77. doi:10.1113/jphysiol.1949.sp004310. PMC 1392331. PMID 18128147.
- ^ Hodgkin AL, Huxley AF, Katz B (tháng 4 năm 1952). “Measurement of current-voltage relations in the membrane of the giant axon of Loligo”. The Journal of Physiology. 116 (4): 424–48. doi:10.1113/jphysiol.1952.sp004716. PMC 1392219. PMID 14946712.* Hodgkin AL, Huxley AF (tháng 4 năm 1952). “Currents carried by sodium and potassium ions through the membrane of the giant axon of Loligo”. The Journal of Physiology. 116 (4): 449–72. doi:10.1113/jphysiol.1952.sp004717. PMC 1392213. PMID 14946713.
- Hodgkin AL, Huxley AF (tháng 4 năm 1952). “The components of membrane conductance in the giant axon of Loligo”. The Journal of Physiology. 116 (4): 473–96. doi:10.1113/jphysiol.1952.sp004718. PMC 1392209. PMID 14946714.
- Hodgkin AL, Huxley AF (tháng 4 năm 1952). “The dual effect of membrane potential on sodium conductance in the giant axon of Loligo”. The Journal of Physiology. 116 (4): 497–506. doi:10.1113/jphysiol.1952.sp004719. PMC 1392212. PMID 14946715.
- Hodgkin AL, Huxley AF (tháng 8 năm 1952). “A quantitative description of membrane current and its application to conduction and excitation in nerve”. The Journal of Physiology. 117 (4): 500–44. doi:10.1113/jphysiol.1952.sp004764. PMC 1392413. PMID 12991237.
- ^ Neher E, Sakmann B (tháng 4 năm 1976). “Single-channel currents recorded from membrane of denervated frog muscle fibres”. Nature. 260 (5554): 799–802. Bibcode:1976Natur.260..799N. doi:10.1038/260799a0. PMID 1083489. S2CID 4204985.* Hamill OP, Marty A, Neher E, Sakmann B, Sigworth FJ (tháng 8 năm 1981). “Improved patch-clamp techniques for high-resolution current recording from cells and cell-free membrane patches”. Pflügers Archiv. 391 (2): 85–100. doi:10.1007/BF00656997. PMID 6270629. S2CID 12014433.
- Neher E, Sakmann B (tháng 3 năm 1992). “The patch clamp technique”. Scientific American. 266 (3): 44–51. Bibcode:1992SciAm.266c..44N. doi:10.1038/scientificamerican0392-44. PMID 1374932.
- ^ Yellen G (tháng 9 năm 2002). “The voltage-gated potassium channels and their relatives”. Nature. 419 (6902): 35–42. Bibcode:2002Natur.419...35Y. doi:10.1038/nature00978. PMID 12214225. S2CID 4420877.
- ^ Doyle DA, Morais Cabral J, Pfuetzner RA, Kuo A, Gulbis JM, Cohen SL, và đồng nghiệp (tháng 4 năm 1998). “The structure of the potassium channel: molecular basis of K+ conduction and selectivity”. Science. 280 (5360): 69–77. Bibcode:1998Sci...280...69D. doi:10.1126/science.280.5360.69. PMID 9525859.* Zhou Y, Morais-Cabral JH, Kaufman A, MacKinnon R (tháng 11 năm 2001). “Chemistry of ion coordination and hydration revealed by a K+ channel-Fab complex at 2.0 A resolution”. Nature. 414 (6859): 43–8. Bibcode:2001Natur.414...43Z. doi:10.1038/35102009. PMID 11689936. S2CID 205022645.
- Jiang Y, Lee A, Chen J, Ruta V, Cadene M, Chait BT, MacKinnon R (tháng 5 năm 2003). “X-ray structure of a voltage-dependent K+ channel”. Nature. 423 (6935): 33–41. Bibcode:2003Natur.423...33J. doi:10.1038/nature01580. PMID 12721618. S2CID 4347957.
- ^ Cha A, Snyder GE, Selvin PR, Bezanilla F (tháng 12 năm 1999). “Atomic scale movement of the voltage-sensing region in a potassium channel measured via spectroscopy”. Nature. 402 (6763): 809–13. Bibcode:1999Natur.402..809C. doi:10.1038/45552. PMID 10617201. S2CID 4353978.* Glauner KS, Mannuzzu LM, Gandhi CS, Isacoff EY (tháng 12 năm 1999). “Spectroscopic mapping of voltage sensor movement in the Shaker potassium channel”. Nature. 402 (6763): 813–7. Bibcode:1999Natur.402..813G. doi:10.1038/45561. PMID 10617202. S2CID 4417476.
- Bezanilla F (tháng 4 năm 2000). “The voltage sensor in voltage-dependent ion channels”. Physiological Reviews. 80 (2): 555–92. doi:10.1152/physrev.2000.80.2.555. PMID 10747201. S2CID 18629998.
- ^ Catterall WA (tháng 2 năm 2001). “A 3D view of sodium channels”. Nature. 409 (6823): 988–9, 991. Bibcode:2001Natur.409..988C. doi:10.1038/35059188. PMID 11234048. S2CID 4371677.* Sato C, Ueno Y, Asai K, Takahashi K, Sato M, Engel A, Fujiyoshi Y (tháng 2 năm 2001). “The voltage-sensitive sodium channel is a bell-shaped molecule with several cavities”. Nature. 409 (6823): 1047–51. Bibcode:2001Natur.409.1047S. doi:10.1038/35059098. PMID 11234014. S2CID 4430165.
- ^ Goldman DE (tháng 9 năm 1943). “Potential, Impedance, and Rectification in Membranes”. The Journal of General Physiology. 27 (1): 37–60. doi:10.1085/jgp.27.1.37. PMC 2142582. PMID 19873371.
- ^ Skou JC (tháng 2 năm 1957). “The influence of some cations on an adenosine triphosphatase from peripheral nerves”. Biochimica et Biophysica Acta. 23 (2): 394–401. doi:10.1016/0006-3002(57)90343-8. PMID 13412736. S2CID 32516710.
- ^ Hodgkin AL, Keynes RD (tháng 4 năm 1955). “Active transport of cations in giant axons from Sepia and Loligo”. The Journal of Physiology. 128 (1): 28–60. doi:10.1113/jphysiol.1955.sp005290. PMC 1365754. PMID 14368574.
- ^ Caldwell PC, Hodgkin AL, Keynes RD, Shaw TL (tháng 7 năm 1960). “The effects of injecting 'energy-rich' phosphate compounds on the active transport of ions in the giant axons of Loligo”. The Journal of Physiology. 152 (3): 561–90. doi:10.1113/jphysiol.1960.sp006509. PMC 1363339. PMID 13806926.
- ^ Caldwell PC, Keynes RD (tháng 6 năm 1957). “The utilization of phosphate bond energy for sodium extrusion from giant axons”. The Journal of Physiology. 137 (1): 12–3P. doi:10.1113/jphysiol.1957.sp005830. PMID 13439598. S2CID 222188054.
- ^ Morth JP, Pedersen BP, Toustrup-Jensen MS, Sørensen TL, Petersen J, Andersen JP, và đồng nghiệp (tháng 12 năm 2007). “Crystal structure of the sodium-potassium pump”. Nature. 450 (7172): 1043–9. Bibcode:2007Natur.450.1043M. doi:10.1038/nature06419. PMID 18075585. S2CID 4344526.
- ^ Lee AG, East JM (tháng 6 năm 2001). “What the structure of a calcium pump tells us about its mechanism”. The Biochemical Journal. 356 (Pt 3): 665–83. doi:10.1042/0264-6021:3560665. PMC 1221895. PMID 11389676.
- ^ Hodgkin AL, Huxley AF, Katz B (tháng 4 năm 1952). “Measurement of current-voltage relations in the membrane of the giant axon of Loligo”. The Journal of Physiology. 116 (4): 424–48. doi:10.1113/jphysiol.1952.sp004716. PMC 1392219. PMID 14946712.* Hodgkin AL, Huxley AF (tháng 4 năm 1952). “Currents carried by sodium and potassium ions through the membrane of the giant axon of Loligo”. The Journal of Physiology. 116 (4): 449–72. doi:10.1113/jphysiol.1952.sp004717. PMC 1392213. PMID 14946713.
- Hodgkin AL, Huxley AF (tháng 4 năm 1952). “The components of membrane conductance in the giant axon of Loligo”. The Journal of Physiology. 116 (4): 473–96. doi:10.1113/jphysiol.1952.sp004718. PMC 1392209. PMID 14946714.
- Hodgkin AL, Huxley AF (tháng 4 năm 1952). “The dual effect of membrane potential on sodium conductance in the giant axon of Loligo”. The Journal of Physiology. 116 (4): 497–506. doi:10.1113/jphysiol.1952.sp004719. PMC 1392212. PMID 14946715.
- Hodgkin AL, Huxley AF (tháng 8 năm 1952). “A quantitative description of membrane current and its application to conduction and excitation in nerve”. The Journal of Physiology. 117 (4): 500–44. doi:10.1113/jphysiol.1952.sp004764. PMC 1392413. PMID 12991237.
- ^ * Fitzhugh R (tháng 5 năm 1960). “Thresholds and plateaus in the Hodgkin-Huxley nerve equations”. The Journal of General Physiology. 43 (5): 867–96. doi:10.1085/jgp.43.5.867. PMC 2195039. PMID 13823315.* Kepler TB, Abbott LF, Marder E (1992). “Reduction of conductance-based neuron models”. Biological Cybernetics. 66 (5): 381–7. doi:10.1007/BF00197717. PMID 1562643. S2CID 6789007.
- ^ Morris C, Lecar H (tháng 7 năm 1981). “Voltage oscillations in the barnacle giant muscle fiber”. Biophysical Journal. 35 (1): 193–213. Bibcode:1981BpJ....35..193M. doi:10.1016/S0006-3495(81)84782-0. PMC 1327511. PMID 7260316.
- ^ Fitzhugh R (tháng 7 năm 1961). “Impulses and Physiological States in Theoretical Models of Nerve Membrane”. Biophysical Journal. 1 (6): 445–66. Bibcode:1961BpJ.....1..445F. doi:10.1016/S0006-3495(61)86902-6. PMC 1366333. PMID 19431309.* Nagumo J, Arimoto S, Yoshizawa S (1962). “An active pulse transmission line simulating nerve axon”. Proceedings of the IRE. 50 (10): 2061–2070. doi:10.1109/JRPROC.1962.288235. S2CID 51648050.
- ^ Bonhoeffer KF (tháng 9 năm 1948). “Activation of passive iron as a model for the excitation of nerve”. The Journal of General Physiology. 32 (1): 69–91. doi:10.1085/jgp.32.1.69. PMC 2213747. PMID 18885679.* Bonhoeffer KF (1953). “Modelle der Nervenerregung”. Naturwissenschaften. 40 (11): 301–311. Bibcode:1953NW.....40..301B. doi:10.1007/BF00632438. S2CID 19149460.
- Van der Pol B (1926). “On relaxation-oscillations”. Philosophical Magazine. 2: 977–992.
- Van der Pol B, Van der Mark J (1928). “The heartbeat considered as a relaxation oscillation, and an electrical model of the heart”. Philosophical Magazine. 6: 763–775. doi:10.1080/14786441108564652.
- Van der Pol B, van der Mark J (1929). “The heartbeat considered as a relaxation oscillation, and an electrical model of the heart”. Arch. Neerl. Physiol. 14: 418–443.
- ^ Evans JW (1972). “Nerve axon equations. I. Linear approximations”. Indiana Univ. Math. J. 21 (9): 877–885. doi:10.1512/iumj.1972.21.21071.* Evans JW, Feroe J (1977). “Local stability theory of the nerve impulse”. Math. Biosci. 37: 23–50. doi:10.1016/0025-5564(77)90076-1.
- ^ Keener JP (1983). “Analogue circuitry for the Van der Pol and FitzHugh-Nagumo equations”. IEEE Transactions on Systems, Man and Cybernetics. 13 (5): 1010–1014. doi:10.1109/TSMC.1983.6313098. S2CID 20077648.
- ^ Hooper SL (tháng 3 năm 2000). “Central pattern generators”. Current Biology. 10 (5): R176–R179. CiteSeerX 10.1.1.133.3378. doi:10.1016/S0960-9822(00)00367-5. PMID 10713861. S2CID 11388348.
Sách[sửa | sửa mã nguồn]
- Anderson JA, Rosenfeld E biên tập (1988). Neurocomputing: Foundations of Research. Cambridge, Massachusetts: The MIT Press. ISBN 978-0-262-01097-9. LCCN 87003022. OCLC 15860311.
- Bernstein J (1912). Elektrobiologie, die Lehre von den elektrischen Vorgängen im Organismus auf moderner Grundlage dargestellt [Electric Biology, the study of the electrical processes in the organism represented on a modern basis]. Braunschweig: Vieweg und Sohn. LCCN 12027986. OCLC 11358569.
- Bower JM, Beeman D (1995). The Book of GENESIS: Exploring Realistic Neural Models with the GEneral NEural SImulation System. Santa Clara, Calif.: TELOS. ISBN 978-0-387-94019-9. LCCN 94017624. OCLC 30518469.
- Brazier MA (1961). A History of the Electrical Activity of the Brain. London: Pitman. LCCN 62001407. OCLC 556863.
- Bullock TH, Horridge GA (1965). Structure and Function in the Nervous Systems of Invertebrates. A series of books in biology. San Francisco: W. H. Freeman. LCCN 65007965. OCLC 558128.
- Bullock TH, Orkand R, Grinnell A (1977). Introduction to Nervous Systems. A series of books in biology. San Francisco: W. H. Freeman. ISBN 978-0-7167-0030-2. LCCN 76003735. OCLC 2048177.
- Field J biên tập (1959). Handbook of Physiology: a Critical, Comprehensive Presentation of Physiological Knowledge and Concepts: Section 1: Neurophysiology. 1. Washington, DC: American Physiological Society. LCCN 60004587. OCLC 830755894.
- Ganong, WF (1991). Review of Medical Physiology. Ganong's Review of Medical Physiology (ấn bản 15). Norwalk, Conn.: Appleton and Lange. ISBN 978-0-8385-8418-7. ISSN 0892-1253. LCCN 87642343. OCLC 23761261.
- Guckenheimer J, Holmes P biên tập (1986). Nonlinear Oscillations, Dynamical Systems and Bifurcations of Vector Fields. Applied Mathematical Sciences. 42 (ấn bản 2). New York: Springer Verlag. ISBN 978-0-387-90819-9. OCLC 751129941.
- Hoppensteadt FC (1986). An Introduction to the Mathematics of Neurons. Cambridge studies in mathematical biology. 6. Cambridge: Cambridge University Press. ISBN 978-0-521-31574-6. LCCN 85011013. OCLC 12052275.
- Junge D (1981). Nerve and Muscle Excitation (ấn bản 2). Sunderland, Mass.: Sinauer Associates. ISBN 978-0-87893-410-2. LCCN 80018158. OCLC 6486925.
- Kettenmann H, Grantyn R biên tập (1992). Practical Electrophysiological Methods: A Guide for in Vitro Studies in Vertebrate Neurobiology. New York: Wiley. ISBN 978-0-471-56200-9. LCCN 92000179. OCLC 25204689.
- Keynes RD, Aidley DJ (1991). Nerve and Muscle (ấn bản 2). Cambridge: Cambridge University Press. ISBN 978-0-521-41042-7. LCCN 90015167. OCLC 25204483.
- Koch C, Segev I biên tập (1989). Methods in Neuronal Modeling: From Synapses to Networks. Cambridge, Massachusetts: The MIT Press. ISBN 978-0-262-11133-1. LCCN 88008279. OCLC 18384545.
- Lavallée M, Schanne OF, Hébert NC biên tập (1969). Glass Microelectrodes. New York: Wiley. ISBN 978-0-471-51885-3. LCCN 68009252. OCLC 686.
- McCulloch WS (1988). Embodiments of Mind. Cambridge, Massachusetts: The MIT Press. ISBN 978-0-262-63114-3. LCCN 88002987. OCLC 237280.
- McHenry LC, Garrison FH (1969). Garrison's History of Neurology. Springfield, Ill.: Charles C. Thomas. OCLC 429733931.
- Silverthorn DU (2010). Human Physiology: An Integrated Approach (ấn bản 5). San Francisco: Pearson. ISBN 978-0-321-55980-7. LCCN 2008050369. OCLC 268788623.
- Spanswick RM, Lucas WJ, Dainty J biên tập (1980). Plant Membrane Transport: Current Conceptual Issues. Developments in Plant Biology. 4. Amsterdam: Elsevier Biomedical Press. ISBN 978-0-444-80192-0. LCCN 79025719. OCLC 5799924.
- Purves D, Augustine GJ, Fitzpatrick D, Hall WC, Lamantia AS, McNamara JO, Williams SM (2001). “Release of Transmitters from Synaptic Vesicles”. Neuroscience (ấn bản 2). Sunderland, MA: Sinauer Associates. ISBN 978-0-87893-742-4. LCCN 00059496. OCLC 806472664.
- Purves D, Augustine GJ, Fitzpatrick D, Hall WC, Lamantia AS, McNamara JO, White LE (2008). Neuroscience (ấn bản 4). Sunderland, MA: Sinauer Associates. ISBN 978-0-87893-697-7. LCCN 2007024950. OCLC 144771764.
- Reeke GN, Poznanski RR, Sporns O, Rosenberg JR, Lindsay KA biên tập (2005). Modeling in the Neurosciences: from Biological Systems to Neuromimetic Robotics. Boca Raton, Fla.: Taylor & Francis. ISBN 978-0-415-32868-5. LCCN 2005298022. OCLC 489024131.
- Schmidt-Nielsen K (1997). Animal Physiology: Adaptation and Environment (ấn bản 5). Cambridge: Cambridge University Press. ISBN 978-0-521-57098-5. LCCN 96039295. OCLC 35744403.
- Schwann HP biên tập (1969). Biological Engineering. Inter-University Electronics Series. 9. New York: McGraw-Hill. ISBN 978-0-07-055734-5. LCCN 68027513. OCLC 51993.
- Stevens CF (1966). Neurophysiology: A Primer. New York: John Wiley and Sons. ISBN 9780471824367. LCCN 66015872. OCLC 1175605.
- Waxman SG biên tập (2007). Molecular Neurology. Burlington, Mass.: Elsevier Academic Press. ISBN 978-0-12-369509-3. LCCN 2008357317. OCLC 154760295.
- Worden FG, Swazey JP, Adelman G biên tập (1975). The Neurosciences, Paths of Discovery. Cambridge, Massachusetts: The MIT Press. ISBN 978-0-262-23072-8. LCCN 75016379. OCLC 1500233.
Trang web[sửa | sửa mã nguồn]
- ^ “The Nobel Prize in Physiology or Medicine 1991” (Thông cáo báo chí). The Royal Swedish Academy of Science. 1991. Lưu trữ bản gốc 24 Tháng Ba năm 2010. Truy cập 21 Tháng hai năm 2010.
- ^ “The Nobel Prize in Physiology or Medicine 1906” (Thông cáo báo chí). The Royal Swedish Academy of Science. 1906. Lưu trữ bản gốc 4 Tháng mười hai năm 2008. Truy cập 21 Tháng hai năm 2010.
- ^ “The Nobel Prize in Chemistry 1997” (Thông cáo báo chí). The Royal Swedish Academy of Science. 1997. Lưu trữ bản gốc 23 tháng Mười năm 2009. Truy cập 21 Tháng hai năm 2010.
Đọc thêm[sửa | sửa mã nguồn]
- Aidley DJ, Stanfield PR (1996). Ion Channels: Molecules in Action. Cambridge: Cambridge University Press. ISBN 978-0-521-49882-1.
- Bear MF, Connors BW, Paradiso MA (2001). Neuroscience: Exploring the Brain. Baltimore: Lippincott. ISBN 0-7817-3944-6.
- Clay JR (tháng 5 năm 2005). “Axonal excitability revisited”. Progress in Biophysics and Molecular Biology. 88 (1): 59–90. doi:10.1016/j.pbiomolbio.2003.12.004. PMID 15561301.
- Deutsch S, Micheli-Tzanakou E (1987). Neuroelectric Systems. New York: New York University Press. ISBN 0-8147-1782-9.
- Hille B (2001). Ion Channels of Excitable Membranes (ấn bản 3). Sunderland, MA: Sinauer Associates. ISBN 978-0-87893-321-1.
- Johnston D, Wu SM (1995). Foundations of Cellular Neurophysiology. Cambridge, Massachusetts: Bradford Book, The MIT Press. ISBN 0-262-10053-3.
- Kandel ER, Schwartz JH, Jessell TM (2000). Principles of Neural Science (ấn bản 4). New York: McGraw-Hill. ISBN 0-8385-7701-6.
- Miller C (1987). “How ion channel proteins work”. Trong Kaczmarek LK, Levitan IB (biên tập). Neuromodulation: The Biochemical Control of Neuronal Excitability. New York: Oxford University Press. tr. 39–63. ISBN 978-0-19-504097-5.
- Nelson DL, Cox MM (2008). Lehninger Principles of Biochemistry (ấn bản 5). New York: W. H. Freeman. ISBN 978-0-7167-7108-1.
Liên kết ngoài[sửa | sửa mã nguồn]
- Ionic flow in action potentials at Blackwell Publishing
- Action potential propagation in myelinated and unmyelinated axons at Blackwell Publishing
- Generation of AP in cardiac cells and generation of AP in neuron cells
- Resting membrane potential from Life: The Science of Biology, by WK Purves, D Sadava, GH Orians, and HC Heller, 8th edition, New York: WH Freeman, ISBN 978-0-7167-7671-0.
- Ionic motion and the Goldman voltage for arbitrary ionic concentrations at The University of Arizona
- A cartoon illustrating the action potential
- Action potential propagation
- Production of the action potential: voltage and current clamping simulations[liên kết hỏng]
- Open-source software to simulate neuronal and cardiac action potentials at SourceForge.net
- Introduction to the Action Potential, Neuroscience Online (electronic neuroscience textbook by UT Houston Medical School)
- Khan Academy: Electrotonic and action potential Lưu trữ 2014-07-02 tại Wayback Machine

![{\displaystyle E={\frac {RT}{nF}}\ln {\frac {\left[\mathrm {outside\ ion\ concentration} \right]}{\left[\mathrm {inside\ ion\ concentration} \right]}}.}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a43d936a817a4c714cfaf607a74166d13d4207fc)
![{\displaystyle E_{m}={\frac {RT}{F}}\ln {\left({\frac {P_{\mathrm {K} }[\mathrm {K} ^{+}]_{\mathrm {out} }+P_{\mathrm {Na} }[\mathrm {Na} ^{+}]_{\mathrm {out} }+P_{\mathrm {Cl} ^{-}}[\mathrm {Cl} ^{-}]_{\mathrm {in} }}{P_{\mathrm {K} }[\mathrm {K} ^{+}]_{\mathrm {in} }+P_{\mathrm {Na} }[\mathrm {Na} ^{+}]_{\mathrm {in} }+P_{\mathrm {Cl} }[\mathrm {Cl} ^{-}]_{\mathrm {out} }}}\right)}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e908e251d34fed6f3d862dfa9fce13b182bbb1ae)



