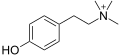
Tyramin
 | |
 | |
| Dữ liệu lâm sàng | |
|---|---|
| Mã ATC |
|
| Dữ liệu dược động học | |
| Chuyển hóa dược phẩm | CYP2D6, FMO3, MAO-A, MAO-B, PNMT, DBH, others |
| Chất chuyển hóa | 4-hydroxyphenylacetaldehyde, dopamine, N-methyltyramine, octopamine |
| Các định danh | |
Tên IUPAC
| |
| Số đăng ký CAS | |
| PubChem CID | |
| IUPHAR/BPS | |
| ChemSpider | |
| Định danh thành phần duy nhất | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| ECHA InfoCard | 100.000.106 |
| Dữ liệu hóa lý | |
| Công thức hóa học | C8H11NO |
| Khối lượng phân tử | 137.179 |
| Mẫu 3D (Jmol) | |
| Điểm nóng chảy | 164,5 °C (328,1 °F) [1] |
| Điểm sôi | 206 °C (403 °F) at 25 mmHg; 166 °C at 2 mmHg[1] |
SMILES
| |
Định danh hóa học quốc tế
| |
Tyramine (/ˈtaɪrəmiːn/ TY—rə meen) (tyramin cũng đánh vần), còn được gọi dưới nhiều tên khác, là một cách tự nhiên xảy ra dấu vết amin có nguồn gốc từ các amino acid tyrosine.[2] Tyramine hoạt động như một chất giải phóng catecholamine. Đáng chú ý, nó không thể vượt qua hàng rào máu não, chỉ dẫn đến các hiệu ứng giao cảm ngoại biên không hoạt động sau khi uống. Tuy nhiên, một cuộc khủng hoảng tăng huyết áp có thể dẫn đến việc ăn các thực phẩm giàu tyramine kết hợp với việc sử dụng các chất ức chế monoamin oxydase (MAOIs).
Hiện diện[sửa | sửa mã nguồn]
Tyramine xảy ra rộng rãi trong thực vật [3] và động vật, và được chuyển hóa bởi các enzyme khác nhau, bao gồm cả các oxit monoamin. Trong thực phẩm, nó thường được sản xuất bởi sự khử carboxyl của tyrosine trong quá trình lên men hoặc phân rã. Thực phẩm chứa một lượng tyramine đáng kể bao gồm các loại thịt có khả năng bị hỏng hoặc ngâm, già, hun khói, lên men hoặc ướp (một số cá, thịt gia cầm và thịt bò); hầu hết thịt lợn (trừ giăm bông chữa khỏi); cá trích. Các thực phẩm khác có chứa lượng tyramine đáng kể là sô cô la; đồ uống có cồn; và thực phẩm lên men, chẳng hạn như hầu hết các pho mát (trừ ricotta, tiểu, Monterey Jack, kem và Neufchatel pho mát), kem chua, sữa chua, mắm tôm, nước sốt đậu nành, đậu tương gia vị, nước sốt teriyaki, tempeh, súp miso, dưa cải bắp, kim chi, rộng (fava) đậu, vỏ đậu xanh, Ý phẳng (Romano) đậu, đậu Hà Lan tuyết, edamame, bơ, chuối, nho khô, ngày, dứa, cà tím, quả sung, màu đỏ mận, mâm xôi, đậu phộng, các loại hạt Brazil, dừa, thịt chế biến, nấm men, một loạt xương rồng và cây tầm gửi ngày lễ.
Tác dụng vật lý và dược lý[sửa | sửa mã nguồn]
Bằng chứng cho sự hiện diện của tyramine trong não người đã được xác nhận bằng phân tích hậu sản.[4] Ngoài ra, khả năng tyramine hoạt động trực tiếp như một chất điều chế thần kinh đã được tiết lộ khi phát hiện ra thụ thể kết hợp protein G có ái lực cao với tyramine, được gọi là TAAR1.[5][6] Thụ thể TAAR1 được tìm thấy trong não, cũng như các mô ngoại biên, bao gồm cả thận.[7] Tyramine liên kết với cả TAAR1 và TAAR2 như một chất chủ vận ở người.[8]
Tyramine được chuyển hóa sinh lý bởi các oxit monoamin (chủ yếu là MAO-A), FMO3, PNMT, DBH và CYP2D6.[9][10][11][12][13] người, nếu sự trao đổi chất monoamine được ảnh hưởng bởi việc sử dụng các thuốc ức chế monoamine oxidase (MAOIs) và thực phẩm giàu chất tyramine được ăn vào bụng, một cuộc khủng hoảng tăng huyết áp có thể gây ra, như tyramine cũng có thể thay thế các monoza được lưu trữ, chẳng hạn như dopamine, norepinephrine và epinephrine, từ các túi tiền synap.
Sinh tổng hợp[sửa | sửa mã nguồn]
Về mặt sinh hóa, tyramine được tạo ra bởi quá trình decarboxyl hóa tyrosine thông qua hoạt động của enzyme tyrosine decarboxylase.[14] Tyramine có thể được chuyển đổi thành các dẫn xuất alkaloid bị methyl hóa <i id="mwiA">N</i> -methyltyramine, <i id="mwig">N</i>, <i id="mwiw">N</i> -dimethyltyramine (hordenine) và <i id="mwjQ">N</i>, <i id="mwjg">N</i>, <i id="mwjw">N</i> -trimethyltyramine (candicine).
-
Tyramine
-
N -Methyltyramin
-
N, N -Dimethyltyramine (hordenine)
-
N, N, N -Trimethyltyramine (candicine)
Ở người, tyramine được sản xuất từ tyrosine, như thể hiện trong sơ đồ sau.
Hóa học[sửa | sửa mã nguồn]
Trong phòng thí nghiệm, tyramine có thể được tổng hợp theo nhiều cách khác nhau, đặc biệt là bằng cách khử carboxyl của tyrosine.[15][16][17]

Ghi chú[sửa | sửa mã nguồn]
Tham khảo[sửa | sửa mã nguồn]
- ^ a b The Merck Index, 10th Ed. (1983), p. 1405, Rahway: Merck & Co.
- ^ “tyramine | C8H11NO”. PubChem (bằng tiếng Anh). Truy cập ngày 8 tháng 4 năm 2017.
- ^ T. A. Smith (1977) Phytochemistry 16 9–18.
- ^ Philips, Rozdilsky Boulton (tháng 2 năm 1978). “Evidence for the presence of m-tyramine, p-tyramine, tryptamine, and phenylethylamine in the rat brain and several areas of the human brain”. Biological Psychiatry. 13 (1): 51–57. PMID 623853.
- ^ Navarro, Gilmour Lewin (ngày 10 tháng 7 năm 2006). “A Rapid Functional Assay for the Human Trace Amine-Associated Receptor 1 Based on the Mobilization of Internal Calcium”. J Biomol Screen. 11 (6): 668–693. doi:10.1177/1087057106289891. PMID 16831861.
- ^ Liberles, Buck (ngày 10 tháng 8 năm 2006). “A second class of chemosensory receptors in the olfactory epithelium”. Nature. 442 (7103): 645–650. doi:10.1038/nature05066. PMID 16878137.
- ^ Xie, Westmoreland Miller (tháng 5 năm 2008). “Modulation of monoamine transporters by common biogenic amines via trace amine-associated receptor 1 and monoamine autoreceptors in human embryonic kidney 293 cells and brain synaptosomes”. J. Pharm. 325 (2): 629–640. doi:10.1124/jpet.107.135079. PMID 18310473.
- ^ Khan MZ, Nawaz W (tháng 10 năm 2016). “The emerging roles of human trace amines and human trace amine-associated receptors (hTAARs) in central nervous system”. Biomed. Pharmacother. 83: 439–449. doi:10.1016/j.biopha.2016.07.002. PMID 27424325.
- ^ Trimethylamine monooxygenase (Homo sapiens). Technische Universität Braunschweig. tháng 7 năm 2016. Truy cập ngày 18 tháng 9 năm 2016.
- ^ Krueger SK, Williams DE (tháng 6 năm 2005). “Mammalian flavin-containing monooxygenases: structure/function, genetic polymorphisms and role in drug metabolism”. Pharmacol. Ther. 106 (3): 357–387. doi:10.1016/j.pharmthera.2005.01.001. PMC 1828602. PMID 15922018.
Table 5: N-containing drugs and xenobiotics oxygenated by FMO - ^ a b Broadley KJ (March 2010). "The vascular effects of trace amines and amphetamines". Pharmacol. Ther. 125 (3): 363–375. doi:10.1016/j.pharmthera.2009.11.005. PMID 19948186.
- ^ Lindemann L, Hoener MC (May 2005). "A renaissance in trace amines inspired by a novel GPCR family". Trends Pharmacol. Sci. 26 (5): 274–281. doi:10.1016/j.tips.2005.03.007. PMID 15860375.
- ^ Wang X, Li J, Dong G, Yue J (February 2014). "The endogenous substrates of brain CYP2D". Eur. J. Pharmacol. 724: 211–218. doi:10.1016/j.ejphar.2013.12.025. PMID 24374199.
- ^ Tyrosine metabolism - Reference pathway Lưu trữ 2019-07-26 tại Wayback Machine, Kyoto Encyclopedia of Genes and Genomes (KEGG)
- ^ G. Barger (1909). “CXXVII.?Isolation and synthesis of p-hydroxyphenylethylamine, an active principle of ergot hòa tan trong nước”. J. Chem. Soc. 95: 1123–1128. doi:10.1039/ct9099501123.
- ^ Waser, Ernst (1925). “Untersuchungen in der Phenylalanin-Reihe VI. Decarboxylierung des Tyrosins und des Leucins”. Helvetica Chimica Acta. 8: 758–773. doi:10.1002/hlca.192500801106.
- ^ Buck, Johannes S. (1933). “Reduction of Hydroxymandelonitriles. A New Synthesis of Tyramine”. Journal of the American Chemical Society. 55 (8): 3388–3390. doi:10.1021/ja01335a058.