Yếu tố kích thích dòng bạch cầu hạt - đại thực bào
| Yếu tố kích thích dòng bạch cầu hạt - đại thực bào | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| |||||||||
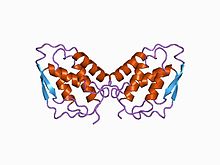
| Cấu trúc 3D của yếu tố kích thích dòng bạch cầu hạt - đại thực bào tái tổ hợp ở người (rhGM_CSF) | |||||||||
| Danh pháp | |||||||||
| Ký hiệu | GM_CSF | ||||||||
| Pfam | PF01109 | ||||||||
| Pfam clan | CL0053 | ||||||||
| InterPro | IPR000773 | ||||||||
| PROSITE | PDOC00584 | ||||||||
| SCOP | 2gmf | ||||||||
| |||||||||
 | |
| Dữ liệu lâm sàng | |
|---|---|
| Mã ATC | |
| Các định danh | |
Tên IUPAC
| |
| Số đăng ký CAS | |
| DrugBank | |
| ChemSpider |
|
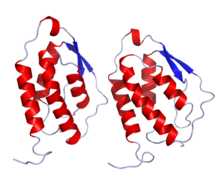
| Dữ liệu hóa lý | |
| Công thức hóa học | C639H1006N168O196S8 |
| Khối lượng phân tử | 14.434,54 g·mol−1 |
| | |
Yếu tố kích thích dòng bạch cầu hạt - đại thực bào (tiếng Anh: granulocyte-macrophage colony-stimulating factor, viết tắt: GM-CSF), hay yếu tố kích thích phát triển đơn dòng 2 (colony-stimulating factor 2, viết tắt: CSF2) là một glycoprotein đơn phân tử được tạo ra bởi đại thực bào, tế bào T, dưỡng bào, tế bào NK, tế bào nội mô và nguyên bào sợi, có chức năng như một cytokine.[3] Sargramostim và molgramostim là hai đồng phân cấu trúc của GM-CSF được tạo ra bằng công nghệ DNA tái tổ hợp dùng trong điều trị kích thích miễn dịch.[4][5][6]
Trong khi yếu tố kích thích dòng bạch cầu hạt (G-CSF) chỉ kích thích đặc hiệu trên sự tăng sinh và phát triển của bạch cầu hạt trung tính, GM-CSF có tác dụng trên nhiều dòng tế bào, đặc biệt là đại thực bào và bạch cầu ưa acid.[7]
Chức năng[sửa | sửa mã nguồn]
GM-CSF kích thích các tế bào gốc sản sinh ra bạch cầu hạt (bạch cầu hạt trung tính, bạch cầu ưa acid và bạch cầu ưa kiềm) và bạch cầu đơn nhân. Bạch cầu đơn nhân sau khi được sinh ra trong hệ tuần hoàn sẽ di chuyển đến các mô, nơi chúng được biệt hóa thành các đại thực bào và tế bào tua. Vì vậy, GM-CSF được xem như một thành phần của trong chuỗi tín hiệu viêm/miễn dịch tạo ra số lượng lớn đại thực bào giúp chống lại sự viêm nhiễm.[8]
Ở các tế bào trưởng thành của hệ miễn dịch, GM-CSF làm tăng sự di chuyển của bạch cầu trung tính và thay đổi mức độ biểu hiện các thụ thể trên bề mặt tế bào.[9]
GM-CSF truyền tín hiệu thông qua STAT3/5 (protein chuyển đổi và hoạt hóa tín hiệu phiên mã 3/5),[10] kích thích đại thực bào làm tăng hàm lượng gốc tự do oxy hoạt động (reactive oxygen species) và gây thiếu hụt hàm lượng kẽm tự do nội bào, dẫn đến ức chế sự phát triển của nấm bệnh.[11] Bằng cách này, GM-CSF hỗ trợ sự phát triển của hệ thống miễn dịch và thúc đẩy sự bảo vệ chống lại các nhiễm trùng.
Trong quá trình phát triển phôi thai, GM-CSF được xem như một embryokine, làm thay đổi sự biểu hiện gene (đặc biệt là các gene liên quan đến quá trình biệt hóa và chết rụng tế bào) và làm tăng số lượng tế bào bên trong khối nội phôi (embryoblast).[12]
Di truyền học[sửa | sửa mã nguồn]
GM-CSF được mã hóa bởi gene CSF2 (~2.5 kbp), nằm cạnh gene IL3 (gene mã hóa interleukin 3) thuộc chùm gene T helper type 2-associated cytokine, nhiễm sắc thể 5, cánh q, băng 31 (5q31). Vùng nhiễm sắc thể này có liên quan đến hội chứng mất đoạn 5q và bệnh bạch cầu dòng tủy cấp tính (AML). Giữa CSF2 và IL3 là trình tự cách ly (insulator), nên chúng được điều hòa riêng biệt.[13]
Lịch sử[sửa | sửa mã nguồn]
CSF2 được giải trình tự và clone lần đầu tiên vào năm 1985. Bằng công nghệ DNA tái tổ hợp, các clone của GM-CSF đã được nghiên cứu sản xuất sau đó và trở thành các dược phẩm tiềm năng. Molgramostim được tạo ra từ Escherichia coli, không glycosyl hóa (Genetics Institute, Inc.);[14] sargramostim được tạo ra từ Saccharomyces cerevisae, leucine ở vị trí 23 được thay thế bằng proline, glycosyl hóa ít (Immunex); và regramostim được tạo ra từ tế bào buồng trứng chuột Hamster Trung Quốc (CHO cell), glycosyl hóa nhiều hơn sargramostim (Sandoz).[15] Sự glycosyl hóa có liên quan đến sự tương tác giữa thuốc và cơ thể.[16]
Molgramostim cuối cùng được đồng phát triển và tiếp thị bởi Novartis và Schering-Plough dưới tên thương mại là Leucomax, sử dụng trong hỗ trợ khôi phục hàm lượng bạch cầu sau hóa trị. Năm 2002, Novartis đã nhượng quyền sở hữu của mình cho Schering-Plough.[17][18]
Năm 1991, sargramostim được Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) chấp thuận dưới tên thương mại Leukine, cho phép sử dụng trong ghép tủy với tác dụng tăng tái tạo bạch cầu. Sau nhiều lần chuyển nhượng, Leukine hiện tại thuộc quyền sở hữu của Partner Therapeutics (PTx).[19]
Năm 2015, FDA và EMA đều chấp thuận liệu pháp điều trị ung thư bằng virus (oncolytic virotherapy) talimogene laherparepvec (tên thương mại Imlymic) được phát triển bởi Amgen Inc. Talimogene laherparepvec là một loại virus biến đổi gene, khi vào cơ thể sẽ tạo ra GM-CSF từ chính khối u giúp phân hủy của các tế bào ung thư.
Ý nghĩa lâm sàng[sửa | sửa mã nguồn]
GM-CSF được sinh ra nhiều trong khớp ở các bệnh nhân viêm khớp dạng thấp. Vì thế, GM-CSF được xem như đích tác dụng sinh học trong trường hợp này, ức chế GM-CSF có thể làm giảm các thương tổn và viêm nhiễm. Một số thuốc đã được phát triển để ức chế GM-CSF như otilimab, namilumab và lenzilumab.[20] GM-CSF cũng được áp dụng trong điều trị các trường hợp suy giảm miễn dịch ở các bệnh hiễm nghèo, giúp khôi phục chức năng bạch cầu đơn nhân và bạch cầu trung tính. Tuy nhiên, tác động lên kết quả điều trị của bệnh nhân hiện vẫn chưa rõ ràng và cần các nghiên cứu thử nghiệm chuyên sâu cho việc trị liệu này.
Thử nghiệm lâm sàng[sửa | sửa mã nguồn]
Các kháng thể đơn dòng chống lại GM-CSF đang được sử dụng trong các thử nghiệm lâm sàng điều trị viêm khớp dạng thấp, viêm cột sống dính khớp và COVID-19.[21]
Xem thêm[sửa | sửa mã nguồn]
Tham khảo[sửa | sửa mã nguồn]
- ^ a b c GRCh38: Ensembl release 89: ENSG00000164400 - Ensembl, May 2017
- ^ “Human PubMed Reference:”.
- ^ Francisco-Cruz, Alejandro; Aguilar-Santelises, Miguel; Ramos-Espinosa, Octavio; Mata-Espinosa, Dulce; Marquina-Castillo, Brenda; Barrios-Payan, Jorge; Hernandez-Pando, Rogelio (tháng 1 năm 2014). “Granulocyte-macrophage colony-stimulating factor: not just another haematopoietic growth factor”. Medical Oncology (Northwood, London, England). 31 (1): 774. doi:10.1007/s12032-013-0774-6. ISSN 1559-131X. PMID 24264600.
- ^ Cantrell, M A; Anderson, D; Cerretti, D P; Price, V; McKereghan, K; Tushinski, R J; Mochizuki, D Y; Larsen, A; Grabstein, K (tháng 9 năm 1985). “Cloning, sequence, and expression of a human granulocyte/macrophage colony-stimulating factor”. Proceedings of the National Academy of Sciences (bằng tiếng Anh). 82 (18): 6250–6254. doi:10.1073/pnas.82.18.6250. ISSN 0027-8424. PMC 391030. PMID 3898082.
- ^ Wong, Gordon G.; Witek, JoAnn S.; Temple, Patricia A.; Wilkens, Kathleen M.; Leary, Anne C.; Luxenberg, Deborah P.; Jones, Simon S.; Brown, Eugene L.; Kay, Robert M. (17 tháng 5 năm 1985). “Human GM-CSF: Molecular Cloning of the Complementary DNA and Purification of the Natural and Recombinant Proteins”. Science (bằng tiếng Anh). 228 (4701): 810–815. doi:10.1126/science.3923623. ISSN 0036-8075.
- ^ Burgess, A. W.; Begley, C. G.; Johnson, G. R.; Lopez, A. F.; Williamson, D. J.; Mermod, J. J.; Simpson, R. J.; Schmitz, A.; DeLamarter, J. F. (tháng 1 năm 1987). “Purification and properties of bacterially synthesized human granulocyte-macrophage colony stimulating factor”. Blood. 69 (1): 43–51. ISSN 0006-4971. PMID 3024761.
- ^ Root, R. K.; Dale, D. C. (tháng 3 năm 1999). “Granulocyte colony-stimulating factor and granulocyte-macrophage colony-stimulating factor: comparisons and potential for use in the treatment of infections in nonneutropenic patients”. The Journal of Infectious Diseases. 179 Suppl 2: S342–352. doi:10.1086/513857. ISSN 0022-1899. PMID 10081506.
- ^ Chen, BD; Clark, CR; Chou, TH (1 tháng 4 năm 1988). “Granulocyte/macrophage colony-stimulating factor stimulates monocyte and tissue macrophage proliferation and enhances their responsiveness to macrophage colony-stimulating factor”. Blood. 71 (4): 997–1002. doi:10.1182/blood.v71.4.997.997. ISSN 0006-4971.
- ^ Gasson, Jc (15 tháng 3 năm 1991). “Molecular physiology of granulocyte-macrophage colony-stimulating factor”. Blood (bằng tiếng Anh). 77 (6): 1131–1145. doi:10.1182/blood.V77.6.1131.1131. ISSN 0006-4971.
- ^ Voehringer, David (tháng 10 năm 2012). “Basophil modulation by cytokine instruction”. European Journal of Immunology. 42 (10): 2544–2550. doi:10.1002/eji.201142318. ISSN 1521-4141. PMID 23042651.
- ^ Gessini, L.; Jandolo, B.; Pietrangeli, A. (1985). “Pseudoclaudication in lumbar disc protrusions. Contribution in understanding the etio-pathogenetic factors of the syndrome and surgical results in eight cases”. Journal of Neurosurgical Sciences. 29 (4): 317–322. ISSN 0390-5616. PMID 3841917.
- ^ Hansen, Peter J.; Dobbs, Kyle B.; Denicol, Anna C. (tháng 9 năm 2014). “Programming of the preimplantation embryo by the embryokine colony stimulating factor 2”. Animal Reproduction Science (bằng tiếng Anh). 149 (1–2): 59–66. doi:10.1016/j.anireprosci.2014.05.017.
- ^ Bowers, Sarion R.; Mirabella, Fabio; Calero-Nieto, Fernando J.; Valeaux, Stephanie; Hadjur, Suzana; Baxter, Euan W.; Merkenschlager, Matthias; Cockerill, Peter N. (tháng 4 năm 2009). “A conserved insulator that recruits CTCF and cohesin exists between the closely related but divergently regulated interleukin-3 and granulocyte-macrophage colony-stimulating factor genes”. Molecular and Cellular Biology. 29 (7): 1682–1693. doi:10.1128/MCB.01411-08. ISSN 1098-5549. PMC 2655614. PMID 19158269.
- ^ “Molgramostim - AdisInsight”. adisinsight.springer.com. Truy cập ngày 5 tháng 9 năm 2023.
- ^ Hussein, A. M.; Ross, M.; Vredenburgh, J.; Meisenberg, B.; Hars, V.; Gilbert, C.; Petros, W. P.; Coniglio, D.; Kurtzberg, J. (tháng 11 năm 1995). “Effects of granulocyte-macrophage colony stimulating factor produced in Chinese hamster ovary cells (regramostim), Escherichia coli (molgramostim) and yeast (sargramostim) on priming peripheral blood progenitor cells for use with autologous bone marrow after high-dose chemotherapy”. European Journal of Haematology. 55 (5): 348–356. doi:10.1111/j.1600-0609.1995.tb00713.x. ISSN 0902-4441. PMID 7493686.
- ^ Armitage, J. O. (15 tháng 12 năm 1998). “Emerging applications of recombinant human granulocyte-macrophage colony-stimulating factor”. Blood. 92 (12): 4491–4508. ISSN 0006-4971. PMID 9845514.
- ^ “Press release: Novartis Oncology sharpens focus on key growth drivers”. www.sec.gov. Novartis via SEC Edgar. 30 tháng 10 năm 2002. Truy cập ngày 5 tháng 9 năm 2023.
- ^ “Scientific Conclusions and Grounds for Amendment of the Summary of Product Characteristics Presented by the EMEA” (PDF). EMA CPMP. 27 tháng 6 năm 2000.
- ^ Inc, Partner Therapeutics. “Partner Therapeutics (PTx) Acquires Leukine® from Sanofi”. www.prnewswire.com (bằng tiếng Anh). Truy cập ngày 5 tháng 9 năm 2023.
- ^ Bykerk, Vivian P (tháng 11 năm 2020). “The efficacy and safety of targeting GM-CSF in arthritis”. The Lancet Rheumatology (bằng tiếng Anh). 2 (11): e648–e650. doi:10.1016/S2665-9913(20)30352-0. PMC 7541049. PMID 33047107.
- ^ Lee, Kevin M. C.; Achuthan, Adrian A.; Hamilton, John A. (2020). “GM-CSF: A Promising Target in Inflammation and Autoimmunity”. ImmunoTargets and Therapy. 9: 225–240. doi:10.2147/ITT.S262566. ISSN 2253-1556. PMC 7605919. PMID 33150139.