Hydro disulfide
| Hydro disulfide | |
|---|---|
 | |
 | |
| Danh pháp IUPAC | Dihydrogen disulfide |
| Tên khác | Hydrogen disulphide; Hydrogen persulfide; Hydrogen persulphide, Dihydrogen disulfide, thiosulfenic acid |
| Nhận dạng | |
| Số CAS | |
| PubChem | |
| ChEBI | |
| Ảnh Jmol-3D | ảnh |
| SMILES | đầy đủ
|
| InChI | đầy đủ
|
| Thuộc tính | |
| Bề ngoài | chất lỏng màu vàng |
| Khối lượng riêng | 1,334 g cm−3 |
| Điểm nóng chảy | −89,6 °C (183,6 K; −129,3 °F) |
| Điểm sôi | 70,7 °C (343,8 K; 159,3 °F) |
| Độ hòa tan trong nước | CS2 |
| Cấu trúc | |
| Các nguy hiểm | |
| Điểm bắt lửa | flammable |
| Các hợp chất liên quan | |
| Hợp chất liên quan | Hydrogen peroxide Hydrogen sulfide Hydrogen diselenide Hydrogen ditelluride |
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |
Hydro disulfide là hợp chất vô cơ với công thức H2S2. Chloride hydro này là một chất lỏng dễ bay hơi màu vàng với mùi camphor. Nó phân hủy dễ dàng đến hydrogen sulfide (H2S) và lưu huỳnh nguyên tố[1].
Cấu trúc
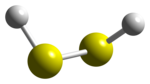
[sửa | sửa mã nguồn]Cấu trúc hydrogen disulfide tương tự như hydrogen peroxide, với sự đối xứng của nhóm điểm C2. Cả hai phân tử rõ ràng là không phẳng. Góc hai mặt là 90,6 °, so với 111,5 ° trong H2O2. Góc liên kết H-S-S là 92 °, gần 90 o đối với không lưu huỳnh hai lần không liên hợp[1].
Tổng hợp và phản ứng
[sửa | sửa mã nguồn]Sulphua hydro có thể được tổng hợp bằng cách hòa tan các polysulfid kim loại kiềm hoặc kim loại kiềm thổ trong nước. Khi dung dịch được pha với axit clohiđric ở -15 °C, một loại dầu màu vàng có chứa hỗn hợp polysulfanes (H2Sn) sẽ lắng xuống dưới lớp nước. Chưng cất phân đoạn của dầu này cho hydrogen disulfide tách khỏi các polysulfit khác (chủ yếu là trisulfide)[2][3][4][1].
Hydro disulfide dễ bị phân hủy dưới điều kiện xung quanh tới hydrogen sulfide và lưu huỳnh. Trong hóa học hữu cơ sulfur, hydrogen disulfide thêm vào alkenes để cung cấp disulfit và thiol[5].
Đường hầm lượng tử và sự đàn áp của nó trong deuterium disulfide
[sửa | sửa mã nguồn]Hình thức deuterated của hydrogen disulfide DSSD, có hình học tương tự với HSSH, nhưng thời gian đường hầm của nó chậm hơn, làm cho nó trở thành một trường hợp thử nghiệm thuận lợi cho hiệu ứng lượng tử Zeno, trong đó quan sát thường xuyên của một hệ lượng tử ngăn chặn sự tiến hóa bình thường của nó. Trost và Hornberger[6] đã tính toán rằng trong khi một phân tử DSSD cô lập tự động dao động giữa các hình thức chiral trái và phải với thời gian là 5,6 giây, sự hiện diện của một lượng nhỏ khí helium trơ sẽ ổn định trạng thái chiral, va chạm của Các nguyên tử heli có hiệu lực "quan sát" chirality tạm thời của phân tử và ngăn chặn sự tiến hóa tự phát đến trạng thái chiral khácref>[1]</ref>.
Các hiệu ứng sức khỏe
[sửa | sửa mã nguồn]Hydrogen disulfide đã được miêu tả là "có mùi nặng và khó chịu" giống như long não hoặc sulfide chloride, gây ra "nước mắt và cảm giác mệt mỏi ở mũi". Nếu nó có trong nồng độ cao, nó có thể gây chóng mặt, mất phương hướng và cuối cùng vô thức[7].
Tham khảo
[sửa | sửa mã nguồn]- ^ a b c R. Steudel "Inorganic Polysulfanes H2Sn with n > 1" in Elemental Sulfur and Sulfur-Rich Compounds II (Topics in Current Chemistry) 2003, Volume 231, pp 99-125. doi:10.1007/b13182
- ^ De, A. K. (ngày 15 tháng 1 năm 2001). A Text Book of Inorganic Chemistry. ISBN 978-81-224-1384-7.
- ^ Walton and Parson; Parsons, Llewellyn B. (1921). “Preparation and Properties of the Persulfides of Hydrogen”. J. Amer. Chem. Soc. 43: 2539–48. doi:10.1021/ja01445a008.
- ^ Georg Brauer: Handbook of Preparative Inorganic Chemistry Volume I, page 391, Wiley, 1963.
- ^ Hazardous Reagents, Robinson Brothers
- ^ Trost, J.; Hornberger, K. (2009). “Hund's Paradox and the Collisional Stabilization of Chiral Molecules”. Phys. Rev. Lett. 103: 023202. doi:10.1103/PhysRevLett.103.023202. PMID 19659202.
- ^ Stein, Wilkinson, G (2007). Seminars in general adult psychiatry. Royal College of Psychiatrists. ISBN 978-1-904671-44-2.
