Isoquinolin

| |||
| |||
| Names | |||
|---|---|---|---|
| Preferred IUPAC name
Isoquinoline[1] | |||
| Other names
Benzo[c]pyridine
2-benzanine
| |||
| Identifiers | |||
3D model (JSmol)
|
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.003.947 | ||
| EC Number | 204-341-8 | ||
PubChem <abbr title="<nowiki>Compound ID</nowiki>">CID
|
|||
| UNII |
| ||
CompTox Dashboard (<abbr title="<nowiki>U.S. Environmental Protection Agency</nowiki>">EPA)
|
|||
| |||
| |||
| Properties | |||
| C9H7N | |||
| Molar mass | 129.162 g·mol−1 | ||
| Appearance | yellowish oily liquid, hygroscopic platelets when solid | ||
| Density | 1.099 g/cm³ | ||
| Melting point | 26 to 28 °C (79 to 82 °F; 299 to 301 K) | ||
| Boiling point | 242 °C (468 °F; 515 K) | ||
| Acidity (pKa) | pKBH+=5.14[2] | ||
| -83.9·10−6 cm³/mol | |||
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa). | |||
| Infobox references | |||
Isoquinoline là một hợp chất hữu cơ thơm dị vòng. Nó là một đồng phân cấu trúc của quinoline. Isoquinoline và quinoline là các benzopyridine, được cấu tạo từ một vòng benzen hợp nhất với vòng pyridine. Theo nghĩa rộng hơn, thuật ngữ isoquinoline được sử dụng để tham chiếu đến các dẫn xuất isoquinoline. 1-Benzylisoquinoline là xương sống cấu trúc trong các alcaloid tự nhiên bao gồm papaverine. Vòng isoquinoline trong các hợp chất tự nhiên này có nguồn gốc từ tyrosine amino acid thơm.[3][4][5][6][7][8]
Tính chất[sửa | sửa mã nguồn]
Isoquinoline là một chất lỏng hút ẩm không màu ở nhiệt độ trên điểm nóng chảy của nó với một mùi khó chịu, thâm nhập. Các mẫu tạp chất có thể xuất hiện màu nâu, như là điển hình cho dị vòng nitơ. Nó kết tinh trong tiểu cầu có độ hòa tan trong nước thấp nhưng hòa tan tốt trong ethanol, acetone, dietyl ete, carbon disulfide và các dung môi hữu cơ phổ biến khác. Nó cũng hòa tan trong axit loãng như là dẫn xuất proton.
Là một chất tương tự của pyridine, isoquinoline là một base yếu, với p Ka là 5,14.[2] Nó proton tạo thành muối khi xử lý bằng axit mạnh, chẳng hạn như HCl. Nó tạo thành các chất gây nghiện với axit Lewis, chẳng hạn như BF3.
Sản xuất[sửa | sửa mã nguồn]
Isoquinoline lần đầu tiên được phân lập từ nhựa than đá vào năm 1885 bởi Hoogewerf và van Dorp.[9] Họ đã phân lập nó bằng cách kết tinh phân đoạn của axit sunfat. Weissgerber đã phát triển một tuyến đường nhanh hơn vào năm 1914 bằng cách khai thác có chọn lọc nhựa than đá, khai thác thực tế là isoquinoline cơ bản hơn quinoline. Isoquinoline sau đó có thể được phân lập từ hỗn hợp bằng cách kết tinh phân đoạn của axit sunfat.
Mặc dù các dẫn xuất isoquinoline có thể được tổng hợp bằng một số phương pháp, nhưng tương đối ít phương pháp trực tiếp cung cấp isoquinoline không phân hủy. Phản ứng Pomeranzifer Fritsch cung cấp một phương pháp hiệu quả để điều chế isoquinoline. Phản ứng này sử dụng một benzaldehyde và aminoacetoaldehyde diethyl acetal, mà trong một axit vừa phản ứng để tạo thành isoquinoline.[10] Ngoài ra, có thể sử dụng benzylamine và glyoxal acetal, để tạo ra kết quả tương tự bằng cách sử dụng phép biến đổi Schlittler-Müller.[11]
Một số phương pháp khác hữu ích cho việc điều chế các dẫn xuất isoquinoline khác nhau.
Trong phản ứng Bischler-Napieralski, một β-phenylethylamine bị acyl hóa và cyclode bị mất nước bởi một axit Lewis, chẳng hạn như phosphoryl chloride hoặc phospho pentoxit. Kết quả là 3,4-dihydroisoquinoline sau đó có thể được khử hydro bằng paladi. Phản ứng Bischler-Napieralski sau đây tạo ra papaverine. 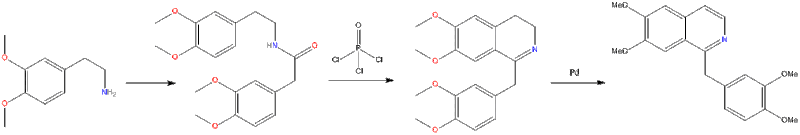
Phản ứng Pictet-Gams và phản ứng Pictet-Spengler là cả hai biến thể của phản ứng Bischler-Napieralski. Một phản ứng Gamet của Gamet hoạt động tương tự như phản ứng Bischler-Napieralski; sự khác biệt duy nhất là một nhóm hydroxy bổ sung trong chất phản ứng cung cấp một vị trí mất nước trong cùng điều kiện phản ứng như sự chu kỳ để cung cấp isoquinoline thay vì yêu cầu một phản ứng riêng biệt để chuyển đổi một chất trung gian dihydroisoquinoline.
Trong một phản ứng Pictet-Spengler, một sự ngưng tụ của β- phenylethylamine và một aldehyd tạo thành một imine, trải qua một chu kỳ để tạo thành tetrahydroisoquinoline thay vì dihydroisoquinoline. Trong enzyme, enzyme (S) -norcoclaurine synthase (EC) là một enzyme xúc tác cho quá trình tổng hợp sinh học hình ảnh sinh học:

Phản ứng nội phân tử aza Wittig cũng có khả năng isoquinolines.
Các ứng dụng của dẫn xuất[sửa | sửa mã nguồn]
Isoquinolines tìm thấy nhiều ứng dụng, bao gồm:
- gây mê; dimethisoquin là một ví dụ (hiển thị bên dưới).
- thuốc chống tăng huyết áp, chẳng hạn như quinapril, quinapirilat và debrisoquine (tất cả có nguồn gốc từ 1,2,3,4-tetrahydroisoquinoline).
- thuốc chống nấm, chẳng hạn như 2,2′-hexadecamethylenediisoquinolinium dichloride, cũng được sử dụng như một chất khử trùng tại chỗ. Dẫn xuất này, được hiển thị dưới đây, được điều chế bằng N -alkylation isoquinoline với dihalide thích hợp.
- chất khử trùng, như N-laurylisoquinolinium bromide (hiển thị bên dưới), được điều chế bằng N-alkylation đơn giản của isoquinoline.
- thuốc giãn mạch, một ví dụ nổi tiếng, papaverine, được hiển thị dưới đây.
Các hợp chất Bcdenzylisoquinolinium là các hợp chất có cấu trúc tương tự tubocurarine. Chúng có hai cấu trúc isoquinolinium, được liên kết bởi một chuỗi carbon, chứa hai liên kết este.
Công dụng khác[sửa | sửa mã nguồn]
Isoquinolines được sử dụng trong sản xuất thuốc nhuộm, sơn, thuốc trừ sâu và thuốc chống nấm. Nó cũng được sử dụng làm dung môi để chiết xuất nhựa và terpen, và như một chất ức chế ăn mòn.
Xem thêm[sửa | sửa mã nguồn]
- Naphthalene, một chất tương tự không có nguyên tử nitơ.
- Nhân hương phương cơ bản
Tham khảo[sửa | sửa mã nguồn]
- ^ Nomenclature of Organic Chemistry: IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge: The Royal Society of Chemistry. 2014. p. 212. doi:10.1039/9781849733069-FP001. ISBN 978-0-85404-182-4.
- ^ a b Brown, H.C., et al., in Baude, E.A. and Nachod, F.C., Determination of Organic Structures by Physical Methods, Academic Press, New York, 1955.
- ^ Gilchrist, T.L. (1997). Heterocyclic Chemistry (3rd ed.). Essex, UK: Addison Wesley Longman.
- ^ Harris, J.; Pope, W.J. "isoQuinoline and the isoQuinoline-Reds" Journal of the Chemical Society (1922) volume 121, pp. 1029–1033.
- ^ Katritsky, A.R.; Pozharskii, A.F. (2000). Handbook of Heterocyclic Chemistry (2nd ed.). Oxford, UK: Elsevier.
- ^ Katritsky, A.R.; Rees, C.W.; Scriven, E.F. (Eds.). (1996). Comprehensive Heterocyclic Chemistry II: A Review of the Literature 1982–1995 (Vol. 5). Tarrytown, NY: Elsevier.
- ^ Nagatsu, T. "Isoquinoline neurotoxins in the brain and Parkinson's disease" Neuroscience Research (1997) volume 29, pp. 99–111.
- ^ O'Neil, Maryadele J. (Ed.). (2001). The Merck Index (13th ed.). Whitehouse Station, NJ: Merck.
- ^ S. Hoogewerf and W.A. van Dorp (1885) "Sur un isomére de la quinoléine" (On an isomer of quinoline), Recueil des Travaux Chemiques des Pays-Bas (Collection of Work in Chemistry in the Netherlands), vol.4, no. 4, pages 125–129. See also: S. Hoogewerf and W.A. van Dorp (1886) "Sur quelques dérivés de l'isoquinoléine" (On some derivatives of isoquinoline), Recueil des Travaux Chemiques des Pays-Bas, vol.5, no. 9, pages 305–312.
- ^ Li, J. J. (2014). “Pomeranz–Fritz reaction”. Name Reactions: A Collection of Detailed Mechanisms and Synthetic Applications (ấn bản 5). Springer. tr. 490–491. ISBN 9783319039794.
- ^ Li, J. J. (2014). “Schlittler–Müller modification”. Name Reactions: A Collection of Detailed Mechanisms and Synthetic Applications (ấn bản 5). Springer. tr. 492. ISBN 9783319039794.
Liên kết ngoài[sửa | sửa mã nguồn]
. Encyclopædia Britannica. 22 (ấn bản 11). 1911. tr. 758–759. Bách khoa toàn thư Britannica. 22 (lần thứ 11). 1911. Trang. 758 mỏ759.