Cholesterol
Cholesterol là một chất béo steroid, mềm, màu vàng nhạt, có ở màng tế bào của tất cả các mô trong cơ thể, và được vận chuyển trong huyết tương của mọi động vật. Nó được sản xuất hàng ngày trong gan (nguồn gốc nội sinh), mỗi ngày từ 1,5g – 2g. Nguồn gốc cholesterol ngoại sinh là từ việc ăn uống các chất mỡ động vật. Cholesterol hiện diện với nồng độ cao ở các mô tổng hợp nó hoặc có mật độ màng dày đặc, như gan, tuỷ sống, não và mảng xơ vữa động mạch. Cholesterol đóng vai trò trung tâm trong nhiều quá trình sinh hoá, nhưng lại được biết đến nhiều nhất do liên hệ đến bệnh tim mạch gây ra bởi nồng độ cholesterol trong máu tăng.

Lịch sử tên gọi[sửa | sửa mã nguồn]
Tên gọi xuất phát từ tiếng Hi Lạp chole- (mật) và stereos (rắn), vì nó được phát hiện lần đầu ở dạng rắn trong sỏi mật.
Sinh lý học[sửa | sửa mã nguồn]
Tổng hợp[sửa | sửa mã nguồn]
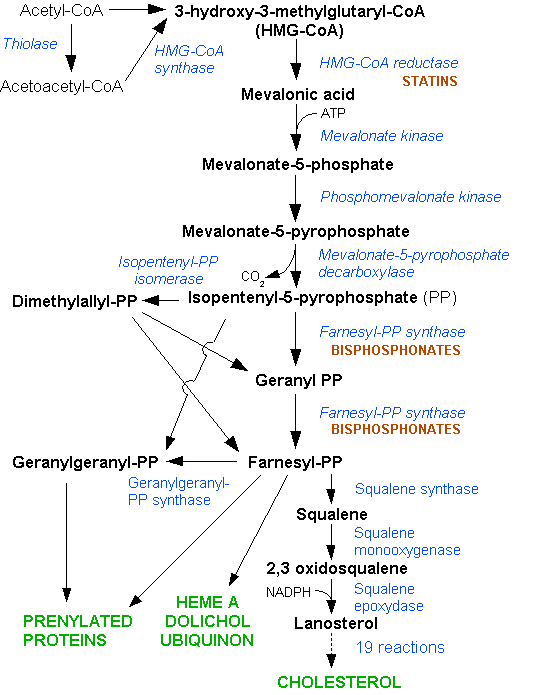
Cholesterol được tổng hợp chủ yếu từ acetyl CoA theo đường HMG-CoA reductase ở nhiều tế bào/mô. Khoảng 20–25% lượng cholesterol tổng hợp mỗi ngày (~1 g/ngày) xảy ra ở gan, các vị trí khác có tỉ lệ tổng hợp cao gồm ruột, tuyến thượng thận và cơ quan sinh sản. Với một người khoảng 68 kg, tổng lượng cholesterol trung bình trong cơ thể khoảng 35g (35.000 mg). Trong một ngày lượng nội sinh trung bình khoảng 1000 mg và từ thức ăn trung bình khoảng 200 đến 300 mg. Sự di chuyển cholesterol trong cơ thể có tính chất tuần hoàn. Nó được bài tiết ở gan qua mật đến cơ quan tiêu hóa. Khoảng 50% lượng cholesterol bài tiết được tái hấp thu ở ruột non vào hệ tuần hoàn. Phytosterols có thể cạnh tranh với cholesterol trong công tác tái hấp thu của ruột vì vậy làm suy giảm độ tái hấp thu của cholesterol vào máu.
Tính chất[sửa | sửa mã nguồn]
Cholesterol kém tan trong nước; nó không thể tan và di chuyển ở dạng tự do trong máu. Thay vào đó, nó được vận chuyển trong máu bởi các lipoprotein; đó là các "va-li phân tử" tan trong nước và bên trong mang theo cholesterol và mỡ. Các protein tham gia cấu tạo bề mặt của mỗi loại hạt lipoprotein quyết định cholesterol sẽ được lấy khỏi tế bào nào và sẽ được cung cấp cho nơi đâu.
Lipoprotein lớn nhất, chủ yếu vận chuyển mỡ từ niêm mạc ruột đến gan, được gọi là chylomicron. Chylomicron có thành phần giàu triglyceride. Chúng chuyên chở triglyceride và cholesterol (từ thức ăn và đặc biệt là cholesterol được tiết từ gan vào mật) đến các mô như gan, mỡ và cơ vân. Tại các nơi đó, lipoprotein lipase (LPL) thủy phân triglyceride trong chylomicron thành acid béo tự do; các acid béo này được dùng để tổng hợp lipoprotein tỉ trọng rất thấp (VLDL) ở gan hoặc được oxi hoá sinh năng lượng ở cơ hoặc được dự trữ ở mô mỡ. Chylomicron sau khi mất triglyceride trở thành các hạt còn lại (chylomicron remnant) và được vận chuyển đến gan để được xử lý tiếp.
VLDL là lipoprotein tương tự như chylomicron, có thành phần triglyceride cao. VLDL được tổng hợp từ acid béo tự do có nguồn gốc từ chuyển hoá chylomicron ở gan hoặc nội sinh. Triglyceride của VLDL bị thủy phân bởi lipoprotein lipase mao mạch để cung cấp acid béo cho mô mỡ và cơ. Phần lipid còn lại gọi là lipoprotein tỉ trọng trung gian (IDL). Sau đó IDL chuyển thành lipoprotein tỉ trọng thấp (LDL) bởi tác dụng của lipase gan hoặc được gan bắt giữ qua thụ thể LDL.
Các hạt LDL chuyên chở phần lớn lượng cholesterol có trong máu, cung cấp cholesterol cho tế bào. Thụ thể LDL ở tế bào ngoại biên hoặc gan bắt giữ LDL và lấy nó ra khỏi máu. Tế bào ngoại biên dùng cholesterol trong LDL cho cấu trúc màng cũng như để sản xuất hormone. LDL là lipoprotein tạo xơ vữa động mạch; nồng độ LDL cao liên hệ với tăng nguy cơ bệnh tim mạch. Các hạt LDL đặc, nhỏ chứa nhiều cholesterol ester (phenotype B) được cho là có tính sinh xơ vữa động mạch cao hơn do nhạy cảm với các thay đổi oxy hóa và vì vậy có độc tính cho nội mạch so với các hạt LDL lớn, bộng (phenotype A). Ở người khoẻ mạnh, các hạt LDL có kích thước lớn và số lượng ít. Ngược lại, nếu có nhiều các hạt LDL nhỏ sẽ dẫn đến nguy cơ xơ vữa động mạch.
Các hạt lipoprotein tỉ trọng cao (HDL) được tổng hợp và chuyển hoá ở gan và ruột. HDL sơ khai lấy cholesterol từ mô ngoại biên; quá trình này được hỗ trợ bởi men lecithin:cholesterol acyltransferase (LCAT) trong hệ tuần hoàn qua phản ứng ester hoá cholesterol tự do. Khi cholesterol được ester hoá, nó tạo gradient nồng độ và hút cholesterol từ mô ngoại biên và từ các lipoprotein khác và trở nên ít đặc hơn. Song song đó, protein di chuyển cholesterol ester (cholesterol ester transfer protein) lại mang cholesterol ester từ HDL sang VLDL, LDL và một phần nhỏ hơn sang chylomicron, làm giảm gradient nồng độ và cho phép triglyceride di chuyển theo chiều ngược lại, từ đó làm giảm ức chế LCAT do sản phẩm. Vì vậy, phần lớn cholesterol ester được tạo bởi LCAT sẽ được vận chuyển về gan qua phần còn lại của VLDL (IDL) và LDL. Đồng thời, HDL giàu triglyceride sẽ giải phóng triglyceride ở gan khi bị bắt giữ hoặc khi triglyceride được thủy phân bởi lipase gan nhạy cảm heparin (heparin-releasable hepatic lipase). Số lượng các hạt HDL to càng nhiều thì hệ quả sức khoẻ càng tốt; và ngược lại, số lượng này càng ít thì càng có nguy cơ xơ vữa động mạch. (Các xét nghiệm lipid truyền thống không cho biết được kích thước và số lượng của các hạt LDL và HDL.)
Điều hoà[sửa | sửa mã nguồn]
Sinh tổng hợp cholesterol được điều hoà trực tiếp bởi nồng độ cholesterol nội bào, nhưng cơ chế hằng định nội môi có liên quan chưa được hiểu rõ ràng. Lượng nhập trong thức ăn tăng sẽ làm giảm lượng nội sinh và ngược lại. Cơ chế điều hoà chính là phát hiện cholesterol nội bào ở lưới nội sinh chất bởi protein SREBP (Sterol Regulatory Element Binding Protein 1 và 2). Khi có mặt cholesterol, SREBP gắn với 2 protein khác: SCAP (SREBP-cleavage activating protein) và Insig-1. Khi nồng độ cholesterol giảm, Insig-1 tách khỏi phức hợp SREBP-SCAP, cho phép phức hợp di chuyển vào bộ máy Golgi, ở đó SREBP bị cắt bởi S1P và S2P (site 1/2 protease), hai men này được hoạt hoá bởi SCAP khi nồng độ cholesterol thấp. SREBP đã bị cắt sau đó di chuyển đến nhân và đóng vai trò yếu tố phiên mã (transcription factor) gắn với "Yếu tố Điều hoà Sterol" (Sterol Regulatory Element) của một số gene để kích thích phiên mã. Trong số các gene phiên mã có thụ thể LDL và HMG-CoA reductase. Thụ thể LDL thu bắt LDL trong tuần hoàn, còn HMG-CoA reductase làm tăng sản xuất cholesterol nội sinh.
Phần lớn cơ chế này được Michael S. Brown và Joseph L. Goldstein làm sáng tỏ vào thập kỉ 1970. Hai ông đoạt Giải Nobel về Sinh lý và Y khoa cho công trình của mình vào năm 1985.
Lượng cholesterol trung bình trong máu thay đổi theo tuổi tác, thường tăng dần cho đến khi khoảng 60 tuổi. Nghiên cứu của Ockrene và cs cho thấy nồng độ cholesterol cũng thay đổi theo mùa ở người, cao hơn vào mùa đông.
Chức năng[sửa | sửa mã nguồn]
Cholesterol là thành phần quan trọng của màng tế bào, nó giúp tính lỏng của màng ổn định trong khoảng dao động nhiệt độ rộng hơn. Nhóm hydroxyl trên phân tử tương tác với đầu phosphate của màng còn gốc steroid và chuỗi hydrocarbon gắn sâu vào màng. Nó là tiền chất chính để tổng hợp vitamin D, nhiều loại hormone steroid, bao gồm cortisol, cortisone, và aldosterone ở tuyến thượng thận, và các hormone sinh dục progesterone, estrogen, và testosterone. Các nghiên cứu gần đây cho thấy cholesterol có vai trò quan trọng đối với các synapse ở não cũng như hệ miễn dịch, bao gồm việc chống ung thư.
Bài tiết[sửa | sửa mã nguồn]
Cholesterol được bài tiết từ gan vào mật và được tái hấp thu ở ruột. Trong một số trường hợp, khi bị cô đặc, như ở túi mật, nó kết tinh và là thành phần cấu tạo chính của hầu hết sỏi mật, bên cạnh sỏi lecitin và bilirubin ít gặp hơn.
Trong thức ăn[sửa | sửa mã nguồn]
Danh sách bên dưới liệt kê hàm lượng cholesterol trong 100g thức ăn, cho một số loại thức ăn có nguồn gốc động vật:
|
|
|
Xem thêm[sửa | sửa mã nguồn]
Tham khảo[sửa | sửa mã nguồn]
- ^ a b c d e f g h i j “Cholesterol trong một số thức ăn”. Bản gốc lưu trữ ngày 24 tháng 9 năm 2011. Truy cập ngày 23 tháng 8 năm 2011.
- ^ a b c “Tham khảo cholesterol trong thịt”. Bản gốc lưu trữ ngày 26 tháng 10 năm 2011. Truy cập ngày 23 tháng 8 năm 2011.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab Tham khảo cholesterol trong nội tạng
- Anderson RG. Joe Goldstein and Mike Brown: from cholesterol homeostasis to new paradigms in membrane biology. Trends Cell Biol 2003:13:534-9. PMID 14507481.
- Ockene IS, Chiriboga DE, Stanek EJ 3rd, Harmatz MG, Nicolosi R, Saperia G, Well AD, Freedson P, Merriam PA, Reed G, Ma Y, Matthews CE, Hebert JR. Seasonal variation in serum cholesterol levels: treatment implications and possible mechanisms. Arch Intern Med 2004;164:863-70. PMID 15111372.
Liên kết ngoài[sửa | sửa mã nguồn]
| Wikimedia Commons có thêm hình ảnh và phương tiện truyền tải về Cholesterol. |
- Các khía cạnh của tiêu hoá và chuyển hoá mỡ - Báo cáo của LHQ/TCYTTG 1994
- Hội Tim mạch Mỹ
- Hội Weston A. Price Lưu trữ 2005-03-03 tại Wayback Machine: nhóm nghi vấn về mối liên hệ giữa cholesterol và xơ vữa động mạch.
- Cholesterol (tiêu đề) Lưu trữ 2006-07-21 tại Wayback Machine
