Germani dioxide
| Germani dioxide | |||
|---|---|---|---|
| |||
| Danh pháp IUPAC | Germanium dioxide | ||
| Tên khác | Germani(IV) Oxide Germania ACC10380 G-15 Germanic Oxide | ||
| Nhận dạng | |||
| Số CAS | |||
| PubChem | |||
| Số RTECS | LY5240000 | ||
| Ảnh Jmol-3D | ảnh | ||
| SMILES | đầy đủ
| ||
| InChI | đầy đủ
| ||
| ChemSpider | |||
| UNII | |||
| Thuộc tính | |||
| Công thức phân tử | GeO2 | ||
| Khối lượng mol | 104,6088 g/mol | ||
| Bề ngoài | Bột trắng hoặc tinh thể không màu | ||
| Khối lượng riêng | 4,228 g/cm³ | ||
| Điểm nóng chảy | 1.115 °C (1.388 K; 2.039 °F) | ||
| Điểm sôi | |||
| Độ hòa tan trong nước | 4,47 g/L (25 ℃) 10,7 g/L (100 ℃) | ||
| Độ hòa tan | tan trong HF, không tan trong axit khác và kiềm | ||
| MagSus | -34,3·10-6 cm³/mol | ||
| Chiết suất (nD) | 1,65 | ||
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |||
Germani dioxide, còn được gọi dưới nhiều cái tên khác là germanic Oxide và germania, là một hợp chất vô cơ với công thức hóa học GeO2. Hợp chất này rất có giá trị kinh tế và là là nguồn thương mại chính của nguyên tố germani. GeO2 cũng được hình thành như một lớp thụ động trên germani thuần khiết khi tiếp xúc với oxy trong khí quyển.
Phản ứng hóa học[sửa | sửa mã nguồn]
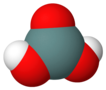
Là một Oxide axit, germani dioxide tác dụng với nước tạo thành axit metagermanic (H2GeO3):
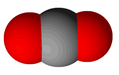 + + 
|
|---|
hoặc axit orthogermanic (H4GeO4):
 + 2 + 2 
|
|---|
Ứng dụng[sửa | sửa mã nguồn]
Hỗn hợp silic dioxide và germani dioxide ("silica germania") được sử dụng làm vật liệu quang học cho sợi quang và ống dẫn sóng quang.[1] Kiểm soát tỷ lệ của các phần tử cho phép điều khiển chính xác chỉ số khúc xạ. Kính silica-germania có độ nhớt thấp hơn và chỉ số khúc xạ cao hơn so với silic tinh khiết. Germania thay thế titania như là chất phụ gia silica cho sợi silica, loại bỏ nhu cầu xử lý nhiệt tiếp theo, và có tác dụng làm giòn cho các sợi này.[2]
Độc tính và y tế[sửa | sửa mã nguồn]
Germani dioxide có độc tính thấp, nhưng ở liều cao nó có gây độc.
Germani dioxide được sử dụng như là một chất bổ sung germani trong một số chất bổ sung dinh dưỡng và "chữa bệnh thần kỳ".[3] Liều cao trong việc điều trị này dẫn đến một vài trường hợp bị ngộ độc germani.
Tham khảo[sửa | sửa mã nguồn]
- ^ Robert D. Brown, Jr. (2000). “Germanium” (PDF). U.S. Geological Survey.
- ^ Chapter Iii: Optical Fiber For Communications Lưu trữ 2006-06-15 tại Wayback Machine
- ^ Tao, S.H.; Bolger, P.M. (tháng 6 năm 1997). “Hazard Assessment of Germanium Supplements”. Regulatory Toxicology and Pharmacology. 25 (3): 211–219. doi:10.1006/rtph.1997.1098. PMID 9237323.



