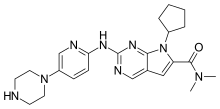
Ribociclib
 | |
| Dữ liệu lâm sàng | |
|---|---|
| Tên thương mại | Kisqali |
| Đồng nghĩa | LEE 011 |
| AHFS/Drugs.com | entry |
| MedlinePlus | a617008 |
| Dược đồ sử dụng | By mouth (tablets) |
| Mã ATC | |
| Tình trạng pháp lý | |
| Tình trạng pháp lý |
|
| Dữ liệu dược động học | |
| Sinh khả dụng | Unknown |
| Liên kết protein huyết tương | ~70% |
| Chuyển hóa dược phẩm | Liver (CYP3A4) |
| Chu kỳ bán rã sinh học | 32.0 (29.7–54.7) hrs |
| Bài tiết | 69% feces, 23% urine |
| Các định danh | |
Tên IUPAC
| |
| Số đăng ký CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| Định danh thành phần duy nhất | |
| KEGG | |
| ChEMBL | |
| ECHA InfoCard | 100.234.566 |
| Dữ liệu hóa lý | |
| Công thức hóa học | C23H30N8O |
| Khối lượng phân tử | 434,55 g·mol−1 |
| Mẫu 3D (Jmol) | |
SMILES
| |
Định danh hóa học quốc tế
| |
Ribociclib (tên thương mại Kisqali [1]) là chất ức chế cyclin D1/CDK4 và CDK6, và được sử dụng để điều trị một số loại ung thư vú.[2] Nó cũng đang được nghiên cứu như là một điều trị cho các bệnh ung thư kháng thuốc khác.[3] Nó được phát triển bởi Novartis và Astex Enterprises.[4]
Sử dụng trong y tế[sửa | sửa mã nguồn]
Ribociclib đã được FDA Hoa Kỳ phê duyệt vào tháng 3 năm 2017 và Cơ quan Dược phẩm Châu Âu vào tháng 8 năm 2017 để sử dụng kết hợp với chất ức chế aromatase (như letrozole) để điều trị ung thư vú di căn dương tính, HER2 âm tính hoặc di căn.[1][5]
Trong thử nghiệm lâm sàng liên quan đến sự chấp thuận của thuốc, ribociclib cải thiện đáng kể tỷ lệ sống không tiến triển (PFS), nghĩa là khoảng thời gian ung thư không trở nên tồi tệ hơn. Đối với bệnh nhân dùng giả dược cộng với letrozole, PFS trung bình là 16 tháng, trong khi theo ribociclib cộng với letrozole, PFS là 25 tháng kể từ phân tích tháng 1 năm 2017.[5] Nghiên cứu dự kiến sẽ được thực hiện cho đến tháng 9 năm 2020.[6]
Tác dụng phụ[sửa | sửa mã nguồn]
Các tác dụng phụ phổ biến nhất trong các nghiên cứu là giảm số lượng tế bào máu, chủ yếu là giảm bạch cầu trung tính (ở 75% bệnh nhân, so với 5% trong giả dược), nhưng cũng thiếu máu (18% so với 5%). Rối loạn tiêu hóa cũng rất phổ biến, ví dụ buồn nôn (52% so với 29%) và tiêu chảy (35% so với 22%), cũng như rụng tóc (33% so với 16%). Thuốc cũng làm tăng thời gian QT và men gan (alanine transaminase, aspartate transaminase).[2][5]
Tương tác[sửa | sửa mã nguồn]
Vì ribociclib được chuyển hóa chủ yếu bởi enzyme gan CYP3A4, các chất ức chế enzyme này làm tăng nồng độ của nó trong cơ thể và có thể làm tăng tác dụng phụ và độc tính. Ví dụ về các chất ức chế như vậy bao gồm ketoconazole và các loại thuốc chống nấm tương tự, ritonavir, clarithromycin, cũng như bưởi. Ngược lại, các loại thuốc gây ra CYP3A4, như rifampicin và St John's Wort, có thể làm giảm nồng độ ribociclib.[2][5]
Ribociclib tự nó là một chất ức chế CYP3A4 vừa đến mạnh và do đó có thể làm tăng nồng độ của các loại thuốc khác có chung chuyển hóa này, như đã được chứng minh với midazolam. Nó cũng ức chế một số protein vận chuyển và do đó về mặt lý thuyết có thể can thiệp vào việc vận chuyển các loại thuốc khác trong cơ thể. Nó cũng có thể khuếch đại kéo dài QT của các loại thuốc khác như thuốc chống loạn nhịp, clarithromycin và haloperidol.[2][5]
Dược lý[sửa | sửa mã nguồn]
Cơ chế hoạt động[sửa | sửa mã nguồn]
Kinase phụ thuộc cyclin (CDK) 4 và 6 là các enzyme đã được chứng minh là thúc đẩy sự phân chia và nhân lên của tế bào trong cả tế bào ung thư và bình thường. Nhiều tế bào ung thư đã cho thấy những bất thường làm tăng hoạt động của CDK, dẫn đến sự bất hoạt của một số gen ức chế khối u.[3][7]
Khi được sử dụng kết hợp với các loại thuốc khác như thuốc ức chế ALK hoặc MEK, ribociclib đã được chứng minh là có tác dụng hiệp đồng, dẫn đến phản ứng được cải thiện.[8][9] Một lần nữa, đây có thể là kết quả của " nhiễu xuyên âm " giữa các đường dẫn tín hiệu. Đơn giản chỉ cần chặn một con đường trong nguyên nhân khối u ung thư đôi khi có thể dẫn đến "bù khối u", trong đó khối u bù cho con đường truyền tín hiệu bị chặn bằng cách sử dụng các con đường khác để sống sót. Bằng cách chặn một số con đường cùng một lúc, người ta nghĩ rằng khối u ít có khả năng bù đắp, và một phản ứng chống khối u lớn hơn thường được quan sát. Sử dụng ribociclib kết hợp với các tác nhân khác đã được chứng minh là làm giảm sự phát triển đề kháng với các tác nhân này.[3] Nói cách khác, sự phát triển kháng thuốc của ung thư có thể được giảm thiểu bằng việc bổ sung ribociclib vào chế độ trị liệu.
Dược động học[sửa | sửa mã nguồn]
Tỷ lệ ribociclib được hấp thụ trong ruột chưa được xác định. Nồng độ huyết tương cao nhất đạt được sau một đến bốn giờ; và sau khi dùng liều lặp lại, nồng độ trạng thái ổn định đạt được sau khoảng tám ngày. Lượng thức ăn không ảnh hưởng đến tỷ lệ hấp thụ. Khi trong máu, khoảng 70% ribociclib liên kết với protein huyết tương.[2][5]
Chất này được chuyển hóa chủ yếu bởi CYP3A4 và sau đó là các enzyme pha II khác nhau, dẫn đến một số lượng lớn các chất chuyển hóa. Những người có nồng độ trong huyết tương cao nhất ở người được gọi là CCI284 (một sản phẩm N - hydroxylation không xác định), LEQ804 (sản phẩm N - demethylation) và M1 (một glucuronide). Tất cả các chất chuyển hóa có hoạt động lâm sàng không đáng kể.[2][5]
Ribociclib có xu hướng tích lũy nhẹ trong cơ thể. Nó được loại bỏ với thời gian bán hủy sinh học trung bình là 32 giờ, chủ yếu là (69%) qua phân, nhưng cũng (23%) qua nước tiểu. Thuốc không thay đổi chiếm 17% chất trong phân và 12% chất trong nước tiểu, phần còn lại là chất chuyển hóa.[2][5]
Nghiên cứu[sửa | sửa mã nguồn]
Tính đến tháng 9 năm 2017[cập nhật], ribociclib đang trong giai đoạn phát triển II cho một số chỉ định, bao gồm liposarcoma,[10] ung thư biểu mô nội mạc tử cung [11] và khối u thần kinh nội tạng của foregut.[12]
Hóa học[sửa | sửa mã nguồn]
Ribociclib được sử dụng dưới dạng muối tartrate của nó. Nó là một loại bột tinh thể màu vàng đến hơi hút ẩm có thể hòa tan trong axit nước.[13]
Xem thêm[sửa | sửa mã nguồn]
- Palbociclib, một loại thuốc có cơ chế và chỉ định tương tự
Tham khảo[sửa | sửa mã nguồn]
- ^ a b FDA Clears Novartis Kisqali for Combination Breast Cancer Therapy. March 2017
- ^ a b c d e f g Thông tin thuốc chuyên nghiệp FDA on Kisqali. Accessed 2017-09-08.
- ^ a b c Samson, Kurt (2014). “LEE011 CDK Inhibitor Showing Early Promise in Drug-Resistant Cancers”. Oncology Times. 36 (3): 39–40. doi:10.1097/01.COT.0000444043.33304.c1.
- ^ “Novartis LEE011 (ribociclib) granted FDA Priority Review for first-line treatment of HR+/HER2- advanced breast cancer”. Novartis. 1 tháng 11 năm 2016. Bản gốc lưu trữ ngày 25 tháng 9 năm 2018. Truy cập ngày 17 tháng 8 năm 2019. Đã bỏ qua tham số không rõ
|=(trợ giúp) - ^ a b c d e f g h “Kisqali: EPAR – Product Information” (PDF). European Medicines Agency. 31 tháng 8 năm 2017. Bản gốc (PDF) lưu trữ ngày 18 tháng 6 năm 2018. Truy cập ngày 17 tháng 8 năm 2019.
- ^ Clinical trial number NCT01958021 for "Study of Efficacy and Safety of LEE011 in Postmenopausal Women With Advanced Breast Cancer.(MONALEESA-2)" at ClinicalTrials.gov
- ^ Kim, S.; Loo, A.; Chopra, R.; Caponigro, G.; Huang, A.; Vora, S.; Parasuraman, S.; Howard, S.; Keen, N. (2014). “Abstract PR02: LEE011: An orally bioavailable, selective small molecule inhibitor of CDK4/6- Reactivating Rb in cancer”. Molecular Cancer Therapeutics. 12 (11_Supplement): PR02. doi:10.1158/1535-7163.TARG-13-PR02.
- ^ Sosman, Jeffrey Alan; Kittaneh, Muaiad; Lolkema, Martijn P. J. K.; Postow, Michael Andrew; Schwartz, Gary; Franklin, Catherine; Matano, Alessandro; Bhansali, Suraj; Parasuraman, Sudha (2014). “A phase 1b/2 study of LEE011 in combination with binimetinib (MEK162) in patients with NRAS-mutant melanoma: Early encouraging clinical activity”. Journal of Clinical Oncology. 32 (15 Suppl): 9009. doi:10.1200/jco.2014.32.15_suppl.9009. Bản gốc lưu trữ ngày 7 tháng 10 năm 2015. Truy cập ngày 17 tháng 8 năm 2019. Đã bỏ qua tham số không rõ
|=(trợ giúp) - ^ Wood, Andrew C.; Krytska, Kateryna; Ryles, Hannah; Sano, Renata; Li, Nanxin; King, Frederick; Smith, Timothy; Tuntland, Tove; Kim, Sunkyu (2014). “Abstract 1000: Combination CDK4/6 and ALK inhibition demonstrates on-target synergy against neuroblastoma”. Cancer Research. 74 (19 Supplement): 1000. doi:10.1158/1538-7445.AM2014-1000.
- ^ Clinical trial number NCT03096912 for "A Study Assessing Efficacy & Safety of Ribociclib in Patients With Advanced Well/Dedifferentiated Liposarcoma" at ClinicalTrials.gov
- ^ Clinical trial number NCT03008408 for "Study of Ribociclib (LEE011), Everolimus, and Letrozole, in Patients With Advanced or Recurrent Endometrial Carcinoma" at ClinicalTrials.gov
- ^ Clinical trial number NCT02420691 for "LEE011 in Neuroendocrine Tumors of Foregut Origin" at ClinicalTrials.gov
- ^ “Kisqali: EPAR – Public assessment report” (PDF). European Medicines Agency. 31 tháng 8 năm 2017. Bản gốc (PDF) lưu trữ ngày 18 tháng 6 năm 2018. Truy cập ngày 17 tháng 8 năm 2019.
