Ung thư phổi
| Ung thư phổi | |
|---|---|
 | |
| Bức ảnh X quang chụp ngực cho thấy một khối u trong phổi (đánh dấu mũi tên) | |
| Chuyên khoa | Oncology |
| ICD-10 | C33-C34 |
| ICD-9-CM | 162 |
| OMIM | 211980 |
| DiseasesDB | 7616 |
| MedlinePlus | 007194 |
| eMedicine | med/1333 med/1336 emerg/335 radio/807 radio/405 radio/406 |
| Patient UK | Ung thư phổi |
| MeSH | D002283 |
Ung thư phổi là căn bệnh trong đó xuất hiện một khối u ác tính được mô tả qua sự tăng sinh tế bào không thể kiểm soát trong các mô phổi.[1] Nếu người bệnh không được điều trị, sự tăng trưởng tế bào này có thể lan ra ngoài phổi đến các mô hoặc bộ phận khác của cơ thể, quá trình này gọi là di căn.[2] Hầu hết các loại ung thư khởi nguồn từ trong phổi (ung thư phổi nguyên phát) là ung thư biểu mô,.[3] Ung thư phổi được chia làm hai loại chính là ung thư phổi tế bào nhỏ (SCLC) và ung thư phổi không phải tế bào nhỏ (NSCLC).[4] Triệu chứng phổ biến nhất của căn bệnh này là ho (bao gồm cả ho ra máu), sụt cân, khó thở, và đau ngực.[5]
Đa phần các ca ung thư phổi (85%) có nguyên nhân bắt nguồn từ việc hút thuốc lá trong một thời gian dài.[6] Khoảng 10–15% trường hợp còn lại bệnh xảy ra ở những người chưa từng hút thuốc.[7] Đối với những trường hợp này, nguyên nhân là do sự kết hợp của các nhân tố di truyền, việc tiếp xúc trực tiếp với khí radon, amiăng, hút thuốc thụ động, hay không khí ô nhiễm.[8][9][10][11] Ung thư phổi có thể quan sát qua những tấm ảnh X quang ngực và chụp cắt lớp vi tính (CT).[6] Cách thức chẩn đoán là làm sinh thiết và thường được thực hiện bằng nội soi phế quản hay theo chỉ dẫn của chụp cắt lớp.[12][13]
Phương pháp phòng bệnh là tránh các nhân tố nguy cơ như khói thuốc và không khí ô nhiễm.[14] Việc điều trị và kết quả lâu dài phụ thuộc vào loại ung thư, giai đoạn bệnh (mức độ lây lan của khối u), và sức khỏe của người bệnh.[6] Đa số trường hợp là không thể chữa khỏi.[4] Các phương pháp chữa trị phổ biến gồm có phẫu thuật, hóa trị và xạ trị.[6] Ung thư phổi không phải tế bào nhỏ đôi khi áp dụng phương pháp phẫu thuật, còn với ung thư phổi tế bào nhỏ thì hóa trị và xạ trị thường đạt hiệu quả tốt hơn.[15]
Tính trên phạm vi toàn thế giới trong năm 2012, số ca mắc ung thư phổi là 1,8 triệu, trong đó 1,6 triệu người đã tử vong.[16] Điều này làm cho ung thư phổi là loại ung thư khiến số nam giới tử vong là cao nhất và số nữ giới tử vong là cao thứ nhì sau ung thư vú.[17] Độ tuổi chẩn đoán thường gặp nhất là 70.[18] Tại Mỹ, 17,4% số bệnh nhân sống sót sau năm năm kể từ thời điểm xác định mắc bệnh,[18] còn đối với những nước đang phát triển kết quả về mặt trung bình là kém hơn.[19]
Dấu hiệu và triệu chứng[sửa | sửa mã nguồn]
Những dấu hiệu và triệu chứng có thể là của ung thư phổi bao gồm:[5]
- Triệu chứng về đường hô hấp: ho, ho ra máu, thở khò khè, khó thở
- Triệu chứng toàn thân: sụt cân, mệt mỏi, sốt, móng tay dùi trống
- Triệu chứng do ung thư chèn ép nhiều sang các cơ quan kề bên: đau ngực, đau xương, tắc nghẽn tĩnh mạch chủ trên, khó nuốt
Nếu ung thư phát triển ở đường thở, nó có thể chặn dòng khí lưu thông, gây ra chứng khó thở. Sự cản trở này có thể dẫn tới việc tích lũy chất bài tiết phía sau chỗ tắc, qua đó mở đường cho viêm phổi.[5]
Tùy thuộc vào loại khối u, hội chứng cận ung thư (paraneoplastic syndrome) có thể là dấu hiệu thu hút sự chú ý ban đầu đến căn bệnh.[20] Đối với ung thư phổi, những hiện tượng này có thể bao gồm chứng tăng calci huyết, hội chứng tăng tiết hormone chống bài niệu không phù hợp (SIADH, nước tiếu đậm đặc và máu loãng một cách bất thường), hormon vỏ thượng thận (ACTH) sản xuất lệch vị trí, hội chứng nhược cơ Lambert–Eaton (cơ bắp yếu đi do rối loạn tự miễn dịch). Các khối u trên đỉnh phổi, biết đến với tên gọi khối u Pancoast, có thể xâm lấn hệ thần kinh giao cảm, dẫn tới hội chứng horner (sụp mí mắt và co đồng tử cùng bên) và gây tổn hại đến đám rối thần kinh cánh tay (brachial plexus).[5]
Phần lớn các triệu chứng của ung thư phổi (chán ăn, sụt cân, sốt, mệt mỏi) là không đặc biệt.[12] Đối với nhiều người, vào thời điểm họ phát hiện ra những dấu hiệu bệnh tật và đi tìm sự chăm sóc y tế, khối u đã lan ra ngoài địa điểm khởi phát.[21] Các triệu chứng có thể báo hiệu quá trình di căn đã xuất hiện bao gồm sụt cân, đau xương và các triệu chứng về thần kinh (đau đầu, ngất xỉu, co giật, yếu chi).[5] Những địa điểm khối u lan sang thường gặp đó là não, xương, tuyến thượng thận, lá phổi còn lại, gan, màng ngoài tim, và thận.[21] Khoảng 10% số ca ung thư phổi không thấy những triệu chứng khi chẩn đoán, những trường hợp này bệnh tình cờ phát hiện nhờ việc chụp X quang ngực định kỳ.[13]
Nguyên nhân[sửa | sửa mã nguồn]

Ung thư phát triển từ tổn thương DNA về mặt di truyền và những sự biến đổi ngoại di truyền (epigenetic). Những đột biến này ảnh hưởng đến các chức năng bình thường của tế bào, bao gồm sự tăng sinh tế bào, quá trình chết theo chương trình của tế bào (apoptosis) và sửa chữa DNA. Tổn thương tích lũy càng nhiều thì nguy cơ mắc ung thư càng tăng lên.[22]
Hút thuốc[sửa | sửa mã nguồn]
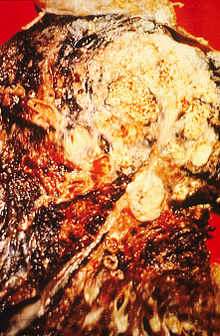
Hút thuốc, đặc biệt là thuốc lá điếu, cho đến nay là tác nhân chính gây ra ung thư phổi. Trong khói thuốc lá có chứa ít nhất 73 chất gây ung thư đã biết,[23] như là benzo(a)pyren,[24] NNK, buta-1,3-dien, và một đồng vị phóng xạ của poloni đó là poloni-210.[23] Tại các nước phát triển, 90% số ca tử vong do ung thư phổi ở nam giới trong năm 2000 được cho là do hút thuốc, tỉ lệ này đối với phụ nữ là 70%.[25] Hút thuốc cũng là nguyên nhân của khoảng 85% số ca mắc bệnh.[6]
Việc hít phải khói thuốc từ một người khác đang hút thuốc, hay thường được gọi là hút thuốc thụ động, là một trong những nguyên nhân gây ra ung thư phổi ở những người không hút thuốc. Các nghiên cứu tới từ Mỹ,[26][27][28] châu Âu,[29] và Anh[30] đã cùng nhất quán chỉ ra mức độ rủi ro là gia tăng đáng kể đối với những trường hợp hút thuốc thụ động.[31] Nguy cơ mắc bệnh đối với những người sống cùng với người hút thuốc tăng lên từ 20–30% trong khi đối với những người làm việc trong môi trường có khói thuốc là 16–19%.[32] Các nghiên cứu chỉ ra khói thuốc bay ra ngoài không khí từ điếu thuốc cháy (sidestream smoke) nguy hiểm hơn nhiều so với loại khói mà người hút thuốc trực tiếp hít vào (mainstream smoke).[33]
Khói cần sa cũng chứa nhiều chất gây ung thư tương tự như khói thuốc lá.[34] Tuy nhiên, mối quan hệ giữa việc hút cần sa và nguy cơ mắc ung thư phổi là không rõ ràng.[35][36] Một cuộc xem xét lại thực hiện năm 2013 đã không tìm thấy sự gia tăng nguy cơ từ việc dùng cần sa ít đến trung bình.[37] Tuy nhiên đợt kiểm tra năm 2014 lại chỉ ra hút cần sa làm tăng gấp đôi nguy cơ mắc ung thư phổi.[38]
Khí Radon[sửa | sửa mã nguồn]
Radon là một loại khí không màu, không mùi được tạo ra từ hoạt động phân rã chất phóng xạ radi là sản phẩm phân rã của urani và được tìm thấy trong lớp vỏ Trái Đất. Các sản phẩm phân rã của quá trình phóng xạ ion hóa vật chất di truyền, gây ra những sự đột biến mà đôi khi chuyển đổi thành ung thư. Tại Mỹ, Radon là nguyên nhân gây ra ung thư phổi phổ biến thứ hai[39] khiến khoảng 21.000 người tử vong mỗi năm.[40] Mức độ tập trung khí Radon tăng lên mỗi 100 Bq/m³ thì nguy cơ mắc bệnh tăng lên từ 8–16%.[41] Hàm lượng khí Radon có sự khác biệt tùy vào khu vực và thành phần đất đá ở dưới mặt đất.[42]
Amiăng[sửa | sửa mã nguồn]
Amiăng là loại chất có thể gây ra nhiều loại bệnh ở phổi khác nhau, trong đó có ung thư phổi. Hút thuốc lá và amiăng có ảnh hưởng kết hợp trong việc dẫn tới sự hình thành ung thư phổi.[8] Đối với những người hút thuốc có tiếp xúc với amiăng, nguy cơ mắc bệnh tăng tới 45 lần.[43] Ngoài ra amiăng còn có thể gây ra ung thư màng phổi, được gọi là u trung biểu mô màng phổi (khác với ung thư phổi).[44]
Ô nhiễm không khí[sửa | sửa mã nguồn]
Ô nhiễm không khí ngoài trời có một tác động nhỏ đến sự gia tăng nguy cơ mắc ung thư phổi. Các hạt vật chất nhỏ (bụi PM2.5) và các sol khí sunfat (có trong khí thải xe cộ) có liên quan tới sự gia tăng nguy cơ nhẹ.[45] Lượng nitơ dioxide trong không khí tăng lên 10 phần tỉ sẽ làm tăng nguy cơ mắc bệnh lên 14%.[46] Theo ước tính, ô nhiễm không khí ngoài trời là nguyên nhân của 1–2% số trường hợp mắc ung thư phổi.
Có bằng chứng tạm thời ủng hộ rằng ô nhiễm không khí trong nhà liên quan tới việc đốt củi, than, phân hay tàn dư thực vật phục vụ cho nấu nướng hay sưởi ấm trong gia đình làm gia tăng nguy cơ mắc ung thư phổi.[47] Phụ nữ tiếp xúc (phơi nhiễm) với khói than trong nhà có nguy cơ khoảng chừng gấp đôi và các sản phẩm phụ của việc đốt cháy sinh khối là, hoặc bị nghi ngờ là tác nhân gây ung thư.[48] Nguy cơ này ảnh hưởng đến khoảng 2,4 tỉ người trên toàn cầu[47] và người ta tin rằng nó là nguyên nhân của 1,5% số ca tử vong do ung thư phổi.[48]
Di truyền[sửa | sửa mã nguồn]
Khoảng 8% số ca ung thư phổi có nguyên nhân tới từ các yếu tố di truyền.[49] Một người có quan hệ họ hàng với người bị ung thư phổi thì nguy cơ mắc bệnh sẽ tăng lên 2,4 lần. Điều này khả năng là do sự kết hợp gen.[50] Tính đa hình của các nhiễm sắc thể 5, 6 và 15 có tác động đến nguy cơ mắc ung thư phổi.[51]
Nguyên nhân khác[sửa | sửa mã nguồn]
Ngoài các nguyên nhân kể trên, còn nhiều yếu tố khác có mối liên hệ với ung thư phổi, như các chất (hóa học), nghề nghiệp, và kiểu tình trạng tiếp xúc với môi trường. Cơ quan Nghiên cứu Ung thư Quốc tế (IARC) phát biểu rằng có "bằng chứng đầy đủ" chỉ ra các yếu tố dưới đây là tác nhân gây ra ung thư ở phổi:[52]
- Một số kim loại (sản phẩm nhôm, cadmi và các hợp chất của cadmi, các hợp chất crom (VI), beryli và các hợp chất của beryli, sắt và thép nóng chảy, các hợp chất của niken, asen và các hợp chất vô cơ của asen, hematit khai thác dưới mặt đất)
- Một số sản phẩm của sự cháy (cháy không hoàn toàn, than đá [khí thải phát ra trong nhà từ việc đốt than], khí hóa than, dầu nhựa than đá, than cốc, bồ hóng, khí thải động cơ diesel)
- Bức xạ ion hóa (bức xạ tia X, bức xạ gamma, plutoni)
- Một số khí độc (metyl ete [dùng trong công nghiệp], Bis-(clorometyl) ete, mù tạc lưu huỳnh, MOPP [ hỗn hợp vincristin-prednison-mù tạc nitơ-procarbazin ], hơi sơn)
- Sản phẩm cao su và bụi silic oxide kết tinh (bụi tinh thể SiO2)
Sự phát sinh[sửa | sửa mã nguồn]
Tương tự như nhiều loại ung thư khác, ung thư phổi khởi nguồn từ sự hoạt hóa các gen gây ung thư (oncogene) hoặc sự bất hoạt các gen ức chế khối u (hay gen chống ung thư, antioncogene).[53] Các tác nhân gây ung thư gây ra đột biến ở những gen này, qua đó mở đường cho sự phát triển của bệnh.[54]
Những đột biến trong gene tiền ung thư (proto-oncogene) K-ras là nguyên nhân của 10–30% số ca ung thư biểu mô tuyến phổi.[55][56] Khoảng 4% số trường hợp ung thư phổi không phải tế bào nhỏ có liên quan tới gen tổ hợp tyrosine kinase EML4-ALK.[57]
Những đột biến ngoại di truyền (epigenetic); như sự biến đổi quá trình metyl hóa DNA, sự sửa đổi đuôi histon, hay sự điều chỉnh microRNA; có thể làm cho các gen ức chế khối u ngừng hoạt động.[58]
Thụ thể yếu tố tăng trưởng thượng bì (EGFR) điều chỉnh quá trình tăng sinh tế bào, quá trình chết theo chương trình của tế bào (apoptosis), tân sinh mạch (angiogenesis), và sự xâm lấn của khối u.[55] Những đột biến và khuếch đại EGFR thường gặp ở ung thư phổi không phải tế bào nhỏ cung cấp cơ sở cho việc điều trị bằng các chất ức chế EGFR. Thụ thể HER2/neu ít bị ảnh hưởng thường xuyên.[55] Các gen thường bị đột biến hay khuếch đại khác là c-MET, NKX2-1, LKB1, PIK3CA, và BRAF.[55]
Cho tới nay con người chưa hiểu biết hết về các dòng tế bào gốc.[5] Cơ chế có thể liên quan tới sự hoạt hóa một cách bất thường các tế bào gốc. Trong đường thở gần (hay đường dẫn khí, [proximal airways—tạm dịch], khí quản—phần gần nhất với đỉnh của cây hô hấp), các tế bào gốc biểu hiện keratin 5 nhiều khả năng bị tác động và thường dẫn tới ung thư phổi tế bào vảy (ung thư biểu mô tế bào vảy của phổi). Trong đường thở giữa (middle airways), các tế bào gốc liên quan bao gồm tế bào club (ban đầu được biết đến với tên gọi tế bào Clara) và tế bào biểu mô thần kinh biểu lộ protein chế tiết của tế bào club. Ung thư phổi tế bào nhỏ có thể có nguồn gốc từ những dòng tế bào này[59] hoặc tế bào thần kinh nội tiết,[5] và có thể biểu hiện glycoprotein CD44.[59]
Sự di căn của ung thư phổi đòi hỏi quá trình chuyển đổi kiểu tế bào từ biểu mô thành trung mô. Điều này có thể xảy ra thông qua sự hoạt hóa các đường truyền tín hiệu như Akt/GSK3Beta, MEK-ERK, Fas, và Par6.[60]
Chẩn đoán[sửa | sửa mã nguồn]

Chiếu chụp lồng ngực bằng tia X là một trong những bước khảo sát đầu tiên nếu người bệnh thông báo các triệu chứng có thể là của ung thư phổi. Việc làm này có thể tiết lộ một trung thất khuếch trương dễ quan sát, tình trạng xẹp phổi, viêm phổi hoặc tràn dịch màng phổi.[6] Ảnh chụp cắt lớp vi tính (CT) thường được sử dụng để cung cấp thêm thông tin về loại bệnh và mức độ bệnh. Nội soi phế quản hoặc làm sinh thiết theo chỉ dẫn CT thường được dùng để lấy mẫu khối u phục vụ cho việc khám nghiệm mô (mô bệnh học).[13]
Ung thư phổi thường xuất hiện với hình ảnh một nốt phổi đơn độc (SPN) trên ảnh X quang chụp lồng ngực. Tuy nhiên, phạm vi chẩn đoán phân biệt là rộng. Dấu hiệu này cũng có ở nhiều loại bệnh khác như lao, nhiễm nấm, ung thư di căn hay viêm phổi tổ chức hóa. Ngoài ra còn các nguyên nhân ít gặp hơn cũng làm xuất hiện nốt đơn độc ở phổi là u mô thừa, nang phế quản, u tuyến, dị dạng động tĩnh mạch, phổi biệt lập, nốt thấp, granulomatosis với polyangiitis (trước đây gọi là u hạt wegener), hoặc lymphoma (u lympho hay ung thư hạch bạch huyết).[61] Ung thư phổi còn có thể được phát hiện một cách tình cờ (incidentaloma) nhờ quan sát thấy hình ảnh nốt phổi đơn độc trên ảnh X quang lồng ngực hoặc ảnh chụp cắt lớp vi tính thực hiện vì một lý do không liên quan.[62] Chẩn đoán xác định ung thư phổi dựa trên kết quả kiểm tra các mô đáng ngờ[5] xét trong bối cảnh các đặc điểm lâm sàng và X quang.[12]
Các hướng dẫn thực hành lâm sàng (CPG) khuyên áp dụng việc giám sát nốt phổi thường xuyên.[63] Không nên lạm dụng việc chụp CT lâu dài hoặc thường xuyên hơn so với chỉ định bởi kéo dài thời hạn và mức độ sẽ làm con người phơi nhiễm với sự gia tăng bức xạ.[64]
Phân loại[sửa | sửa mã nguồn]
Ung thư phổi được phân loại dựa theo kết quả xét nghiệm mô bệnh học.[12] Sự phân loại này là quan trọng cho việc theo dõi, điều trị và dự đoán kết quả bệnh. Các loại ung thư phổi là ung thư biểu mô, những khối u ác tính phát sinh từ tế bào biểu mô. Ung thư biểu mô phổi được phân theo kích cỡ và diện mạo của các tế bào ác tính quan sát thấy dưới kính hiển vi bởi một nhà mô bệnh học. Để phục vụ cho mục đích điều trị, người ta phân ra hai loại lớn: ung thư phổi không phải tế bào nhỏ và ung thư phổi tế bào nhỏ.[65]
Ung thư phổi không phải tế bào nhỏ[sửa | sửa mã nguồn]
| Loại ung thư | Tỷ lệ mắc mỗi 100.000 người mỗi năm |
|---|---|
| Tất cả | 66,9 |
| Ung thư biểu mô tuyến | 22,1 |
| Ung thư biểu mô tế bào vảy | 14,4 |
| Ung thư biểu mô tế bào nhỏ | 9,8 |

Ung thư phổi không phải tế bào nhỏ (NSCLC) được chia thành các loại nhỏ hơn, ba loại chính trong đó là ung thư biểu mô tuyến, ung thư biểu mô tế bào vảy và ung thư biểu mô tế bào lớn.[5]
Gần 40% số ca ung thư phổi là ung thư biểu mô tuyến, loại này thường bắt nguồn từ mô phổi ngoại vi.[12] Mặc dù hầu hết các ca ung thư biểu mô tuyến có liên quan tới việc hút thuốc, nhưng đây cũng là hình thái ung thư phổ biến nhất ở những người hút ít hơn 100 điếu thuốc trong suốt cuộc đời ("những người không hút thuốc")[5][66] và những người có tiền sử hút thuốc khiêm tốn.[5] Một phân loại phụ của ung thư biểu mô tuyến, AIS (tạm dịch: Ung thư biểu mô tuyến phổi tại chỗ, trước đây gọi là ung thư biểu mô bronchioloalveolar), thường gặp hơn ở những nữ giới không hút thuốc và có thể khả năng sống sót về lâu dài là cao hơn.[67]
Ung thư biểu mô tế bào vảy chiếm khoảng 30% số trường hợp ung thư phổi. Loại này thường xảy ra ở gần đường dẫn khí lớn. Một khoảng trống và sự chết tế bào thường được tìm thấy ở trung tâm khối u.[12] Khoảng 9% số ca ung thư phổi thuộc loại ung thư biểu mô tế bào lớn. Sở dĩ tên gọi như vậy vì tế bào ung thư là lớn, với sự dư thừa tế bào chất, nhân tế bào lớn và hạch nhân dễ thấy.[12]
Ung thư phổi tế bào nhỏ[sửa | sửa mã nguồn]

Ở ung thư phổi tế bào nhỏ (SCLC), các tế bào chứa dày đặc các hạt tiết thể dịch thần kinh (các túi tiết chứa hormon thần kinh nội tiết), do đó khối u loại này có liên đới với hội chứng cận ung thư/nội tiết.[68] Đa số trường hợp bệnh phát sinh ở đường dẫn khí lớn (phế quản chính và phế quản thùy).[13] 60 đến 70% trường hợp bệnh đã lan rộng (không thể xạ trị tại một phạm vi đơn lẻ) tại thời điểm quan sát.[5]
Loại khác[sửa | sửa mã nguồn]
Có bốn loại phụ chính được công nhận, mặc dù một số trường hợp có thể bao hàm sự kết hợp của các loại phụ khác nhau[69] như ung thư biểu mô tuyến vảy.[12] Các loại phụ hiếm gặp gồm có U carcinoid, ung thư biểu mô tuyến phế quản, và ung thư biểu mô sarcomatoid.[12]
Di căn[sửa | sửa mã nguồn]
Phổi là nơi thường chứng kiến khối u từ các bộ phận khác của cơ thể lây lan sang. Ung thư thứ phát được phân loại dựa theo địa điểm phát sinh ban đầu, ví dụ: ung thư vú lan sang phổi được gọi là ung thư vú di căn. Khối u di căn thường có diện mạo tròn trên ảnh X quang.[70]
Những trường hợp ung thư phổi nguyên phát hay di căn tới não, xương, gan, và tuyến thượng thận.[12] Nhuộm miễn dịch (immunostaining) một mẫu sinh thiết thường giúp ích cho việc xác định nguồn gốc.[71] Sự hiện diện của các loại protein Napsin-A, TTF-1, CK7 và CK20 giúp xác định loại ung thư phổi. Ung thư phổi tế bào nhỏ có nguồn gốc từ các tế bào thần kinh nội tiết có thể biểu hiện CD56, phân tử kết dính tế bào thần kinh, synaptophysin hoặc chromogranin.[5]
Tham khảo[sửa | sửa mã nguồn]
- ^ “Non-Small Cell Lung Cancer Treatment –Patient Version (PDQ®)”. NCI. ngày 12 tháng 5 năm 2015. Truy cập ngày 5 tháng 3 năm 2016.
- ^ Falk, S; Williams, C (2010). “Chapter 1”. Lung Cancer—the facts (ấn bản 3). Oxford University Press. tr. 3–4. ISBN 978-0-19-956933-5.
- ^ World Cancer Report 2014. World Health Organization. 2014. tr. Chapter 5.1. ISBN 92-832-0429-8.
- ^ a b “Lung Cancer—Patient Version”. NCI. Truy cập ngày 5 tháng 3 năm 2016.
- ^ a b c d e f g h i j k l m Horn, L; Lovly, CM; Johnson, DH (2015). “Chapter 107: Neoplasms of the lung”. Trong Kasper, DL; Hauser, SL; Jameson, JL; Fauci, AS; Longo, DL; Loscalzo, J (biên tập). Harrison's Principles of Internal Medicine (ấn bản 19). McGraw-Hill. ISBN 978-0-07-180216-1.
- ^ a b c d e f Keith, Robert L (tháng 3 năm 2018). “Lung Carcinoma: Tumors of the Lungs”. Merck Manual. Merck Manual Professional Edition, Online edition. Bản gốc lưu trữ ngày 17 tháng 12 năm 2019. Truy cập ngày 17 tháng 12 năm 2019.
- ^ Thun MJ, Hannan LM, Adams-Campbell LL, và đồng nghiệp (tháng 9 năm 2008). “Lung cancer occurrence in never-smokers: an analysis of 13 cohorts and 22 cancer registry studies”. PLoS Medicine. 5 (9): e185. doi:10.1371/journal.pmed.0050185. PMC 2531137. PMID 18788891.
- ^ a b O'Reilly, KM; Mclaughlin AM; Beckett WS; Sime PJ (tháng 3 năm 2007). “Asbestos-related lung disease”. American Family Physician. 75 (5): 683–688. PMID 17375514. Bản gốc lưu trữ ngày 29 tháng 9 năm 2007. Truy cập ngày 6 tháng 3 năm 2016.
- ^ Alberg AJ, Samet JM (2010). “Chapter 46”. Murray & Nadel's Textbook of Respiratory Medicine (ấn bản 5). Saunders Elsevier. ISBN 978-1-4160-4710-0.
- ^ Carmona, RH (ngày 27 tháng 6 năm 2006). “The Health Consequences of Involuntary Exposure to Tobacco Smoke: A Report of the Surgeon General”. U.S. Department of Health and Human Services.
Secondhand smoke exposure causes disease and premature death in children and adults who do not smoke.
Retrieved 2014-06-16 - ^ “Tobacco Smoke and Involuntary Smoking” (PDF). IARC Monographs on the Evaluation of Carcinogenic Risks to Humans. WHO International Agency for Research on Cancer. 83. 2004.
There is sufficient evidence that involuntary smoking (exposure to secondhand or 'environmental' tobacco smoke) causes lung cancer in humans. ... Involuntary smoking (exposure to secondhand or 'environmental' tobacco smoke) is carcinogenic to humans (Group 1).
- ^ a b c d e f g h i j Lu C, Onn A, Vaporciyan AA, và đồng nghiệp (2010). “78: Cancer of the Lung”. Holland-Frei Cancer Medicine (ấn bản 8). People's Medical Publishing House. ISBN 978-1-60795-014-1.
- ^ a b c d Collins, LG; Haines C; Perkel R; Enck RE (tháng 1 năm 2007). “Lung cancer: diagnosis and management”. American Family Physician. American Academy of Family Physicians. 75 (1): 56–63. PMID 17225705. Bản gốc lưu trữ ngày 29 tháng 9 năm 2007. Truy cập ngày 6 tháng 3 năm 2016.
- ^ “Lung Cancer Prevention–Patient Version (PDQ®)”. NCI. ngày 4 tháng 11 năm 2015. Truy cập ngày 5 tháng 3 năm 2016.
- ^ Chapman, S; Robinson G; Stradling J; West S (2009). “Chapter 31”. Oxford Handbook of Respiratory Medicine (ấn bản 2). Oxford University Press. ISBN 978-0-19-954516-2.
- ^ World Cancer Report 2014. World Health Organization. 2014. tr. Chapter 5.1. ISBN 9283204298.
- ^ World Cancer Report 2014. World Health Organization. 2014. tr. Chapter 1.1. ISBN 9283204298.
- ^ a b “Surveillance, Epidemiology and End Results Program”. National Cancer Institute. Truy cập ngày 5 tháng 3 năm 2016.
- ^ Majumder, edited by Sadhan (2009). Stem cells and cancer . New York: Springer. tr. 193. ISBN 978-0-387-89611-3.Quản lý CS1: văn bản dư: danh sách tác giả (liên kết)
- ^ Honnorat, J; Antoine JC (tháng 5 năm 2007). “Paraneoplastic neurological syndromes”. Orphanet Journal of Rare Diseases. BioMed Central. 2 (1): 22. doi:10.1186/1750-1172-2-22. PMC 1868710. PMID 17480225. Lưu trữ bản gốc ngày 27 tháng 9 năm 2007.
- ^ a b Greene, Frederick L. (2002). AJCC cancer staging manual. Berlin: Springer-Verlag. ISBN 0-387-95271-3.
- ^ Brown KM, Keats JJ, Sekulic A, và đồng nghiệp (2010). “Chapter 8”. Holland-Frei Cancer Medicine (ấn bản 8). People's Medical Publishing House USA. ISBN 978-1-60795-014-1.
- ^ a b Hecht, SS (2012). “Lung carcinogenesis by tobacco smoke”. International Journal of Cancer. 131 (12): 2724–2732. doi:10.1002/ijc.27816. PMC 3479369. PMID 22945513.
- ^ Kumar, V; Abbas AK; Aster JC (2013). “Chapter 5”. Robbins Basic Pathology (ấn bản 9). Elsevier Saunders. tr. 199. ISBN 978-1-4377-1781-5.
- ^ Peto R, Lopez AD, Boreham J, và đồng nghiệp (2006). Mortality from smoking in developed countries 1950–2000: Indirect estimates from National Vital Statistics. Oxford University Press. ISBN 0-19-262535-7. Lưu trữ bản gốc ngày 5 tháng 9 năm 2007.
- ^ California Environmental Protection Agency (1997). “Health effects of exposure to environmental tobacco smoke. California Environmental Protection Agency”. Tobacco Control. 6 (4): 346–353. doi:10.1136/tc.6.4.346. PMC 1759599. PMID 9583639.
- ^ Centers for Disease Control and Prevention (CDC) (tháng 12 năm 2001). “State-specific prevalence of current cigarette smoking among adults, and policies and attitudes about secondhand smoke—United States, 2000”. Morbidity and Mortality Weekly Report. Atlanta, Georgia: CDC. 50 (49): 1101–1106. PMID 11794619.
- ^ Alberg, AJ; Samet JM (tháng 9 năm 2007). “Epidemiology of lung cancer”. Chest. American College of Chest Physicians. 132 (S3): 29S–55S. doi:10.1378/chest.07-1347. PMID 17873159. Bản gốc lưu trữ ngày 29 tháng 3 năm 2020. Truy cập ngày 7 tháng 3 năm 2016.
- ^ Jaakkola, MS; Jaakkola JJ (tháng 8 năm 2006). “Impact of smoke-free workplace legislation on exposures and health: possibilities for prevention”. European Respiratory Journal. 28 (2): 397–408. doi:10.1183/09031936.06.00001306. PMID 16880370.
- ^ Parkin, DM (tháng 12 năm 2011). “Tobacco—attributable cancer burden in the UK in 2010”. British Journal of Cancer. 105 (Suppl. 2): S6–S13. doi:10.1038/bjc.2011.475. PMC 3252064. PMID 22158323.
- ^ Taylor, R; Najafi F; Dobson A (tháng 10 năm 2007). “Meta-analysis of studies of passive smoking and lung cancer: effects of study type and continent”. International Journal of Epidemiology. 36 (5): 1048–1059. doi:10.1093/ije/dym158. PMID 17690135.
- ^ “Frequently asked questions about second hand smoke”. World Health Organization. Truy cập ngày 25 tháng 7 năm 2012.
- ^ Schick, S; Glantz S (tháng 12 năm 2005). “Philip Morris toxicological experiments with fresh sidestream smoke: more toxic than mainstream smoke”. Tobacco Control. 14 (6): 396–404. doi:10.1136/tc.2005.011288. PMC 1748121. PMID 16319363.
- ^ Greydanus, DE; Hawver EK; Greydanus MM (tháng 10 năm 2013). “Marijuana: current concepts”. Frontiers in Public Health. 1 (42). doi:10.3389/fpubh.2013.00042. PMC 3859982. PMID 24350211.
- ^ Owen, KP; Sutter, ME; Albertson, TE (tháng 2 năm 2014). “Marijuana: respiratory tract effects”. Clinical reviews in allergy & immunology. 46 (1): 65–81. doi:10.1007/s12016-013-8374-y. PMID 23715638.
- ^ Joshi, M; Joshi, A; Bartter, T (tháng 3 năm 2014). “Marijuana and lung diseases”. Current Opinion in Pulmonary Medicine. 20 (2): 173–179. doi:10.1097/mcp.0000000000000026. PMID 24384575.
- ^ Tashkin, DP (tháng 6 năm 2013). “Effects of marijuana smoking on the lung”. Annals of the American Thoracic Society. 10 (3): 239–47. doi:10.1513/annalsats.201212-127fr. PMID 23802821.
- ^ Underner, M; Urban T; Perriot J (tháng 6 năm 2014). “Cannabis smoking and lung cancer”. Revue des Maladies Respiratoires. 31 (6): 488–498. doi:10.1016/j.rmr.2013.12.002. PMID 25012035.
- ^ Choi, H; Mazzone, P (tháng 9 năm 2014). “Radon and lung cancer: assessing and mitigating the risk”. Cleveland Clinic Journal of Medicine. 81 (9): 567–575. doi:10.3949/ccjm.81a.14046. PMID 25183848.
- ^ “Radon (Rn) Health Risks”. EPA.
- ^ Schmid K, Kuwert T, Drexler H (tháng 3 năm 2010). “Radon in Indoor Spaces: An Underestimated Risk Factor for Lung Cancer in Environmental Medicine”. Dtsch Arztebl Int. 107 (11): 181–6. doi:10.3238/arztebl.2010.0181. PMC 2853156. PMID 20386676.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- ^ EPA (tháng 2 năm 2013). “Radiation information: radon”. EPA. Lưu trữ bản gốc ngày 29 tháng 4 năm 2009.
- ^ Tobias, J; Hochhauser D (2010). “Chapter 12”. Cancer and its Management (ấn bản 6). Wiley-Blackwell. tr. 199. ISBN 978-1405-170154.
- ^ Davies, RJO; Lee YCG (2010). “18.19.3”. Oxford Textbook Medicine (ấn bản 5). OUP Oxford. ISBN 978-0-19-920485-4.
- ^ Chen, H; Goldberg MS; Villeneuve PJ (Oct–Dec 2008). “A systematic review of the relation between long-term exposure to ambient air pollution and chronic diseases”. Reviews on Environmental Health. 23 (4): 243–297. doi:10.1515/reveh.2008.23.4.243. PMID 19235364.
- ^ Clapp, RW; Jacobs MM; Loechler EL (Jan–Mar 2008). “Environmental and Occupational Causes of Cancer New Evidence, 2005–2007”. Reviews on Environmental Health. 23 (1): 1–37. doi:10.1515/REVEH.2008.23.1.1. PMC 2791455. PMID 18557596.
- ^ a b Lim, WY; Seow, A (tháng 1 năm 2012). “Biomass fuels and lung cancer”. Respirology (Carlton, Vic.). 17 (1): 20–31. doi:10.1111/j.1440-1843.2011.02088.x. PMID 22008241.
- ^ a b Sood, A (tháng 12 năm 2012). “Indoor fuel exposure and the lung in both developing and developed countries: an update”. Clinics in chest medicine. 33 (4): 649–65. doi:10.1016/j.ccm.2012.08.003. PMID 23153607.
- ^ Yang, IA; Holloway, JW; Fong, KM (tháng 10 năm 2013). “Genetic susceptibility to lung cancer and co-morbidities”. Journal of Thoracic Disease. 5 (Suppl. 5): S454–S462. doi:10.3978/j.issn.2072-1439.2013.08.06. PMC 3804872. PMID 24163739.
- ^ Kern JA, McLennan G (2008). Fishman's Pulmonary Diseases and Disorders (ấn bản 4). McGraw-Hill. tr. 1802. ISBN 0-07-145739-9.
- ^ Larsen, JE; Minna D (tháng 12 năm 2011). “Molecular biology of lung cancer: clinical implications”. Clinics in Chest Medicine. 32 (4): 703–740. doi:10.1016/j.ccm.2011.08.003. PMC 3367865. PMID 22054881.
- ^ Cogliano, VJ; Baan, R; Straif, K; Grosse, Y; Lauby-Secretan, B; El Ghissassi, F; Bouvard, V; Benbrahim-Tallaa, L; Guha, N; Freeman, C; Galichet, L; Wild, CP (ngày 21 tháng 12 năm 2011). “Preventable exposures associated with human cancers” (PDF). Journal of the National Cancer Institute. 103 (24): 1827–39. doi:10.1093/jnci/djr483. PMID 22158127. Bản gốc (PDF) lưu trữ ngày 20 tháng 9 năm 2012. Truy cập ngày 8 tháng 3 năm 2016.Quản lý CS1: sử dụng tham số tác giả (liên kết)
- ^ Cooper, WA; Lam DLC; O'Toole SA (tháng 10 năm 2013). “Molecular biology of lung cancer” (PDF). Journal of Thoracic Disease. 5 (Suppl. 5): S. 479–490. doi:10.3978/j.issn.2072-1439.2013.08.03. PMC 3804875. PMID 24163741.
- ^ Tobias, J; Hochhauser D (2010). “Chapter 12”. Cancer and its Management (ấn bản 6). Wiley-Blackwell. tr. 200. ISBN 978-1405-170154.
- ^ a b c d Herbst, RS; Heymach JV; Lippman SM (tháng 9 năm 2008). “Lung cancer”. New England Journal of Medicine. 359 (13): 1367–1380. doi:10.1056/NEJMra0802714. PMID 18815398. Lưu trữ bản gốc ngày 28 tháng 9 năm 2008.
- ^ Aviel-Ronen, S; Blackhall FH; Shepherd FA; Tsao MS (tháng 7 năm 2006). “K-ras mutations in non-small-cell lung carcinoma: a review”. Clinical Lung Cancer. Cancer Information Group. 8 (1): 30–38. doi:10.3816/CLC.2006.n.030. PMID 16870043.
- ^ Kumar, V; Abbas AK; Aster JC (2013). “Chapter 5”. Robbins Basic Pathology (ấn bản 9). Elsevier Saunders. tr. 212. ISBN 978-1-4377-1781-5.
- ^ Jakopovic, M; Thomas A; Balasubramaniam S (tháng 10 năm 2013). “Targeting the epigenome in lung cancer: expanding approaches to epigenetic therapy” (PDF). Frontiers in Oncology. 3 (261). doi:10.3389/fonc.2013.00261. PMC 3793201. PMID 24130964.
- ^ a b Mulvihill, MS; Kratz JR; Pham P (tháng 2 năm 2013). “The role of stem cells in airway repair: implications for the origins of lung cancer”. Chinese Journal of Cancer. 32 (2): 71–74. doi:10.5732/cjc.012.10097. PMC 3845611. PMID 23114089.
- ^ Powell, CA; Halmos B; Nana-Sinkam SP (tháng 7 năm 2013). “Update in lung cancer and mesothelioma 2012” (PDF). American Journal of Respiratory and Critical Care Medicine. 188 (2): 157–166. doi:10.1164/rccm.201304-0716UP. PMC 3778761. PMID 23855692.
- ^ Miller, WT (2008). Fishman's Pulmonary Diseases and Disorders (ấn bản 4). McGraw-Hill. tr. 486. ISBN 0-07-145739-9.
- ^ Kaiser, LR (2008). Fishman's Pulmonary Diseases and Disorders (ấn bản 4). McGraw-Hill. tr. 1815–1816. ISBN 0-07-145739-9.
- ^ American College of Chest Physicians; American Thoracic Society (tháng 9 năm 2013), “Five Things Physicians and Patients Should Question”, Choosing Wisely: an initiative of the ABIM Foundation, American College of Chest Physicians and American Thoracic Society, Bản gốc lưu trữ ngày 3 tháng 11 năm 2013, truy cập ngày 6 tháng 1 năm 2013
- ^ American College of Chest Physicians; American Thoracic Society (tháng 9 năm 2013), “Five Things Physicians and Patients Should Question”, Choosing Wisely: an initiative of the ABIM Foundation, American College of Chest Physicians and American Thoracic Society, lưu trữ bản gốc 3 Tháng mười một năm 2013, truy cập ngày 6 tháng 1 năm 2013 Đã định rõ hơn một tham số trong
|archiveurl=và|archive-url=(trợ giúp) - ^ Kumar, V; Abbas AK; Aster JC (2013). “12”. Robbins Basic Pathology (ấn bản 9). Elsevier Saunders. tr. 505. ISBN 978-1-4377-1781-5.
- ^ Subramanian, J; Govindan R (tháng 2 năm 2007). “Lung cancer in never smokers: a review”. Journal of Clinical Oncology. American Society of Clinical Oncology. 25 (5): 561–570. doi:10.1200/JCO.2006.06.8015. PMID 17290066.
- ^ Raz, DJ; He B; Rosell R; Jablons DM (tháng 3 năm 2006). “Bronchioloalveolar carcinoma: a review”. Clinical Lung Cancer. 7 (5): 313–322. doi:10.3816/CLC.2006.n.012. PMID 16640802.
- ^ Rosti G, Bevilacqua G, Bidoli P, và đồng nghiệp (tháng 3 năm 2006). “Small cell lung cancer”. Annals of Oncology. 17 (Suppl. 2): 5–10. doi:10.1093/annonc/mdj910. PMID 16608983.
- ^ Kumar, V; Abbas AK; Aster JC (2013). “12”. Robbins Basic Pathology (ấn bản 9). Elsevier Saunders. tr. 505. ISBN 978-1-4377-1781-5.
- ^ Seo JB, Im JG, Goo JM, và đồng nghiệp (ngày 1 tháng 3 năm 2001). “Atypical pulmonary metastases: spectrum of radiologic findings”. Radiographics. 21 (2): 403–417. doi:10.1148/radiographics.21.2.g01mr17403. PMID 11259704. Lưu trữ bản gốc ngày 11 tháng 10 năm 2007.
- ^ Tan D, Zander DS (2008). “Immunohistochemistry for Assessment of Pulmonary and Pleural Neoplasms: A Review and Update”. Int J Clin Exp Pathol. 1 (1): 19–31. PMC 2480532. PMID 18784820.
Liên kết ngoài[sửa | sửa mã nguồn]
| Wikimedia Commons có thêm hình ảnh và phương tiện truyền tải về Ung thư phổi. |
