Amino acid
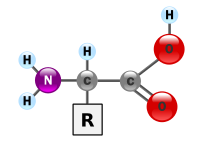
Amino acid, còn được viết là acid amin (bắt nguồn từ danh xưng Pháp ngữ acide aminé),[1] là những hợp chất hữu cơ sinh học quan trọng chứa nhóm chức amin (-NH2) và acid carboxylic (-COOH), cùng với một mạch bên (side-chain; nhóm R) nhất định ở mỗi amino acid.[2][3][4] Các nguyên tố chính của amino acid là carbon, hydro, oxy, và nitơ, và một số nguyên tố khác có mặt trong mạch bên của từng amino acid. Tồn tại khoảng 500 amino acid đã được biết đến và phân loại theo nhiều cách khác nhau.[5] Chúng có thể được phân loại tuân theo vị trí của nhóm chức trong cấu trúc chính như alpha- (α-), beta- (β-), gamma- (γ-) hoặc delta- (δ-) amino acid; các phân loại khác liên quan đến mức độ phân cực, độ pH, và kiểu mạch bên (hợp chất không vòng, hợp chất acyclic, tính thơm, chứa hydroxyl hoặc lưu huỳnh, vv.). Trong phân tử protein, amino acid chiếm số lượng nhiều thứ hai (nước là nhiều nhất) ở cơ, tế bào và mô.[6] Bên ngoài protein, amino amino acido có vai trò quan trọng trong các quá trình như vận chuyển chất dẫn truyền thần kinh và sinh tổng hợp.
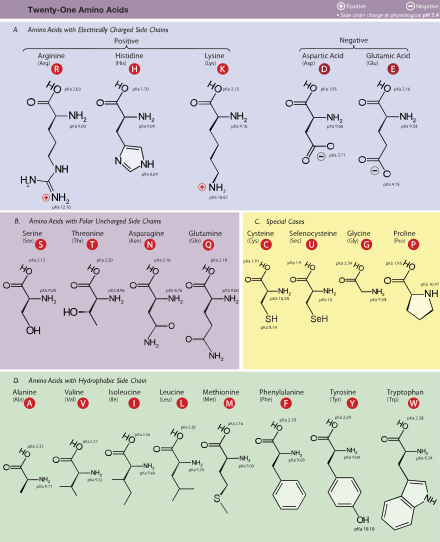
Trong ngành hóa sinh, amino acid đều có nhóm amin và nhóm acid carboxylic liên kết với nguyên tử carbon alpha đầu tiên có tính quan trọng đặc biệt. Chúng được biết đến như là 2-, alpha-, hoặc α-amino acid (công thức tổng quát H2NCHRCOOH trong hầu hết các trường hợp,[7] với R là một nhóm hữu cơ gọi là "mạch bên");[8] thường thuật ngữ "amino acid" là nhắc tới cụ thể hợp chất hóa học này. Chúng bao gồm 22 amino acid cấu thành nên protein,[9][10][11] mà khi kết hợp lại thành những chuỗi peptide ("polypeptide") để tạo thành những viên gạch của vô số protein.[12] Tất cả chúng là những L-đồng phân lập thể (các đồng phân "thuận tay trái" (left-handed)), mặc dù một số nhỏ D-amino acid ("thuận tay phải") xuất hiện ở vỏ tế bào vi khuẩn, như chất điều biến neuron (neuromodulator; D-serine), và ở một số kháng sinh.[13] 20 loại amino acid sinh protein được mã hóa trực tiếp bởi bộ ba mã hóa codon trong mã di truyền và được coi là những amino acid "chuẩn". Ba amino acid khác ("không chuẩn" hoặc "không chính tắc") là selenocysteine (có mặt ở nhiều sinh vật nhân sơ cũng như ở hầu hết sinh vật nhân thực, nhưng không do DNA mã hóa trực tiếp), pyrrolysine (chỉ thấy xuất hiện ở một số vi khuẩn cổ và một vi khuẩn) và N-formylmethionine (mà là amino acid khởi đầu của protein trong vi khuẩn, ty thể, và lục lạp). Pyrrolysine và selenocysteine được mã hóa thông qua một số codon khác nhau; ví dụ, selenocysteine được mã hóa bởi codon kết thúc (stop codon) và phần tử SECIS (SECIS element).[14][15][16] Tổ hợp Codon–tRNA không tìm thấy trong tự nhiên cũng được sử dụng để "mở rộng" mã di truyền và tạo ra các protein chuyên biệt như alloprotein chứa các amino acid không chuẩn.[17][18][19]
Nhiều amino acid chuẩn và các amino acid không chuẩn cũng có vai trò quan trọng khác bên trong cơ thể ngoài việc cấu tạo nên protein. Ví dụ, trong não người, glutamat (acid glutamic chuẩn) và acid gamma-amino-butyric ("GABA", acid gamma-amino không chuẩn) lần lượt là chất dẫn truyền thần kinh kích thích và ức chế (excitatory and inhibitory neurotransmitters);[20] hydroxyproline (một thành phần chính trong collagen của mô liên kết) được tổng hợp từ proline; amino acid chuẩn glycine dùng để tổng hợp porphyrin ở hồng cầu; và amino acid không chuẩn carnitine tham gia vào quá trình vận chuyển lipid.
Có 9 amino acid sinh protein "thiết yếu" ở cơ thể người do chúng không được tổng hợp từ những hợp chất khác trong cơ thể do vậy cơ thể cần các amino acid này thông qua thức ăn đưa vào. Ngoài ra một số amino acid thiết yếu có điều kiện, nghĩa là bình thường chúng không nhất thiết phải có trong thức ăn, nhưng lại cần có trong khẩu phần của những người không tổng hợp được chúng với một lượng đủ. Amino acid thiết yếu cũng khác nhau tùy từng loài cụ thể.[21]
Bởi vì ý nghĩa sinh học của chúng, các amino acid là những chất dinh dưỡng quan trọng và thường sử dụng trong bổ sung dinh dưỡng, phân bón, và công nghệ thực phẩm. Công nghiệp sử dụng bao gồm các sản phẩm thuốc, nhựa phân hủy bằng sinh học (biodegradable plastic), và các chất xúc tác bất đối xứng (chiral catalysts).
Lịch sử[sửa | sửa mã nguồn]
Một vài amino acid đầu tiên đã được khám phá vào đầu thế kỷ 19. Năm 1806, hai nhà hóa học người Pháp Louis-Nicolas Vauquelin và Pierre Jean Robiquet đã cô lập hợp chất trong măng tây (asparagus) mà sau đó người ta đặt tên nó là asparagine, trở thành amino acid được khám phá đầu tiên.[22][23] Cystine được phát hiện vào năm 1810,[24] cho dù monome của nó, cysteine, chưa bị phát hiện cho đến tận năm 1884.[23][25] Glycine và leucine được phát hiện vào năm 1820.[26] Amino acid cuối cùng trong 20 amino acid phổ biến là threonine được William Cumming Rose phát hiện vào năm 1935, ông cũng xác định các amino acid thiết yếu và thiết lập mức nhu cầu đòi hỏi tối thiểu về amino acid hàng ngày cho sự phát triển tối ưu.[27][28]
Thuật ngữ amino acid sử dụng trong tiếng Anh xuất hiện từ năm 1898.[29] Các nhà hóa học tìm thấy protein cho thu được các amino acid từ các enzim tiêu hóa hoặc thủy phân acid. Năm 1902, Emil Fischer và Franz Hofmeister đề xuất protein hình thành từ liên kết giữa nhóm amin của một amino acid với nhóm carboxyl của amino acid bên cạnh, tạo thành mạch thẳng mà Fischer đặt tên là "peptide".[30]
Cấu trúc tổng quát[sửa | sửa mã nguồn]
Cấu trúc trong hình ở đầu trang, R tương ứng với một mạch bên đặc thù cho mỗi amino acid. Nguyên tử carbon nằm kế bên nhóm carboxyl được gọi là carbon-α. Amino acid gồm có nhóm amin liên kết trực tiếp tới carbon alpha được gọi là amino acid alpha.[31] Chúng gồm có những amino acid như proline bao gồm amin bậc 2, nó còn được gọi là "imin acid".[32][33][34]
Đồng phân[sửa | sửa mã nguồn]
Amino acid alpha là loại amino acid phổ biến nhất trong tự nhiên; trong đó, đồng phân-L là loại thông thường nhất. Carbon alpha là nguyên tử carbon có tính chất bất đối xứng (chirality) ngoại trừ glycine vì nó có hai nguyên tử hydro giống nhau xung quanh carbon alpha.[35] Bởi vậy, tất cả amino acid alpha ngoài trừ glycine chỉ có thể tồn tại ở hai thể đồng phân đối quang (enantiomer) L hoặc D, hai thể này là hình phản chiếu từ gương của nhau. Tất cả các amino acid trong protein đều là thể L được tạo ra từ ribosome còn thể D thường được tìm thấy trong các protein được cấu thành bởi enzym hậu dịch mã và sau khi chúng được chuyển tới mạng lưới nội chất, ví dụ thể D được tìm thấy trong sinh vật lạ ốc nón sống ở biển.[36] Thành tế bào của vi khuẩn cũng chứa nhiều thể D,[37] và serine D có thể đóng vai trò là chất dẫn truyền thần kinh trong não.[38] amino acid D được dùng trong kỹ thuật triệt quang (racemic crystallography) để tạo ra các tinh thể đối xứng; kỹ thuật này có thể giúp xác định cấu trúc protein chính xác và dễ dàng hơn đối với một số protein.[39] amino acid được xếp vào thể L hay D không dựa vào hoạt động quang phổ của amino acid đó mà dựa vào hoạt động quang phổ thuộc đồng phân của glyceraldehyde; chất glyceraldehyde là chất cần thiết để cấu tạo thành amino acid. Glyceraldehyde D là hữu tuyền (dextrorotatory); glyceraldehyde L là tả tuyền (levorotatory). Ký tự S và R thì được dùng để mô tả cấu trúc tuyệt đối của amino acid. Hầu như tất cả các amino acid có carbon α là S với cysteine là R và glycine có tính chất đối xứng.[40] Cysteine có mạch bên nằm ở vị trí 3D giống như các amino acid khác nhưng có ký tự R bởi vì mạch bên của nó có sulfur, nó là nguyên tử có số nguyên tử cao hơn so với nhóm chức carboxyl. Các amino acid khác là S bởi vì mạch bên của chúng có số nguyên tử thấp hơn nhóm chức carboxyl.[41]
Mạch bên[sửa | sửa mã nguồn]
Amino acid α là các amino acid có nguyên tử nitơ liên kết với nguyên tử carbon kế bên nhóm chức carboxyl cấu thành nên cấu trúc con N–C–CO2. Amino acid có cấu trúc con N–C–C–CO2 thì được gọi là amino acid β. Amino acid γ có cấu trúc con là N–C–C–C–CO2 và vân vân.[42]
Amino acid thường được xếp thành bốn nhóm khác nhau dựa trên tính chất hóa học của mạch bên. Mạch bên có thể khiến amino acid thành acid yếu, base yếu, chất ưa nước nếu như mạch bên là phân cực, hoặc chất kị nước nếu như mạch bên không phải là phân cực.[35] "Amino acid chuỗi nhánh" là các amino acid có mạch bên không vòng và hình thẳng gồm có leucine, isoleucine, và valine. Proline là amino acid proteinogenic duy nhất có mạch bên liên kết với nhóm amin α, và nó cũng là amino acid proteinogenic duy nhất có amin bậc 2 tại vị trí carbon α.[35] Theo phân loại hóa học, proline đáng ra phải là acid imin bởi vì nó không có nhóm amin bậc 1.[43] Tuy nhiên, hiện tại nó vẫn được gọi là amino acid trong danh pháp hóa sinh[44] và còn được gọi là "amino acid alpha alkyl hóa N".[45]
Tham khảo[sửa | sửa mã nguồn]
- ^ Đặng Thái Minh, "Dictionnaire vietnamien - français. Les mots vietnamiens d’origine française", Synergies Pays riverains du Mékong, n° spécial, năm 2011. ISSN: 2107-6758. Trang 49.
- ^ “Amino”. Dictionary.com. 2015. Truy cập ngày 3 tháng 7 năm 2015.
- ^ “amino acid”. Cambridge Dictionaries Online. Cambridge University Press. 2015. Truy cập ngày 3 tháng 7 năm 2015.
- ^ “amino”. FreeDictionary.com. Farlex. 2015. Truy cập ngày 3 tháng 7 năm 2015.
- ^ Wagner I, Musso H (tháng 11 năm 1983). “New Naturally Occurring Amino Acids”. Angewandte Chemie International Edition in English. 22 (11): 816–28. doi:10.1002/anie.198308161.
- ^ Latham, Michael C. (1997). “Chapter 8. Body composition, the functions of food, metabolism and energy”. Human nutrition in the developing world. Food and Nutrition Series - No. 29. Rome: Food and Agriculture Organization of the United Nations.
- ^ Proline là một trường hợp ngoại lệ đối với công thức này. Nó thiếu nhóm NH2 do cấu trúc vòng của mạch bên và được biết đến như là axit imin (imino acid); nó được xếp vào nhóm amino acid có cấu trúc đặc biệt.
- ^ Clark, Jim (tháng 8 năm 2007). “an introduction to amino acids”. chemguide. Truy cập ngày 4 tháng 7 năm 2015.
- ^ Jakubke, Hans-Dieter; Sewald, Norbert (2008). “Amino acids”. Peptides from A to Z: A Concise Encyclopedia. Germany: Wiley-VCH. tr. 20. ISBN 9783527621170 – qua Google Books.
- ^ Pollegioni, Loredano; Servi, Stefano biên tập (2012). Unnatural Amino Acids: Methods and Protocols. Methods in Molecular Biology - Volume 794. Humana Press. tr. v. ISBN 978-1-61779-331-8. OCLC 756512314.
- ^ Hertweck C (2011). “Biosynthesis and Charging of Pyrrolysine, the 22nd Genetically Encoded Amino Acid”. Angewandte Chemie International Edition. 50 (41): 9540–1. doi:10.1002/anie.201103769. PMID 21796749.
- ^ “Chapter 1: Proteins are the Body's Worker Molecules”. The Structures of Life. National Institute of General Medical Sciences. ngày 27 tháng 10 năm 2011. Bản gốc lưu trữ ngày 7 tháng 6 năm 2014. Truy cập ngày 20 tháng 5 năm 2008.
- ^ Michal, Gerhard; Schomburg, Dietmar biên tập (2012). Biochemical Pathways: An Atlas of Biochemistry and Molecular Biology (ấn bản 2). Wiley. tr. 5.
- ^ Modeling Electrostatic Contributions to Protein Folding and Binding – Tjong, p.1 footnote
- ^ Frontiers in Drug Design and Discovery ed. Atta-Ur-Rahman & others, p.299
- ^ Elzanowski A, Ostell J (ngày 7 tháng 4 năm 2008). “The Genetic Codes”. National Center for Biotechnology Information (NCBI). Truy cập ngày 10 tháng 3 năm 2010.
- ^ Xie J, Schultz PG (tháng 12 năm 2005). “Adding amino acids to the genetic repertoire”. Current Opinion in Chemical Biology. 9 (6): 548–54. doi:10.1016/j.cbpa.2005.10.011. PMID 16260173.
- ^ Wang Q, Parrish AR, Wang L (tháng 3 năm 2009). “Expanding the genetic code for biological studies”. Chem. Biol. 16 (3): 323–36. doi:10.1016/j.chembiol.2009.03.001. PMC 2696486. PMID 19318213.
- ^ Simon M (2005). Emergent computation: emphasizing bioinformatics. New York: AIP Press/Springer Science+Business Media. tr. 105–106. ISBN 0-387-22046-1.
- ^ Petroff OA (tháng 12 năm 2002). “GABA and glutamate in the human brain”. Neuroscientist. 8 (6): 562–573. doi:10.1177/1073858402238515. PMID 12467378. Bản gốc lưu trữ ngày 24 tháng 9 năm 2019. Truy cập ngày 20 tháng 4 năm 2015.
- ^ Ví dụ, ở động vật nhai lại như bò lấy một số amino acid thông qua vi sinh vật trong ngăn ruột tiêu hóa của chúng.
- ^ Vauquelin LN, Robiquet PJ (1806). “The discovery of a new plant principle in Asparagus sativus”. Annales de Chimie. 57: 88–93.
- ^ a b Anfinsen CB, Edsall JT, Richards FM (1972). Advances in Protein Chemistry. New York: Academic Press. tr. 99, 103. ISBN 978-0-12-034226-6.
- ^ Wollaston WH (1810). “On cystic oxide, a new species of urinary calculus”. Philosophical Transactions of the Royal Society. 100: 223–30. doi:10.1098/rstl.1810.0015.
- ^ Baumann E (1884). “Über cystin und cystein”. Z Physiol Chem. 8 (4): 299–305. Lưu trữ bản gốc ngày 14 tháng 3 năm 2011. Truy cập ngày 28 tháng 3 năm 2011.
- ^ Braconnot HM (1820). “Sur la conversion des matières animales en nouvelles substances par le moyen de l'acide sulfurique”. Annales de Chimie et de Physique. 2nd Series. 13: 113–25.
- ^ Robert D. Simoni; Robert L. Hill; Martha Vaughan (ngày 13 tháng 9 năm 2002). “The Discovery of the Amino Acid Threonine: the Work of William C. Rose”. Journal of Biological Chemistry. 277 (37): 56–58. PMID 12218068.
- ^ McCoy, R. H.; Meyer, C. E. & Rose, W. C. (1935). “Feeding Experiments with Mixtures of Highly Purified Amino Acids. VIII. Isolation and Identification of a New Essential Amino Acid”. Journal of Biological Chemistry. 112: 283–302.
- ^ “etymonline.com entry for amino”. www.etymonline.com. Bản gốc lưu trữ ngày 20 tháng 10 năm 2012. Truy cập ngày 19 tháng 7 năm 2010.
- ^ Joseph S. Fruton (1990). “Chapter 5- Emil Fischer and Franz Hofmeister”. Contrasts in Scientific Style: Research Groups in the Chemical and Biochemical Sciences,. 191. American Philosophical Society. tr. 163–165. ISBN 0-87169-191-4.
- ^ “Alpha amino acid”. The Merriam-Webster.com Medical Dictionary. Merriam-Webster Inc.
- ^ MeSH Proline
- ^ Matts, R. L. (2005). “Amino acids”. Biochemistry 5753: Principles of Biochemistry. Bản gốc lưu trữ ngày 18 tháng 1 năm 2008. Truy cập ngày 3 tháng 1 năm 2015.
- ^ International Union of Pure and Applied Chemistry. "Imino acids". Toàn văn bản Giản Lược Thuật Ngữ Hoá Học.
- ^ a b c Creighton, Thomas H. (1993). “Chapter 1”. Proteins: structures and molecular properties. San Francisco: W. H. Freeman. ISBN 978-0-7167-7030-5.
- ^ Pisarewicz K, Mora D, Pflueger FC, Fields GB, Marí F (tháng 5 năm 2005). “Polypeptide chains containing D-gamma-hydroxyvaline”. Journal of the American Chemical Society. 127 (17): 6207–6215. doi:10.1021/ja050088m. PMID 15853325.
- ^ van Heijenoort J (tháng 3 năm 2001). “Formation of the glycan chains in the synthesis of bacterial peptidoglycan”. Glycobiology. 11 (3): 25R–36R. doi:10.1093/glycob/11.3.25R. PMID 11320055.
- ^ Wolosker H, Dumin E, Balan L, Foltyn VN (tháng 7 năm 2008). “D-Amino acids in the brain: D-serine in neurotransmission and neurodegeneration”. The FEBS Journal. 275 (14): 3514–3526. doi:10.1111/j.1742-4658.2008.06515.x. PMID 18564180.
- ^ Matthews BW (tháng 6 năm 2009). “Racemic crystallography—easy crystals and easy structures: What's not to like?”. Protein Science. 18 (6): 1135–1138. doi:10.1002/pro.125. PMC 2774423. PMID 19472321.
- ^ Hatem, Salama Mohamed Ali (2006). “Gas chromatographic determination of Amino Acid Enantiomers in tobacco and bottled wines”. University of Giessen. Bản gốc lưu trữ ngày 22 tháng 1 năm 2009. Truy cập ngày 17 tháng 11 năm 2008.
- ^ Mitchell, Bailey (2019). Cell and Molecular Biology. Scientific e-Resources. tr. 294-295. ISBN 9781839474460.
|ngày truy cập=cần|url=(trợ giúp) - ^ “Nomenclature and Symbolism for Amino Acids and Peptides”. IUPAC-IUB Joint Commission on Biochemical Nomenclature. 1983. Bản gốc lưu trữ ngày 9 tháng 10 năm 2008. Truy cập ngày 17 tháng 11 năm 2008.
- ^ Jodidi, S. L. (ngày 1 tháng 3 năm 1926). “The Formol Titration of Certain Amino Acids”. Journal of the American Chemical Society. 48 (3): 751–753. doi:10.1021/ja01414a033.
- ^ Liebecq, Claude biên tập (1992). Biochemical Nomenclature and Related Documents (ấn bản 2). Portland Press. tr. 39–69. ISBN 978-1-85578-005-7.
- ^ Smith, Anthony D. (1997). Oxford Dictionary of Biochemistry and Molecular Biology. Oxford: Oxford University Press. tr. 535. ISBN 978-0-19-854768-6. OCLC 37616711.
Liên kết ngoài[sửa | sửa mã nguồn]
| Wikimedia Commons có thêm hình ảnh và phương tiện truyền tải về Amino acid. |
- Molecular Expressions: The Amino Acid Collection - Chứa các thông tin chi tiết và hình vi ảnh của mỗi amino acid.
- 22nd amino acid Lưu trữ 2005-12-15 tại Wayback Machine - Bản phát hành từ Ohio State tuyên bố việc tìm ra amino acid thứ 22.
- Amino acid properties Lưu trữ 2007-09-27 tại Wayback Machine - Tính chất của amino acid (công cụ nhằm mục đích tìm hiểu ý nghĩa của việc đột biến)
- Tổng hợp acid amin và dẫn xuất
- Right-handed acid amin were left behind Lưu trữ 2007-09-30 tại Wayback Machine
