Caesi iodide
| Caesi iodide | |
|---|---|
 Mẫu chất rắn caesi iodide | |
| Danh pháp IUPAC | Caesium iodide |
| Tên khác | Cesium iodide |
| Nhận dạng | |
| Số CAS | |
| Ảnh Jmol-3D | ảnh |
| SMILES | đầy đủ
|
| InChI | đầy đủ
|
| Thuộc tính | |
| Công thức phân tử | CsI |
| Khối lượng mol | 259,809 g/mol[1] |
| Bề ngoài | chất rắn tinh thể màu trắng |
| Khối lượng riêng | 4,51 g/cm³[1] |
| Điểm nóng chảy | 632 °C (905 K; 1.170 °F)[1] |
| Điểm sôi | 1.280 °C (1.550 K; 2.340 °F)[1] |
| Độ hòa tan trong nước | 848 g/L (25 ℃)[1], xem thêm bảng độ tan |
| MagSus | -82,6·10-6 cm³/mol[2] |
| Chiết suất (nD) | 1,9790 (0,3 µm) 1,7873 (0,59 µm) 1,7694 (0,75 µm) 1,7576 (1 µm) 1,7428 (5 µm) 1,7280 (20 µm)[3] |
| Cấu trúc | |
| Cấu trúc tinh thể | CsCl, cP2 |
| Nhóm không gian | Pm3m, No. 221[4] |
| Hằng số mạng | a = 0,4503 nm |
| Tọa độ | Lập phương (Cs+) Lập phương (I−) |
| Nhiệt hóa học | |
| Enthalpy hình thành ΔfH | -346,6 kJ/mol[5] |
| Entropy mol tiêu chuẩn S | 123,1 J/mol·K[5] |
| Nhiệt dung | 52,8 J/mol·K[5] |
| Các nguy hiểm | |
| Điểm bắt lửa | Không bắt lửa |
| LD50 | 2386 mg/kg (đường miệng, chuột)[6] |
| Các hợp chất liên quan | |
| Anion khác | Caesi fluoride Caesi chloride Caesi bromide |
| Cation khác | Lithi iodide Natri iodide Kali iodide Rubiđi iodide Franci iodide |
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |
Caesi iodide (công thức hóa học CsI) là một hợp chất của caesi và iod. Nó thường được sử dụng làm chất phosphor đầu vào của một ống tăng cường hình ảnh tia X được tìm thấy trong thiết bị fluoroscopy. Các photocathode ion caesi iodide có hiệu suất cao ở bước sóng siêu trên cực tím.[7]
Tổng hợp và cấu trúc[sửa | sửa mã nguồn]
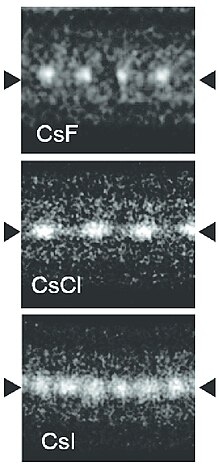
Các tinh thể caesi iodide có cấu trúc tinh thể giống CsCl, nhưng cấu trúc của các màng mỏng CsI kích cỡ nanomet phụ thuộc vào chất nền – nó là CsCl cho mica và NaCl cho các chất nền LiF, NaBr và NaCl.[9]
Các chuỗi nguyên tử caesi iodide có thể được trồng bên trong các ống nanô cácbon hai lớp tường. Trong các chuỗi như vậy, các nguyên tử iod xuất hiện sáng hơn các nguyên tử caesi trong các bức xạ vi điện tử mặc dù có một khối lượng nhỏ hơn. Sự khác biệt này được giải thích bởi sự khác biệt giữa các nguyên tử Cs (tích cực), các bức tường nano bên trong (âm) và các nguyên tử I (âm). Kết quả là các nguyên tử Cs bị hút vào các bức tường và rung động mạnh hơn các nguyên tử I, mà được đẩy về phía trục ống nano.[8]
Tham khảo[sửa | sửa mã nguồn]
- ^ a b c d e Haynes, tr. 4.57
- ^ Haynes, tr. 4.132
- ^ Haynes, tr. 10.240
- ^ Huang, Tzuen-Luh; Ruoff, Arthur L. (1984). “Equation of state and high-pressure phase transition of CsI”. Physical Review B. 29 (2): 1112. doi:10.1103/PhysRevB.29.1112.
- ^ a b c Haynes, tr. 5.10
- ^ Cesium iodide. U.S. National Library of Medicine
- ^ Kowalski, M. P.; Fritz, G. G.; Cruddace, R. G.; Unzicker, A. E.; Swanson, N. (1986). “Quantum efficiency of cesium iodide photocathodes at soft x-ray and extreme ultraviolet wavelengths”. Applied Optics. 25 (14): 2440. doi:10.1364/AO.25.002440. PMID 18231513.
- ^ a b Senga, Ryosuke; Komsa, Hannu-Pekka; Liu, Zheng; Hirose-Takai, Kaori; Krasheninnikov, Arkady V.; Suenaga, Kazu (2014). “Atomic structure and dynamic behaviour of truly one-dimensional ionic chains inside carbon nanotubes”. Nature Materials. 13 (11): 1050. doi:10.1038/nmat4069. PMID 25218060.
- ^ Schulz, L. G. (1951). “Polymorphism of cesium and thallium halides”. Acta Crystallographica. 4 (6): 487. doi:10.1107/S0365110X51001641.
Sách tham khảo[sửa | sửa mã nguồn]
- Haynes, William M. biên tập (2011). CRC Handbook of Chemistry and Physics (ấn bản 92). Boca Raton, FL: CRC Press. ISBN 1439855110.
| HI | He | ||||||||||||||||
| LiI | BeI2 | BI3 | CI4 | NI3 | I2O4, I2O5, I4O9 |
IF, IF3, IF5, IF7 |
Ne | ||||||||||
| NaI | MgI2 | AlI3 | SiI4 | PI3, P2I4 |
S | ICl, ICl3 |
Ar | ||||||||||
| KI | CaI2 | ScI3 | TiI2, TiI3, TiI4 |
VI2, VI3, VOI2 |
CrI2, CrI3, CrI4 |
MnI2 | FeI2, FeI3 |
CoI2 | NiI2 | CuI, CuI2 |
ZnI2 | GaI, GaI2, GaI3 |
GeI2, GeI4 |
AsI3 | Se | IBr | Kr |
| RbI | SrI2 | YI3 | ZrI2, ZrI4 |
NbI2, NbI3, NbI4, NbI5 |
MoI2, MoI3, MoI4 |
TcI3, TcI4 |
RuI2, RuI3 |
RhI3 | PdI2 | AgI | CdI2 | InI3 | SnI2, SnI4 |
SbI3 | TeI4 | I | Xe |
| CsI | BaI2 | HfI4 | TaI3, TaI4, TaI5 |
WI2, WI3, WI4 |
ReI, ReI2, ReI3, ReI4 |
OsI, OsI2, OsI3 |
IrI, IrI2, IrI3 |
PtI2, PtI3, PtI4 |
AuI,AuI3 | Hg2I2, HgI2 |
TlI, TlI3 |
PbI2, PbI4 |
BiI2, BiI3 |
PoI2. PoI4 |
AtI | Rn | |
| Fr | Ra | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| ↓ | |||||||||||||||||
| LaI2, LaI3 |
CeI2, CeI3 |
PrI2, PrI3 |
NdI2, NdI3 |
PmI3 | SmI2, SmI3 |
EuI2, EuI3 |
GdI2, GdI3 |
TbI3 | DyI2, DyI3 |
HoI3 | ErI3 | TmI2, TmI3 |
YbI2, YbI3 |
LuI3 | |||
| Ac | ThI2, ThI3, ThI4 |
PaI3, PaI4, PaI5 |
UI3, UI4, UI5 |
NpI3 | PuI3 | AmI2, AmI3 |
CmI2, CmI3 |
BkI3 | CfI2, CfI3 |
EsI3 | Fm | Md | No | Lr | |||
