Khác biệt giữa bản sửa đổi của “Kali iodide”
n chính tả, replaced: vói → với using AWB |
Không có tóm lược sửa đổi |
||
| Dòng 4: | Dòng 4: | ||
| ImageFile = Potassium iodide.jpg |
| ImageFile = Potassium iodide.jpg |
||
| ImageFile1 = Potassium-iodide-3D-ionic.png |
| ImageFile1 = Potassium-iodide-3D-ionic.png |
||
| IUPACName = Kali iođua |
| IUPACName = Kali iođua |
||
| OtherNames = |
| OtherNames = |
||
| Section1 = {{Chembox Identifiers |
| Section1 = {{Chembox Identifiers |
||
| Dòng 58: | Dòng 58: | ||
}} |
}} |
||
'''Kali iođua''' hay '''kali iotua''' là hợp chất vô cơ có [[công thức hóa học]] '''KI'''. Đây là muối iođua phổ biến nhất trên thị trường, với sản lượng khoảng 37.000 tấn năm 1985. KI ít hút ẩm hơn so với NaI. Muối KI để lâu hoặc |
'''Kali iođua''' hay '''kali iotua''' là hợp chất vô cơ có [[công thức hóa học]] '''KI'''. Đây là muối iođua phổ biến nhất trên thị trường, với sản lượng khoảng 37.000 tấn năm 1985. KI ít hút ẩm hơn so với NaI. Muối KI để lâu hoặc không nguyên chất thường có màu vàng. |
||
| ⚫ | |||
| ⚫ | |||
| ⚫ | |||
KI được điều chế bằng phản ứng giữa KOH và [[iốt]]: 6KOH + 3I<sub>2</sub> → 5KI + KIO<sub>3</sub> + 3H<sub>2</sub>O |
|||
== Ứng dụng == |
|||
| ⚫ | |||
* KI cũng được sử dụng trong dạng dung dịch bão hòa với khoảng 1000 mg KI/ml. |
|||
* KI hoặc KIO<sub>3</sub> thường được trộn vào muối ăn làm [[muối iốt]].<ref>Sách giáo khoa Hóa học 10 nâng cao, trang 146, Nhà xuất bản Giáo dục Việt Nam.</ref> |
|||
| ⚫ | |||
| ⚫ | |||
== Tính chất == |
== Tính chất == |
||
=== Hóa vô cơ === |
=== Hóa vô cơ === |
||
Ion iodua bị oxi hóa thành iod tự do bởi các chất oxi hóa mạnh như [[acid sulfuric|axit sunfuric]] đặc, [[kali pemanganat]], khí [[clo]]: |
Ion iodua bị oxi hóa thành iod tự do bởi các chất oxi hóa mạnh như [[acid sulfuric|axit sunfuric]] đặc, [[kali pemanganat]], khí [[clo]]: |
||
: |
:4KI + 2CO<sub>2</sub> + O<sub>2</sub> → 2K<sub>2</sub>CO<sub>3</sub> + 2I<sub>2</sub> |
||
Phản ứng này dùng để phân tách iod từ khoáng chất thiên nhiên. |
Phản ứng này dùng để phân tách iod từ khoáng chất thiên nhiên. |
||
| Dòng 75: | Dòng 84: | ||
=== Hóa hữu cơ === |
=== Hóa hữu cơ === |
||
Trong lĩnh vực này, KI được sử dụng như 1 nguồn cung cấp |
Trong lĩnh vực này, KI được sử dụng như 1 nguồn cung cấp iốt cho các phản ứng tổng hợp hữu cơ, ví dụ như phản ứng điều chế các muối arenediazonium: |
||
[[Tập tin:KI Sandmeyer.png|400px]] |
[[Tập tin:KI Sandmeyer.png|400px]] |
||
==Tham khảo== |
==Tham khảo== |
||
{{tham khảo}} |
{{tham khảo}} |
||
{{Sơ khai hóa học}} |
<references />{{Sơ khai hóa học}} |
||
{{Hợp chất Kali}} |
|||
[[Thể loại:Hợp chất kali]] |
[[Thể loại:Hợp chất kali]] |
||
Phiên bản lúc 13:50, ngày 7 tháng 2 năm 2017
| Kali iođua | |
|---|---|
 | |
 | |
| Danh pháp IUPAC | Kali iođua |
| Nhận dạng | |
| Số CAS | |
| PubChem | |
| KEGG | |
| ChEMBL | |
| Số RTECS | TT2975000 |
| Ảnh Jmol-3D | ảnh |
| SMILES | đầy đủ
|
| InChI | đầy đủ
|
| UNII | |
| Thuộc tính | |
| Công thức phân tử | KI |
| Khối lượng mol | 166.0028 g/mol |
| Bề ngoài | chất rắn màu trắng |
| Khối lượng riêng | 3.123 g/cm3 |
| Điểm nóng chảy | 681 °C (954 K; 1.258 °F) |
| Điểm sôi | 1.330 °C (1.600 K; 2.430 °F) |
| Độ hòa tan trong nước | 128 g/100 ml (0 °C) 140 g/100 mL (20 °C) 176 g/100 mL (60 °C) 206 g/100 mL (100 °C) |
| Độ hòa tan | 2 g/100 mL (ethanol) tan trong acetone (1.31 g/100 mL) tan ít trong ether, ammonia |
| Cấu trúc | |
| Các nguy hiểm | |
| MSDS | External MSDS |
| Chỉ mục EU | Không |
| NFPA 704 |
|
| Các hợp chất liên quan | |
| Anion khác | Kali florua Kali clorua Kali bromua |
| Cation khác | Liti iođua Natri iođua Rubiđi iođua Xêsi iođua |
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |
Kali iođua hay kali iotua là hợp chất vô cơ có công thức hóa học KI. Đây là muối iođua phổ biến nhất trên thị trường, với sản lượng khoảng 37.000 tấn năm 1985. KI ít hút ẩm hơn so với NaI. Muối KI để lâu hoặc không nguyên chất thường có màu vàng.
Cấu trúc và Điều chế
Kali iodua là hợp chất ion, cấu trúc tinh thể ở dạng như muối ăn NaCl.
KI được điều chế bằng phản ứng giữa KOH và iốt: 6KOH + 3I2 → 5KI + KIO3 + 3H2O
Ứng dụng
- KI với liều lượng 130 mg thường được dùng cho mục đích cấp cứu phơi nhiễm phóng xạ.
- KI cũng được sử dụng trong dạng dung dịch bão hòa với khoảng 1000 mg KI/ml.
Tính chất
Hóa vô cơ
Ion iodua bị oxi hóa thành iod tự do bởi các chất oxi hóa mạnh như axit sunfuric đặc, kali pemanganat, khí clo:
- 4KI + 2CO2 + O2 → 2K2CO3 + 2I2
Phản ứng này dùng để phân tách iod từ khoáng chất thiên nhiên.
Cũng giống như các muối iodua khác, KI tạo muối triiođua I3- khi xử lý với I2:
- KI(l) + I2 (r) → KI3 (l)
KI cũng được sử dụng trong việc tráng phim:
- KI(l) + AgNO3 (l) → AgI(r) + KNO3 (l)
Hóa hữu cơ
Trong lĩnh vực này, KI được sử dụng như 1 nguồn cung cấp iốt cho các phản ứng tổng hợp hữu cơ, ví dụ như phản ứng điều chế các muối arenediazonium:
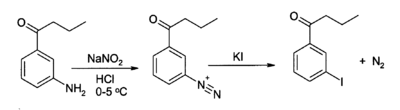
Tham khảo
- ^ Sách giáo khoa Hóa học 10 nâng cao, trang 146, Nhà xuất bản Giáo dục Việt Nam.

