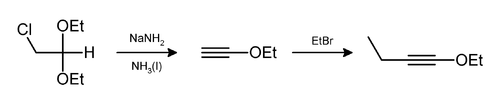Natri amide
| Natri amide | |
|---|---|
 Công thức cấu tạo của natri amide | |
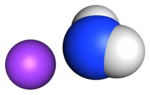 Mô hình phân tử natri amide | |
| Danh pháp IUPAC | Natri amide |
| Tên khác | Sodamide |
| Nhận dạng | |
| Số CAS | |
| PubChem | |
| Số EINECS | |
| Ảnh Jmol-3D | ảnh |
| SMILES | đầy đủ
|
| ChemSpider | |
| Thuộc tính | |
| Công thức phân tử | NaNH2 |
| Khối lượng mol | 39,01088 g/mol chính xác: 39,008493744 g/mol |
| Bề ngoài | tinh thể không màu |
| Khối lượng riêng | 1,39 g/cm³ |
| Điểm nóng chảy | 210 °C (483 K; 410 °F) |
| Điểm sôi | 400 °C (673 K; 752 °F) |
| Độ axit (pKa) | 38 (acid liên hợp)[1] |
| Cấu trúc | |
| Cấu trúc tinh thể | trực thoi |
| Các nguy hiểm | |
| Chỉ mục EU | không có trong danh sách |
| NFPA 704 |
|
| Điểm bắt lửa | 4,44 ℃ |
| Các hợp chất liên quan | |
| Anion khác | Natri bis(trimethylsilyl)amide [(CH3)3Si]2NNa |
| Cation khác | Kali amide |
| Hợp chất liên quan | Amonia |
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |
Natri amide, thường được gọi là sodamide, là một hợp chất vô cơ có công thức hóa học NaNH2. Chất rắn này, phản ứng mãnh liệt với nước, có màu trắng khi tinh khiết, nhưng trong thương mại lại có màu xám do sự có mặt của một lượng nhỏ sắt kim loại trong quá trình sản xuất. Sự không tinh khiết này không ảnh hưởng nhiều đến chất lượng thuốc thử. NaNH2 có ứng dụng quan trọng trong tổng hợp hữu cơ với vai trò một base mạnh.
Điều chế và cấu trúc[sửa | sửa mã nguồn]
Natri amide có thể được điều chế bằng phản ứng giữa natri và khí amonia,[2] nhưng thông thường là phản ứng với dung dịch amonia với xúc tác sắt(III) nitrat. Phản ứng xảy ra nhanh nhất tại điểm sôi của amonia -33 ℃.[3]
- 2Na + 2NH3 → 2NaNH2 + H2↑
NaNH2 là một chất có dạng muối và vì thế nó kết tinh dưới dạng polyme vô hạn.[4] Dạng hình học là tứ diện.[5] Trong amonia, NaNH2 tạo thành dung dịch có tính dẫn, gồm cation Na(NH3)6+ và anion NH2-.
Sử dụng[sửa | sửa mã nguồn]
Natri amide được dùng trong các công nghiệp sản xuất thuốc nhuộm, hydrazin và natri cyanide.[6] Nó là chất tham gia cho việc làm khô amonia (dạng lỏng và khí) và được dùng rộng rãi như một base mạnh trong hoá hữu cơ, chủ yếu trong dung dịch amonia. Một trong những thuận lợi lớn trong việc sử dụng sodamide là natri amide là một base tốt và ít khi phản ứng như một nucleophin. Tuy nhiên nó tan rất hạn chế nên bị thay thế bằng các chất khác có liên quan như natri hydride, natri bis(trimethylsilyl)amide (NaHMDS), và lithi diisopropylamide (LDA - [(CH3)2CH]2NLi).
Điều chế alkyn[sửa | sửa mã nguồn]
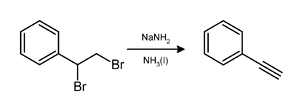
Natri amide làm tách hai phân tử HBr ra khỏi dibromalkan để tạo một liên kết ba C-C, như phản ứng điều chế phenylacetylen dưới đây.[7] Thông thường hai phân tử natri amide sẽ nhường chỗ cho alkyn. Tuy nhiên, ba phân tử sẽ cần thiết cho việc điều chế một alkyn cuối, như alkyn này chẳng hạn, nguyên tử hydro có tính acid sẽ lập tức đưa thêm một proton vào base.
HCl và/hoặc ethanol có thể được loại bỏ ra theo cách này,[8] như trong phản ứng điều chế 1-etoxy-1-butyn.[9]
Các phản ứng tạo vòng[sửa | sửa mã nguồn]
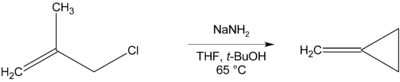
Nơi nào có nguyên tử β-hydro bị loại bỏ, các hợp chất có mạch vòng có thể được hình thành, như trong phản ứng điều chế methylencyclopropan dưới đây.[10]
Cyclopropen,[11] aziridine[12] và cyclobutan[13] có thể được tạo thành theo cách tương tự.
Khử proton trong các acid chứa carbon và nitơ[sửa | sửa mã nguồn]
Các acid chứa carbon mà có thể bị khử proton bởi natri amide trong dung dịch amonia bao gồm các alkyn cuối (có liên kết ba ở ngoài cùng),[14] các methyl ceton,[15] cyclohexanon,[16] acid phenylacetic và các dẫn xuất của nó[17]: diphenylmethan.[18] acetylaceton mất hai proton để tạo ra dianion.[19]
Natri amide còn khử proton của indole[20] và piperidine.[21]
Các phản ứng khác[sửa | sửa mã nguồn]
- Phản ứng khử proton ở vị trí ortho[22]
- Tổng hợp oxiran[23]
- Tổng hợp indole[24]
- Phản ứng Chichibabin
An toàn[sửa | sửa mã nguồn]
Natri amide phản ứng mãnh liệt với nước thoát khí amonia và tạo ra natri peroxide và cháy trong không khí tạo ra natri oxit và oxit nitơ.
Trong điều kiện giới hạn không khí và độ ẩm, như trong bình hở, một hỗn hợp chất oxi hoá dễ cháy được tạo thành. Điều này đi kèm với một chất rắn màu vàng hoặc nâu. Vì vậy, natri amide nên được bảo quản trong một bình kín đậy chặt, và trong khí nitơ nếu cần. Các mẫu natri amide ngả màu nên được tiêu huỷ ngay lập tức: một phương pháp tiêu huỷ là cho 2-propanol vào để giữ natri amide trong dung môi hydrocarbon.
Natri amide có thể làm bỏng da, mắt và màng nhầy. Việc chăm sóc nên được tiến hành để tránh sự phân tán của hoá chất.
Tham khảo[sửa | sửa mã nguồn]
- ^ Buncel; Menon J. Organomet. Chem. 1977, 141, 1.
- ^ Bergstrom, F. W. (1955). "Natri amide". Org. Synth. Coll. Vol. 3: 778.
- ^ Greenlee, K. W.; Henne, A. L. (1946). "Natri amide". Tổng hợp hữu cơ volume 2, p. 128–35.doi:10.1002/9780470132333.ch38.
- ^ Zalkyn, A.; Templeton, D. H. "Cấu trúc tinh thể của natri amide" Journal of Physical Chemistry 1956, Volume 60, pp 821 - 823. DOI: 10.1021/j150540a042
- ^ Wells, A.F. (1984) Structural Inorganic Chemistry, Oxford: Clarendon Press. ISBN 0-19-855370-6.
- ^ Bản mẫu:Merck12th
- ^ Campbell, Kenneth N.; Campbell, Barbara K. (1950). "Phenylacetylen". Org. Synth. 30: 72; Coll. Vol. 4: 763.
- ^ Jones, E. R. H.; Eglinton, Geoffrey; Whiting, M. C.; Shaw, B. L. (1954). "Etoxyacetylen". Org. Synth. 34: 46; Coll. Vol. 4: 404.
Bou, Anna; Pericàs, Miquel A.; Riera, Antoni; Serratosa, Fèlix (1987). "Các dialkoxyacetylen: di-tert-butoxyethyn, một chất trung gian tổng hợp đầy giá trị". Org. Synth. 65: 68; Coll. Vol. 8: 161.
Magriotis, Plato A.; Brown, John T. (1995). "Phenylthioacetylen". Org. Synth. 72: 252; Coll. Vol. 9: 656.
Ashworth, P. J.; Mansfield, G. H.; Whiting, M. C. (1955). "2-butyn-1-ol". Org. Synth. 35: 20; Coll. Vol. 4: 128. - ^ Newman, Melvin S.; Stalick, W. M. (1977). "1-Etoxy-1-butyn". Org. Synth. 57: 65; 6: 564.
- ^ Salaun, J. R.; Champion, J.; Conia, J. M. (1977). "Cyclobutanon từ methylencyclopropan thông qua oxaspiropentan". Org. Synth. 57: 36; Coll. Vol. 6: 320.
- ^ Nakamura, Masuharu; Wang, Xio Qun; Isaka, Masahiko; Yamago, Shigeru; Nakamura, Eiichi (2003). "Tổng hợp và mở rộng vòng một 2,2-dialkoxi-1-methylencyclopropan: 6,6-dimethyl-1-methylen-4,8-dioxaspiro(2.5)octan và cis-5-(5,5-dimethyl-1,3-dioxan-2-yliden)hexahydro-1(2H)-pentalen-2-on". Org. Synth. 80: 144.
- ^ Bottini, Albert T.; Olsen, Robert E. (1964). "N-Ethylenediamine". Org. Synth. 44: 53; Coll. Vol. 5: 541.
- ^ Skorcz, J. A.; Kaminski, F. E. (1968). "1-Cyanobenzocyclobuten". Org. Synth. 48: 55; Coll. Vol. 5: 263.
- ^ Saunders, J. H. (1949). "1-Ethylcyclohexanol". Org. Synth. 29: 47; Coll. Vol. 3: 416.
Peterson, P. E.; Dunham, M. (1977). "(Z)-4-chloro-4-hexenyl trifluoroacetat". Org. Synth. 57: 26; Coll. Vol. 6: 273.
Kauer, J. C.; Brown, M. (1962). "Acid tetrolic". Org. Synth. 42: 97; Coll. Vol. 5: 1043. - ^ Coffman, Donald D. (1940). "Dimethylethylcarbinol". Org. Synth. 20: 40; Coll. Vol. 3: 320.
Hauser, C. R.; Adams, J. T.; Levine, R. (1948). "diisovalerylmethan". Org. Synth. 28: 44; Coll. Vol. 3: 291. - ^ Vanderwerf, Calvin A.; Lemmerman, Leo V. (1948). "2-Allylcyclohexanon". Org. Synth. 28: 8; Coll. Vol. 3: 44.
- ^ Hauser, Charles R.; Dunnavant, W. R. (1960). "Acid α,β-diphenylpropionic". Org. Synth. 40: 38; Coll. Vol. 5: 526.
Kaiser, Edwin M.; Kenyon, William G.; Hauser, Charles R. (1967). "Ethyl 2,4-diphenylbutanoat". Org. Synth. 47: 72; Coll. Vol. 5: 559.
Wawzonek, Stanley; Smolin, Edwin M. (1951). "α,β-diphenylcinnamonitrin". Org. Synth. 31: 52; Coll. Vol. 4: 387. - ^ Murphy, William S.; Hamrick, Phillip J.; Hauser, Charles R. (1968). "1,1-diphenylpentan". Org. Synth. 48: 80; Coll. Vol. 5: 523.
- ^ Hampton, K. Gerald; Harris, Thomas M.; Hauser, Charles R. (1971). "Phenylation của diphenyliodoni chloride: 1-phenyl-2,4-pentandion". Org. Synth. 51: 128; Coll. Vol. 6: 928.
Hampton, K. Gerald; Harris, Thomas M.; Hauser, Charles R. (1967). - ^ Potts, K. T.; Saxton, J. E. (1960). "1-Methylindole". Org. Synth. 40: 68; Coll. Vol. 5: 769.
- ^ Bunnett, J. F.; Brotherton, T. K.; Williamson, S. M. (1960). "N-β-Naphthylpiperidin". Org. Synth. 40: 74; Coll. Vol. 5: 816.
- ^ Brazen, W. R.; Hauser, C. R. (1954). "2-Methylbenzyldimethylamin". Org. Synth. 34: 61; Coll. Vol. 4: 585.
- ^ Allen, C. F. H.; VanAllen, J. (1944). "Este phenylmethylglycidic". Org. Synth. 24: 82; Coll. Vol. 3: 727.
- ^ Allen, C. F. H.; VanAllen, James (1942). "2-Methylindole". Org. Synth. 22: 94; Coll. Vol. 3: 597.