Acid
| Acid và base |
|---|
| Các dạng acid |
| Các dạng base |

Acid (bắt nguồn từ tiếng Pháp: acide [a.sid]),[1] thường được phiên âm là axít,[1] là một phân tử hoặc ion có khả năng cho 1 proton (tức là ion hydro, H+), được gọi là acid Brønsted–Lowry, hoặc hình thành liên kết cộng hóa trị với một cặp electron, được gọi là acid Lewis.[2][3]
Thể loại acid đầu tiên là chất cho proton, hay acid Brønsted–Lowry. Trong trường hợp đặc biệt của dung dịch nước, chất cho proton tạo thành ion hydroni H3O+ và được gọi là acid Arrhenius.
Định nghĩa và khái niệm[sửa | sửa mã nguồn]
Các định nghĩa hiện đại liên quan đến các phản ứng hóa học cơ bản phổ biến cho tất cả các acid.
Hầu hết các acid gặp phải trong cuộc sống hàng ngày là dung dịch nước, hoặc có thể hòa tan trong nước, vì vậy định nghĩa Arrhenius và Brønsted–Lowry là phù hợp nhất.
Định nghĩa Brønsted–Lowry là định nghĩa được sử dụng rộng rãi nhất, các phản ứng acid–base được cho là liên quan đến việc chuyển proton (H+) từ acid sang base.
Các ion hydroni là acid theo cả ba định nghĩa. Mặc dù rượu và amin có thể là acid Brønsted–Lowry, chúng cũng có thể hoạt động như các base Lewis do các cặp electron đơn độc trên các nguyên tử oxy và nitơ của chúng.
Acid Arrhenius[sửa | sửa mã nguồn]

Nhà hóa học người Thụy Điển Svante Arrhenius quy các tính chất của acid cho các ion hydro (H+) hoặc proton vào năm 1884. Acid Arrhenius là 1 chất mà khi thêm vào nước sẽ làm tăng nồng độ của các ion H+ trong nước.[4][5] Lưu ý rằng các nhà hóa học thường viết H+ (aq) và đề cập đến ion hydro khi mô tả các phản ứng acid–base nhưng hạt nhân hydro tự do và 1 proton, không tồn tại một mình trong nước, nó tồn tại dưới dạng ion hydroni, H3O+. Do đó, acid Arrhenius cũng có thể được mô tả như 1 chất làm tăng nồng độ của các ion hydroni khi thêm vào nước. Ví dụ bao gồm các chất phân tử như acid hydrochloric và acid acetic.
Mặt khác, base Arrhenius là 1 chất làm tăng nồng độ của các ion hydroxide (OH-) khi hòa tan trong nước. Điều này làm giảm nồng độ hydroni vì các ion phản ứng tạo thành các phân tử H2O:
Do trạng thái cân bằng này, bất kỳ sự gia tăng nồng độ hydroni đều đi kèm với việc giảm nồng độ hydroxide. Do đó, acid Arrhenius cũng có thể được coi là 1 chất làm giảm nồng độ hydroxide, trong khi base Arrhenius làm tăng nó.
Trong dung dịch acid, nồng độ của các ion hydroni lớn hơn 10−7mol/lít. Do pH được định nghĩa là logarit âm của nồng độ các ion hydroni, do đó các dung dịch acid có độ pH nhỏ hơn 7.
Acid Bronsted–Lowry[sửa | sửa mã nguồn]
Mặc dù lý thuyết Arrhenius rất hữu ích để mô tả nhiều phản ứng, nhưng nó cũng khá hạn chế trong phạm vi của nó. Năm 1923, các nhà hóa học, Julian Nicolaus Brønsted và Thomas Martin Lowry đã công nhận độc lập rằng các phản ứng acid–base liên quan đến việc chuyển 1 proton. Acid Brønsted–Lowry (hay đơn giản là acid Brønsted) tặng 1 proton cho base Brønsted–Lowry.[5] Lý thuyết acid–base Brønsted–Lowry có một số lợi thế so với lý thuyết Arrhenius. Hãy xem xét các phản ứng sau đây của acid acetic (CH3COOH), acid hữu cơ mang đến cho giấm hương vị đặc trưng của nó:
- CH
3COOH + H
2O ⇌ CH
3COO−
+ H
3O+ - CH
3COOH + NH
3 ⇌ CH
3COO−
+ NH+
4
Cả hai lý thuyết đều dễ dàng mô tả phản ứng đầu tiên: CH3COOH hoạt động như acid Arrhenius vì nó hoạt động như 1 nguồn H3O+ khi hòa tan trong nước và nó hoạt động như 1 acid Brønsted bằng cách cho proton vào nước. Trong ví dụ thứ 2 CH3COOH trải qua quá trình biến đổi tương tự, trong trường hợp này tặng 1 proton cho amonia (NH3), nhưng không liên quan đến định nghĩa Arrhenius của 1 acid vì phản ứng không tạo ra hydroni. Tuy nhiên, CH3COOH vừa là Arrhenius vừa là acid Brønsted–Lowry.
Lý thuyết Brønsted–Lowry có thể được sử dụng để mô tả các phản ứng của các hợp chất phân tử trong dung dịch không màu hoặc pha khí. Hydro chloride (HCl) và amonia kết hợp trong một số điều kiện khác nhau để tạo thành amoni chloride (NH4Cl). Trong dung dịch nước HCl hoạt động như acid hydrochloric và tồn tại dưới dạng ion hydroni và chloride. Các phản ứng sau đây minh họa những hạn chế trong định nghĩa của Arrhenius:
Như với các phản ứng acid acetic, cả hai định nghĩa đều hoạt động trong ví dụ đầu tiên, trong đó nước là dung môi và ion hydroni được tạo thành bởi chất tan HCl. 2 phản ứng tiếp theo không liên quan đến sự hình thành các ion nhưng vẫn là phản ứng chuyển proton. Trong phản ứng thứ 2 hydro chloride và amonia (hòa tan trong benzen) phản ứng tạo thành amoni chloride rắn trong dung môi benzen và trong khí HCl và NH3 dạng khí thứ 3 kết hợp với nhau tạo thành chất rắn.
Acid Lewis[sửa | sửa mã nguồn]
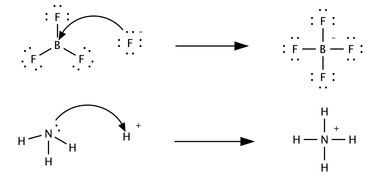
Một khái niệm thứ 3, chỉ liên quan đến lề được đề xuất vào năm 1923 bởi Gilbert N. Lewis, bao gồm các phản ứng với các đặc tính acid–base không liên quan đến việc chuyển proton. Acid Lewis là 1 acid chấp nhận 1 cặp electron từ các chất khác; nói cách khác, nó là 1 acid chấp nhận cặp electron.[5] Phản ứng acid–base Brønsted là phản ứng chuyển proton trong khi phản ứng acid–base Lewis là chuyển cặp electron. Nhiều acid Lewis không phải là acid Brønsted–Lowry. Tương phản như thế nào các phản ứng sau được mô tả về mặt hóa học acid–base:
Trong phản ứng đầu tiên, 1 ion fluoride, F-, từ bỏ 1 cặp electron thành boron trifluoride để tạo thành sản phẩm tetrafluoroborate. Fluoride "mất" một cặp electron hóa trị vì các electron được chia sẻ trong liên kết B lợi F nằm ở vùng không gian giữa 2 hạt nhân nguyên tử và do đó ở xa hạt nhân fluoride hơn so với ion fluoride đơn độc. Bor trifluoride là acid Lewis vì nó chấp nhận cặp electron từ fluoride. Phản ứng này không thể được mô tả theo lý thuyết Brønsted vì không có sự chuyển proton. Phản ứng thứ 2 có thể được mô tả bằng cách sử dụng 1 trong 2 lý thuyết. 1 proton được chuyển từ acid Brønsted không xác định sang amonia, 1 base Brønsted; cách khác, amonia hoạt động như base Lewis và chuyển 1 cặp electron đơn độc để tạo liên kết với ion hydro. Chất thu được cặp electron là acid Lewis; ví dụ, nguyên tử oxy trong H3O+ thu được 1 cặp electron khi 1t trong các liên kết H–O bị phá vỡ và các electron được chia sẻ trong liên kết trở thành cục bộ trên oxy. Tùy thuộc vào ngữ cảnh, acid Lewis cũng có thể được mô tả là chất oxy hóa hoặc chất điện ly. Các acid Brønsted hữu cơ, như acid acetic, acid citric hoặc acid oxalic, chứ không phải là acid Lewis.[4] Chúng phân ly trong nước để tạo ra acid Lewis, H+, nhưng đồng thời cũng tạo ra 1 lượng tương đương với base Lewis (tương ứng acetate, citrate hoặc oxalate cho các acid được đề cập).
Tính chất chung[sửa | sửa mã nguồn]
Tính chất vật lý[sửa | sửa mã nguồn]
- Vị giác: acid có vị chua khi hòa tan trong nước (chỉ một số acid có vị chua).
- Xúc giác: acid có cảm giác bỏng rát (với các acid mạnh) khi rơi trên da.
- Độ dẫn điện: acid là các chất điện ly nên có khả năng dẫn điện.
Tính chất hóa học[sửa | sửa mã nguồn]
Làm đổi màu chất chỉ thị (làm quỳ tím hóa đỏ hoặc hồng).
Tác dụng với kim loại (lithi, kali, bari, caesi, calci, natri, magnesi, nhôm, mangan, kẽm, chromi, sắt, cobalt, nickel, thiếc, chì) tạo thành muối và giải phóng khí hydro.
Ví dụ:
Trong trường hợp kim loại tác dụng với:
Acid sulfuric (H2SO4) đặc sẽ tạo ra muối, khí lưu huỳnh dioxide (SO2) và nước (H2O).
Ví dụ:
Acid nitric (HNO3) sẽ tan, tạo ra muối, khí nitơ monoxide và nước.
Ví dụ:
HNO3 đặc sẽ tạo ra muối, khí nitơ dioxide và H2O.
Ví dụ:
Tác dụng với base: xem phần phản ứng trung hòa.
Tác dụng với oxide base / lưỡng tính (tạo thành muối và nước).
Ví dụ:
Tác dụng với muối (tạo acid mới và muối mới).
Ví dụ:
Tính điện ly[sửa | sửa mã nguồn]
Trong nước phản ứng sau diễn ra giữa acid và nước, là chất đóng vai trò của 1 base:
Hằng số acid (hay hằng số phân ly acid) là hằng số cân bằng cho phản ứng của acid với nước:
Các acid mạnh có giá trị Ka lớn (có nghĩa là cân bằng của phản ứng nghiêng về bên phải, có rất nhiều ion H3O+ tồn tại; acid gần như điện ly hoàn toàn). Ví dụ, giá trị của Ka đối với acid hydrochloric (HCl) là 107.
Các acid yếu có giá trị Ka nhỏ (có nghĩa là ở mức cân bằng thì có 1 lượng đáng kể của AH và A- tồn tại cùng nhau trong dung dịch; các ion H3O+ tồn tại ở mức vừa phải; acid chỉ điện ly một phần). Ví dụ, giá trị của Ka cho acid acetic là 1,8 x 10−5.
Các acid mạnh bao gồm các acid của các halogen như acid hydrochloric, acid hydrobromic và acid hydroiodic. (Tuy nhiên, acid hydrofluoric (HF) lại tương đối yếu). Các acid chứa oxy, có xu hướng với các nguyên tử trung tâm ở các trạng thái oxy hóa cao, được oxy bao quanh, cũng là các acid mạnh chẳng hạn acid nitric, acid sulfuric, acid perchloric. Phần lớn các acid hữu cơ là acid yếu.[6]
Chú ý:
- Thuật ngữ "ion hydro" và "proton" được sử dụng tương đương; cả hai đều chỉ tới H+.
- Trong các phản ứng hóa học H+ thông thường được viết tuy rằng trong nước nó thực sự là H3O+.
- Cường độ acid được đo bằng giá trị Ka của nó. Độ pH đo xem có bao nhiêu ion hydro tồn tại, điều này phụ thuộc vào dạng acid (base) và phụ thuộc vào lượng của nó trong dung dịch.
- Cường độ acid được định nghĩa bằng pKa= - log(Ka).
Phản ứng trung hòa[sửa | sửa mã nguồn]
Phản ứng trung hòa là phản ứng hóa học giữa acid và base. Sản phẩm tạo thành là muối và nước. Vì thế nó còn được gọi là phản ứng tạo nước. Ví dụ:
Dạng phản ứng này tạo thành nền tảng của các phương pháp thử chuẩn độ để phân tích acid, trong đó các chất chỉ thị độ pH chỉ ra điểm trung hòa.
Bậc điện ly acid[sửa | sửa mã nguồn]
Một số phân tử acid có thể cung cấp nhiều hơn 1 ion H+ (proton). Các acid mà chỉ có thể cho 1 ion H+ trên 1 phân tử được gọi là acid monoproton, các phân tử acid nào mà có thể cung cấp 2 ion H+ là acid diproton, các phân tử acid nào có thể cho 3 ion H+ là acid triproton,... 1 acid monoproton chỉ có 1 nấc điện ly (đôi khi gọi là ion hóa) như sau và đơn giản chỉ có 1 hằng số điện ly:
1 acid diproton (được ký hiệu tượng trưng là H2A) có thể có 1 hoặc 2 nấc điện ly phụ thuộc vào các điều kiện môi trường (tức pH). Mỗi nấc điện ly có hằng số điện ly riêng, là Ka1 và Ka2.
- Ka1
- Ka2
Thông thường hằng số điện ly thứ nhất lớn hơn so với hằng số điện ly thứ 2; hay Ka1 > Ka2. Ví dụ, acid sulfuric (H2SO4) có thể cho 1 ion H+ để tạo ra một anion bisulfat (HSO4-), với hệ số Ka1 là rất lớn; sau đó nó có thể cho tiếp ion H+ thứ 2 để tạo ra anion sulfat (SO4−2) trong đó Ka2 là có giá trị trung bình. Giá trị lớn của Ka1 cho nấc điện ly thứ nhất làm cho acid sulfuric là 1 acid mạnh. Tương tự, acid yếu và không ổn định như acid carbonic (H2CO3) có thể mất 1 ion H+ để tạo ra anion bicarbonat (HCO3-) và mất tiếp ion H+ thứ hai để tạo ra anion carbonat (CO32-). Cả hai giá trị Ka đều nhỏ, nhưng Ka1 > Ka2.
Tương tự, 1 acid triproton (H3A) có thể có 1, 2, 3 nấc điện ly và có ba hằng số điện ly, trong đó Ka1 > Ka2 > Ka3.
- Ka1
- Ka2
- Ka3
Một ví dụ của acid triproton vô cơ là acid orthophosphoric (H3PO4), thông thường gọi là acid phosphoric. 3 nguyên tử hydro của nó có thể kế tiếp nhau mất đi như là ion H+ (hay H3O+ trong nước) để sinh ra H2PO4-, sau đó là HPO42−, và cuối cùng là PO43−, ion orthophosphat mang điện tích -3, thông thường gọi là phosphat. Ví dụ của acid triproton hữu cơ là acid citric, nó cũng có thể kế tiếp nhau mất 3 ion H+ để cuối cùng tạo ra ion citrat mang điện tích -3. Mặc dù vị trí của cả ba nguyên tử H trong phân tử gốc có thể là tương đương, nhưng các giá trị Ka kế tiếp nhau sẽ giảm dần do về mặt năng lượng, nó càng khó mất ion H+ hơn nếu ion mang điện tích âm cao dần lên và thường giảm khoảng 1.000 lần qua mỗi bậc.
Chỉ số acid[sửa | sửa mã nguồn]
Chỉ số này được sử dụng để định lượng số lượng acid tồn tại, chẳng hạn như trong dầu diesel sinh học. Nó là lượng base, biểu diễn theo lượng miligam kali hydroxide (KOH), cần phải có để trung hòa các thành phần acid trong 1 g mẫu thử.
- AN = (Veq - beq) × N × 56,1/Wđầu
Veq là lượng chất thử chuẩn (ml) được tiêu thụ bởi 1 mẫu dầu mỏ và 1 ml (spiking solution?) ở điểm tương đương, và beq là lượng chất thử chuẩn (ml) được tiêu thụ bởi 1 ml (spiking solution?) ở điểm tương đương.
Nồng độ phân tử gam của chất thử chuẩn (N) được tính như sau:
N = 1000 × WKHP / (204,23 × Veq).
Trong đó, WKHP là lượng (g) của KHP trong 50 ml dung dịch KHP tiêu chuẩn, và Veq là lượng của chất thử chuẩn (ml) được tiêu thụ bởi 50ml dung dịch KHP tiêu chuẩn ở điểm tương đương.
Chỉ số acid (mg KOH/g dầu) cho dầu diesel sinh học được ưa chuộng phải thấp hơn 3.
Ứng dụng của acid[sửa | sửa mã nguồn]
Có rất nhiều ứng dụng cho acid. Acid thường được sử dụng để loại bỏ sự gỉ sắt và sự ăn mòn khác từ kim loại trong quá trình được gọi là tẩy. Chúng có thể được sử dụng như 1 chất điện phân trong pin, chẳng hạn như acid sulfuric trong pin xe hơi. Acid mạnh, đặc biệt là acid sulfuric, được sử dụng rộng rãi trong chế biến khoáng sản. Ví dụ, khoáng chất phosphat phản ứng với acid sulfuric để tạo ra acid phosphoric để sản xuất phân bón phosphat, và kẽm được tạo ra bằng cách hòa tan kẽm oxide thành acid sulfuric, làm sạch dung dịch và electrowinning. Trong ngành công nghiệp hóa học, acid phản ứng trong phản ứng trung hòa để tạo ra muối. Ví dụ, acid nitric phản ứng với amonia để tạo ra amoni nitrat, 1 phân bón. Ngoài ra, các acid carboxylic có thể được este hóa với rượu cồn, để tạo ra este. Acid được sử dụng làm chất phụ gia cho đồ uống và thực phẩm, vì chúng làm thay đổi khẩu vị và phục vụ như chất bảo quản. Acid phosphoric, ví dụ, là 1 thành phần của đồ uống cola. Acid acetic được sử dụng trong cuộc sống hàng ngày như dấm. Acid carbonic là một phần quan trọng của một số loại nước uống cola và soda. Acid citric được sử dụng làm chất bảo quản trong nước sốt và dưa chua. Acid tartaric là 1 thành phần quan trọng của một số thực phẩm thông dụng như xoài chưa chín và me. Trái cây và rau quả tự nhiên cũng chứa acid. Acid citric có trong cam, chanh và các loại quả có múi khác. Acid oxalic có trong cà chua, rau bina, và đặc biệt là carambola và đại hoàng; lá rhubarb và carambolas chưa chín là độc tính vì nồng độ cao của acid oxalic.
Acid ascorbic (vitamin C) là 1 vitamin cần thiết cho cơ thể con người và có trong các loại thực phẩm như amla (quả mâm xôi Ấn Độ), chanh, quả cam, quýt và ổi.
Một số acid được sử dụng làm thuốc. Acid acetylsalicylic (aspirin) được sử dụng như thuốc giảm đau và làm giảm cơn sốt.
Acid đóng vai trò quan trọng trong cơ thể con người. Acid hydrochloric có trong dạ dày giúp tiêu hóa bằng cách phá vỡ các phân tử thức ăn lớn và phức tạp. amino acid được yêu cầu để tổng hợp các protein cần thiết cho sự phát triển và sửa chữa các mô cơ thể.[7] Acid béo cũng cần cho sự phát triển và sửa chữa các mô của cơ thể. Các acid nucleic rất quan trọng cho việc sản xuất DNA và RNA và chuyển các đặc tính sang con lai qua gen. Acid carbonic rất quan trọng để duy trì độ cân bằng pH trong cơ thể.
Tên gọi của acid[sửa | sửa mã nguồn]
Các acid được đặt tên phù hợp với anion của chúng. Phần cuối của ion bị bỏ đi và thay thế với các hậu tố mới theo bảng dưới đây.
| Phần cuối anion | Hậu tố acid |
|---|---|
| at | acid + ic |
| it | acid + ơ |
| ide | acid + hydro...ic |
Ví dụ:
- Sulfat → acid sulfuric
- Sulfit → acid sulfurơ
- Sulfide → acid hydrosulfuric
- Perchlorat → acid perchloric
- Chloride → acid hydrochloric
Acid không có oxy[sửa | sửa mã nguồn]
Đối với acid không có oxy: tên acid: acid + hydro + tên phi kim + ic.[8]
Ví dụ: HCl: acid hydrochloric; H2S: acid hydrosulfuric.
Gốc acid tương ứng là: -Cl: chloride; =S: sulfide.
Acid có oxy[sửa | sửa mã nguồn]
Acid có nhiều nguyên tử oxy: tên acid: acid + tên của phi kim + ic.[8]
Ví dụ: HNO3: acid nitric; H2SO4: acid sulfuric; H3PO4: acid phosphoric.
NO3: nitrat; = SO4: sulfat; = PO4: phosphat.
Acid có ít nguyên tử oxy[sửa | sửa mã nguồn]
Đối với acid có ít nguyên tử oxy: tên acid: acid + tên phi kim + ơ.
Ví dụ: H2SO3: acid sulfurơ; SO3: sulfit.
Các acid điển hình[sửa | sửa mã nguồn]
Acid được phân thành hai loại lớn có cấu tạo phân tử rất khác nhau: acid hữu cơ và acid vô cơ.[9]
Acid vô cơ mạnh[sửa | sửa mã nguồn]
- Acid hydrochloric HCl.
- Acid hydrobromic HBr.
- Acid hydroiodic HI.
- Acid nitric HNO3.
- Acid sulfuric H2SO4.
- Acid chloric HClO3.
- Acid perchloric HClO4.
- Acid selenic H2SeO4.
- Acid permanganic HMnO4.
- Acid fluoroantimonic xHF·ySbF5 (phổ biến là HSbF6, H2SbF7).
Acid vô cơ yếu hay trung bình[sửa | sửa mã nguồn]
- Acid boric H3BO3.
- Acid phosphoric H3PO4.
- Acid carbonic H2CO3.
- Acid diphosphoric H4P2O7
- Acid hydrofluoric HF.
- Acid sulfurơ H2SO3.
- Acid selenơ H2SeO3.
- Acid nitrơ HNO2.
- Acid phosphorơ H3PO3.
- Acid hypochlorơ HClO.
- Acid chlorơ HClO2.
- Acid silicic H2SiO3.
- Acid hydrocyanic HCN.
- Acid chloroauric HAuCl4.
Acid hữu cơ[sửa | sửa mã nguồn]
- Acid acetic CH3-COOH (C2H4O2).
- Acid oxalic COOH-COOH (C2H2O4).
- Acid benzoic C6H5-COOH (C7H6O2).
- Acid butyric CH3-(CH2)2-COOH (C4H8O2).
- Acid citric COOH-CH2-C(COOH(OH))-CH2-COOH (C6H8O7).
- Acid formic H-COOH (CH2O2).
- Acid lactic CH3-CH(OH)-COOH (C3H6O3).
- Acid malic COOH-CH2-CH(OH)-COOH (C4H6O5).
- Acid propionic CH3-CH2-COOH (C3H6O2).
- Acid pyruvic CH3-C(=O)-COOH (chứa nhóm chức keton) (C3H4O3).
- Acid valeric CH3-(CH2)3-COOH (C5H10O2).
Acid trong chế biến thực phẩm[sửa | sửa mã nguồn]
- Acid acetic hay acid etanoic: (E260) tìm thấy trong giấm và nước sốt cà chua.
- Acid adipic: (E355).
- Acid alginic: (E400).
- Acid benzoic: (E210).
- Acid boric: (E284).
- Acid ascorbic (vitamin C): (E300) tìm thấy trong các loại quả.
- Acid citric: (E330) tìm thấy trong quả các loại cam chanh.
- Acid carbonic: (E290) tìm thấy trong các nước uống carbonat hóa nhẹ.
- Acid carminic: (E120).
- Acid cyclamic: (E952).
- Acid erythorbic: (E315).
- Acid erythorbic: (E317).
- Acid formic: (E236).
- Acid fumaric: (E297).
- Acid gluconic: (E574).
- Acid glutamic: (E620).
- Acid guanylic: (E626).
- Acid hydrochloric: (E507).
- Acid inosinic: (E630).
- Acid lactic: (E270) tìm thấy trong các sản phẩm sữa như sữa chua.
- Acid malic: (E296).
- Acid metatartaric: (E353).
- Acid nicotinic: (E375).
- Acid oxalic: tìm thấy trong rau chân vịt và đại hoàng.
- Acid pectic: tìm thấy trong một số loại quả và rau.
- Acid phosphoric: (E338).
- Acid propionic: (E280).
- Acid sorbic: (E200) tìm thấy trong đồ uống và thực phẩm.
- Acid stearic: (E570) một loại acid béo.
- Acid succinic: (E363).
- Acid sulfuric: (E513).
- Acid tannic: tìm thấy trong chè.
- Acid tartaric: (E334) tìm thấy trong nho.
Tham khảo[sửa | sửa mã nguồn]
- ^ a b Đặng Thái Minh, "Dictionnaire Vietnamien — Français. Les mots Vietnamiens d'origine Française", Synergies Pays riverains du Mékong, № spécial, năm 2011. ISSN: 2107-6758. Trang 49.
- ^ IUPAC Gold Book - acid
- ^ Aihara, Herman (1920). Acid và kiềm. ISBN 978-604-77-5011-5. OCLC 1088505798.
- ^ a b Otoxby, D. W.; Gillis, H. P.; Butler, L. J. (2015). Principles of Modern Chemistry (ấn bản 8). Brooks Cole. tr. 617. ISBN 978-1305079113.
- ^ a b c Ebbing, D.D., & Gammon, S. D. (2005). General chemistry (8th ed.). Boston, MA: Houghton Mifflin. ISBN 0-618-51177-6
- ^ Chahardoli, Azam; Jalilian, Fereshteh; Memariani, Zahra; Hosein Farzaei, Mohammad; Shokoohinia, Yalda. Analysis of organic acids. doi:10.1016/B978-0-12-816455-6.00026-3.
- ^ Barrett, G. C.; Elmore, D. T. (tháng 6 năm 2012). 8 - Biological roles of amino acids and peptides - University Publishing Online. doi:10.1017/CBO9781139163828. ISBN 9780521462921. Bản gốc lưu trữ ngày 2 tháng 3 năm 2016.
- ^ a b Theo TCVN 5529:2010 và TCVN 5530:2010
- ^ Fire Sr., Frank; L. Fire, Frank (2009). The Common Sense Approach to Hazardous Materials (bằng tiếng Anh). ISBN 9781593701949.
| Wikimedia Commons có thêm hình ảnh và phương tiện truyền tải về Acid. |















![{\displaystyle K_{a}={[A^{-}]\cdot [{\mbox{H}}_{3}{\mbox{O}}^{+}] \over [HA]}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/90bbd37fc2a8d627472f0b75da1a67a410b0162b)





