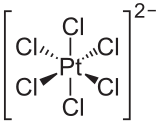Platin
| Platin, 78Pt | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tính chất chung | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tên, ký hiệu | Platin, Pt | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Phiên âm | /ˈplæt.n.əm/ or /ˈplæt.nəm/ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hình dạng | Xám trắng | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Platin trong bảng tuần hoàn | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Số nguyên tử (Z) | 78 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Khối lượng nguyên tử chuẩn (Ar) | 195,084 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Phân loại | kim loại chuyển tiếp | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nhóm, phân lớp | 10, d | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chu kỳ | Chu kỳ 6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cấu hình electron | [Xe] 4f14 5d9 6s1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
mỗi lớp | 2, 8, 18, 32, 17, 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tính chất vật lý | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Màu sắc | Xám trắng | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Trạng thái vật chất | Chất rắn | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nhiệt độ nóng chảy | 2041,4 K (1768,3 °C, 3214,9 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nhiệt độ sôi | 4098 K (3825 °C, 6917 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mật độ | 21,45 g·cm−3 (ở 0 °C, 101.325 kPa) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mật độ ở thể lỏng | ở nhiệt độ nóng chảy: 19,77 g·cm−3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nhiệt lượng nóng chảy | 22.17 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nhiệt bay hơi | 469 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nhiệt dung | 25,86 J·mol−1·K−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Áp suất hơi
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tính chất nguyên tử | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Trạng thái oxy hóa | 6, 5, 4, 3, 2, 1, -1, -2 base nhẹ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Độ âm điện | 2,28 (Thang Pauling) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Năng lượng ion hóa | Thứ nhất: 870 kJ·mol−1 Thứ hai: 1791 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bán kính cộng hoá trị | thực nghiệm: 139 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bán kính liên kết cộng hóa trị | 136±5 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bán kính van der Waals | 175 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Thông tin khác | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cấu trúc tinh thể | Lập phương tâm mặt | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Độ giãn nở nhiệt | 8,8 µm·m−1·K−1 (ở 25 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Độ dẫn nhiệt | 71,6 W·m−1·K−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Điện trở suất | ở 20 °C: 105 n Ω·m | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tính chất từ | Thuận từ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mô đun Young | 168 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mô đun cắt | 61 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mô đun khối | 230 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hệ số Poisson | 0,38 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Độ cứng theo thang Mohs | 3,5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Độ cứng theo thang Vickers | 400-550 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Độ cứng theo thang Brinell | 300-500 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Số đăng ký CAS | 7440-06-4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Đồng vị ổn định nhất | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bài chính: Đồng vị của Platin | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Platin hay còn gọi là bạch kim là một nguyên tố hóa học, ký hiệu Pt có số nguyên tử 78 trong bảng tuần hoàn các nguyên tố hóa học. Tên platin bắt nguồn từ thuật ngữ tiếng Tây Ban Nha platina del Pinto, nghĩa đen là "sắc hơi óng ánh bạc của sông Pinto".[7] Platin là một kim loại chuyển tiếp quý hiếm, màu xám trắng, đặc dẻo, dễ uốn. Mặc dù nó có sáu đồng vị tự nhiên, nhưng platin vẫn là một trong những nguyên tố hiếm nhất trong lớp vỏ Trái Đất với mật độ phân bố trung bình khoảng 0,005 mg/kg. Platin thường được tìm thấy ở một số quặng nickel và đồng, chủ yếu là ở Nam Phi chiếm 80% tổng sản lượng trên toàn thế giới.
Platin thuộc nhóm 10 của bảng tuần hoàn cho nên nó có tính trơ, rất ít bị ăn mòn thậm chí ở nhiệt độ cao, vì vậy nó được xem là một kim loại quý. Platin thường xuất hiện ở trong bồi tích tự nhiên của một số con sông, nó lần đầu tiên được sử dụng để sản xuất các đồ tạo tác bởi người bản xứ Nam Mỹ thời kỳ tiền Columbus. Platin đã từng được nhắc đến trong các bản thảo ở châu Âu vào đầu thế kỷ XVI, nhưng vẫn không được phổ biến cho đến năm 1748, khi Antonio de Ulloa báo cáo về một loại kim loại mới có nguồn gốc từ Colombia, sau đó platin đã trở thành tâm điểm của các cuộc điều tra khoa học.
Platin được sử dụng trong làm chất xúc tác, trang thiết bị phòng thí nghiệm, thiết bị điện báo, các điện cực, nhiệt kế điện trở bạch kim, thiết bị nha khoa, và đồ trang sức. Platin là một vật liệu khan hiếm, quý và rất có giá trị bởi vì sản lượng khai thác hằng năm chỉ tầm vài trăm tấn. Vì là một kim loại nặng, nó có ảnh hưởng không tốt đối với sức khỏe khi tiếp xúc với các muối của nó, nhưng do khả năng chống ăn mòn cho nên nó ít độc hại hơn so với các kim loại khác. Một số hợp chất của Platin, đặc biệt là cisplatin, được sử dụng để dùng trong hóa trị liệu chống lại một số loại ung thư.
Từ nguyên[sửa | sửa mã nguồn]
Cách gọi "platin" là cách gọi quy ước của người Việt đối với tên các nguyên tố tiếng Latin: bỏ tiếp vĩ ngữ "-um". Tên gọi Latin "platinum" có gốc từ tiếng Tây Ban Nha "platina", nghĩa đen là "bạc nhỏ".
"Bạch kim" (白金 "vàng trắng") là tên gọi khác của cả hai kim loại Ag và Pt. Platin có tên Hán Việt là "bạc" (鉑). Chữ Hán "鉑" hợp thành từ "金" ("kim loại vàng") và "白" ("màu trắng"). Trong tiếng Việt, "bạc" lại bị hiểu thành kim loại có ký hiệu hoá học là Ag.
Đặc điểm[sửa | sửa mã nguồn]
Tính chất vật lý[sửa | sửa mã nguồn]
Ở dạng tinh khiết, platin có màu trắng bạc, sáng bóng, dẻo và dễ uốn.[8] Nó không bị oxy hóa ở bất cứ nhiệt độ nào, tuy nhiên có thể bị ăn mòn bởi các halogen, cyanide, lưu huỳnh và dung dịch kiềm ăn da. Platin không hòa tan trong axit clohiđric và axit nitric, nhưng tan trong nước cường toan để tạo thành axit hexacloroplatinic(IV), H2PtCl6.[9] Platin ít bị mài mòn và mờ cho nên rất thích hợp để làm đồ trang sức mỹ nghệ. Kim loại này khó bị ăn mòn, chịu được nhiệt độ cao và có tính dẫn điện ổn định cho nên được sử dụng trong các ứng dụng công nghiệp.[10]
Tính chất hóa học[sửa | sửa mã nguồn]

Platin thường có số oxy hóa phổ biến nhất là +2 và +4, các số oxy hóa +1 và +3 ít phổ biến hơn. Ngoài ra các số oxy hóa khác của platin như +5 (trong PtF5) hay +6 (trong PtO3) cũng tồn tại. Tinh thể platin(II) tam phối tử (tetracoordinate) có dạng hình vuông phẳng 16 electron. Platin hòa tan trong nước cường toan cho ra axit hexacloroplatinic(IV) tan ("H2PtCl6", (H3O)2PtCl6.nH2O):[11]
- Pt + 4HNO3 + 6HCl → H2PtCl6 + 4NO2↑ + 4H2O
Platin có tính axit nhẹ nên nó có ái lực lớn đối với lưu huỳnh, ví dụ lưu huỳnh trong dimethyl sulfoxid (DMSO), tạo thành một số phức chất DMSO tùy theo dung môi phản ứng.[12]
Đồng vị[sửa | sửa mã nguồn]
Platin có sáu đồng vị tự nhiên: 190Pt, 192Pt, 194Pt, 195Pt, 196Pt, và 198Pt. Phổ biến nhất trong số này là 195Pt, chiếm tỉ lệ 33,83%. Đây là đồng vị ổn định duy nhất có spin khác 0; spin l=1/2. Đồng vị 190Pt là hiếm nhất, chỉ chiếm 0,01%. Trong số các đồng vị tự nhiên, chỉ có 190Pt là không ổn định, mặc dù nó bị phân rã với chu kỳ bán rã 6,5 × 1011 năm.198Pt cũng phân rã alpha, nhưng với chu kỳ bán rã lớn hơn 3,2 × 1014 năm, cho nên nó được coi là ổn định. Platin cũng có 31 đồng vị tổng hợp khác nhau, có khối lượng nguyên tử từ 166 đến 202, nâng tổng số đồng vị lên 37. Trong số các đồng vị này, 166Pt là ít ổn định nhất với chu kỳ bán rã 300 μs, ổn định nhất là 193Pt với chu kỳ bán rã 50 năm. Hầu hết các đồng vị platin phân rã hạt nhân theo kiểu kết hợp giữa phân rã beta và phân rã alpha.188Pt, 191Pt, và 193Pt thường phân rã khi bắt electron.190Pt và 198Pt phân rã beta kép.[13]
Phân bố[sửa | sửa mã nguồn]

Platin là một kim loại cực kỳ hiếm,[14] nó chỉ chiếm mật độ 0,005ppm trong lớp vỏ Trái Đất[15][16]. Platin tự nhiên thường được tìm thấy ở dạng tinh khiết và hợp kim với iriđi như platiniridi. Phần lớn platin tự nhiên được tìm thấy ở các lớp trầm tích đại trung sinh. Các mỏ bồi tích được khai thác bởi người Nam Mỹ thời kỳ tiền Columbus ở Chocó Department, Colombia vẫn còn là nguồn cung cấp các kim loại nhóm platin. Một mỏ bồi tích lớn khác ở dãy núi Ural, Nga cũng đang được khai thác.[9]
Trong các mỏ nickel và đồng, các kim loại nhóm platin thường xuất hiện ở dạng muối sulfide như (Pt,Pd)S, Te2− như PtBiTe, antimonua (PdSb), asenua như PtAs2 và các dạng hợp kim với Ni và Cu. PtAs2 là nguồn platin chính trong quặng nickel ở mỏ Sudbury Basin, Ontario Canada. Mỏ Merensky Reef ở Gauteng, Nam Phi chứa nhiều quặng sulfide của các kim loại quý hiếm Pt, Pd và Ni.[17]
Năm 1865, crom đã được phát hiện trong khu vực Bushveld của Nam Phi, tiếp theo sau đó là platin vào năm 1906.[18] Đây là nơi có trữ lượng platin lớn nhất được biết đến.[19] Ngoài ra còn 2 mỏ đồng-nickel trữ lượng lớn gần Norilsk ở Nga và lưu vực Sudbury Canada. Ở lưu vực sông Sudbury, mật độ platin trong quặng nickel thực tế hiện nay chỉ là 0,5 ppm. Các mỏ nhỏ hơn có thể được tìm thấy ở Hoa Kỳ,[19] ví dụ như trong dãy Absaroka ở Montana.[20] Trong năm 2009, Nam Phi là nước sản xuất platin hàng đầu, chiếm gần 80% tổng sản lượng toàn thế giới, tiếp theo là Nga với 11%.[21]
Platin tồn tại với mật độ phân bố cao ở Mặt Trăng và các thiên thạch. Tương ứng, platin được tìm thấy hơi nhiều ở những nơi bị sao băng va chạm trên Trái Đất kết hợp với tác động của núi lửa, các lưu vực Sudbury là một ví dụ.[22]
Hợp chất[sửa | sửa mã nguồn]
Halogen[sửa | sửa mã nguồn]
Axit hexacloroplatinic(IV) có lẽ là hợp chất bạch kim quan trọng nhất, vì nó tạo nên các hợp chất platin khác. Bản thân axit này được ứng dụng trong nhiếp ảnh, khắc kẽm, mực in không phai, mạ, làm gương, nhuộm màu sứ, và như một chất xúc tác.[23]
Tác dụng của axit hexacloroplatinic(IV) với muối amoni, chẳng hạn như amoni chloride, tạo thành amoni hexacloroplatinat(IV)[11] gần như không tan trong dung dịch amonia. Đốt nóng muối amoni này với sự có mặt của hiđrô sẽ tạo ra platin nguyên chất.[24] Kali hexacloroplatinat(IV) cũng không tan, và axit hexacloroplatinic(IV) đã được sử dụng trong việc xác định ion kali bằng phương pháp phân tích trọng lượng.[25]
Khi axit hexacloroplatinic(IV) được đun nóng, nó phân hủy thành PtCl4 và PtCl2 rồi thành platin nguyên tố theo các bước phản ứng sau:[26]
- (H3O)2PtCl6·nH2O ⇌ PtCl4 + 2HCl + (n + 2)H2O
- PtCl4 ⇌ PtCl2 + Cl2↑
- PtCl2 ⇌ Pt + Cl2↑
Cả ba phản ứng đều là phản ứng thuận nghịch. Platin(II) bromide và platin(IV) bromide cũng có những phản ứng tương tự. Platin hexaflorua là một chất oxy hóa mạnh có khả năng oxy hóa cả oxy.
- O2 + PtF6 → O2PtF6
Oxit[sửa | sửa mã nguồn]
Platin(IV) oxit, PtO2, còn được gọi là chất xúc tác của Adams, là một chất bột màu đen hòa tan trong dung dịch KOH và axit đậm đặc.[27] PtO2 và hiếm hơn PtO (tím đen) đều bị phân hủy khi đun nóng.[8] Platin(II, IV) oxit, Pt3O4, được hình thành từ phản ứng sau đây:
- 2Pt2+ + Pt4+ + 4O2− → Pt3O4
Pt3O4 tạo thành chất bột màu đen.
Pt cũng có thể tạo ra platin(III) oxit (Pt2O3), trước đây chỉ được biết đến dưới dạng ngậm nước.[28]
Sự tồn tại của platin(V) oxit chưa rõ, mặc dù hợp chất được xác định là chất rắn màu đỏ nâu.[29]
Platin cũng tạo một trioxit với số oxy hóa +6. PtO3 là chất bột màu đỏ nâu, nhưng không ổn định. Hợp chất thu được bằng cách oxy hóa PtO2 trong KOH. PtO3 có tính oxy hóa mạnh (oxy hóa HCl thành Cl2).[30]
Muối[sửa | sửa mã nguồn]
Hầu hết các hợp chất Pt(IV) thường có màu từ vàng đến cam (như Pt(SO4)2)[31]. Pt(IV) cũng có màu nâu sáng, như Pt(NO3)4 trong dung dịch.
Chỉ có ít muối Pt(III) được biết đến, như PtCl3, PtBr3, PtI3 và phức PtBr3.2NH3.[32]
Pt(II) tạo muối không tan trong nước, như các halide của Pt(II) (trừ PtF2).[33] Các muối chứa oxy của Pt(II) như PtSO4, Pt(NO3)2 cũng được biết đến.[34] Các muối nitrat đã kể trên tan được trong nước, nhưng dung dịch dễ bị phân hủy tạo muối cơ bản.[33]
Các hợp chất khác[sửa | sửa mã nguồn]
-
Ion hexacloroplatinat(IV)
-
Anion của muối Zeize
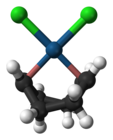
-
Dicloro(cyclocta-1,5-dien)platin(II)
-
Cisplatin
Hình ảnh[sửa | sửa mã nguồn]
-
Nguyên tố Bạch kim
-
Đồng 100oz có hình đại bàng bạch kim
-
Mảnh bạch kim vụn
Xem thêm[sửa | sửa mã nguồn]
Tham khảo[sửa | sửa mã nguồn]
- ^ Được cho là trải qua quá trình phân rã alpha thành 188Os với chu kỳ bán rã hơn 6×1016 năm.
- ^ Được cho là trải qua quá trình phân rã alpha thành 190Os.
- ^ Được cho là trải qua quá trình phân rã alpha thành 191Os.
- ^ Có thể trải qua phân rã β- ở trạng thái giới hạn thành 195Au.
- ^ Được cho là trải qua quá trình phân rã alpha thành 192Os.
- ^ Được cho là trải qua phân rã β−β− thành 198Hg với chu kỳ bán rã hơn 3,2×1014 năm.
- ^ Woods, Ian (2004). The Elements: Platinum. The Elements. Benchmark Books. ISBN 978-0761415503.
- ^ a b Lagowski, J. J. biên tập (2004). Chemistry Foundations and Applications. 3. Thomson Gale. tr. 267–268. ISBN 0-02-865724-1.
- ^ a b CRC contributors (2007–2008). “Platinum”. Trong Lide, David R. (biên tập). CRC Handbook of Chemistry and Physics. 4. New York: CRC Press. tr. 26. ISBN 978-0-8493-0488-0.
- ^ Craig, Bruce D; Anderson, David S; International, A.S.M. (tháng 1 năm 1995). “Platinum”. Handbook of corrosion data. tr. 8–9. ISBN 9780871705181.Quản lý CS1: sử dụng tham số tác giả (liên kết)
- ^ a b Kauffman, George B.; Thurner, Joseph J.; Zatko, David A. (1967). “Ammonium Hexachloroplatinate(IV)”. Inorganic Syntheses. 9: 182–185. doi:10.1002/9780470132401.ch51.
- ^ Han, Y.; Huynh, H. V.; Tan, G. K. (2007). “Mono- vs Bis(carbene) Complexes: A Detailed Study on Platinum(II)−Benzimidazolin-2-ylidenes”. Organometallics. 26 (18): 4612. doi:10.1021/om700543p.
- ^ Audi, G. (2003). “The NUBASE Evaluation of Nuclear and Decay Properties”. Nuclear Physics A. Atomic Mass Data Center. 729: 3–128. doi:10.1016/j.nuclphysa.2003.11.001.
- ^ Earth's natural wealth: an audit. New Scientist. ngày 23 tháng 5 năm 2007.
- ^ Stellman, Jeanne Mager (1998). Encyclopaedia of Occupational Health and Safety: Chemical, industries and occupations. International Labour Organization. tr. 141. ISBN 9221098168.
- ^ Murata, K. J. (1958). in Symposium on Spectrocemical Analysis for Trace Elements. ASTM International. tr. 71.
- ^ Xiao, Z.; Laplante, A. R. (2004). “Characterizing and recovering the platinum group minerals—a review”. Minerals Engineering. 17: 961–979. doi:10.1016/j.mineng.2004.04.001.
- ^ Dan Oancea: Platinum In South Africa http://www.infomine.com/publications/docs/Mining.com/Sep2008e.pdf
- ^ a b R. J. Seymour & O'Farrelly, J. I. (2001). “Platinum-group metals”. Kirk Othmer Encyclopedia of Chemical Technology. Wiley. doi:10.1002/0471238961.1612012019052513.a01.pub2.Quản lý CS1: sử dụng tham số tác giả (liên kết)
- ^ “Mining Platinum in Montana”. New York Times. ngày 13 tháng 8 năm 1998. Truy cập ngày 9 tháng 9 năm 2008.
- ^ “Platinum–Group Metals” (PDF). U.S. Geological Survey, Mineral Commodity Summaries. 2010. Truy cập ngày 9 tháng 9 năm 2010.
- ^ Koeberl, Christian (1998). “Identification of meteoritic components in imactites”. Meteorites: flux with time and impact effects. tr. 133–155. ISBN 9781862390171.
- ^ Krebs, Robert E. (1998). “Platinum”. The History and Use of our Earth's Chemical Elements. Greenwood Press. tr. 124–127. ISBN 0-313-30123-9.
- ^ Cotton, S. A. Chemistry of Precious Metals, Chapman and Hall (London): 1997. ISBN 0-7514-0413-6.
- ^ Smith, G. F.; Gring, J. L. (1933). “The Separation and Determination of the Alkali Metals Using Perchloric Acid. V. Perchloric Acid and Chloroplatinic Acid in the Determination of Small Amounts of Potassium in the Presence of Large Amounts of Sodium”. Journal of the American Chemical Society. 55 (10): 3957–3961. doi:10.1021/ja01337a007.
- ^ Schweizer, A. E.; Kerr, G. T. (1978). “Thermal Decomposition of Hexachloroplatinic Acid”. Inorganic Chemistry. 17 (8): 2326–2327. doi:10.1021/ic50186a067.
- ^ Perry, D. L. (1995). Handbook of Inorganic Compounds. CRC Press. tr. 296–298. ISBN 0849386713.
- ^ Platinum Sesquioxide, Pt2O3 - atomistry.com Lưu trữ 2021-11-26 tại Wayback Machine
- ^ Inorganic Chemistry, trang 1516 - https://books.google.com.vn/books?id=Mtth5g59dEIC&printsec=frontcover&dq=&hl=vi&sa=X&ved=0ahUKEwiaj6eTs6XoAhWlyIsBHc15BlIQuwUIOzAB#v=onepage&q=pto&f=false. Truy cập 19 tháng 3 năm 2020.
- ^ Inorganic Chemistry, trang 1521 - https://books.google.com.vn/books?id=Mtth5g59dEIC&printsec=frontcover&dq=&hl=vi&sa=X&ved=0ahUKEwiaj6eTs6XoAhWlyIsBHc15BlIQuwUIOzAB#v=onepage&q=pto&f=false. Truy cập 19 tháng 3 năm 2020.
- ^ Platinum Disulphate, Pt(SO4)2 - atomistry.com Lưu trữ 2021-11-26 tại Wayback Machine
- ^ Handbook of inorganic substances 2017 - https://books.google.com.vn/books?id=ROEsDwAAQBAJ&dq=&hl=vi&source=gbs_navlinks_s.
- ^ a b Inorganic Reactions in Water, trang 248 (2007) - https://books.google.com.vn/books?id=Dv_F03cdKPUC&printsec=frontcover&dq=&hl=vi&sa=X&ved=0ahUKEwiahIycuqXoAhWYwYsBHf1ABa4QuwUILzAA#v=onepage&q&f=false. Truy cập 19 tháng 3 năm 2020.
- ^ A Dictionary of Chemistry and the Allied Branches of Other Sciences, Tập 4 + 5 - https://books.google.com.vn/books?id=PshJAQAAMAAJ&hl=vi&source=gbs_navlinks_s. Truy cập 19 tháng 3 năm 2020.
Liên kết ngoài[sửa | sửa mã nguồn]
| Wikimedia Commons có thêm hình ảnh và phương tiện truyền tải về Platin. |
- Platinum (chemical element) tại Encyclopædia Britannica (tiếng Anh)
- Platin tại Từ điển bách khoa Việt Nam
- Platinum at The Periodic Table of Videos (University of Nottingham)
- Nuclides and Isotopes Lưu trữ 2011-02-02 tại Wayback Machine Fourteenth Edition: Chart of the Nuclides, General Electric Company, 1989.
- NIOSH Pocket Guide to Chemical Hazards – Platinum Centers for Disease Control and Prevention
- “The PGM Database”. Bản gốc lưu trữ ngày 1 tháng 7 năm 2019. Truy cập ngày 12 tháng 12 năm 2018.
- “A balanced historical account of the sequence of discoveries of platinum; illustrated”.
- “Johnson Matthey Technology Review: A free, quarterly journal of research exploring science and technology in industrial applications (formerly published as Platinum Metals Review)”. Bản gốc lưu trữ ngày 7 tháng 11 năm 2018. Truy cập ngày 12 tháng 12 năm 2018.
- “Platinum-Group Metals Statistics and Information”. United States Geological Survey.
- “International Platinum Group Metals Association”.
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | |||||||||||||||
| 1 | H | He | ||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | ||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | ||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |