Oxy
| Oxy, 8O | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 Oxy lỏng sôi (O2) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Quang phổ vạch Oxy | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tính chất chung | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tên, ký hiệu | Oxy, O | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hình dạng | Khí: không màu, trong suốt (ở thể O 3, khí màu xanh) xanh nhạt ở thể lỏng, phát ánh sáng tím ở thể plasma Lỏng và rắn: xanh nhạt | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxy trong bảng tuần hoàn | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Số nguyên tử (Z) | 8 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Khối lượng nguyên tử chuẩn (Ar) | 15,99903[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Phân loại | phi kim | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nhóm, phân lớp | 16, p | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chu kỳ | Chu kỳ 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cấu hình electron | [He] 2s2 2p4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
mỗi lớp | 2, 6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tính chất vật lý | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Màu sắc | Trong suốt, không màu O 2 (Xanh nhạt O 3) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Trạng thái vật chất | Thể khí | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nhiệt độ nóng chảy | (O 2) 54.36 K (-218,79 °C, -361,82 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nhiệt độ sôi | (O 2) 90,20 K (-182,95 °C, -297,31 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mật độ | 1,429 g·cm−3 (ở 0 °C, 101.325 kPa) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mật độ ở thể lỏng | ở nhiệt độ nóng chảy: 1,141 g·cm−3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Điểm ba | 154,59 K, 5,043 kPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nhiệt lượng nóng chảy | (O2) 0,444 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nhiệt bay hơi | (O2) 6,82 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nhiệt dung | (O2) 29,378 J·mol−1·K−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Áp suất hơi
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tính chất nguyên tử | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Trạng thái oxy hóa | 2, 1, 0, -1, -2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Độ âm điện | 3,44 (Thang Pauling) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Năng lượng ion hóa | Thứ nhất: 1313,9 kJ·mol−1 Thứ hai: 3388,3 kJ·mol−1 Thứ ba: 5300,5 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bán kính liên kết cộng hóa trị | 66±2 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bán kính van der Waals | 152 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Thông tin khác | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cấu trúc tinh thể | Lập phương | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vận tốc âm thanh | (thể khí, 27°C) 330 m·s−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Độ dẫn nhiệt | 26,58×10-3 W·m−1·K−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tính chất từ | Thuận từ[2] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Độ cảm từ (χmol) | +3449,0×10−6 cm3/mol (293 K)[3] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Số đăng ký CAS | 7782-44-7 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lịch sử | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Phát hiện | Michael Sendivogius Carl Wilhelm Scheele (1604, 1771) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Đặt tên chính bởi | Antoine Lavoisier (1777) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Đồng vị ổn định nhất | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bài chính: Đồng vị của Oxy | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Oxy (tiếng Anh: oxygen /ˈɒksɪdʒən/; bắt nguồn từ từ tiếng Pháp oxygène [ɔsiʒɛn][4]), hay dưỡng khí, là một nguyên tố hóa học có ký hiệu O và số hiệu nguyên tử 8. Nó là một thành viên của nhóm chalcogen trong bảng tuần hoàn, một phi kim phản ứng mạnh và là một chất oxy hóa dễ tạo oxide với hầu hết các nguyên tố cũng như với các hợp chất khác. Sau hydro và heli, oxy là nguyên tố phong phú thứ ba trong vũ trụ tính theo khối lượng.
Oxy là nguyên tố phi kim hoạt động rất mạnh. Nó có thể tạo thành hợp chất oxide với hầu hết các nguyên tố khác.[5] Ở điều kiện nhiệt độ và áp suất tiêu chuẩn hai nguyên tử oxy kết hợp với nhau tạo thành phân tử oxy không màu, không mùi, không vị có công thức là O
2. Khí oxy hóa lỏng ở nhiệt độ -183oC, màu xanh nhạt. Oxy phân tử (O2, thường được gọi là oxy tự do) trên Trái Đất là không ổn định về mặt nhiệt động lực học. Sự xuất hiện trong thời kỳ đầu tiên của nó trên Trái Đất là do các hoạt động quang hợp của vi khuẩn kỵ khí (vi khuẩn cổ và vi khuẩn). Sự phổ biến của nó từ sau đó đến ngày nay là do hoạt động quang hợp của tảo biển. Oxy là nguyên tố phổ biến xếp hàng thứ 3 trong vũ trụ theo khối lượng sau hydro và heli[6] và là nguyên tố phổ biến nhất theo khối lượng trong vỏ Trái Đất,[7] chiếm gần một nửa vỏ Trái đất ở dạng oxide.[8] Khí oxy chiếm 20,9% về thể tích trong không khí.[9]
Oxy phân tử cung cấp năng lượng được giải phóng trong quá trình đốt cháy [10] và hô hấp tế bào hiếu khí,[11] và nhiều lớp phân tử hữu cơ chính trong cơ thể sống chứa các nguyên tử oxy, chẳng hạn như protein, acid nucleic, carbohydrate và chất béo, cũng như thành phần chính vô cơ hợp chất của vỏ, răng và xương động vật. Phần lớn khối lượng của các sinh vật sống là oxy như một thành phần của nước, thành phần chính của các dạng sống. Oxy liên tục được bổ sung trong bầu khí quyển của Trái đất bằng quá trình quang hợp, sử dụng năng lượng của ánh sáng mặt trời để tạo ra oxy từ nước và carbon dioxide. Oxy quá phản ứng hóa học để vẫn là một phần tử tự do trong không khí mà không được bổ sung liên tục bởi hoạt động quang hợp của các sinh vật sống. Một dạng khác (dạng allotrope) của oxy, ozon (O
3) hấp thụ mạnh mẽ bức xạ tia cực tím UVB và tầng ozon ở độ cao giúp bảo vệ sinh quyển khỏi bức xạ cực tím. Tuy nhiên, ozon hiện diện trên bề mặt là sản phẩm phụ của khói và do đó là chất ô nhiễm.[12]
Oxy được Michael Sendivogius phân lập trước năm 1604, nhưng người ta thường tin rằng nguyên tố này được phát hiện độc lập bởi Carl Wilhelm Scheele, ở Uppsala, vào năm 1773 hoặc sớm hơn, và Joseph Priestley ở Wiltshire, vào năm 1774. Người ta thường ưu tiên cho Priestley vì tác phẩm của ông được xuất bản trước. Tuy nhiên, Priestley gọi oxy là "không khí khử khoáng chất" và không công nhận nó là một nguyên tố hóa học. Tên gọi oxy được đặt ra vào năm 1777 bởi Antoine Lavoisier, người đầu tiên công nhận oxy như một nguyên tố hóa học và mô tả chính xác vai trò của nó trong quá trình cháy.[13]
Các ứng dụng phổ biến của oxy bao gồm sản xuất thép, nhựa và hàng dệt, hàn và cắt thép và các kim loại khác, đẩy tên lửa, liệu pháp oxy và các hệ thống hỗ trợ sự sống trong máy bay, tàu ngầm, tàu vũ trụ và lặn dưới nước.
Lịch sử
Các thí nghiệm ban đầu
Một trong những thí nghiệm đầu tiên được biết về mối quan hệ giữa đốt cháy và không khí đã được thực hiện vào thế kỷ thứ 2 TCN. Tác giả người Hy Lạp về cơ học, Philo của Byzantium. Trong tác phẩm Pneumatica của mình, Philo đã quan sát thấy rằng việc đảo một ống nghiệm qua một ngọn nến đang cháy và bao quanh cổ của ống bằng nước dẫn đến một số nước dâng lên.[14] Philo phỏng đoán không chính xác rằng các phần của không khí trong ống đã được chuyển thành nguyên tố cổ điển lửa và do đó có thể thoát ra qua các lỗ của ống thủy tinh. Nhiều thế kỷ sau Leonardo da Vinci đã phát triển dựa trên công trình của Philo bằng cách quan sát rằng một phần không khí được tiêu thụ trong quá trình đốt cháy và hô hấp.[15]
Vào cuối thế kỷ 17, Robert Boyle đã chứng minh rằng không khí là cần thiết cho quá trình đốt cháy. Nhà hóa học người Anh John Mayow (1641-1679) đã tinh chỉnh công trình này bằng cách chỉ ra rằng lửa chỉ cần một phần không khí mà ông gọi là Spiritus nitroaereus. Trong một thí nghiệm, ông đã phát hiện ra rằng việc đặt một con chuột hoặc một ngọn nến sáng trong một hộp kín trên mặt nước đã khiến nước dâng lên và thay thế một phần mười bốn thể tích không khí trước khi dập tắt lửa.[16] Từ đó, ông phỏng đoán rằng oxygen được tiêu thụ trong cả hai quá trình hô hấp và đốt cháy.
Mayow quan sát thấy antimon sẽ tăng trọng lượng khi được đun nóng và suy ra rằng nitroaereus phải kết hợp với nó. Ông cũng cho rằng phổi tách nitroaereus khỏi không khí và truyền nó vào máu và nhiệt trong động vật và chuyển động cơ bắp là do phản ứng của nitroaereus với một số chất trong cơ thể. Các ghi chép về những suy xét này và các thí nghiệm và ý tưởng khác đã được xuất bản năm 1668 trong tác phẩm Tractatus của ông trong phần "Hô hấp".[16]
Lý thuyết phlogiston
Robert Hooke, Ole Borch, Mikhail Lomonosov và Pierre Bayen đều tạo ra oxy trong các thí nghiệm vào thế kỷ 17 và 18 nhưng không ai trong số họ công nhận nó là một nguyên tố hóa học.[17] Điều này có thể một phần là do sự phổ biến của học thuyết về đốt cháy và ăn mòn được gọi là lý thuyết phlogiston, khi đó là lời giải thích được ưa chuộng của các quá trình trên.[18]
Được nhà giả kim người Đức JJ Becher thành lập vào năm 1667, và được nhà hóa học Georg Ernst Stahl sửa đổi vào năm 1731,[19] lý thuyết phlogiston tuyên bố rằng tất cả các vật liệu dễ cháy được làm từ hai phần. Một phần, được gọi là phlogiston, đã bị loại bỏ khi chất chứa nó bị đốt cháy, trong khi phần không bị loại bỏ được cho là dạng thật của nó, với tên khác là calx.[15]
Các vật liệu dễ cháy mà để lại ít cặn, như gỗ hoặc than, được cho là được làm chủ yếu từ phlogiston; các chất không cháy mà có thể bị ăn mòn, như sắt, được cho là chứa rất ít phlogiston. Không khí không đóng một vai trò trong lý thuyết phlogiston, cũng không có bất kỳ thí nghiệm định lượng ban đầu nào được thực hiện để kiểm tra ý tưởng; thay vào đó, nó dựa trên các quan sát về những gì xảy ra khi một thứ gì đó cháy, rằng hầu hết các vật thể thông thường dường như trở nên nhẹ hơn và dường như mất đi thứ gì đó trong quá trình cháy.[15]
Khám phá

Nhà giả kim, nhà triết học và bác sĩ người Ba Lan Michael Sendivogius (Michał Sędziwój) trong tác phẩm của mình De Lapide Philosophorum Tractatus duodecim e naturae fonte et Manuali experientia depromti (1604) đã mô tả một chất có trong không khí.[20]), và chất này giống hệt với oxy.[21] Sendivogius, trong các thí nghiệm được thực hiện từ năm 1598 đến 1604, đã nhận ra một cách đúng đắn rằng chất này tương đương với sản phẩm phụ dạng khí được giải phóng do sự phân hủy nhiệt của kali nitrat. Theo quan điểm của Bugaj, sự cô lập oxy và sự liên kết thích hợp của chất này với phần không khí cần thiết cho sự sống, tạo ra đủ bằng chứng cho việc Sendivogius đã phát hiện ra oxy.[21] Tuy nhiên, phát hiện này của Sendivogius thường bị các thế hệ các nhà khoa học và nhà hóa học từ chối.[20]
Người ta cũng thường cho rằng oxy được phát hiện lần đầu tiên bởi dược sĩ Thụy Điển Carl Wilhelm Scheele. Ông đã tạo ra khí oxy bằng cách đun nóng oxide thủy ngân (HgO) và các nitrat khác nhau vào năm 1771–2.[15][22][23] Scheele gọi khí là "không khí lửa" vì khi đó nó là tác nhân duy nhất được biết đến để hỗ trợ quá trình đốt cháy. Ông đã viết một tường thuật về khám phá này trong một bản thảo có tựa đề Luận về không khí và lửa, mà ông đã gửi cho nhà xuất bản của mình vào năm 1775. Tài liệu đó được xuất bản năm 1777.[24]
Cùng lúc đó, vào ngày 1 tháng 8 năm 1774, một thí nghiệm do giáo sĩ người Anh Joseph Priestley tiến hành đã tập trung ánh sáng mặt trời vào oxide thủy ngân chứa trong một ống thủy tinh, nó giải phóng một loại khí mà ông đặt tên là "không khí khử chất độc".[23] Ông lưu ý rằng nến cháy sáng hơn trong khí và một con chuột hoạt động nhiều hơn và sống lâu hơn khi hít thở nó. Sau khi tự mình hít thở khí, Priestley viết: "Cảm giác của nó đối với phổi của tôi không khác nhiều so với không khí thông thường, nhưng tôi tưởng tượng rằng vú của tôi cảm thấy nhẹ và dễ dàng một cách kỳ lạ trong một thời gian sau đó." [17] Priestley công bố những phát hiện của mình vào năm 1775 trong một bài báo có tiêu đề "Ghi chép về những khám phá sâu hơn trong không khí", nằm trong tập thứ hai của cuốn sách của ông có tựa đề Thí nghiệm và quan sát về các loại không khí khác nhau.[15][25] Vì ông đã công bố những phát hiện của mình trước, nên Priestley thường được ưu tiên trong việc xác định ai khám phá ra oxy.
Nhà hóa học người Pháp Antoine Laurent Lavoisier sau đó tuyên bố đã phát hiện ra chất mới một cách độc lập. Priestley đến thăm Lavoisier vào tháng 10 năm 1774 và nói với anh ta về thí nghiệm của mình và cách anh ta giải phóng khí mới. Scheele cũng đã gửi một bức thư cho Lavoisier vào ngày 30 tháng 9 năm 1774, trong đó mô tả việc ông đã khám phá ra chất trước đây chưa từng được biết đến, nhưng Lavoisier không bao giờ thừa nhận đã nhận nó. (Một bản sao của bức thư được tìm thấy trong đồ đạc của Scheele sau khi ông qua đời.)[24]
Đóng góp của Lavoisier

Lavoisier đã tiến hành các thí nghiệm định lượng đầy đủ đầu tiên về quá trình oxy hóa và đưa ra lời giải thích chính xác đầu tiên về cách thức hoạt động của quá trình đốt cháy.[23] Ông đã sử dụng những thí nghiệm này và những thí nghiệm tương tự, tất cả đều bắt đầu vào năm 1774, để làm mất uy tín của thuyết phlogiston và để chứng minh rằng chất được phát hiện bởi Priestley và Scheele là một nguyên tố hóa học.
Trong một thí nghiệm, Lavoisier đã quan sát thấy rằng không có sự gia tăng tổng thể về trọng lượng khi thiếc và không khí được đốt nóng trong một thùng kín.[23] Ông lưu ý rằng không khí tràn vào khi ông mở thùng chứa, điều này cho thấy một phần không khí bị mắc kẹt đã được tiêu thụ. Ông cũng lưu ý rằng khối lượng thiếc đã tăng lên và sự gia tăng đó cũng giống như trọng lượng của không khí lao vào. Điều này và các thí nghiệm khác về quá trình đốt cháy đã được ông ghi lại trong cuốn sách Sur la combustion en général, được xuất bản năm 1777.[23] Trong công trình đó, ông đã chứng minh rằng không khí là hỗn hợp của hai chất khí; 'không khí quan trọng', cần thiết cho quá trình đốt cháy và hô hấp, và azote (Gk. ἄζωτον "vô hồn"), cũng không hỗ trợ. Azote sau đó trở thành nitơ trong tiếng Anh, mặc dù nó vẫn giữ tên trước đó trong tiếng Pháp và một số ngôn ngữ châu Âu khác.[23]
Lavoisier đổi tên 'không khí quan trọng' thành oxygène vào năm 1777 từ gốc Hy Lạp ὀξύς (oxys) (acid, theo nghĩa đen là "sắc", từ mùi vị của acid) và -γενής (-genēs) (người sản xuất, nghĩa đen là người sinh ra), bởi vì ông ấy đã nhầm tưởng rằng oxy là thành phần của tất cả các acid.[26] Các nhà hóa học (chẳng hạn như Sir Humphry Davy vào năm 1812) cuối cùng xác định rằng Lavoisier đã sai trong vấn đề này (hydro tạo cơ sở cho hóa học acid), nhưng khi đó cái tên này đã quá nổi tiếng.[27]
Oxygen đã đi vào ngôn ngữ tiếng Anh bất chấp sự phản đối của các nhà khoa học Anh và thực tế là Priestley người Anh đã đầu tiên cô lập chất khí này và viết về nó. Điều này một phần là do một bài thơ ca ngợi khí có tựa đề "Oxygen" trong cuốn sách nổi tiếng The Botanic Garden (1791) của Erasmus Darwin, ông nội của Charles Darwin.[24]
Lịch sử sau này

Giả thuyết nguyên tử ban đầu của John Dalton cho rằng tất cả các nguyên tố đều là nguyên tố cấu tạo và các nguyên tử trong các hợp chất thông thường sẽ có tỷ lệ nguyên tử đơn giản nhất so với nhau. Ví dụ, Dalton giả định rằng công thức của nước là HO, dẫn đến kết luận rằng khối lượng nguyên tử của oxy gấp 8 lần khối lượng của hydro, thay vì giá trị hiện đại là khoảng 16.[28] Năm 1805, Joseph Louis Gay-Lussac và Alexander von Humboldt đã chỉ ra rằng nước được tạo thành từ hai thể tích hydro và một thể tích oxy; và đến năm 1811 Amedeo Avogadro đã đưa ra cách giải thích chính xác về thành phần của nước, dựa trên cái mà ngày nay gọi là định luật Avogadro và các phân tử nguyên tố gồm hai nguyên tử trong các khí đó.[29] [a]
Vào cuối thế kỷ 19, các nhà khoa học nhận ra rằng không khí có thể được hóa lỏng và các thành phần của nó được cô lập bằng cách nén và làm mát nó. Sử dụng phương pháp phân tầng, nhà hóa học và vật lý người Thụy Sĩ Raoul Pierre Pictet đã làm bay hơi lưu huỳnh dioxide lỏng để hóa lỏng carbon dioxide, sau đó được làm bay hơi để làm lạnh khí oxy đủ để hóa lỏng nó. Ông đã gửi một bức điện vào ngày 22 tháng 12 năm 1877 cho Viện Hàn lâm Khoa học Pháp ở Paris thông báo về phát hiện của ông về oxy lỏng.[30] Chỉ hai ngày sau, nhà vật lý người Pháp Louis Paul Cailletet đã công bố phương pháp hóa lỏng oxy phân tử của riêng mình.[30] Chỉ một vài giọt chất lỏng được tạo ra trong mỗi trường hợp và không thể tiến hành phân tích có ý nghĩa. Oxy được hóa lỏng ở trạng thái ổn định lần đầu tiên vào ngày 29 tháng 3 năm 1883 bởi các nhà khoa học Ba Lan từ Đại học Jagiellonian, Zygmunt Wróblewski và Karol Olszewski.[31]

Năm 1891, nhà hóa học người Scotland James Dewar đã có thể sản xuất đủ oxy lỏng cho nghiên cứu.[32] Quy trình sản xuất oxy lỏng đầu tiên có tính khả thi về mặt thương mại được phát triển độc lập vào năm 1895 bởi kỹ sư người Đức Carl von Linde và kỹ sư người Anh William Hampson. Cả hai người đều hạ nhiệt độ của không khí cho đến khi nó hóa lỏng và sau đó chưng cất các khí thành phần bằng cách đun sôi từng chất một và thu giữ chúng riêng biệt.[33] Sau đó, vào năm 1901, hàn oxyacetylene lần đầu tiên được chứng minh bằng cách đốt cháy hỗn hợp acetylene và O
2 nén. Phương pháp hàn và cắt kim loại này sau đó trở nên phổ biến.[33]
Năm 1923, nhà khoa học người Mỹ Robert H. Goddard trở thành người đầu tiên phát triển động cơ tên lửa đốt nhiên liệu lỏng; động cơ sử dụng xăng để làm nhiên liệu và oxy lỏng làm chất oxy hóa. Goddard đã bay thành công một tên lửa nhỏ chạy bằng nhiên liệu lỏng 56 m ở 97 km/h vào ngày 16 tháng 3 năm 1926 tại Auburn, Massachusetts, Hoa Kỳ.[33][34]
Trong các phòng thí nghiệm hàn lâm, oxy có thể được điều chế bằng cách đun nóng kali chlorat trộn với một tỷ lệ nhỏ mangan đioxide.[35]
Mức độ oxy trong khí quyển đang có xu hướng giảm nhẹ trên toàn cầu, có thể do quá trình đốt cháy nhiên liệu hóa thạch.[36]
Đặc điểm
Cấu trúc

Ở nhiệt độ và áp suất tiêu chuẩn, oxy là chất khí không màu, không mùi, không vị, có công thức phân tử O
2, được gọi là dioxygen.[38][39]
Là dioxygen, hai nguyên tử oxy liên kết hóa học với nhau. Liên kết có thể được mô tả khác nhau dựa trên mức độ lý thuyết, nhưng được mô tả một cách hợp lý và đơn giản là một liên kết đôi cộng hóa trị là kết quả của việc lấp đầy các orbital phân tử được hình thành từ các orbital nguyên tử của các nguyên tử oxy riêng lẻ, việc lấp đầy chúng dẫn đến liên kết thứ tự của hai. Cụ thể hơn, liên kết đôi là kết quả của sự lấp đầy liên tục, năng lượng từ thấp đến cao, hay Aufbau, lấp đầy các orbital, và kết quả là sự hủy bỏ các đóng góp từ các electron 2s, sau khi lấp đầy liên tiếp các orbital σ và σ* thấp; Sự xen phủ σ của hai orbital nguyên tử 2p nằm dọc theo trục phân tử OO và sự xen phủ π của hai cặp orbital nguyên tử 2p vuông góc với trục phân tử OO, và sau đó loại bỏ sự đóng góp của hai trong số sáu electron 2p còn lại sau khi chúng lấp đầy một phần của các orbital π và π * thấp nhất.[37]
Sự kết hợp của hủy và σ và chồng chéo kết quả π trong nhân vật dioxy của đôi trái phiếu và độ phản ứng, và một bộ ba điện tử trạng thái cơ bản. Cấu hình electron có hai electron chưa ghép đôi, như được tìm thấy trong các orbital dioxygen (xem các orbital π * được điền đầy trong sơ đồ) có năng lượng bằng nhau - tức là suy biến - là cấu hình được gọi là trạng thái bộ ba spin. Do đó, trạng thái cơ bản của O
2 phân tử được gọi là oxy bộ ba.[40] [b] Các orbital có năng lượng cao nhất, được lấp đầy một phần là phản liên kết, và do đó sự lấp đầy của chúng làm suy yếu thứ tự liên kết từ ba thành hai. Do các điện tử chưa ghép đôi của nó, oxy bộ ba chỉ phản ứng chậm với hầu hết các phân tử hữu cơ có spin điện tử đã ghép đôi; điều này ngăn cản quá trình đốt cháy tự phát.[10]

Ở dạng bộ ba, O
2 phân tử đều thuận từ. Có nghĩa là, chúng truyền đặc tính từ cho oxy khi nó có mặt từ trường, do mômen từ spin của các electron chưa ghép đôi trong phân tử và năng lượng trao đổi âm giữa các phân tử O
2 lân cận.[32] Oxy lỏng có từ tính đến mức, trong các cuộc thử nghiệm trong phòng thí nghiệm, một cầu nối oxy lỏng có thể chống lại trọng lượng của chính nó giữa các cực của một nam châm mạnh.[41] [c]
Oxy đơn là tên được đặt cho một số loại phân tử O
2 có năng lượng cao hơn O
2 trong đó tất cả các spin điện tử đều được ghép đôi. Nó phản ứng nhiều hơn với các phân tử hữu cơ thông thường hơn là oxy phân tử. Trong tự nhiên, oxy đơn thường được hình thành từ nước trong quá trình quang hợp, sử dụng năng lượng của ánh sáng mặt trời.[42] Nó cũng được tạo ra trong tầng đối lưu bằng quá trình quang phân ozon bằng ánh sáng có bước sóng ngắn [43] và bởi hệ thống miễn dịch như một nguồn oxy hoạt tính.[44] Carotenoid trong các sinh vật quang hợp (và có thể cả động vật) đóng một vai trò chính trong việc hấp thụ năng lượng từ oxy đơn và chuyển nó về trạng thái cơ bản chưa được kích thích trước khi nó có thể gây hại cho các tế bào.[45]
Oxy mức 3 (không phải ozon, O
3) mà là trạng thái năng lượng cơ bản của phân tử O
2.[46] Cấu hình electron của phân tử này có 2 electron không tạo cặp mà tách ra riêng lẻ chiếm 2 orbital phân tử suy biến.[47] Các orbital này được xếp vào nhóm phản liên kết (làm suy giảm bậc liên kết từ 3 xuống còn 2), vì vậy liên kết oxy 2 nguyên tử yếu hơn liên kết 3 của 2 nguyên tử nitơ, theo đó tất cả các orbital nguyên tử liên kết đều được lấp đầy còn các orbital phản liên kết thì không đầy.[46]
Các dạng thù hình
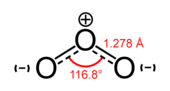
Dạng thù hình chung của nguyên tố oxy trên Trái đất được gọi là dioxygen, O
2, phần chính của oxy trong khí quyển của Trái đất. O2 có độ dài liên kết là 121 pm và năng lượng liên kết là 498 kJ / mol,[48] nhỏ hơn năng lượng của các liên kết đôi hoặc các cặp liên kết đơn khác trong sinh quyển và gây ra phản ứng tỏa nhiệt của O2 với bất kỳ phân tử hữu cơ nào.[10][49] Do hàm lượng năng lượng của nó, O2 được sử dụng bởi các dạng sống phức tạp, chẳng hạn như động vật, trong hô hấp tế bào. Các khía cạnh khác của O
2 được đề cập trong phần còn lại của bài viết này.
Trioxygen (O
3) thường được gọi là ozon và là một dạng phản ứng rất mạnh của oxy gây tổn hại đến mô phổi.[50] Ozon được tạo ra trong tầng khí quyển trên khi O
2 kết hợp với oxy nguyên tử được tạo ra bởi sự phân tách của O
2 bằng bức xạ tia cực tím (UV).[26] Do ozon hấp thụ mạnh trong vùng UV của quang phổ, nên tầng ozon của tầng trên khí quyển có chức năng như một lá chắn bức xạ bảo vệ hành tinh.[26] Gần bề mặt Trái đất, nó là một chất ô nhiễm được hình thành như một sản phẩm phụ của khí thải ô tô.[50] Ở độ cao quỹ đạo trái đất thấp, lượng oxy nguyên tử đủ để gây ra sự ăn mòn tàu vũ trụ.[51]
Các dạng phân tử oxozon O
4) được phát hiện vào năm 2001,[52][53] và được cho là tồn tại ở một trong sáu pha của oxy rắn. Năm 2006, nó đã được chứng minh rằng giai đoạn này, được tạo ra bằng cách điều áp O
2 đến 20 GPa, trên thực tế là một khối tứ diện O
8.[54] Cụm này có khả năng trở thành một chất oxy hóa mạnh hơn nhiều so với O
2 hoặc O
3 và do đó có thể được sử dụng trong nhiên liệu tên lửa.[52][53] Một pha kim loại được phát hiện vào năm 1990 khi oxy rắn chịu áp suất trên 96 GPa [55] và năm 1998 nó được chứng minh rằng ở nhiệt độ rất thấp, pha này trở thành siêu dẫn.[56]
Tính chất vật lý

Oxy hòa tan trong nước nhiều hơn so với nitơ; nước chứa khoảng một phân tử O
2 cho mỗi 2 phân tử N
2, so với tỉ số trong không khí là 1:4. Độ hòa tan của oxy trong nước phụ thuộc vào nhiệt độ, và ở 0 °C thì lượng hòa tan tăng gấp đôi (14,6 mg·L−1) so với ở 20 °C (7,6 mg·L−1).[57][58] Ở nhiệt động không khí 25 °C và 1 atm, nước ngọt chứa khoảng 6,04 mililit (mL) oxy trong một lít, trong khi đó, nước biển chứa khoảng 4,95 mL/L.[59] Ở 5 °C, độ hòa tan tăng đến 9,0 mL/L (tăng 50% so với ở 25 °C) trong nước ngọt và 7,2 mL/L (tăng hơn 45%) đối với nước biển.
Oxy ngưng tụ ở 90,20 K (−182.95 °C, −297.31 °F), và đóng băng ở 54,36 K (−218.79 °C, −361.82 °F).[60] Cả hai dạng lỏng và rắn O
2 là những chất trong suốt với màu xanh da trời nhạt do gây ra bởi sự hấp thụ ánh sáng đỏ (ngược lại với màu xanh da trời là do sự tán xạ Rayleigh của ánh sáng xanh). O
2 tinh khiết cao thường được chưng cất phân đoạn từ không khí lỏng;[61] Oxy lỏng cũng có thể được sản xuất từ sự ngưng tụ không khí bằng cách sử dụng chất làm lạnh là nitơ lỏng.
Oxy là một chất dễ phản ứng và phải được cất giữ cách xa các vật liệu dễ cháy.[62]
Quang phổ của oxy phân tử có liên quan đến các quá trình cực quang và phát sáng trong khí quyển.[63] Sự hấp thụ trong dải liên tục Herzberg và dải Schumann – Runge trong tia cực tím tạo ra oxy nguyên tử quan trọng trong hóa học của tầng giữa khí quyển.[64] Oxy phân tử đơn ở trạng thái bị kích thích chịu trách nhiệm cho sự phát quang hóa học màu đỏ trong dung dịch.[65]
Đồng vị và nguồn gốc sao

Oxy có mặt trong tự nhiên là hỗn hợp của 3 đồng vị bền gồm, 16O, 17O, và 18O, với 16O chiếm nhiều nhất (99,762%).[66]
Hầu hết 16O được tổng hợp ở giai đoạn cuối của quá trình phản ứng tổng hợp heli trong các sao lớn nhưng một số hình thành trong quá trình đốt cháy neon.[67] 17O chủ yếu được hình thanh trong quá trìn đốt cháy hydro thành heli trong chu trình CNO, do vậy nó là đồng vị phổ biến trong các đới đốt cháy hydro của các sao.[67] Hầu hết 18O được tạo ra khi 14N (hình thành phổ biến trong quá trình đốt cháy CNO) bắt các hạt nhân 4He, nên 18O phổ biến trong các đới giàu heli của quá trình tiến hóa sao lớn.[67]
14 đồng vị phóng xạ của oxy đã được xác định. Đồng vị bền nhất là 15O với chu kỳ bán rã 122,24 giây và 14O có chu kỳ bán rã 70,606 giây.[66] Tất cả các đồng vị phóng xạ còn là có chu kỳ bán rã dưới 27 s và phổ biến là dưới 83 milli giây.[66] Cơ chế phân rã phổ biến nhất của các đồng vị nhẹ hơn 16O là phân rã β+[68][69][70] để tạo ra nitơ, và cơ chế phân rã phổ biến nhất của các đồng vị nặng hơn 18O là phân rã beta để tạo ra fluor.[66]
Sự phổ biến
Oxy là nguyên tố hóa học phong phú nhất theo khối lượng trong sinh quyển, không khí, biển và đất liền của Trái Đất. Oxy là nguyên tố hóa học phong phú thứ ba trong vũ trụ, sau hydro và heli.[71] Khoảng 0,9% khối lượng của Mặt trời là oxy.[23] Oxy chiếm 49,2% khối lượng của vỏ Trái đất [72] như một phần của các hợp chất oxide như silic dioxide và là nguyên tố có nhiều nhất theo khối lượng trong vỏ Trái đất. Nó cũng là thành phần chính của các đại dương trên thế giới (88,8% khối lượng).[23] Khí oxy là thành phần phổ biến thứ hai của bầu khí quyển Trái đất, chiếm 20,8% thể tích và 23,1% khối lượng của nó (khoảng 10 15 tấn).[23][73] [d] Trái đất khác thường trong số các hành tinh của Hệ Mặt trời khi có nồng độ khí oxy cao như vậy trong bầu khí quyển của nó: Sao Hỏa (với 0,1% O
2 theo khối lượng) và sao Kim có ít hơn nhiều. Lượng O
2 xung quanh những hành tinh đó chỉ được tạo ra bởi tác động của bức xạ tia cực tím lên các phân tử chứa oxy như carbon dioxide.

2hơn.
Nồng độ khí oxy cao bất thường trên Trái Đất là kết quả của chu trình oxy. Chu trình sinh địa hóa này mô tả sự di chuyển của oxy bên trong và giữa ba hồ chứa chính của nó trên Trái đất: khí quyển, sinh quyển và thạch quyển. Yếu tố thúc đẩy chính của chu trình oxy là quang hợp, nguyên nhân tạo nên bầu khí quyển của Trái đất hiện đại. Quá trình quang hợp giải phóng oxy vào khí quyển, trong khi quá trình hô hấp, phân hủy và đốt cháy loại bỏ nó khỏi khí quyển. Ở trạng thái cân bằng hiện tại, sản xuất và tiêu dùng oxy diễn ra với tốc độ như nhau.[27]
Oxy tự do cũng xuất hiện trong dung dịch trong các thủy vực trên thế giới. Sự hòa tan tăng dần của O
2 ở nhiệt độ thấp hơn (xem Đặc tính vật lý) có ý nghĩa quan trọng đối với sự sống của đại dương, vì các đại dương ở vùng cực có mật độ sự sống cao hơn nhiều do hàm lượng oxy cao hơn.[74] Nước bị ô nhiễm bởi các chất dinh dưỡng thực vật như nitrat hoặc phosphat có thể kích thích sự phát triển của tảo bằng một quá trình gọi là hiện tượng phú dưỡng và sự phân hủy của các sinh vật này và các vật liệu sinh học khác có thể làm giảm O
2 nội dung trong thủy vực phú dưỡng. Các nhà khoa học đánh giá khía cạnh này của chất lượng nước bằng cách đo nhu cầu oxy sinh hóa của nước, hoặc lượng O
2 cần thiết để khôi phục nó về nồng độ bình thường.[75]
Phân tích

Các nhà cổ sinh vật học đo tỷ lệ oxy-18 và oxy-16 trong vỏ và xương của các sinh vật biển để xác định khí hậu hàng triệu năm trước (xem chu kỳ tỷ lệ đồng vị oxy). Các phân tử nước biển có chứa đồng vị nhẹ hơn, oxy-16, bay hơi với tốc độ nhanh hơn một chút so với các phân tử nước có chứa 12% oxy-18 nặng hơn, và sự chênh lệch này tăng lên ở nhiệt độ thấp hơn.[76] Trong thời gian nhiệt độ toàn cầu thấp hơn, tuyết và mưa từ đó nước bốc hơi có xu hướng cao hơn ở oxy-16, và nước biển bị bỏ lại có xu hướng cao hơn ở oxy-18. Các sinh vật biển sau đó kết hợp nhiều oxy-18 vào bộ xương và vỏ của chúng hơn là khi chúng ở trong môi trường khí hậu ấm hơn.[76] Các nhà cổ sinh vật học cũng trực tiếp đo tỷ lệ này trong phân tử nước của các mẫu lõi băng có tuổi đời hàng trăm nghìn năm.
Vai trò sinh học
Quang hợp và hô hấp

2 tự do và cố định CO
2 thành đường theo chu trình Calvin.
Trong tự nhiên, oxy tự do được sinh ra từ việc phân giải nước trong quá trình quang hợp oxy dưới tác động của ánh sáng. Theo một vài ước tính, tảo lục và cyanobacteria trong các môi trường biển cung cấp khoảng 70% oxy tự do được tạo ra trên Trái Đất và phần còn lại là từ thực vật trên đất liền.[77] Các tính toán khác về sự đóng góp từ đại dương vào oxy trong khí quyển cao hơn, trong khi một vài ước tính thì thấp hơn, đề xuất rằng các đại dương tạo ra khoảng 45% oxy trong khí quyển mỗi năm.[78]
Công thức tính đơn giản từ quá trình quang hợp là:[79]
- 6 CO2 + 6 H
2O + photon → C
6H
12O
6 + 6 O
2
- 6 CO2 + 6 H
Tiến hóa oxy Photolytic xảy ra trong màng thylakoid của các sinh vật quang hợp và cần năng lượng của 4 photon.[e] Mặc dù trải qua nhiều công đoạn, nhưng kết quả là tạo thành sự chênh lệch proton qua màng thylakoid, nó được sử dụng để tổng hợp ATP qua photophosphoryl hóa.[80] Phân tử O
2 còn lại sau khi oxy hóa phân tử nước được giải phóng vào khí quyển.[f]
Phân tử O
2 là cần thiết cho việc hô hấp của tế bào trong tất cả các sinh vật hiếu khí. Oxy được sử dụng trong mitochondria để giúp tạo ra adenosine triphosphate (ATP) trong quá trình phosphoryl hóa oxy hóa. Phản ứng của hô hấp hiếu khí là quá trình ngược lại với quang hợp::
- C
6H
12O
6 + 6 O
2 → 6 CO2 + 6 H
2O + 2880 kJ·mol−1
- C
Ở động vật có xương sống, O
2 khuếch tán qua các màng trong phổi và đi vào các tế bào máu đỏ. Hemoglobin kết hợp với O
2, làm thay đổi màu sắc của nó từ đỏ thẩm sang đỏ tươi[81] (CO
2 được giải phóng từ phần khác của hemoglobin tua hiệu ứng Bohr). Các động vật khác sử dụng hemocyanin (Mollusca và một số arthropoda) hoặc hemerythrin (nhện và tôm hùm).[82] Một lít máu có thể hòa tan 200 cm³ O
2.[82]
Các loại oxy phản ứng như ion superoxide (O−
2) và hydrogen peroxide (H
2O
2), là các sản phẩm phụ nguy hiểm của oxy sử dụng trong sinh vật.[82] Tuy nhiên, các bộ phận của hệ miễn dịch của các sinh vật bậc cao, tạo ra peroxide, superoxide, và oxy nguyên tử để phá hủy các vi sinh vật xâm nhập. Loại oxy phản ứng cũng có vai trò quan trọng trong phản ứng siêu nhạy cảm của thực vật chống lại các tác nhân gây bệnh.[80]
Một người trưởng thành hít 1,8-2,4 gam chất oxy mỗi phút.[83] Lượng này tương đương 6 triệu tấn oxy được hít vào do con người mỗi năm.[g]
Hàm lượng trong cơ thể
| Đơn vị | Áp suất khí phế nang phổi |
Oxy động mạch | Khí máu tĩnh mạch |
|---|---|---|---|
| kPa | 14,2 | 11[84]-13[84] | 4.0[84]-5.3[84] |
| mmHg | 107 | 75[85]-100[85] | 30[86]-40[86] |
Áp suất riêng phần của oxy tự do trong cơ thể của động vật có xương sống còn sống là cao nhất trong hệ hô hấp, và giảm dọc theo hệ động mạch, mô ngoại vi và hệ tĩnh mạch..[87]
Tạo nên khí quyển

2 tạo nên khí quyển Trái Đất: 1) O
2 không được tạo ra; 2) O
2 được tạo ra, nhưng bị hấp thụ trong đại dương và đá dưới đáy biển; 3) O
2 bắt đầu hình thành ở dạng khí thoát ra khỏi đại dương, nhưng được hấp thụ trong các bề mặt đất và hình thành tầng ozon; 4–5) O
2 lắng đọng dưới biển đầy và tích tục ở dạng khí trong khí quyển
Khí oxy tự do hầu như không tồn tại trong khí quyển Trái Đất trước khi archaea và vi khuẩn tiến hóa, có lẽ vào khoảng 3,5 tỉ năm trước. Oxy tự do xuất hiện đầu tiên với một lượng lớn trong suốt đại cổ sinh (giữa 3,0 và 2,3 tỉ năm trước).[88] Trong 1 tỉ năm đầu, bất kỳ dạng oxy tự do được sinh ra từ các sinh vật này đã kết hợp với sắt hòa tan trong các đại dương để hình thành nên các tầng sắt tạo dãi. Khi oxy này chìm xuống trở nên bão hòa, oxy tự do bắt đầu thoát ra ở dạng khí từ các đại dương cách nay 3–2,7 tỉ năm, đạt đến 10% với mức như hiện nay vào khoảng 1,7 tỉ năm trước.[88][89]
Sự có mặt của một lượng lớn oxy hòa tan và oxy tự do trong các đại dương và trong khí quyển có thể đã thúc đẩy các sinh vật yếm khí đang sống đến bờ vực tuyệt chủng trong suốt thảm họa Oxy cách nay khoảng 2,4 tỉ năm. Tuy nhiên, việc hô hấp của tế bào sử dụng O
2 cho phép các sinh vật hiếu khí tạo ra nhiều ATP hơn sinh vật yếm khí, giúp cho sinh vật hiếu khí chiếm phần lớn trong sinh quyển Trái Đất.[90]
Từ khi bắt đầu kỷ Cambri cách nay 540 triệu năm, hàm O
2 dao động trong khoảng 15% và 30% theo thể tích.[91] Càng về cuối kỷ Cacbon (300 triệu năm trước) mức O
2 khí quyển đạt đến giá trị lớn nhất chiếm 35% thể tích,[91] điều này đã góp phần làm cho côn trùng và lưỡng cư có kích thước lớn vào thời điểm đó.[92] Hoạt động của con người như đốt 7 tỉ tấn nhiên liệu hóa thạch mỗi năm đã có ảnh hưởng rất ít đến hàm lượng oxy tự do trong khí quyển.[93] Với tốc độ quang hợp hiện nay, có thể sẽ mất khoảng 2.000 năm để tạo ra toàn bộ O
2 trong khí quyển hiện tại.[94]
Ứng dụng
Oxy được sử dụng làm chất oxy hóa, chỉ có fluor có độ âm điện cao hơn nó. Oxy lỏng được sử dụng làm chất oxy hóa trong tên lửa đẩy. Oxy là chất duy trì sự hô hấp, vì thế việc cung cấp bổ sung oxy được thấy rộng rãi trong y tế. Những người leo núi hoặc đi trên máy bay đôi khi cũng được cung cấp bổ sung oxy. Oxy được sử dụng trong công nghệ hàn cũng như trong sản xuất thép và rượu methanol.
Oxy, như là một chất kích thích nhẹ, có lịch sử trong việc sử dụng trong giải trí mà hiện nay vẫn còn sử dụng. Các cột chứa oxy có thể nhìn thấy trong các buổi lễ hội ngày nay. Trong thế kỷ XIX, oxy thường được trộn với nitơ oxide để làm các thuốc giảm đau.
Hợp chất
Vì độ âm điện cao của nó, oxy tạo thành các liên kết hóa học với phần lớn các nguyên tố khác (đây chính là nguồn gốc của định nghĩa nguyên thủy của từ oxy hóa). Các nguyên tố duy nhất có thể tránh không bị oxy hóa chỉ là một số khí trơ. Phổ biến nhất trong số các oxide tất nhiên là hydro oxide, hay nước (H2O). Các chất khác cũng được nhắc đến nhiều là hợp chất của carbon và oxy, như carbon dioxide (CO2), các chất như rượu (R-OH), aldehyde (R-CHO), và acid carboxylic (R-COOH). Các gốc oxy hóa như chlorat (ClO3−), perchlorat (ClO4−), chromat (CrO42−), dichromat (Cr2O72−), permanganat (MnO4−), và nitrat (NO3−) là những chất oxy hóa rất mạnh. Rất nhiều kim loại như sắt chẳng hạn liên kết với các nguyên tử oxy, tạo thành oxide sắt (III) (Fe2O3). Ozon (O3) được tạo thành trong quá trình phóng tĩnh điện với sự có mặt của oxy phân tử. Oxy phân tử đôi (O2)2 hiện nay đã biết và tìm thấy như là một phần nhỏ trong oxy lỏng. Các êpoxide là các ête trong đó nguyên tử oxy là một phần của vòng gồm ba nguyên tử.
Phòng ngừa
Oxy có thể là một chất độc khi nó có áp suất thành phần được nâng cao. Để dễ hiểu có thể giải thích nôm na là thông thường oxy chiếm khoảng 21% thể tích của không khí. Nếu có thể tăng lượng oxy này lên thành 50% thì không khí khi đó sẽ không tốt cho sự hô hấp.
Một vài dẫn xuất của oxy, như ozon (O3), hydro peroxide H2O2 (nước oxy già), các gốc hiđroxyl và superoxide, cũng là những chất độc mạnh. Cơ thể động vật nói chung và con người nói riêng có cơ chế để tự bảo vệ chống lại các chất độc này. Ví dụ, glutathion có nguồn gốc tự nhiên có thể phản ứng như một chất chống oxy hóa, cũng giống như bilirubin là chất tách ra được từ hemoglobin. Các nguồn có chứa nhiều oxy xúc tiến sự cháy nhanh và vì vậy là vật nguy hiểm về cháy nổ với sự có mặt của các nhiên liệu. Điều này cũng đúng với các hợp chất của oxy như chlorat, perchlorat, dichromat, v.v. Các hợp chất với khả năng oxy hóa cao thông thường có thể gây ra bỏng hóa học.
Đám cháy đã giết chết phi hành đoàn của tàu Apollo 1 trong khi phóng thử, đã lan quá nhanh vì áp suất của oxy nguyên chất được sử dụng khi đó là bằng áp suất khí quyển bình thường thay vì chỉ là một phần ba lẽ ra được sử dụng cho phóng thật. (Xem thêm áp suất thành phần.)
Điều chế
Trong phòng thí nghiệm
Trong phòng thí nghiệm, O2 được điều chế bằng cách phân hủy những hợp chất giàu oxy và ít bền đối với nhiệt như KMnO4(rắn) hay KClO3 (rắn)[95]
Ví dụ:
2KMnO4 → K2MnO4 + MnO2 + O2
6CO2 + 6H2O → C6H12O6 + 6O2
2KClO3 → 2KCl + 3O2
2H2O2 → 2H2O + O2
2H2O → 2H2 + O2
Ag2O + H2O2 → 2Ag + H2O + O2
2KI + O3 + H2O → I2 + 2KOH + O2
5H2O2 + 2KMnO4 + 3H2SO4 → 2MnSO4 + 5O2 + K2SO4 + 8H2O
Trong công nghiệp
Hai phương pháp chính được ứng dụng để sản xuất 100 triệu tấn O
2 từ không khí dùng cho công nghiệp hàng năm.[96] Phương pháp phổ biến nhất là chưng cất phân đoạn không khí lỏng thành nhiều thành phần khác nhau như N
2 ở dạng hơi trong khi O
2 thì ở dạng lỏng.[96]

Phương pháp thứ hai sản xuất khí O
2 liên quan đến dòng khí khô, sạch đi qua một cặp sàng phân tử giống nhau, chúng hấp thụ nitơ và giải phóng một dòng khí có từ 90% đến 93% O
2.[96] Đồng thời khí nitơ được giải phóng khỏi lớp zeolit bão hòa nitơ bằng cách giảm áp suất vận hành của bồng và chuyển một phần khí oxy từ lớp sản xuất đi qua nó, theo chiều dòng ngược lại. Sau một thời gian thiết lập chu kỳ hoạt động, sự vật hành của hai lớp được thay đổi cho nhau, từ đó cho phép cung cấp liên tục khí oxy, được bơn qua đường ống. Khí oxy thu được càng tăng bằng các công nghệ làm lạnh.[97]
Khí oxy cũng có thể được tạo ra qua quá trình điện phân nước thành phân tử oxy và hydro. Phải dùng dòng điện một chiều, vì nếu dùng dòng hai chiều, khi các khí sinh ra ở một cực sẽ giải phóng đồng thời hydro và oxy, nếu đạt đến tỷ lệ 2:1 sẽ gây nổ. Trái với quan điểm phổ biến, tỉ lệ 2:1 được quan sát trong điện phân dòng điện một chiều của nước acid hóa không chứng minh rằng công thức hóa học thực tế của nước là H2O trừ khi giả định nào đó được thực hiện về công thức phân tử của chính hydro và oxy. Phương pháp tương tự là nung các oxide và ôxoacid có xúc tác của dòng điện để tạo O
2. Các chất xúc tác hóa học cũng có thể được dùng như máy tạo oxy hóa học hay oxygen candle là các chất được dùng một phần trong việc hỗ trợ sự sống được trang bị trong các tàu ngầm, và vẫn là một phần của thiết bị chuẩn trên các chuyến bay thương mại trong trường hợp khẩn khi áp suất trong khoang máy bay giảm. Một công nghệ tách khí khác liên quan đến việc làm cho khí hòa tan vào các màng sứ dự trên zirconi dioxide bằng cách hoặc tạo áp suất cao hoặc dùng dòng điện để tạo ra khí O
2 gần như tinh khiết.[98]
Với số lượng lớn, giá của oxy lỏng năm 2001 vào khoảng 0,21USD/kg.[99] Vì chi phí cơ bản trong sản xuất chủ yếu là chi phí năng lượng để hóa lỏng khí, nên chi phí sản xuất sẽ thay đổi theo chi phí năng lượng.
Vì các lý do kinh tế, oxy thường được vận chuyển trong các bồn ở dạng lỏng đặc biệt các xe bồn cách nhiệt đặc biệt, do một lít oxy lỏng bằng với 840 lít khí oxy ở áp suất khí quyển và nhiệt độ 20 °C (68 °F).[96] Các xe bồn như thế này được dùng để nạp lại oxy lỏng, đặt nằm ngoài các bệnh viện và các việc khác cần sử dụng một lượng lớn oxy tinh khiết. Oxy lỏng được đi qua bộ trao đổi nhiệt để chuyển dạng lỏng đông lạnh thành khí trước khi đi vào tòa nhà. Oxy cũng được chứa trong các bình hình trụ tròn nhỏ hơn ở dạng khí nén; một dạng chứa hữu ích trong các ứng dụng y khoa gọn nhẹ dễ vận chuyển và trong việc cắt-hàn nguyên liệu/xì hàn.[96]
Xem thêm
- Phương pháp Winkler cho oxy hòa tan để xác định lượng oxy hòa tan trong nước sạch
- Sự cháy
- Oxy hóa
Chú thích
- ^ Những kết quả này hầu như bị bỏ qua cho đến năm 1860. Một phần của sự bác bỏ này là do niềm tin rằng các nguyên tử của một nguyên tố sẽ không có ái lực hóa học đối với các nguyên tử của cùng một nguyên tố, và một phần là do những ngoại lệ rõ ràng đối với định luật Avogadro mà mãi sau này mới được giải thích về sự phân ly của các phân tử.
- ^ An orbital is a concept from quantum mechanics that models an electron as a wave-like particle that has a spatial distribution about an atom or molecule.
- ^ Oxygen's paramagnetism can be used analytically in paramagnetic oxygen gas analysers that determine the purity of gaseous oxygen. (“Company literature of Oxygen analyzers (triplet)”. Servomex. Bản gốc lưu trữ ngày 8 tháng 3 năm 2008. Truy cập ngày 15 tháng 12 năm 2007.)
- ^ Figures given are for values up to 80 km (50 mi) above the surface
- ^ Các màng thylakoid là một phần của chloroplast trong tảo và thực thực vật trong khi chúng đon giản là một trong nhiều cấu trúc màng ở cyanobacteria. Thực tế, chloroplast được cho là đã tiến hóa từ cyanobacteria từng là đối tác cộng sinh với các yếu tố tiền phát sinh của thực vật và tảo.
- ^ Water oxidation is catalyzed by a manganese-containing enzyme complex known as the oxygen evolving complex (OEC) or water-splitting complex found associated with the lumenal side of thylakoid membranes. Manganese is an important cofactor, and calci và chloride are also required for the reaction to occur.(Raven 2005)
- ^ (1.8 grams/min/person)×(60 min/h)×(24 h/day)×(365 days/year)×(6.6 billion people)/1,000,000 g/t=6.24 billion tonnes
Tham khảo
- ^ “Trọng lượng nguyên tử tiêu chuẩn: Oxy”.CIAAW.2009
- ^ Magnetic susceptibility of the elements and inorganic compounds Lưu trữ 2011-03-03 tại Wayback Machine, in Handbook of Chemistry and Physics 81st edition, CRC press.
- ^ Weast, Robert (1984). CRC, Handbook of Chemistry and Physics. Boca Raton, Florida: Chemical Rubber Company Publishing. tr. E110. ISBN 0-8493-0464-4.
- ^ Đặng Thái Minh, "Dictionnaire vietnamien - français. Les mots vietnamiens d’origine française", Synergies Pays riverains du Mékong, n° spécial, năm 2011. ISSN: 2107-6758. Trang 163.
- ^ “WebElements: the periodic table on the web – Oxygen: electronegativities”. WebElements.com. Truy cập ngày 7 tháng 11 năm 2011.
- ^ Emsley 2001, tr.297
- ^ “Oxygen”. Los Alamos National Laboratory. Bản gốc lưu trữ ngày 26 tháng 10 năm 2007. Truy cập ngày 16 tháng 12 năm 2007.
- ^ Atkins, P.; Jones, L.; Laverman, L. (2016).Chemical Principles, 7th edition. Freeman. ISBN 978-1-4641-8395-9
- ^ Cook & Lauer 1968, p.500
- ^ a b c Weiss, H. M. (2008). “Appreciating Oxygen”. J. Chem. Educ. 85 (9): 1218–1219. Bibcode:2008JChEd..85.1218W. doi:10.1021/ed085p1218.
- ^ Schmidt-Rohr, K. (2020). "Oxygen Is the High-Energy Molecule Powering Complex Multicellular Life: Fundamental Corrections to Traditional Bioenergetics" ACS Omega 5: 2221-2233. http://dx.doi.org/10.1021/acsomega.9b03352
- ^ “Atomic oxygen erosion”. Bản gốc lưu trữ ngày 13 tháng 6 năm 2007. Truy cập ngày 8 tháng 8 năm 2009.
- ^ G. D. Parks & Mellor, J. W. (1939). Mellor's Modern Inorganic Chemistry (ấn bản 6). London: Longmans, Green and Co.Quản lý CS1: sử dụng tham số tác giả (liên kết)
- ^ Jastrow, Joseph (1936). Story of Human Error. Ayer Publishing. tr. 171. ISBN 978-0-8369-0568-7.
- ^ a b c d e Cook & Lauer 1968, p.499.
- ^ a b World of Chemistry contributors (2005). “John Mayow”. World of Chemistry. Thomson Gale. ISBN 978-0-669-32727-4. Truy cập ngày 16 tháng 12 năm 2007.
- ^ a b Emsley 2001, p.299
- ^ Best, Nicholas W. (2015). “Lavoisier's 'Reflections on Phlogiston' I: Against Phlogiston Theory”. Foundations of Chemistry. 17 (2): 137–151. doi:10.1007/s10698-015-9220-5.
- ^ Morris, Richard (2003). The last sorcerers: The path from alchemy to the periodic table. Washington, D.C.: Joseph Henry Press. ISBN 978-0-309-08905-0.
- ^ a b Marples, Frater James A. “Michael Sendivogius, Rosicrucian, and Father Of Studies of Oxygen” (PDF). Societas Rosicruciana in Civitatibus Foederatis, Nebraska College. tr. 3–4. Truy cập ngày 25 tháng 5 năm 2018.
- ^ a b Bugaj, Roman (1971). “Michał Sędziwój – Traktat o Kamieniu Filozoficznym”. Biblioteka Problemów (bằng tiếng Ba Lan). 164: 83–84. ISSN 0137-5032.
- ^ “Oxygen”. RSC.org. Truy cập ngày 12 tháng 12 năm 2016.
- ^ a b c d e f g h i Cook & Lauer 1968, p. 500
- ^ a b c Emsley 2001, p. 300
- ^ Priestley, Joseph (1775). “An Account of Further Discoveries in Air”. Philosophical Transactions. 65: 384–94. doi:10.1098/rstl.1775.0039.
- ^ a b c Parks, G. D.; Mellor, J. W. (1939). Mellor's Modern Inorganic Chemistry (ấn bản 6). London: Longmans, Green and Co.
- ^ a b Greenwood, Norman N.; Earnshaw, A. (1997), Chemistry of the Elements (ấn bản 2), Oxford: Butterworth-Heinemann, ISBN 0-7506-3365-4
- ^ DeTurck, Dennis; Gladney, Larry; Pietrovito, Anthony (1997). “Do We Take Atoms for Granted?”. The Interactive Textbook of PFP96. University of Pennsylvania. Bản gốc lưu trữ ngày 17 tháng 1 năm 2008. Truy cập ngày 28 tháng 1 năm 2008.
- ^ Roscoe, Henry Enfield; Schorlemmer, Carl (1883). A Treatise on Chemistry. D. Appleton and Co. tr. 38.
- ^ a b Daintith, John (1994). Biographical Encyclopedia of Scientists. CRC Press. tr. 707. ISBN 978-0-7503-0287-6.
- ^ Papanelopoulou, Faidra (2013). “Louis Paul Cailletet: The liquefaction of oxygen and the emergence of low-temperature research”. Notes and Records of the Royal Society of London. 67 (4): 355–73. doi:10.1098/rsnr.2013.0047. PMC 3826198.
- ^ a b Emsley 2001, p.303
- ^ a b c How Products are Made contributors (2002). “Oxygen”. How Products are Made. The Gale Group, Inc. Truy cập ngày 16 tháng 12 năm 2007.
- ^ “Goddard-1926”. NASA. Bản gốc lưu trữ ngày 8 tháng 11 năm 2007. Truy cập ngày 18 tháng 11 năm 2007.
- ^ Flecker, Oriel Joyce (1924). A school chemistry. MIT Libraries. Oxford, Clarendon press. tr. 30.
- ^ Scripps Institute. “Atmospheric Oxygen Research”.
- ^ a b Jack Barrett, 2002, "Atomic Structure and Periodicity, (Basic concepts in chemistry, Vol. 9 of Tutorial chemistry texts), Cambridge, U.K.:Royal Society of Chemistry, p. 153, ISBN 0854046577, see accessed ngày 31 tháng 1 năm 2015.
- ^ “Oxygen Facts”. Science Kids. ngày 6 tháng 2 năm 2015. Truy cập ngày 14 tháng 11 năm 2015.
- ^ Pauling, L. (1960). The nature of the chemical bond and the structure of molecules and crystals: an introduction to modern structural chemistry (ấn bản 3). Ithaca, N.Y.: Cornell University Press.
- ^ Jakubowski, Henry. “Chapter 8: Oxidation-Phosphorylation, the Chemistry of Di-Oxygen”. Biochemistry Online. Saint John's University. Truy cập ngày 28 tháng 1 năm 2008.
- ^ “Demonstration of a bridge of liquid oxygen supported against its own weight between the poles of a powerful magnet”. University of Wisconsin-Madison Chemistry Department Demonstration lab. Bản gốc lưu trữ ngày 17 tháng 12 năm 2007. Truy cập ngày 15 tháng 12 năm 2007.
- ^ Krieger-Liszkay, Anja (ngày 13 tháng 10 năm 2004). “Singlet oxygen production in photosynthesis”. Journal of Experimental Botany. 56 (411): 337–46. doi:10.1093/jxb/erh237. PMID 15310815.
- ^ Harrison, Roy M. (1990). Pollution: Causes, Effects & Control (ấn bản 2). Cambridge: Royal Society of Chemistry. ISBN 978-0-85186-283-5.
- ^ Wentworth, Paul; McDunn, J. E.; Wentworth, A. D.; Takeuchi, C.; Nieva, J.; Jones, T.; Bautista, C.; Ruedi, J. M.; và đồng nghiệp (ngày 13 tháng 12 năm 2002). “Evidence for Antibody-Catalyzed Ozone Formation in Bacterial Killing and Inflammation”. Science. 298 (5601): 2195–219. Bibcode:2002Sci...298.2195W. doi:10.1126/science.1077642. PMID 12434011.
- ^ Hirayama, Osamu; Nakamura, Kyoko; Hamada, Syoko; Kobayasi, Yoko (1994). “Singlet oxygen quenching ability of naturally occurring carotenoids”. Lipids. 29 (2): 149–50. doi:10.1007/BF02537155. PMID 8152349.
- ^ a b Jakubowski, Henry. “Biochemistry Online”. Saint John's University. Truy cập ngày 28 tháng 1 năm 2008.
|chapter=bị bỏ qua (trợ giúp) - ^ Orbital là một khái niệm của cơ học lượng tử lập mô hình một electron như là một hạt tựa như sóng có phân bố không gian xung quanh một nguyên tử hay một phân tử.
- ^ Chieh, Chung. “Bond Lengths and Energies”. University of Waterloo. Bản gốc lưu trữ ngày 14 tháng 12 năm 2007. Truy cập ngày 16 tháng 12 năm 2007.
- ^ Schmidt-Rohr, K. (2015). “Why Combustions Are Always Exothermic, Yielding About 418 kJ per Mole of O2”. J. Chem. Educ. 92 (12): 2094–2099. Bibcode:2015JChEd..92.2094S. doi:10.1021/acs.jchemed.5b00333.
- ^ a b Stwertka, Albert (1998). Guide to the Elements . Oxford University Press. tr. 48–49. ISBN 978-0-19-508083-4.
- ^ “Atomic oxygen erosion”. Bản gốc lưu trữ ngày 13 tháng 6 năm 2007. Truy cập ngày 8 tháng 8 năm 2009.
- ^ a b Cacace, Fulvio; de Petris, Giulia; Troiani, Anna (2001). “Experimental Detection of Tetraoxygen”. Angewandte Chemie International Edition. 40 (21): 4062–65. doi:10.1002/1521-3773(20011105)40:21<4062::AID-ANIE4062>3.0.CO;2-X. PMID 12404493.
- ^ a b Ball, Phillip (ngày 16 tháng 9 năm 2001). “New form of oxygen found”. Nature News. Truy cập ngày 9 tháng 1 năm 2008.
- ^ Lundegaard, Lars F.; Weck, Gunnar; McMahon, Malcolm I.; Desgreniers, Serge; và đồng nghiệp (2006). “Observation of anO
8 molecular lattice in the phase of solid oxygen”. Nature. 443 (7108): 201–04. Bibcode:2006Natur.443..201L. doi:10.1038/nature05174. PMID 16971946. - ^ Desgreniers, S.; Vohra, Y. K.; Ruoff, A. L. (1990). “Optical response of very high density solid oxygen to 132 GPa”. J. Phys. Chem. 94 (3): 1117–22. doi:10.1021/j100366a020.
- ^ Shimizu, K.; Suhara, K.; Ikumo, M.; Eremets, M. I.; và đồng nghiệp (1998). “Superconductivity in oxygen”. Nature. 393 (6687): 767–69. Bibcode:1998Natur.393..767S. doi:10.1038/31656.
- ^ Emsley 2001, p.299
- ^ “Air solubility in water”. The Engineering Toolbox. Truy cập ngày 21 tháng 12 năm 2007.
- ^ David Hudson Evans & Claiborne, James B. (2006). The Physiology of Fishes. CRC Press. tr. 88. ISBN 0849320224.Quản lý CS1: sử dụng tham số tác giả (liên kết)
- ^ Lide, David R. (2003). “Section 4, Properties of the Elements and Inorganic Compounds; Melting, boiling, and critical temperatures of the elements”. CRC Handbook of Chemistry and Physics (ấn bản 84). Boca Raton, fluorrida: CRC Press. ISBN 0849305950.
- ^ “Overview of Cryogenic Air Separation and Liquefier Systems”. Universal Industrial Gases, Inc. Truy cập ngày 15 tháng 12 năm 2007.
- ^ “Liquid Oxygen Material Safety Data Sheet” (PDF). Matheson Tri Gas. Bản gốc (PDF) lưu trữ ngày 27 tháng 2 năm 2008. Truy cập ngày 15 tháng 12 năm 2007.
- ^ Krupenie, Paul H. (1972). “The Spectrum of Molecular Oxygen”. Journal of Physical and Chemical Reference Data. 1 (2): 423–534. Bibcode:1972JPCRD...1..423K. doi:10.1063/1.3253101.
- ^ Guy P. Brasseur; Susan Solomon (ngày 15 tháng 1 năm 2006). Aeronomy of the Middle Atmosphere: Chemistry and Physics of the Stratosphere and Mesosphere. Springer Science & Business Media. tr. 220–. ISBN 978-1-4020-3824-2.
- ^ Kearns, David R. (1971). “Physical and chemical properties of singlet molecular oxygen”. Chemical Reviews. 71 (4): 395–427. doi:10.1021/cr60272a004.
- ^ a b c d “Oxygen Nuclides / Isotopes”. EnvironmentalChemistry.com. Truy cập ngày 17 tháng 12 năm 2007.
- ^ a b c Meyer, B.S. (September 19–21, 2005). “Nucleosynthesis and Galactic Chemical Evolution of the Isotopes of Oxygen” (PDF). Proceedings of the NASA Cosmochemistry Program and the Lunar and Planetary Institute. Workgroup on Oxygen in the Earliest Solar System. Gatlinburg, Tennessee. 9022. Truy cập ngày 22 tháng 1 năm 2007.
- ^ “NUDAT 13O”. Bản gốc lưu trữ ngày 4 tháng 10 năm 2018. Truy cập ngày 6 tháng 7 năm 2009.
- ^ “NUDAT 14O”. Bản gốc lưu trữ ngày 7 tháng 6 năm 2022. Truy cập ngày 6 tháng 7 năm 2009.
- ^ “NUDAT 15O”. Bản gốc lưu trữ ngày 7 tháng 6 năm 2022. Truy cập ngày 6 tháng 7 năm 2009.
- ^ Emsley 2001, p.297
- ^ “Oxygen”. Los Alamos National Laboratory. Bản gốc lưu trữ ngày 26 tháng 10 năm 2007. Truy cập ngày 16 tháng 12 năm 2007.
- ^ Emsley 2001, p.298
- ^ From The Chemistry and Fertility of Sea Waters by H.W. Harvey, 1955, citing C.J.J. Fox, "On the coefficients of absorption of atmospheric gases in sea water", Publ. Circ. Cons. Explor. Mer, no. 41, 1907. Harvey notes that according to later articles in Nature, the values appear to be about 3% too high.
- ^ Emsley 2001, p.301
- ^ a b Emsley 2001, p.304
- ^ Fenical, William (1983). “Marine Plants: A Unique and Unexplored Resource”. Plants: the potentials for extracting protein, medicines, and other useful chemicals (workshop proceedings). DIANE Publishing. tr. 147. ISBN 1-4289-2397-7.
- ^ Walker, J. C. G. (1980). The oxygen cycle in the natural environment and the biogeochemical cycles. Berlin: Springer-Verlag.
- ^ Theodore L. Brown & LeMay, Burslen (2003). Chemistry: The Central Science. Prentice Hall/Pearson Education. tr. 958. ISBN 0-13-048450-4.Quản lý CS1: sử dụng tham số tác giả (liên kết)
- ^ a b Raven 2005, 115–27
- ^ Stwertka, Albert (1998). Guide to the Elements . Oxford University Press. tr. 48–49. ISBN 0-19-508083-1.
- ^ a b c Emsley 2001, p.298
- ^ “"For humans, the normal volume is 6–8 liters per minute."”. Bản gốc lưu trữ ngày 6 tháng 9 năm 2010. Truy cập ngày 4 tháng 12 năm 2013.
- ^ a b c d Derived from mmHg values using 0.133322 kPa/mmHg
- ^ a b Normal Reference Range Table Lưu trữ 2011-12-25 tại Wayback Machine from The University of Texas Southwestern Medical Center at Dallas. Used in Interactive Case Study Companion to Pathologic basis of disease.
- ^ a b The Medical Education Division of the Brookside Associates--> ABG (Arterial Blood Gas) Retrieved on ngày 6 tháng 12 năm 2009
- ^ Charles Henrickson (2005). Chemistry. Cliffs Notes. ISBN 0-7645-7419-1.
- ^ a b doi:10.1038/nature12426
Hoàn thành chú thích này - ^ Neil A. Campbell & Reece, Jane B. (2005). Biology, 7th Edition. San Francisco: Pearson – Benjamin Cummings. tr. 522–23. ISBN 0-8053-7171-0.Quản lý CS1: sử dụng tham số tác giả (liên kết)
- ^ Freeman, Scott (2005). Biological Science, 2nd. Upper Saddle River, NJ: Pearson – Prentice Hall. tr. 214, 586. ISBN 0-13-140941-7.
- ^ a b Berner, Robert A. (1999). “Atmospheric oxygen over Phanerozoic time”. Proceedings of the National Academy of Sciences of the USA. 96 (20): 10955–57. Bibcode:1999PNAS...9610955B. doi:10.1073/pnas.96.20.10955. PMC 34224. PMID 10500106.
- ^ doi:10.1111/j.1472-4669.2009.00188.x
Hoàn thành chú thích này - ^ Emsley 2001, p.303
- ^ Dole, Malcolm (1965). “The Natural History of Oxygen” (PDF). The Journal of General Physiology. 49 (1): 5–27. doi:10.1085/jgp.49.1.5. PMC 2195461. PMID 5859927. Truy cập ngày 16 tháng 12 năm 2007.
- ^ Lê, Xuân Trọng (2014). Hóa học 8 (ấn bản 10). Nhà xuất bản Giáo dục Việt Nam. tr. 92, 93.
- ^ a b c d e Emsley 2001, p. 300
- ^ “Non-Cryogenic Air Separation Processes”. UIG Inc. 2003. Truy cập ngày 16 tháng 12 năm 2007.
- ^ Emsley 2001, p.301
- ^ Space Shuttle Use of Propellants and Fluids. National Aeronautics and Space Administration. 2001–09. Bản gốc lưu trữ ngày 17 tháng 9 năm 2008. Truy cập ngày 16 tháng 12 năm 2007.
NASAFacts FS-2001-09-015-KSC
Kiểm tra giá trị ngày tháng trong:|date=(trợ giúp)
Sách tham khảo
| Wikimedia Commons có thêm hình ảnh và phương tiện truyền tải về Oxy. |
- Oxygen (chemical element) tại Encyclopædia Britannica (tiếng Anh)
- Cook, Gerhard A.; Lauer, Carol M. (1968). “Oxygen”. Trong Clifford A. Hampel (biên tập). The Encyclopedia of the Chemical Elements. New York: Reinhold Book Corporation. tr. 499–512. LCCN 68-29938.
- Emsley, John (2001). “Oxygen”. Nature's Building Blocks: An A-Z Guide to the Elements. Oxford, England, UK: Oxford University Press. tr. 297–304. ISBN 0-19-850340-7.
- Raven, Peter H.; Evert, Ray F.; Eichhorn, Susan E. (2005). Biology of Plants (ấn bản 7). New York: W.H. Freeman and Company Publishers. tr. 115–27. ISBN 0-7167-1007-2.
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | |||||||||||||||
| 1 | H | He | ||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | ||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | ||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |

