Kali
| Kali, 19K | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 Kali được bảo quản trong lọ chứa dầu parafin. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Quang phổ vạch của kali | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tính chất chung | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tên, ký hiệu | Kali, K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hình dạng | Ánh kim trắng bạc | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kali trong bảng tuần hoàn | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Số nguyên tử (Z) | 19 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Khối lượng nguyên tử chuẩn (Ar) | 39,0983(1)[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Phân loại | kim loại kiềm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nhóm, phân lớp | 1, s | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chu kỳ | Chu kỳ 4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cấu hình electron | [Ar] 4s1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
mỗi lớp | 2, 8, 8, 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tính chất vật lý | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Màu sắc | Ánh kim trắng bạc | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Trạng thái vật chất | Chất rắn | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nhiệt độ nóng chảy | 336,53 K (63,38 °C, 146,08 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nhiệt độ sôi | 1032 K (759 °C, 1398 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mật độ | 0,862 g·cm−3 (ở 0 °C, 101.325 kPa) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mật độ ở thể lỏng | ở nhiệt độ nóng chảy: 0,828 g·cm−3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Điểm ba | 336,35 K, kPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Điểm tới hạn | 2223 K, 16 MPa[2] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nhiệt lượng nóng chảy | 2,33 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nhiệt bay hơi | 76,9 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nhiệt dung | 29,6 J·mol−1·K−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tính chất nguyên tử | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Trạng thái oxy hóa | 1, -1 Base mạnh | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Độ âm điện | 0,82 (Thang Pauling) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Năng lượng ion hóa | Thứ nhất: 418,8 kJ·mol−1 Thứ hai: 3052 kJ·mol−1 Thứ ba: 4420 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bán kính cộng hoá trị | thực nghiệm: 227 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bán kính liên kết cộng hóa trị | 203±12 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bán kính van der Waals | 275 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Thông tin khác | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cấu trúc tinh thể | Lập phương tâm khối | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vận tốc âm thanh | que mỏng: 2000 m·s−1 (ở 20 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Độ giãn nở nhiệt | 83,3 µm·m−1·K−1 (ở 25 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Độ dẫn nhiệt | 102,5 W·m−1·K−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Điện trở suất | ở 20 °C: 72 n Ω·m | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tính chất từ | Thuận từ[3] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Độ cảm từ (χmol) | +20,8·10−6 cm3/mol (298 K)[4] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mô đun Young | 3,53 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mô đun cắt | 1,3 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mô đun khối | 3,1 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Độ cứng theo thang Mohs | 0,4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Độ cứng theo thang Brinell | 0,363 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Số đăng ký CAS | 7440-09-7 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lịch sử | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Phát hiện | Humphry Davy (1807) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Đồng vị ổn định nhất | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bài chính: Đồng vị của Kali | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Kali (bắt nguồn từ tiếng Tân Latinh: kalium, danh pháp IUPAC: potassium) là nguyên tố hoá học ký hiệu K, số thứ tự 19 trong bảng tuần hoàn. Ngoài những tên đã nêu, Kali còn được gọi là bồ tạt (nhiều khi được dùng để chỉ kali carbonat K2CO3) hay potassium. Kali nguyên tố là kim loại kiềm mềm, có màu trắng bạc dễ bị oxy hóa trong không khí và phản ứng rất mạnh với nước tạo ra một lượng nhiệt đủ để đốt cháy lượng hydro sinh ra từ phản ứng đã nêu. Kali khi cháy có ngọn lửa màu hoa cà.
Kali và natri có tính chất hóa học rất giống nhau, đều là những nguyên tố nhóm IA trong bảng tuần hoàn. Chúng có cùng mức năng lượng ion hóa thứ nhất, khi được kích hoạt thì nguyên tử của hai nguyên tố này sẽ cho đi electron ngoài cùng duy nhất. Dù là hai nguyên tố khác nhau, nhưng kali và natri có thể kết hợp với những anion giống nhau để tạo nên những muối có tính chất tương tự, điều này đã được nghi ngờ từ năm 1702,[5] và được chứng minh năm 1807 khi kali và natri được cô lập một cách độc lập từ các muối khác nhau bằng cách điện phân. Kali tồn tại trong tự nhiên ở dạng các muối ion. Do đó, nó được tìm thấy ở dạng hòa tan trong nước biển (với khoảng 0,04% kali theo khối lượng[6][7]), và nguyên tố này có mặt trong nhiều khoáng vật.
Hầu hết các ứng dụng trong công nghiệp của kali là nhờ vào khả năng hòa tan tương đối cao của các hợp chất kali trong nước như bánh xà phòng kali. Kim loại kali chỉ có một vài ứng dụng đặc biệt, như là nguyên tố được thay thế cho natri kim loại trong hầu hết các phản ứng hóa học.
Các ion kali có vai trò cần thiết cho chức năng của mọi tế bào sống. Sự khuếch tán ion kali xuyên màng tế bào thần kinh cho phép hoạt động dẫn truyền thần kinh diễn ra bình thường. Sự suy giảm kali trong động vật, bao gồm cả con người, dẫn đến rối loạn các chức năng khác nhau của tim. Cơ thể phản ứng với lượng kali trong chế độ ăn uống, làm tăng nồng độ kali huyết thanh, với sự chuyển đổi kali từ bên ngoài đến bên trong tế bào và tăng thải kali qua thận.
Kali tích lũy trong các tế bào thực vật, và do đó trái cây tươi và rau là những nguồn cung cấp lượng kali tốt cho cơ thể. Sự tồn tại trong thực vật khiến ban đầu kali được cô lập từ potash (các dạng tro của thực vật), nên kali trong tiếng Anh được đặt tên theo hợp chất này. Cũng vì lý do trên nên những vụ canh tác sản lượng lớn đã làm cạn kiệt nguồn kali trong đất một cách nhanh chóng, khiến phân bón nông nghiệp tiêu thụ đến 95% hóa chất chứa kali được sản xuất trên toàn cầu.[8] Ngược lại, ngoại trừ một vài cây chịu mặn đặc biệt, hầu hết thực vật không thể dung nạp ion natri, dẫn đến hệ quả hàm lượng natri thấp trong cơ thể.
Lịch sử
[sửa | sửa mã nguồn]Không phải các muối kali hay natri (với tư cách tách biệt với các loại muối hóa học khác) đã từng được biết đến trong thời kỳ La Mã, và tên gọi Latin của nguyên tố này không phải gốc Latin cổ điển mà là Tân Latin. Tên Latin kalium được chọn từ từ "alkali" đã được chuyển tự từ tiếng Ả Rập: القَلْيَه al-qalyah nghĩa là "tro thực vật". Thuật ngữ alkali trong tiếng Anh tương tự cũng có gốc này (kali trong tiếng Ả Rập chuẩn hiện đại là بوتاسيوم būtāsyūm).[9]

Tên tiếng Anh của nguyên tố này là potassium bắt nguồn từ chữ "potash" (K2CO3; bồ tạt),[10] đề cập đến một phương pháp mà theo đó bồ tạt được sản xuất bằng cách lọc sạch tro gỗ hoặc lá cây và làm bay hơi dung dịch trong một cái nồi. Bồ tạt về bản chất là một hỗn hợp muối kali do thực vật có chứa một ít hoặc không có hàm lượng natri, và phần còn lại của khoáng chất trong thực vật bao gồm các muối calci có tính hòa tan tương đối thấp. Mặc dù kali đã được sử dụng từ thời cổ đại, thành phần hóa học của nó lại không được biết đến. Georg Ernst Stahl đã thu được bằng chứng thực nghiệm cho phép ông kết luận sự khác biệt của hai loại muối kali và natri vào năm 1702,[5] và Henri Louis Duhamel du Monceau đã tái khẳng định sự khác biệt này vào năm 1736.[11] Khi ấy, thành phần hóa học chính xác của các hợp chất cấu tạo từ natri và kali và chính các nguyên tố natri và kali vẫn chưa được biết đến, vì vậy Antoine Lavoisier đã không xếp alkali vào trong danh sách các nguyên tố hóa học của ông năm 1789.[12][13]
Kim loại kali [sic] đã được Humphry Davy phát hiện năm 1807 khi ông đang phân tách kali hydroxide (KOH) nóng chảy. Ấy là kim loại đầu tiên được điều chế với phuơng pháp điện phân sử dụng pin Volta.[14] Cùng năm đó, Davy đã thông báo về việc tách natri kim loại từ muối khoáng vật (natri hydroxide NaOH) cũng bằng kỹ thuật tương tự, và ông đã chứng minh được rằng các nguyên tố tách ra từ hai loại muối kể trên là khác nhau.[12][13][15][16] Mặc dù việc sản xuất kim loại kali và natri đã cho thấy rằng chúng được cấu tạo từ hai nguyên tố khác nhau nhưng phải mất một khoảng thời gian trước khi đề xuất của ông được công nhận rộng rãi.[13]
Trong một thời gian dài, kali chỉ được ứng dụng vào việc sản xuất thủy tinh, thuốc tẩy và xà phòng.[17] Xà phòng kali từ mỡ động vật và dầu thực vật có giá rất cao, do chúng có khuynh hướng hòa tan nhiều hơn trong nước và mềm hơn, nên được gọi là xà phòng mềm.[8] Phát hiện của Justus Liebig năm 1840 cho thấy rằng kali là nguyên tố cần thiết cho thực vật và hầu hết loại đất đều thiếu kali[18] đã làm gia tăng nhu cầu các muối kali. Tro gỗ từ các loại cây linh sam ban đầu được sử dụng như một nguồn cung cấp muối kali ở dạng phân bón, nhưng với việc phát hiện năm 1868 về các mỏ chứa kali chloride gần Staßfurt, Đức thì sản lượng phân bón kali bắt đầu được sản xuất ở quy mô công nghiệp.[19][20][21][22] Các mỏ bồ tạt khác dần được phát hiện, và vào thập niên 1960 Canada trở thành nước cung cấp kali chính trên thị trường quốc tế.[23][24]
Tính chất
[sửa | sửa mã nguồn]Vật lý
[sửa | sửa mã nguồn]Kali là kim loại nhẹ thứ 2 sau lithi. Nó là chất rắn mềm có điểm nóng chảy thấp và có thể dùng dao để cắt dễ dàng. Vết mới cắt của kali có màu bạc, nhưng ngay lập tức sẽ lu mờ chuyển sang màu xám sau khi tiếp xúc với không khí,[25][26] nên nó phải được bảo quản trong dầu mỏ hay dầu lửa. Trong thí nghiệm với ngọn lửa, kali và các hợp chất của nó phát ra màu hoa cà với đỉnh bức xạ ở bước sóng 766,5 nm (xem đoạn phim bên dưới.)[27][26]
Cấu trúc nguyên tử
[sửa | sửa mã nguồn]
Nguyên tử Kali có 19 proton và 19 electron, với đồng vị bền có 20 neutron. Bán kính nguyên tử trung bình 2,77 Å, Vm là 45,46 cm³/mol.[28] Cấu hình điện tử của Kali như sau:
|
K: 1s2 L: 2s2p6 M: 3s2p6 N: 4s1 |
Hóa học
[sửa | sửa mã nguồn]
Các nguyên tử kali có 19 electron nhiều hơn 1 electron so với trạng thái bền vững của khí trơ gần nhất argon. Nguyên tử kali trong trường hợp này dễ mất 1 nguyên tử ngoài cùng hơn là kiếm thêm 1 nữa để đạt trang thái bền; tuy nhiên, các ion K– cũng được biết đến.[29] Do mức năng lượng ion hóa thứ nhất thấp (418,8 kJ/mol) nguyên tử kali dễ dàng mất đi 1 electron và oxy hóa thành cation K+.[30] Quá trình này cần ít năng lượng đến nỗi kali dễ dàng bị oxy hóa bởi oxy trong khí quyển. Ngược lại, mức năng lượng ion hóa thứ hai rất cao (3052 kJ/mol), do phải loại bỏ 2 electron khi phá vỡ trạng thái bền vững của cấu hình khí hiếm.[30] Do đó, kali không sẵn sàng để tạo thành các hợp chất ở trạng thái oxy hóa +2 (hoặc cao hơn).[29]
Kali phản ứng với oxy trong không khí tạo thành kali peroxide và phản ứng với nước tạo thành kali hydroxide. Phản ứng của kali với nước rất nguy hiểm vì tính mãnh liệt của phản ứng và việc tạo ra khí hydro trong phản ứng. Khí hydro tiếp tục phản ứng với oxy trong khí quyển tạo thành nước, lượng nước này lại tiếp tục phản ứng với kali dư.[26] Phản ứng này chỉ cần sự có mặt của một ít nước; vì vậy kali và hợp kim lỏng của nó với natri là NaK là những chất hút ẩm mạnh có thể được dùng để làm khô các dung môi trước khi đưa vào chưng cất.[26][31]
Do tính nhạy cảm của kali với nước và không khí, các phản ứng chỉ có thể xảy ra trong khí quyển trơ như khí argon dùng công nghệ chân không. Kali không phản ứng với hầu hết hydrocarbon như dầu khoáng hoặc kerosene.[26] Nó dễ hòa tan trong amonia lỏng với nồng độ lên đến 480 ppm ở 0 °C. Tùy theo nồng độ, các dung dịch ammoniac sẽ có màu xanh dương đến vàng, và độ dẫn điện của chúng tương tự như độ dẫn điện của kim loại lỏng. Ở dạng dung dịch tinh khiết, ammoniac phản ứng chậm với kali tạo thành KNH2, nhưng phản ứng này được tăng tốc khi thêm một lượng nhỏ muối của các kim loại chuyển tiếp.[32] Bởi vì kali có thể khử các muối thành kim loại, kali thường được dùng làm chất khử trong việc sản xuất các kim loại từ các muối của chúng bằng phương pháp Rieke.[33] Ví dụ, dùng kali làm chất khử để điều chế magnesi bằng phương pháp Rieke từ magnesi chloride:
- MgCl2 + 2 K → Mg + 2 KCl
Hợp chất
[sửa | sửa mã nguồn]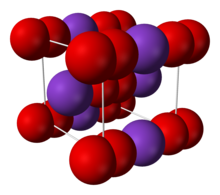
Kali chỉ có một trạng thái oxy hóa phổ biến là +1. Kim loại kali là chất phản ứng mạnh do nó dễ dàng bị oxy hóa tạo ra cation K+. Khi bị oxy hóa nó rất bền và khó bị khử trở lại thành kim loại.[29]
Kali hydroxide dễ dàng phản ứng với carbon dioxide tạo ra kali carbonat, và được dùng để loại các tạp chất khí trong không khí. Nhìn chung, các hợp chất kali hòa tan trong nước rất tốt, do năng lượng hydrat hóa của ion K+ cao. Ion kali không màu khi tan trong nước và rất khó kết tủa; nó có thể kết tủa với natri tetraphenylborat, acid hexachloroplatinic, và natri cobaltinitrit.[26]
Kali oxy hóa nhanh hơn hầu hết các kim loại và tạo thành các oxide với các liên kết oxy-oxy, cũng giống như các kim loại kiềm khác trừ lithi. Có ba loại oxide được hình thành trong phản ứng này gồm kali oxide, kali peroxide, và kali superoxide,[34] gồm 3 kiểu ion gốc oxy khác nhau: oxide (O2−
), peroxide (O2−
2), và superoxide (O−
2). Hai hợp chất sau, đặc biệt là superoxide thì hiếm gặp và chỉ được tạo ra trong phản ứng với các kim loại có tính dương điện cao; các hợp chất này chứa các liên kết oxy-oxy.[32] Tất cả các hợp chất kali hai phân tử đã được biết đến phản ứng rất mãnh liệt với nước tạo thành kali hydroxide, đây là hợp chất có tính kiềm rất mạnh và 1,21 kg chất kiềm này có thể hòa tan trong khoảng 1 lít nước.[35][36]
Các hợp chất kali phân li mạnh và hầu hết chúng có thể hòa tan trong nước. Các dạng chính tồn tại trong nước là các hợp chất phức [K(H2O)n]+ với n = 6 và 7.[37] Một ít muối của nó hòa tan kém trong nước như kali tetraphenylborat, kali hexachloroplatinat, và kali cobaltinitrit.[26][38]
Đồng vị
[sửa | sửa mã nguồn]Có 24 đồng vị của kali đã được biết, trong đó có 3 đồng vị có trong tự nhiên: K39 (93,3%), K40 (0,01%) và K41 (6,7%). Đồng vị tự nhiên K40 có chu kỳ bán rã 1,250×109 năm và phân rã thành Ar40 (11,2%) bằng cách bắt điện tử và bằng bức xạ positron, cũng như phân rã thành đồng vị ổn định Ca40 (88,8%) bằng bức xạ beta.[39]
Sự phân rã của K40 thành Ar40 thông thường được sử dụng làm phương pháp đánh giá tuổi các loại đá. Phương pháp đánh giá tuổi bằng tỷ lệ K/Ar phụ thuộc vào giả thiết rằng các loại đá không chứa argon ở thời điểm tạo ra nó và mọi agon do phóng xạ sinh ra sau đó (Ar40) về mặt lượng là được bảo toàn, tức là một hệ thống kín. Các khoáng chất được xác định tuổi bằng cách đo mật độ của kali cũng như lượng Ar40 do phóng xạ sinh ra đã được tích lũy. Các khoáng chất phù hợp để xác định tuổi là biotit, muscovit, và plutonit/hornblend biến chất, cũng như felspat núi lửa; toàn bộ các mẫu đá từ nham thạch núi lửa và đá xâm nhập nông có thể được xác định tuổi nếu chúng chưa bị thay thế.[39][40] Ngoài ra, các đồng vị kali còn được sử dụng như là chất đánh dấu vết trong nghiên cứu thời tiết. Chúng cũng được sử dụng trong các nghiên cứu về chu trình vận chuyển các chất dinh dưỡng vì kali là chất dinh dưỡng đa lượng cần thiết cho sự sống.[41]
K40 có trong kali tự nhiên (và vì thế có trong các sản phẩm muối thương mại) trong một lượng vừa đủ đến mức một túi lớn của các chất này có thể sử dụng như nguồn phóng xạ cho các minh họa trong lớp học. Ở người và động vật khỏe mạnh, 40K là một nguồn phóng xạ lớn nhất thậm chí còn hơn cả 14C. Trong cơ thể một người nặng 70 kg có khoảng 4.400 hạt nhân 40K phân rã mỗi giây.[42] Mức độ phân rã của kali tự nhiên là 31 Bq/g.[43]
Sự phổ biến
[sửa | sửa mã nguồn]
Kali được hình thành trong vũ trụ bởi quá trình tổng hợp hạt nhân từ các nguyên tử nhẹ hơn. Dạng bền của kali được tạo ra trong các vụ nổ siêu tân tinh bằng quá trình đốt cháy oxy.[44] Kim loại kali không tồn tại trong tự nhiên do độ hoạt động mạnh của nó với nước. Ở dạng hợp chất, nguyên tố này chiếm khoảng 2,4% trọng lượng lớp vỏ Trái Đất và là nguyên tố phổ biến thứ bảy trong lớp này, tương đương với natri là 1,8%.[45]. Trong nước biển, nồng độ của kali là 0,39 g/L[6] rất thấp so với natri là 10,8 g/L.[46][47]
Orthoclase (feldspar kali KAlSi3O8) là một khoáng vật tạo đá phổ biến. Ví dụ như trong đá granit chứa 5% kali, hàm lượng này cao hơn hàm lượng trung bình của kali trong vỏ Trái Đất. Sylvit (KCl), carnallit (KCl·MgCl2·6(H2O)), kainit (MgSO4·KCl·3H2O) và langbeinite (MgSO4·K2SO4)) là các khoáng vật được tìm thấy ở dạng các đá bay hơi của các hồ và nền biển cổ trên khắp thế giới. Các mỏ này thường có sự phân lớp bắt đầu với lớp ít hòa tan nằm dưới đáy và lớp hòa tan nhất nằm ở trên mặt.[47] Các mỏ dạng trứng (kali nitrat) được hình thành từ sự phân rã các khoáng vật hữu cơ trong đới tiếp xúc với khí quyển, hầu hết là trong các hang động; do khả năng hòa tan cao trong nước của chất này nên việc hình thành các mỏ lớn cần có các điều kiện môi trường đặc biệt.[48]
Sản xuất thương mại
[sửa | sửa mã nguồn]


Các muối kali như carnallit, langbeinit, polyhalit, và sylvit tạo nên các mỏ lớn trong các hồ và đáy biển cổ,[46] làm cho việc khai thác các muối kali trong các môi trường này là khả thi về mặt thương mại. Nguồn chủ yếu của kali được khai thác ở Canada, Nga, Belarus, Đức, Israel, Hoa Kỳ, Jordan và nhiều nơi khác nữa trên thế giới.[49][50][51] Mỏ đầu tiên được khai thác nằm gần Staßfurt, Đức, nhưng dãi phân bố mỏ này kéo dài từ Đại Anh qua Đức và đến tận Ba Lan. Chúng nằm trong tầng Zechstein và tích tụ vào kỷ Permi giữa đến muộn. Mỏ lớn nhất từng được phát hiện ở độ sâu khoảng hơn 900 mét dưới bề mặt của Saskatchewan, Canada. Các mỏ này nằm trong Loạt Elk Point hình thành vào Devon giữa. Saskatchewan, nơi có nhiều mỏ lớn được khai thác từ thập niên 1960, đã đi tiên phong trong việc sử dụng phương pháp đóng băng cát ước (hệ tầng Blairmore) để khai thác dạng trục trong chúng (in order to drive mine shafts through them).[52] Nước trong Biển Chết được Israel và Jordan dùng để sản xuất kali, trong khi nồng độ trong các đại dương thông thường quá thấp để có thể sản xuất thương mại với giá hiện thời.[50][51]
Nhiều phương pháp được sử dụng để tách các muối kali ra khỏi các hợp chất có mặt magnesi và natri. Phương pháp được sử dụng nhiều nhất là kết tủa một số hợp chất dựa vào khải năng hòa tan khác nhau của các muối ở những nhiệt độ khác nhau. Tách tĩnh điện của hỗ hợp các muối dưới lòng đất cũng được sử dụng trong một số mỏ. Các chất thải magnesi và natri tách ra hoặc được chứa dưới lòng đất hoặc chất thành các đống xỉ. Hầu hết các khoáng sản kali được khai thác qua quá trình xử lý sẽ cho ra sản phẩm cuối cùng là kali chloride. Ngành công nghiệp khoáng chú trọng đến kali chloride hoặc ở dạng potash, hoặc MOP đơn giản.[47]
Kim loại kali nguyên chất có thể được điều chế bằng phương pháp điện phân các hydroxide của nó theo quy trình đã được Davy điều chỉnh một chút. Mặc dù quá trình điện phân đã được phát triển và sử dụng ở quy mô công nghiệp trong thập niên 1920, phương pháp nhiệt bằng cách phản ứng của natri với kali chloride trong một phản ứng cân bằng hóa học trở thành phương pháp chủ yếu trong thập niên 1950. Việc sản xuất các hợp kim kali natri có thể thực hiện được bằng cách thay đổi thời gian phản ứng và lượng natri được sử dụng trong phản ứng. Công nghệ Griesheimer sử dụng phản ứng giữa kali fluoride với calci carbide cũng được sử dụng để sản xuất kali.[47][53]
- Na + KCl → NaCl + K (phương pháp nhiệt)
- 2 KF + CaC2 → 2K + CaF2 + 2 C (công nghệ Griesheimer)
Kim loại kali cấp chất thử (chỉ thị) có giá khoảng 22 USD/kg) năm 2010 khi mua với số lượng lớn (hàng tấn). Việc buôn bán chất này không ổn định do khó khăn trong việc bảo quản kim loại này. Nó phải được lưu trữ trong điều kiệu không khí chứa toàn khí trơ hoặc dầu khoáng gốc khan để chống việc tạo thành các lớp kali superoxide bọc trên bề mặt của nó. Loại oxide này là một chất nổ nhạy với áp lực nó sẽ nổ khi bị trầy xước. Khi nổ thường sẽ sinh ra ngọn lửa rất khó dập tắt.[54][55]
Vai trò sinh học
[sửa | sửa mã nguồn]Chức năng sinh học
[sửa | sửa mã nguồn]
Kali là nguyên tố phổ biến thứ 8 hoặc 9 theo khối lượng (0,2%) trong cơ thể người, vì vậy một người trưởng thành có cân nặng 60 kg chứa khoảng 120 g kali.[56] Cơ thể người có nhiều kali giống như lưu huỳnh và chlor, và chỉ có các khoáng chất chính như calci và phosphor là dồi dào nhất.[57]
Các cation kali có vai trò quan trọng trong các tế bào thần kinh (não và thần kinh), và trong việc ảnh hưởng đến sự cân bằng thẩm thấu giữa các tế bào và dịch kẽ (ngoại bào chất) với sự phân bố của chúng trong tất cả các môi trường trung gian ở tất cả động vật (không phải ở tất cả thực vật) bằng cách bơm được gọi là Na+/K+-ATPase.[58] Sự bơm ion này sử dụng ATP để bơm 3 ion natri ra khỏi tế bào và 2 ion kali vào bên trong tế bào, do vậy nó tạo ra một gradient điện hóa trên tất cả màng tế bào. Ngoài ra, các kênh ion kali có tính chọn lọc cao có vai trò quan trọng trong sự phân cực, ví dụ trong các nơron, sau khi một điện thế hoạt động được kích hoạt. Kênh ion kali đã được giải quyết gần đây nhất là KirBac3.1, đưa ra tổng cộng 5 kênh ion kali (KcsA, KirBac1.1, KirBac3.1, KvAP, và MthK) có cấu trúc xác định. Tất cả năm kênh đều từ các loài sinh vật nhân sơ.[59]
Kali có thể nhận dạng được thông qua vị của nó do nó tác động vào 3 trong số năm loại của vị giác nhưng tùy thuộc vào nồng độ. Các ion kali trong dung dịch loãng có vị ngọt, cho phép có nồng độ trung bình trong sữa và nước ép trái cây, trong khi nồng độ cao hơn sẽ làm tăng vị đắng do tính kiềm, và cuối cùng là vị mặn. Sự kết hợp của vị đắng và mặn trong các dung dịch có nhiều kali bổ sung trong các đồ uống làm cho chúng có vị ngon là một thách thức.[60][61]
Màng phân cực
[sửa | sửa mã nguồn]Kali cũng có vai trò quan trọng trong chống co cơ và việc gởi tất cả các xung động thần kinh ở động vật qua các tiềm năng hành động (Action potential). Do bản chất của tính điện và hóa của chúng, các ion K+ lớn hơn các ion Na+, và các kênh và các bơm ion trong các màng tế bào có thể phân biệt giữa hai loại ion này, bơm chủ động hay cho phép đi qua thụ động một trong hai ion đồng thời ngăn cản ion còn lại.[62]
Sự thiếu hụt kali trong các dung dịch trong cơ thể có thể gây ra các tình trạng có thể tử vong như thiếu kali máu, đặc biệt gây nôn mửa, tiêu chảy, và/hoặc tăng bài tiết niệu đạo.[63] Các triệu chứng thiếu hụt kali gồm yếu cơ, liệt ruột, bất thường ECG (điệm tâm đồ), giảm phản xạ và trong các trường hợp nghiêm trọng có thể gây liệt hô hấp, alkalosis và rối loạn nhịp tim.[64]
Lọc và bài tiết
[sửa | sửa mã nguồn]Kali là một khoáng chất thiết yếu trong cơ thể con người; nó là cation chính bên trong các tế bào động vật, và do đó nó co vai trò quan trọng trong việc duy trì chất dịch và cân bằng điện giải trong cơ thể. Natri cấu thành nên hầu hết các cation trong huyết tương, khoảng 145 mmol/L (3,345 g)(1 mmol/L = 1mEq/L), và kali cấu thành nên hầu hết các cation trong dịch nội bào với mức khoảng 150 mmol/L (4,8 g). Huyết tương được lọc qua cầu thận của các quả thận mơi một lượng lớn với khoảng 180 L/ngày.[65] Do vậy mỗi ngày có 602 g natri và 33 g kali được lọc. Chỉ có 1–10 g natri và 1–4 g kali có thể có trong thức ăn phải được tái hấp thu. Natri phải được tái hấp thu theo cách giữ một lượng máu chính xác và áp suất thẩm thấu đúng; kali phải được tái hấp thu theo cách nào đó để giữ cho nồng độ huyết thanh càng gần với 4,8 mmol/L (khoảng 0,190 g/L) càng có thể.[66] Các bơm natri trong thận phải luôn hoạt động để bảo tồn natri. Kali đôi khi cũng phải được bảo tồn, nhưng khi lượng kali trong huyết tương rất nhỏ và hồ kali trong các tế bào lớn khoảng 30 lần, tình hình không phải là quá nghiêm trọng đối với kali. Vì kali được di chuyển một cách thụ động[67][68] ngược chiều với natri để đạt cân bằng Donnan (không thực tế),[69] có thể không bao giờ có nồng độ kali nước tiểu nhỏ hơn nồng độ kali trong huyết thanh trừ khi thỉnh thoảng có việc tiết nước chủ động vào giai đoạn cuối của quá trình. Kali được tiết ra hai lần và tái hấp thụ 3 lần trước khi nước tiểu đi đến các ống thu gom.[70] Ở điểm đó, nó thường xuyên có nồng độ kali như huyết tương. Cuối quá trình, kali được tiết ra một lần nữa nếu nồng độ huyết thanh quá cao.
Nếu kali bị loại bỏ từ thức ăn, vẫn có sự đào thải từ thận với khoảng 200 mg ngày khi huyết thanh giảm 3,0–3,5 mmol/L trong khoảng 1 tuần,[71] và có thể không bao giờ bị cắt giảm hoàn toàn, gây ra hạ kali máu và thậm chí là tử vong.[72]
Kali di chuyển một cách thụ động qua các lỗ rỗng của màng tế bào. Khi các ion di chuyển qua các bơm, có một cổng trong các bơm ở mỗi mặt của màng tế bào và chỉ có một cổng có thể mở vào một thời điểm. Kết quả là có khoảng 100 ion bị đẩy qua trong 1 giây. Các lỗ rỗng chỉ có 1 cổng, và chỉ có một loại ion có thể đi qua với số lượng 10 triệu đến 100 triệu ion mỗi giây.[73] Các lỗ chân lông cần calci để mở ra[74] mặc dù người ta nghĩ rằng calci hoạt động ngược lại bằng cách khóa ít nhất một trong số các lỗ rỗng.[75] Các nhóm carbonyl bên trong lỗ rỗng trên các amino acid bắt chước hydrat hóa nước diễn ra trong dung môi nước[76] bởi bản chất tích điện tĩnh điện trên 4 nhóm carbonyl bên trong lỗ rỗng.[77]
Trong khẩu phần ăn
[sửa | sửa mã nguồn]Cung cấp vừa đủ
[sửa | sửa mã nguồn]Cung cấp vừa đủ lượng kali để hỗ trợ sự sống có thể qua việc ăn nhiều loại thực phẩm. Những trường hợp thiếu kali rõ ràng (như các triệu chứng, dấu hiện và hàm lượng nguyên tố trong máu thấp hơn bình thường) thì hiếm gặp ở những cá thể khỏe mạnh. Các loài thực phẩm giàu kali như khoai, rau mùi tây, mơ khô, sữa khô, sô cô la, nhiều loại hạt (đặc biệt là hạnh nhân và hồ trăn), khoai tây, măng, chuối, bơ, nước dừa, đậu nành, và cám, mặc dù nó cũng có với một lượng vừa đủ trong hầu hết trái cây, rau, thịt và cá.[78]
Cung cấp tối đa
[sửa | sửa mã nguồn]Các nghiên cứu dịch tễ học và các nghiên cứu ở động vật về bệnh cao huyết áp chỉ ra rằng khẩu phần ăn có nhiều kali có thể giảm nguy cơ cao huyết áp và đột quỵ (theo một cơ chế độc lập về huyết áp), và việc thiếu hụt kali kết hợp với không cung cấp đủ thiamin đã tạo ra bệnh tim ở chuột.[79] Có một vài tranh cãi liên quan đến lượng cung cấp kali tối đa trong khẩu phần ăn. Ví dụ, các hướng dẫn năm 2004 của Viện Y học Hoa Kỳ (Institute of Medicine) chỉ ra rằng DRI (Dietary reference intake) 4.000 mg kali (100 mEq), mặc dù hầu hết người Mỹ tiêu thụ chỉ phân nửa lượng trên mỗi ngày, điều này có thể làm cho họ thiếu kali liên quan đến hướng dẫn trên.[80][81] Tương tự như thế, ở các nước EU đặc biệt là ở Đức và Ý, kali cung cấp không đủ là khác phổ biến.[82] Các nhà nghiên cứu người Ý, trong một báo cáo năm 2011 khi phân tích rằng khi cung cấp một lượng kali cao hơn 1,64 g mỗi ngày có sự liên hệ với việc giảm 21% nguy cơ đột quỵ.[83]
Dược phẩm và bệnh tật
[sửa | sửa mã nguồn]Lượng Kali trong máu người bình thường là nằm trong khoảng 3,5-5,0 mmol/L.[84][85] Dưới 3,5 sẽ bị chứng giảm kali huyết, trên 5,0 sẽ tăng kali máu. Cả hai khả năng đều có khả năng dẫn đến tử vong.
Bổ sung kali ở dạng dược phẩm được sử dụng phổ biến nhất trong việc kết hợp với loop diuretic và thiazide, các phân loại lợi tiểu giúp tống ra khõi cơ thể natri và nước, nhưng tác dụng phụ cũng gây ra mất kali trong nước tiểu.[86] Nhiều cách bổ sung ở dạng dược phẩm và không phải dược phẩm cũng có mặt. Các muối kali như kali chloride có thể cho hòa tan vào nước, nhưng vị đắng/mặn của các dung dịch có hàm lượng ion kali cao làm cho có cảm giác ngon miệng do việc bổ sung chất lỏng có nồng độ cao khó mà tạo ra được.[60] Những liều bổ sung dạng thuốc đặc biệt dao động từ 10 mmol (400 mg, bằng khoảng 1 cốc sữa hoặc một cốc cam ép 180ml) đến 20 mmol (800 mg) một liều. Các muối kali cũng có ở dạng viên nén hoặc viên nang,[87] dùng cho mục đích điều trị cho phép kali thoát một cách chậm chạp ra khỏi viên thuốc, vì hàm lượng các ion kali rất cao có thể giết chết các mô, và làm tổn thương đến niên mạc dạ dày hoặc niêm mạc ruột. Vì lý do này, các viên thuốc bổ sung kali không kê theo toa bị giới hạn đến 99 mg kali theo luật của Hoa Kỳ.[88]
Ứng dụng
[sửa | sửa mã nguồn]Phân bón
[sửa | sửa mã nguồn]
Các ion kali là thành phần thiết yếu trong dinh dưỡng thực vật và được tìm thấy trong hầu hết các loại đất.[8] Chúng được dùng làm phân bón cho nông nghiệp, trồng trọt và thủy canh ở dạng kali chloride (KCl), kali sulfat (K
2SO
4), hoăc nitrat (KNO
3). Phân bón nông nghiệp tiêu thụ 95% các hóa phẩm của kali trên toàn cầu, và khoảng 90% kali được cung cấp ở dạng KCl.[8] Thành phần kali trong hầu hết thực vật dao động từ 0,5% đến 2% khối lượng các vụ mùa, thường ở dạng K
2O. Các vụ mùa năng suất cao phụ thuộc vào lượng phân bón để bổ sung cho lượng kali mất đi do thực vật hấp thu. Hầu hết phân bón chứa kali chloride, trong khi kali sulfat được dùng cho các vụ mùa nhạy cảm với chloride hoặc vụ mùa cần lượng lưu huỳnh cao hơn. Kali sulfat được tạo ra chủ yếu bằng sự phân giải các khoáng phức của kainit (MgSO4·KCl·3H2O) và langbeinit (MgSO4·K2SO4). Chỉ có rất ít phân bón chứa kali nitrat.[89] Trong năm 2005, khoảng 93% sản lượng kali trên thế giới đã được tiêu thụ bởi các ngành công nghiệp phân bón.[51]
Thực phẩm
[sửa | sửa mã nguồn]Cation kali là dưỡng chất thiết yếu cho con người và sức khỏe. Kali chloride được dùng thay thế cho muối ăn nhằm giảm lượng cung cấp natri để kiểm soát bệnh gây tăng huyết áp. USDA liệt kê pa tê cà chua, nước cam, củ cải đường, đậu trắng, cà chua, chuối và nhiều nguồn thức ăn khác cung cấp kali được xếp theo mức độ giảm dầm hàm lượng kali.[90]
Kali natri tartrat (KNaC4H4O6, muối Rochelle) là một thành phần chính của bột nở; nó cũng được sử dụng trong các gương mạ bạc. Kali bromat (KBrO
3) là một chất oxy hóa mạnh (E924), được dùng để tăng độ dẻo và độ nở cao của bột bánh mì. Kali bisulfit (KHSO
3) được dùng làm chất bảo quản thực phẩm, như trong rượu vang và bia (nhưng không có trong thịt). Nó cũng được sử dụng để tẩy trong dệt-nhuộm và thuộc da.[91][92]
Công nghiệp
[sửa | sửa mã nguồn]Các chất hóa học kali chính là kali hydroxide, kali carbonat, kali sulfat, và kali chloride. Hàng triệu tấn các hợp chất này được sản xuất mỗi năm.[93]
Kali hydroxide KOH là một base mạnh, được dùng ở mức độ công nghiệp để trung hòa các acid mạnh và yếu, để khống chế pH và để sản xuất các muối kali. Nó cũng được dùng để làm bánh xà phòng từ mỡ và dầu trong công nghiệp tẩy rửa và trong các phản ứng thủy phân ester.[94][95]
Kali nitrat (KNO3) được lấy từ các nguồn tự nhiên như guano và evaporit hoặc được sản xuất từ công nghệ Haber; nó là một chất oxy hóa trong thuốc súng (thuốc súng đen) và là một loại phân bón quan trọng. Kali cyanide (KCN) được dùng trong công nghiệp để hòa tan đồng và các kim loại quý, đặc biệt là bạc và vàng, bằng cách tạo ra ở dạng phức chất. Những ứng dụng của nó gồm khai thác vàng, mạ điện, và đúc điện (electroforming) của các kim loại này; nó cũng được dùng trong tổng hợp hữu cơ để tạo ra nitriles. Kali carbonat (K
2CO
3 hay potash) được dùng trong sản xuất thủy tinh, xà phòng, ống phóng màn hình màu, đèn huỳnh quan, dệt nhuộm và chất tạo màu.[96] Kali permanganat (KMnO4) là một chất oxy hóa, có tính tẩy mạnh và được sử dụng trong sản xuất saccharin. Kali chlorat (KClO3) được cho vào vật liệu nổ. Kali bromide (KBr) đước đây được sử dụng làm thuốc an thầnh và trong nhiếp ảnh.[8]
Kali chromat (K2CrO4) được dùng trong mực,[97] nhuộm, chất tạo màu (màu vàng đỏ sáng); trong chất nổ và pháo hoa; trong thuộc da, trong giấy bẫy ruồi và diêm an toàn,[98] tất cả các ứng dụng trên do tính chất của ion cromat hơn là các ion kali.[99]
Hợp kim NaK với điểm nóng chảy thấp và sức căng bề mặt cao được dùng làm chất làm mát trong một số lò phản ứng hạt nhân nhanh và vệ tinh ra đa RORSAT của Liên Xô.[100][101]
Ứng dụng thích hợp khác
[sửa | sửa mã nguồn]
Các hợp chất kali quá phổ biến đến nổi có hàng ngàn ứng dụng nhỏ tại chỗ. Chất rắn màu cam superoxide KO2 là nguồn cung cấp oxy tiện lợi và là chất hấp thụ carbon dioxide. Nó được sử dụng rộng rãi trong hệ thống thông khí mỏ, các tàu ngầm và tàu không gian do nó chứa ít thể tích hơn oxy khí.[102][103]
- 4 KO2 + 2 CO2 → 2 K2CO3 + 3 O2
Kali cobaltinitrit K3[Co(NO2)6] được dùng làm chất tạo màu của các họa sĩ với tên gọi Aureolin hay Cobalt vàng.[104]
Trong phòng thí nghiệm
[sửa | sửa mã nguồn]Hợp kim của natri và kali, NaK ở dạng chất lỏng được dùng làm chất trung gian truyền nhiệt và làm chất hút ẩm để tạo ra một môi trường không khí khô. Nó có thể được sử dụng trong phản ứng chưng cất.[105] Hợp kim gồm 12% Na, 47% K và 41% Cs có nhiệt độ nóng chảy −78 °C, thấp nhất trong tất cả các hợp chất kim loại.[25]
Kali kim loại được dùng ở nhiều dạng khác nhau trong từ kế.[106]
Cảnh báo
[sửa | sửa mã nguồn]Kali nguyên chất phản ứng mãnh liệt với nước và hơi ẩm. Do vậy, nó cần được bảo quản trong dầu khoáng hay dầu lửa và cần phải hết sức thận trọng khi làm việc với nó.
- 2 K (s) + 2 H2O (l) → 2 KOH (aq) + H2↑ (g)
Phản ứng này rất mãnh liệt và giải phóng ra một lượng nhiệt đủ để đốt cháy hydro được tạo ra. Nó có thể chuyển sang nổ nếu có mặt oxy. Kali hydroxide là một chất kiềm mạnh có thể gây bỏng da. Bột kali mịn sẽ cháy trong không khí ở nhiệt độ phòng. Kim loại dạng khối sẽ cháy trong không khí nếu được nung nóng. Do nó có tỷ trọng 0,89 g/cm³, nên đối kali nổi trên nước làm cho nó tiếp xúc với oxy trong khí quyển. Nhiều chất chữa cháy phổ biến, bao gồm cả nước, cũng không có tác dụng hoặc làm đám cháy kali trở nên dữ dội hơn. Nitơ, argon, natri chloride (muối ăn), natri carbonat (tro sô-da), và silic dioxide (cát) có thể dập cháy nếu chúng khô (không chứa nước). Một số chất chữa cháy dạng bột khô nhóm D (natri chloride, natri carbonat, T.E.C.[107][108][109]) được thiết kế riêng cho chữa cháy kim loại cũng hiệu quả. Các chất này lấy đi oxy của đám cháy và làm lạnh kim loại kali.[110]

Kali phản ứng mãnh liệt với các halogen và sẽ phát nổ nếu có mặt brom. Nó cũng phản ứng nổ với acid sulfuric. Việc đốt kali sẽ tạo ra peroxide và superoxide. Các peroxide này có thể phản ứng một cách mãnh liệt với các hợp chất hữu cơ như các loại dầu. Cả peroxide va superoxide có thể phản ứng nổ với kali kim loại.[111]
Do kali phản ứng với hơi nước trong không khí nên nó thường được bảo quản trong các loại dầu khoán anhydrous hoặc kerosen. Không giống lithi và natri, tuy nhiên kali không thể bảo quản trong dầu lâu hơn 6 tháng trừ khi trong môi trường không khí trơ (không có oxy) hoặc môi trường chân không. Sau thời gian cất giữ lâu dài trong không khí, các peroxide nhạy với sốc có thể hình thành trên kim loại và dưới nắp của thùng chứa, và có thể nổ khi mở nắp.[112]
Do tính chất hoạt động cao của kim loại kali, nó phải được vận chuyển một cách cực kỳ cẩn thận, phải có bảo vệ toàn bộ da và mắt và có bộ phận chống nổ cách li giữa người và kim loại. Uống một lượng lớn các hợp chất kali có thể dẫn đến chứng tăng kali máu làm ảnh hưởng mạnh đến hệ tim mạch.[113][114] Kali chloride được dùng ở Hoa Kỳ cho việc hành quyết bằng cách tiêm.[113]
Tham khảo
[sửa | sửa mã nguồn]- ^ Atomic weights of the elements 2013 (IUPAC Technical Report) 88 (3): 265–91. Meija, J.; và cộng sự. Pure and Applied Chemistry (2016) doi:10.1515/pac-2015-0305
- ^ Haynes, William M. biên tập (2011). CRC Handbook of Chemistry and Physics (ấn bản thứ 92). Boca Raton, FL: CRC Press. tr. 4.122. ISBN 1439855110.
- ^ Magnetic susceptibility of the elements and inorganic compounds, in Lide, D. R. biên tập (2005). CRC Handbook of Chemistry and Physics (ấn bản thứ 86). Boca Raton (FL): CRC Press. ISBN 0-8493-0486-5.
- ^ Weast, Robert (1984). CRC, Handbook of Chemistry and Physics. Boca Raton, Florida: Chemical Rubber Company Publishing. tr. E110. ISBN 0-8493-0464-4.
- ^ a b Marggraf, Andreas Siegmund (1761). Chymische Schriften. tr. 167.
- ^ a b Webb, D. A. (1939). “The Sodium and Potassium Content of Sea Water” (PDF). The Journal of Experimental Biology: 183.
- ^ Anthoni, J. (2006). “Detailed composition of seawater at 3.5% salinity”. seafriends.org.nz.
- ^ a b c d e Greenwood 1997, tr. 73.
- ^ Vegetable substances: materials of manufactures trang 270. [published under the superintendence of the Society of the Diffusion of Useful Knowledge] doi:10.5962/bhl.title.28922. Society for the Diffusion of Useful Knowledge (Great Britain)
- ^ Davy, Humphry (1808). “On some new phenomena of chemical changes produced by electricity, in particular the decomposition of the fixed alkalies, and the exhibition of the new substances that constitute their bases; and on the general nature of alkaline bodies”. Philosophical Transactions of the Royal Society of London. 98: 32. doi:10.1098/rstl.1808.0001. ISSN 0261-0523.
- ^ du Monceau, H. L. D. “Sur la Base de Sel Marine”. Memoires de l'Academie royale des Sciences (bằng tiếng Pháp): 65–68.
- ^ a b Weeks, Mary Elvira (1932). “The discovery of the elements. IX. Three alkali metals: Potassium, sodium, and lithium”. Journal of Chemical Education. 9 (6): 1035. Bibcode:1932JChEd...9.1035W. doi:10.1021/ed009p1035.
- ^ a b c Siegfried, R. (1963). “The Discovery of Potassium and Sodium, and the Problem of the Chemical Elements”. Isis. 54 (2): 247–258. doi:10.1086/349704. JSTOR 228541.
- ^ Enghag, P. (2004). “11. Sodium and Potassium”. Encyclopedia of the elements. Wiley-VCH Weinheim. ISBN 3-527-30666-8.
- ^ Davy, Humphry (1808). “On some new phenomena of chemical changes produced by electricity, in particular the decomposition of the fixed alkalies, and the exhibition of the new substances that constitute their bases; and on the general nature of alkaline bodies”. Philosophical Transactions of the Royal Society of London. 98: 1–44. doi:10.1098/rstl.1808.0001.
- ^ Shaposhnik, V. A. (2007). “History of the discovery of potassium and sodium (on the 200th anniversary of the discovery of potassium and sodium)”. Journal of Analytical Chemistry. 62 (11): 1100–1102. doi:10.1134/S1061934807110160.
- ^ Browne, C. A. (1926). “Historical notes upon the domestic potash industry in early colonial and later times”. Journal of Chemical Education. 3 (7): 749–756. Bibcode:1926JChEd...3..749B. doi:10.1021/ed003p749.
- ^ Liebig, Justus von (1840). Die organische Chemie in ihrer Anwendung auf Agricultur und Physiologie (bằng tiếng Đức).
- ^ Cordel, Oskar (1868). Die Stassfurter Kalisalze in der Landwirthschalt: Eine Besprechung... (bằng tiếng Đức). L. Schnock.
- ^ Birnbaum, Karl (1869). Die Kalidüngung in ihren Vortheilen und Gefahren (bằng tiếng Đức).
- ^ Organization, United Nations Industrial Development (ngày 31 tháng 3 năm 1998). Fertilizer Manual. ISBN 978-0-7923-5032-3.
- ^ Organization, United Nations Industrial Development (ngày 31 tháng 3 năm 1998). Fertilizer Manual. ISBN 978-0-7923-5032-3.
- ^ Miller, H. (1980). “Potash from Wood Ashes: Frontier Technology in Canada and the United States”. Technology and Culture. 21 (2): 187–208. doi:10.2307/3103338. JSTOR 3103338.
- ^ Rittenhouse, P. A. (1979). “Potash and polithics”. Economic Geology. 74 (2): 353–357. doi:10.2113/gsecongeo.74.2.353.
- ^ a b Greenwood 1997, tr. 76.
- ^ a b c d e f g Holleman, Arnold F.; Wiberg, Egon; Wiberg, Nils (1985). “Potassium”. Lehrbuch der Anorganischen Chemie (bằng tiếng Đức) . Walter de Gruyter. ISBN 3-11-007511-3.
- ^ Greenwood 1997, tr. 75.
- ^ Periodic Table of Elements: Potassium - K (EnvironmentalChemistry.com) Atomic Structure of Potassium
- ^ a b c Dye, J. L. (1979). “Compounds of Alkali Metal Anions”. Angewandte Chemie International Edition. 18 (8): 587–598. doi:10.1002/anie.197905871.
- ^ a b James, A. M.; Lord, M. P. (1992). Macmillan's chemical and physical data. London: Macmillan. ISBN 0-333-51167-0.
- ^ Burkhardt, trang 35
- ^ a b Burkhardt, trang 32
- ^ Rieke, R. D. (1989). “Preparation of Organometallic Compounds from Highly Reactive Metal Powders”. Science. 246 (4935): 1260–1264. Bibcode:1989Sci...246.1260R. doi:10.1126/science.246.4935.1260. PMID 17832221.
- ^ Lide, David R. (1998). Handbook of Chemistry and Physics (ấn bản thứ 87). Boca Raton, Florida, United States: CRC Press. tr. 477, 520. ISBN 0-8493-0594-2.
- ^ Lide, D. R. biên tập (2005). CRC Handbook of Chemistry and Physics (ấn bản thứ 86). Boca Raton (FL): CRC Press. tr. 4-80. ISBN 0-8493-0486-5.
- ^ Schultz, trang 94
- ^ S. F. Lincoln, D. T. Richens, A. G. Sykes "Metal Aqua Ions" Comprehensive Coordination Chemistry II Volume 1, Pages 515-555. doi:10.1016/B0-08-043748-6/01055-0
- ^ Hyde, Earl K. (1960). The radiochemistry of thorium (PDF). Subcommittee on Radiochemistry, National Academy of Sciences—National Research Council. Bản gốc (PDF) lưu trữ ngày 5 tháng 3 năm 2021. Truy cập ngày 17 tháng 3 năm 2013.
- ^ a b Georges, Audi (2003). “The NUBASE Evaluation of Nuclear and Decay Properties”. Nuclear Physics A. Atomic Mass Data Center. 729: 3–128. Bibcode:2003NuPhA.729....3A. doi:10.1016/j.nuclphysa.2003.11.001.
- ^ Bowen, Robert; Attendorn, H. G. (1988). “Theory and Assumptions in Potassium–Argon Dating”. Isotopes in the Earth Sciences. Springer. tr. 203–208. ISBN 978-0-412-53710-3.
- ^ D. Anaç (ngày 1 tháng 8 năm 1999). Improved crop quality by nutrient management. Springer. tr. 290–. ISBN 978-0-7923-5850-3.
- ^ “Radiation and Radioactive Decay. Radioactive Human Body”. Harvard Natural Sciences Lecture Demonstrations. Lưu trữ bản gốc ngày 19 tháng 9 năm 2004. Truy cập ngày 18 tháng 5 năm 2011.Quản lý CS1: bot: trạng thái URL ban đầu không rõ (liên kết)
- ^ Winteringham, F. P. W (1989). Radioactive fallout in soils, crops and food: a background review. Food & Agriculture Org. tr. 32. ISBN 978-92-5-102877-3.
- ^ Shimansky, V. (2003). “Observational constraints on potassium synthesis during the formation of stars of the Galactic disk”. Astronomy Reports. Truy cập ngày 7 tháng 8 năm 2011.
- ^ Greenwood 1997, tr. 69.
- ^ a b Micale, Giorgio; Cipollina, Andrea; Rizzuti, Lucio (2009). Seawater Desalination: Conventional and Renewable Energy Processes. Springer. tr. 3. ISBN 978-3-642-01149-8.
- ^ a b c d Prud'homme, Michel; Krukowski, Stanley T. (2006). “Potash”. Industrial minerals & rocks: commodities, markets, and uses. Society for Mining, Metallurgy, and Exploration. tr. 723–740. ISBN 978-0-87335-233-8.
- ^ Ross, William H. (1914). “The Origin of Nitrate Deposits”. Popular Science. Bonnier Corporation. tr. 134–145.
- ^ Garrett, Donald E. (ngày 31 tháng 12 năm 1995). Potash: deposits, processing, properties and uses. Springer. ISBN 978-0-412-99071-7.
- ^ a b Ober, Joyce A. “Mineral Commodity Summaries 2008:Potash” (PDF). United States Geological Survey. Truy cập ngày 20 tháng 11 năm 2008.
- ^ a b c Ober, Joyce A. “Mineral Yearbook 2006:Potash” (PDF). United States Geological Survey. Truy cập ngày 20 tháng 11 năm 2008.
- ^ Wishart, David J (2004). Encyclopedia of the Great Plains. U of Nebraska Press. tr. 433. ISBN 978-0-8032-4787-1.
- ^ Chiu, Kuen-Wai (2000). Kirk-Othmer Encyclopedia of Chemical Technology. John Wiley & Sons, Inc. doi:10.1002/0471238961.1615200103080921.a01.pub2. ISBN 9780471238966.
- ^ Burkhardt, trang 34
- ^ Delahunt, J; Lindeman, T (2007). “Review of the safety of potassium and potassium oxides, including deactivation by introduction into water”. Journal of Chemical Health and Safety. 14 (2): 21–32. doi:10.1016/j.jchas.2006.09.010.
- ^ Abdelwahab, M.; Youssef, S.; Aly, A.; Elfiki, S.; Elenany, N.; Abbas, M. (1992). “A simple calibration of a whole-body counter for the measurement of total body potassium in humans”. International Journal of Radiation Applications and Instrumentation. Part A. Applied Radiation and Isotopes. 43 (10): 1285–1289. doi:10.1016/0883-2889(92)90208-V.
- ^ Chang, Raymond (ngày 1 tháng 7 năm 2007). Chemistry. McGraw-Hill Higher Education. tr. 52. ISBN 978-0-07-110595-8.
- ^ Campbell, Neil (1987). Biology. Menlo Park, California: Benjamin/Cummings Pub. Co. tr. 795. ISBN 0-8053-1840-2.
- ^ Hellgren, Mikko; Sandberg, Lars; Edholm, Olle (2006). “A comparison between two prokaryotic potassium channels (KirBac1.1 and KcsA) in a molecular dynamics (MD) simulation study”. Biophysical Chemistry. 120 (1): 1–9. doi:10.1016/j.bpc.2005.10.002. PMID 16253415.
- ^ a b Institute of Medicine (U.S.). Committee on Optimization of Nutrient Composition of Military Rations for Short-Term, High-Stress Situations (2006). Nutrient composition of rations for short-term, high-intensity combat operations. National Academies Press. tr. 287–. ISBN 978-0-309-09641-6.
- ^ Shallenberger, R. S. (1993). Taste chemistry. Springer. tr. 120–. ISBN 978-0-7514-0150-9.
- ^ Lockless, S. W.; Zhou, M.; MacKinnon, R. (2007). “Structural and thermodynamic properties of selective ion binding in a K+ channel”. PLoS Biol. 5 (5): e121. doi:10.1371/journal.pbio.0050121. PMC 1858713. PMID 17472437.
- ^ Slonim, Anthony D.; Pollack, Murray M. (2006). “Potassium”. Pediatric critical care medicine. Lippincott Williams & Wilkins. tr. 812. ISBN 978-0-7817-9469-5.
- ^ Visveswaran, Kasi (2009). “hypokalemia”. Essentials of Nephrology, 2/e. BI Publications. tr. 257. ISBN 978-81-7225-323-3.
- ^ Potts, W. T. W. (1964). Osmotic and ionic regulation in animals. Pergamon Press.
- ^ Lans, H. S.; Stein, I. F.; Meyer, KA (1952). “The relation of serum potassium to erythrocyte potassium in normal subjects and patients with potassium deficiency”. American Journal of Medical Science. 223 (1): 65–74. doi:10.1097/00000441-195201000-00011. PMID 14902792.
- ^ Bennett, C. M.; Brenner, B. M.; Berliner, R. W. (1968). “Micropuncture study of nephron function in the rhesus monkey”. Journal of Clinical Investigation. 47 (1): 203–216. doi:10.1172/JCI105710. PMC 297160. PMID 16695942.
- ^ Solomon, A. K. (1962). “Pumps in the living cell”. Scientific American. 207 (2): 100–8. doi:10.1038/scientificamerican0862-100. PMID 13914986.
- ^ Kernan, Roderick P. (1980). Cell potassium (Transport in the life sciences). New York: Wiley. tr. 40, 48. ISBN 0-471-04806-2.
- ^ Wright, F. S. (1977). “Sites and mechanisms of potassium transport along the renal tubule”. Kidney International. 11 (6): 415–432. doi:10.1038/ki.1977.60. PMID 875263.
- ^ Squires, R. D.; Huth, E. J. (1959). “Experimental potassium depletion in normal human subjects. I. Relation of ionic intakes to the renal conservation of potassium”. Journal of Clinical Investigation. 38 (7): 1134–1148. doi:10.1172/JCI103890. PMC 293261. PMID 13664789.
- ^ Nicholas H. Fiebach (2007). Principles of ambulatory medicine. Lippincott Williams & Wilkins. tr. 748–750. ISBN 978-0-7817-6227-4.
- ^ Gadsby, D. C. (2004). “Ion transport: spot the difference”. Nature. 427 (6977): 795–797. Bibcode:2004Natur.427..795G. doi:10.1038/427795a. PMID 14985745.; for a diagram of the potassium pores are viewed, see Miller, C (2001). “See potassium run”. Nature. 414 (6859): 23–24. doi:10.1038/35102126. PMID 11689922.
- ^ Jiang, Y.; Lee, A.; Chen, J.; Cadene, M.; Chait, B. T.; MacKinnon, R. (2002). “Crystal structure and mechanism of a calcium-gated potassium channel”. Nature. 417 (6888): 515–22. doi:10.1038/417515a. PMID 12037559.
- ^ Shi, N.; Ye, S.; Alam, A.; Chen, L.; Jiang, Y (2006). “Atomic structure of a Na+- and K+-conducting channel”. Nature. 440 (7083): 570–574. Bibcode:2006Natur.440..570S. doi:10.1038/nature04508. PMID 16467789.; includes a detailed picture of atoms in the pump.
- ^ Zhou, Y.; Morais-Cabral, J. H.; Kaufman, A.; MacKinnon, R. (2001). “Chemistry of ion coordination and hydration revealed by a K+ channel-Fab complex at 2.0 A resolution”. Nature. 414 (6859): 43–48. doi:10.1038/35102009. PMID 11689936.
- ^ Noskov, S. Y.; Bernèche, S.; Roux, B. (2004). “Control of ion selectivity in potassium channels by electrostatic and dynamic properties of carbonyl ligands”. Nature. 431 (7010): 830–834. Bibcode:2004Natur.431..830N. doi:10.1038/nature02943. PMID 15483608.
- ^ “Potassium Food Charts”. Asia Pacific Journal of Clinical Nutrition. Bản gốc lưu trữ ngày 13 tháng 2 năm 2019. Truy cập ngày 18 tháng 5 năm 2011.
- ^ Folis, R. H. (1942). “Myocardial Necrosis in Rats on a Potassium Low Diet Prevented by Thiamine Deficiency”. Bull. Johns-Hopkins Hospital. 71: 235.
- ^ DRI, dietary reference intakes for water, potassium, sodium, chloride, and sulfate. Washington, D.C.: National Academies Press. 2005. ISBN 0-309-53049-0.
|first=thiếu|last=(trợ giúp) Pdf - ^ Grim, C. E.; Luft, F. C.; Miller, J. Z.; Meneely, G.R.; Battarbee, H. D.; Hames, C. G.; Dahl, L. K. (1980). “Racial differences in blood pressure in Evans County, Georgia: relationship to sodium and potassium intake and plasma renin activity”. Journal of Chronicle Diseases. 33 (2): 87–94. doi:10.1016/0021-9681(80)90032-6. PMID 6986391.
- ^ Karger, S. (2004). “Energy and nutrient intake in the European Union” (PDF). Annals of Nutrition and Metabolism. 48 (2 (suppl)): 1–16. doi:10.1159/000083041.
- ^ D'Elia, L.; Barba, G.; Cappuccio, F.; Strazzullo (2011). “Potassium Intake, Stroke, and Cardiovascular Disease: A Meta-Analysis of Prospective Studies”. The Journal of the American College of Cardiology. 57 (10): 1210–1219. doi:10.1016/j.jacc.2010.09.070.
- ^ Soar, J; Perkins, GD; Abbas, G; Alfonzo, A; Barelli, A; Bierens, JJ; Brugger, H; Deakin, CD; Dunning, J; Georgiou, M; Handley, AJ; Lockey, DJ; Paal, P; Sandroni, C; Thies, KC; Zideman, DA; Nolan, JP (tháng 10 năm 2010). “European Resuscitation Council Guidelines for Resuscitation 2010 Section 8. Cardiac arrest in special circumstances: Electrolyte abnormalities, poisoning, drowning, accidental hypothermia, hyperthermia, asthma, anaphylaxis, cardiac surgery, trauma, pregnancy, electrocution”. Resuscitation. 81 (10): 1400–33. doi:10.1016/j.resuscitation.2010.08.015. PMID 20956045.
- ^ Pathy, M.S. John (2006). Principles and practice of geriatric medicine (ấn bản thứ 4). Chichester [u.a.]: Wiley. tr. Appendix. ISBN 9780470090558.
- ^ Manual for pharmacy technicians, By Linda Fred, American Society of Health-System Pharmacists, trang 218
- ^ Manual for pharmacy technicians, By Linda Fred, American Society of Health-System Pharmacists, trang 246
- ^ Vitamins and Minerals Demystified, By Steve Blake, trang 172
- ^ Roy, Amit H. (2007). Kent and Riegel's handbook of industrial chemistry and biotechnology. Springer. tr. 1135–1157. ISBN 978-0-387-27843-8.
- ^ “Potassium Content of Selected Foods per Common Measure, sorted by nutrient content” (PDF). USDA National Nutrient Database for Standard Reference, Release 20. Lưu trữ bản gốc ngày 28 tháng 5 năm 2008. Truy cập ngày 9 tháng 9 năm 2015.Quản lý CS1: bot: trạng thái URL ban đầu không rõ (liên kết)
- ^ Figoni, Paula I (2010). “Bleaching and Maturing Agents”. How Baking Works: Exploring the Fundamentals of Baking Science. John Wiley and Sons. tr. 86. ISBN 978-0-470-39267-6.
- ^ Chichester, C. O. (tháng 7 năm 1986). “Uses and Exposure to Sulfites in Food”. Advances in food research. Academic Press. tr. 4–6. ISBN 978-0-12-016430-1.
- ^ H. Schultz, G. Bauer, Erich Schachl, F. Hagedorn, P. Schmittinger "Potassium Compounds" in Ullmann's Encyclopedia of Industrial Chemistry, 2005, Wiley-VCH, Weinheim. doi:10.1002/14356007.a22_039
- ^ Toedt, John (2005). “Personal Cleansing Products: Bar Soap”. Chemical composition of everyday products. Greenwood Publishing Group. ISBN 978-0-313-32579-3.
- ^ Schultz, trang 95
- ^ Schultz, trang 99
- ^ Philosophy of Mathematics, de John Francis Real or fake: studies in authentication de Joe Nickell trang 20: An indigo and iron-gall blue-black ink was produced in 1834, followed by a potassium chromate type of logwood ink in about 1848.
- ^ Siegel, Richard S. (1940). “Ignition of the safety match”. Journal of Chemical Education. 17 (11): 515. Bibcode:1940JChEd..17..515S. doi:10.1021/ed017p515.
- ^ Anger, Gerd; Halstenberg, Jost; Hochgeschwender, Klaus; Scherhag, Christoph; Korallus, Ulrich; Knopf, Herbert; Schmidt, Peter; Ohlinger, Manfred. “Chromium Compounds”. Bách khoa toàn thư Ullmann về Hóa chất công nghiệp. 9. Weinheim: Wiley-VCH. tr. 178. doi:10.1002/14356007.a07_067.
- ^ “Old Nuclear-Powered Soviet Satellite Acts Up”. Space.com. ngày 15 tháng 1 năm 2009. Bản gốc lưu trữ ngày 22 tháng 2 năm 2019. Truy cập ngày 26 tháng 8 năm 2014.
- ^ Klinkrad, Heiner (ngày 23 tháng 2 năm 2006). Space debris: models and risk analysis. tr. 83. ISBN 978-3-540-25448-5.
- ^ Greenwood 1997, tr. 74.
- ^ Marx, Robert F. (1990). The history of underwater exploration. Courier Dover Publications. ISBN 978-0-486-26487-5.
- ^ Gettens, Rutherford John (1966). Painting materials: A short encyclopaedia. Courier Dover Publications. tr. 109–110. ISBN 978-0-486-21597-6.
- ^ Jackson, C. B.; Werner, R. C. (ngày 1 tháng 1 năm 1957). “The Manufacture of Potassium and NaK”. Advances in Chemistry. Advances in Chemistry. 19: 169–173. doi:10.1021/ba-1957-0019.ch018. ISBN 9780841200203.
- ^ Kearey, Philip (2002). “Optical Pumped Magnetometer”. An introduction to geophysical exploration. Wiley-Blackwell. tr. 164. ISBN 978-0-632-04929-5.
- ^ Bằng sáng chế Hoa Kỳ số 3.095.372, filed ngày 5 tháng 7 năm 1960. UK Patent GB884946.
- ^ “The Non Numismatic Bibliography of Dr L.H. Cope”. Truy cập ngày 19 tháng 11 năm 2016.
- ^ Extinguishment of Alkali Metal Fires, S.J. Rodgers and W.A. Everson, Technical Documentary Report APL-TDR 64-114, Air Force Laboratory, Wright-Patterson Air Force Base, Ohio, 1964, pp. 28-31 doi:10.1007/BF02588480.
- ^ Solomon, Robert E. (2002). Fire and Life Safety Inspection Manual. Jones & Bartlett Learning. tr. 459. ISBN 978-0-87765-472-8.
- ^ “DOE Handbook-Alkali Metals Sodium, Potassium, NaK, and Lithium”. Hss.doe.gov. Bản gốc lưu trữ ngày 28 tháng 9 năm 2010. Truy cập ngày 16 tháng 10 năm 2010.
- ^ Wray, Thomas K. “Danger: peroxidazable chemicals” (PDF). Environmental Health & Public Safety ([[North Carolina State University]]). Lưu trữ bản gốc ngày 14 tháng 12 năm 2004. Truy cập ngày 3 tháng 12 năm 2016.Quản lý CS1: bot: trạng thái URL ban đầu không rõ (liên kết)
- ^ a b Schonwald, Seth (2004). “Potassium Chloride and Potassium Permanganate”. Medical toxicology. Lippincott Williams & Wilkins. tr. 903–905. ISBN 978-0-7817-2845-4.
- ^ Markovchick, Vincent J. (2003). Emergency medicine secrets. Elsevier Health Sciences. tr. 223. ISBN 978-1-56053-503-4.
Danh mục tài liệu
[sửa | sửa mã nguồn]- Burkhardt, Elizabeth R. (2006). “Potassium and Potassium Alloys”. Ullmann's Encyclopedia of Industrial Chemistry. A22. tr. 31–38. doi:10.1002/14356007.a22_031.pub2. ISBN 3-527-30673-0.
- Greenwood, Norman N (1997). Chemistry of the Elements (ấn bản thứ 2). Oxford: Butterworth-Heinemann. ISBN 0-08-037941-9.
- Holleman, Arnold F.; Wiberg, Egon; Wiberg, Nils (2007). “Potassium”. Lehrbuch der Anorganischen Chemie (bằng tiếng Đức) . Walter de Gruyter. ISBN 3110177706.
- Schultz, H. (2006). “Potassium compounds”. Ullmann's Encyclopedia of Industrial Chemistry. A22. tr. 39–103. doi:10.1002/14356007.a22_031.pub2. ISBN 3-527-30673-0.
- National Nutrient Database Lưu trữ 2017-12-22 tại Wayback Machine trên Bộ Nông nghiệp Hoa Kỳ
Liên kết ngoài
[sửa | sửa mã nguồn] Tư liệu liên quan tới Potassium tại Wikimedia Commons
Tư liệu liên quan tới Potassium tại Wikimedia Commons
(tiếng Việt)
(tiếng Anh)
- Potassium (K) tại Encyclopædia Britannica (tiếng Anh)
- Kali: the essentials - WebElements.com
- EnvironmentalChemistry.com – Kali
- Kali- Los Alamos National Laboratory
- Kali (Kali) tại The Periodic Table of Videos
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | |||||||||||||||
| 1 | H | He | ||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | ||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | ||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |

